INTRODUCCION
Tras un infarto agudo de miocardio (IAM), el rápido restablecimiento del flujo miocárdico es el objetivo fundamental del tratamiento ya que, en gran medida, de ello depende la recuperación funcional y el pronóstico a corto y medio plazo1,2. En algunos pacientes, a pesar de una correcta apertura arterial, no se consigue una adecuada perfusión del tejido miocárdico3,4. Este fenómeno, conocido como «no-reflujo», se relaciona con la falta de recuperación funcional de la zona dañada5,6. Hasta ahora, los métodos angiográficos empleados han resultado poco útiles a la hora de predecir la recuperación de los segmentos afectados7,8. El empleo de guías de Doppler intracoronario ha permitido estudiar el flujo coronario e identificar algunos patrones que se relacionan con el daño microvascular y con la falta de recuperación funcional9-13.
Recientemente, la disponibilidad de sondas ecocardiográficas de alta frecuencia posibilita el estudio del flujo coronario mediante Doppler transtorácico14. Algunos estudios han demostrado la posibilidad de detectar el daño microvascular mediante este método; sin embargo, faltan estudios que demuestren el valor predictivo independiente de esta técnica asociada con las variables clínicas y del procedimiento que pudieran influir en el daño miocárdico. Por tanto, los objetivos del presente trabajo fueron estudiar los diferentes patrones del flujo coronario de la arteria descendente anterior (ADA) y establecer sus relaciones, junto con otros parámetros clínicos, en la recuperación funcional y el remodelado ventricular a corto plazo tras la angioplastia coronaria transluminal percutánea (ACTP) primaria.
MÉTODOS
Pacientes
Durante un período de inclusión de 2 años, 190 pacientes fueron admitidos en nuestro hospital con criterios de IAM anterior. Se definió como angioplastia primaria a la que se realizó sin tratamiento fibrinolítico previo o concomitante, en pacientes con historia de dolor torácico de menos de 12 h de duración, asociado con elevación del segmento ST en el electrocardiograma (ECG) (de al menos 0,1 mV en 2 o más derivaciones contiguas) o bloqueo de rama izquierda nuevo15. Se consideró la inclusión en el estudio de los 110 pacientes con un primer infarto a los que se les realizó una ACTP primaria. Se excluyó a 30 pacientes que presentaron insuficiencia cardiaca de grado Killip ≥ 3 o 4 que fallecieron en el hospital. Ocho pacientes rehusaron ser incluidos en el estudio. El grupo inicial estaba constituido por 68 pacientes: en 4 no se obtuvo el flujo coronario de la ADA (5,9%) y 7 pacientes no acudieron al control del primer mes. Finalmente, el grupo objeto del estudio estuvo formado por 57 pacientes, 11 mujeres y 46 varones, con una edad media de 59,67 años (rango, 30-85).
Protocolo
El protocolo de estudio fue aprobado por el comité ético de nuestro hospital y todos los pacientes dieron su consentimiento por escrito. En las primeras 24 h desde el inicio de los síntomas, todos los pacientes recibieron angioplastia de la lesión causante del infarto con el eventual implante de un stent intracoronario. En todos los casos, la apertura del vaso fue satisfactoria y quedó una estenosis residual < 30% y un flujo anterógrado TIMI de grado III.
A las 48-72 h de la apertura del vaso se realizó el estudio del flujo coronario de la ADA. La evaluación de las dimensiones y la contractilidad segmentaria del ventrículo izquierdo se realizó a las 72 h y al mes del procedimiento.
Estudio del flujo coronario
Las imágenes de la ADA se obtuvieron con un equipo Sonos 5500 (Philips, Andover, Massachussets), con un transductor de alta frecuencia S12 (5-12 MHz).
La localización de la ADA se obtuvo desde una posición próxima a la línea medioclavicular en el cuarto o quinto espacios intercostales, con el paciente en decúbito lateral izquierdo. Una vez localizado el surco interventricular anterior en el eje corto, el haz de ultrasonidos se rotó lateralmente para visualizar la porción distal de la ADA con mapeo de Doppler color de alta frecuencia (5 MHz) y rango de velocidades de ±15 a ±19 cm/s y profundidad ajustada a 7 cm. La velocidad del flujo sanguíneo se midió con señal de Doppler pulsado, para lo que se intentó alinear el haz de ultrasonidos lo más paralelo posible al flujo de la ADA distal. La frecuencia empleada en el Doppler pulsado fue de 5 MHz, con un tamaño de muestra de 1,9 mm. Para potenciar la señal Doppler color y pulsado, se empleó un agente de contraste (levovist 200 mg/ml en bolos de 0,5 ml).
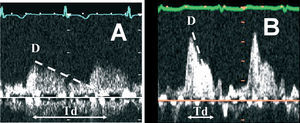
Los registros Doppler del flujo coronario fueron evaluados por un ecocardiografista experimentado que desconocía los datos basales del paciente. Se obtuvieron medidas de la velocidad pico sistólica y diastólica y del tiempo de deceleración de la onda diastólica: tiempo desde el pico de velocidad hasta que la tangente a la curva de deceleración corta el eje de velocidad «0» cm/s (fig. 1). Los pacientes fueron clasificados en 2 grupos según el tipo de flujo coronario. En el grupo 1 se incluyó a los pacientes con patrón de flujo considerado normal (tipo A): onda diastólica con tiempo de deceleración lenta (> 500 ms). En el grupo 2 se incluyó a los pacientes con patrón de flujo anormal (tipo B), caracterizado por una onda diastólica de elevada velocidad y con tiempo de deceleración ≤ 500 ms. Se tomaron 500 ms como punto de corte, de acuerdo con estudios previos realizados con guías Doppler intracoronarias12,13.
Fig. 1. A: patrón normal del flujo coronario de la arteria descendente anterior. Se observa una onda diastólica con una pendiente de deceleración lenta y un tiempo de deceleración prolongado. B: patrón anormal del flujo coronario de la descendente anterior. Se observa una onda diastólica de alta velocidad y rápida deceleración. Td: tiempo de deceleración.
Evaluación de la contractilidad
Para el estudio de las dimensiones y la contractilidad del ventrículo izquierdo se empleó una sonda S3 (Philips, Andover, Massachussets). Se obtuvieron los planos paraesternal largo y de eje corto del ventrículo izquierdo, así como los planos apical de 2 y 4 cámaras. Los estudios fueron grabados y evaluados posteriormente por un observador experimentado que no conocía el flujo coronario.
Se calcularon los volúmenes del ventrículo izquierdo y la fracción de eyección por el método de Simpson de 2 planos. Posteriormente se valoró la contractilidad segmentaria de los 16 segmentos del ventrículo izquierdo según lo propuesto por la Sociedad Americana de Ecocardiografía16. Se adjudicó 1 punto a la contractilidad normal, 2 a la hipocinesia, 3 a la acinesia y 4 a la discinesia. Se calcularon el índice de contractilidad regional global del ventrículo izquierdo y el índice de contractilidad regional en el territorio de la descendente anterior; para este último se seleccionaron los 9 segmentos comúnmente aceptados como dependientes de la ADA: los 4 segmentos apicales, el septal anterior basal y medio, el septal posterior medio y los segmentos anteriores basal y medio.
Las diferencias entre el estudio de la fase aguda y el realizado al mes fueron consideradas significativas cuando superaban la variabilidad intraobservador de nuestro laboratorio: el 5% para la fracción de eyección ventricular izquierda (FEVI) y 5 ml/m² para los volúmenes. Un incremento del índice de volumen sistólico > 5 ml/m² fue indicativo de dilatación ventricular y, por tanto, de remodelado patológico.
La mejoría de 1 punto en al menos 3 segmentos de los 9 considerados fue indicativa de viabilidad de la zona anterior, es decir, de una reducción en el índice de motilidad regional del territorio de la descendente anterior de al menos 0,33.
Análisis estadístico
Las variables continuas se expresan como media ± desviación estándar y se compararon con el test de la t de Student para datos emparejados y no emparejados. Las variables categóricas se representan como porcentajes y se comparan con el test de la χ², o con el test exacto de Fisher en caso necesario. En el análisis multivariable se utilizó un modelo de regresión logística en el que se incluyeron, además de la característica analizada, las siguientes variables: edad, sexo, factores de riesgo coronario, tiempo hasta la apertura del vaso y tratamiento en el momento del alta. Se calcularon los coeficientes de correlación de Spearman en todos los casos. Los valores de p ≤ 0,05 fueron considerados estadísticamente significativos. El análisis estadístico se realizó con el paquete estadístico SPSS versión 9.0.
RESULTADOS
Características basales de los pacientes
El grupo 1 está integrado por 31 (54%) pacientes con patrón de flujo normal. En el grupo 2 se incluyó a 26 (46%) pacientes que presentaban un patrón de flujo anormal (fig. 1). En la tabla 1 se presentan las características clínicas de los pacientes de ambos grupos. La frecuencia de pacientes diabéticos y la edad fueron más altas en el grupo 2. No hubo diferencias en el tiempo hasta la apertura del vaso, en el grado TIMI conseguido y en el nivel máximo de creatincinasa (CK) alcanzado. El estudio basal mostró que los pacientes del grupo 2 tenían un mayor volumen telesistólico, menor FEVI y peores índices de motilidad regional segmentaria.
Evaluación ecocardiográfica al mes
En la evolución al mes del episodio agudo, los pacientes del grupo 1 persistían con cifras de volúmenes ventriculares, motilidad segmentaria y FEVI más favorables que los pacientes del grupo 2 (tabla 2).
Los volúmenes no mostraron diferencias significativas respecto a los datos basales en los pacientes del grupo 1. Por el contrario en el grupo 2 se comprobó un aumento significativo de los índices volumétricos telediastólico (55,8 ± 12,9 frente a 62,9 ± 16,8 ml/m²; p < 0,05) y telesistólico (32,2 ± 9,5 frente a 37,1 ± 14,9 ml/m² p < 0,05) (fig. 2). Los índices de contractilidad regional mejoraron en los pacientes del grupo 1, sin cambios significativos en el grupo 2 (fig. 3).
Fig. 2. Evolución de los índices de los volúmenes del ventrículo izquierdo. Los datos se presentan como valor medio ± desviación estándar. Para evitar superposiciones sólo se presenta una desviación positiva o negativa. Los cuadrados representan el índice de volumen telediastólico y los triángulos el índice del volumen telesistólico. Las figuras oscuras representan a los pacientes del grupo 1 y las claras, a los pacientes del grupo 2. Los pacientes del grupo 2 presentaron un aumento significativo en los volúmenes ventriculares al mes del infarto. IVTD: índice de volumen telediastólico; IVTS: índice del volumen telesistólico.
Fig. 3. Evolución de los índices de motilidad regional de ventrículo izquierdo. Los datos y su dispersión se presentan como en la figura 2. Los cuadros representan el índice de motilidad segmentaria global (IMR) y los triángulos el índice de motilidad regional del territorio anterior (IMRDA). Las figuras oscuras representan a los pacientes del grupo 1 y las claras, a los pacientes del grupo 2. Los pacientes del grupo 2 no experimentan mejoría de la contractilidad regional al mes del infarto, mientras que sí mejoran los pacientes del grupo 1.
Finalmente, la FEVI experimentó una significativa mejoría en los pacientes del grupo 1 al pasar del 46,8 ± 8,6 al 52,6 ± 8,8% (p < 0,01), mientras que en el grupo 2 no hubo variaciones (el 42,4 ± 8,1 frente al 42,4 ± 9,6%; p = NS).
Patrón de flujo coronario y predicción de recuperación funcional y remodelado patológico
Diecisiete pacientes presentaron remodelado ventricular patológico, es decir, aumento del índice de volumen telesistólico (IVTS); de éstos, 12 (70%) presentaban un patrón de flujo tipo B. Por otra parte, al mes de seguimiento la FEVI no experimentó mejoría en 28 pacientes, 17 (61%) de los cuales eran del grupo 2.
En el análisis multivariable, además del patrón de flujo coronario, se incluyeron datos clínicos como la edad y el sexo, factores de riesgo como el tabaquismo, la hipercolesterolemia y la diabetes, y variables del tratamiento, como medicación en el momento del alta y tiempo hasta la ACTP. De todas estas variables, fueron predictores independientes de falta de mejoría en la FEVI el patrón de flujo coronario tipo B (p < 0,05) y la presencia de HTA previa (p < 0,05); los predictores de aumento en el índice del volumen telesistólico del ventrículo izquierdo fueron el patrón de flujo tipo B (p < 0,01) y el tabaquismo (p < 0,05) y, finalmente, los predictores de falta de recuperación funcional en el territorio de la ADA fueron el patrón de flujo coronario tipo B (p < 0,05) y la hipercolesterolemia (p < 0,05) (tabla 3).
El tiempo hasta la revascularización de la arteria causante del infarto fue un factor que mostró una tendencia a asociarse con la falta de viabilidad del territorio anterior, aunque no alcanzó significación estadística (p = 0,098).
DISCUSION
Nuestro estudio demuestra que la evaluación del flujo coronario mediante Doppler transtorácico es un método sencillo y no invasivo que permite identificar a los pacientes que presentan mayor daño microvascular y, como consecuencia, una peor evolución tras la ACTP primaria. En nuestros pacientes, la presencia de un patrón de flujo tipo B, caracterizado por una rápida deceleración de la onda diastólica, se asoció con una falta de recuperación funcional de la zona infartada y con una dilatación ventricular a corto plazo.
Daño microvascular y patrón de flujo coronario en la fase aguda del infarto agudo de miocardio
La preservación del estado de la microvasculatura coronaria tras el infarto de miocardio es fundamental para la recuperación funcional17-19. El daño microvascular se manifiesta fisiopatológicamente como una disminución del lecho capilar y arteriolar en la zona de la cicatriz6,19. Junto a esta pérdida estructural de los grandes infartos transmurales, otros mecanismos fisiopatológicos desencadenados por la reperfusión, como la presencia de radicales libres de oxígeno20, espasmo microvascular21, edema22, o microémbolos23, causan en último término la elevada resistencia al flujo de la arteria coronaria epicárdica de la que depende esa microvasculatura24-26. La consecuencia final es una reducción considerable del lecho capilar efectivo que se rellenaría rápidamente en la fase precoz de la diástole. Esto explicaría el patrón del flujo en la arteria epicárdica: una onda diastólica de alta velocidad seguida de una rápida desaceleración y un flujo lento tardío, como observamos en el patrón de flujo tipo B de la figura 1.
Evaluación transtorácica del daño microvascular postinfarto agudo de miocardio
La detección de daño microvascular es de gran importancia en la estratificación pronóstica tras el IAM reperfundido17. Hasta ahora, el método más fiable había sido el análisis del flujo coronario con el empleo de guías de Doppler intracoronario12,13. Este método permitió describir un patrón de flujo, similar al que encontramos con Doppler transtorácico, que se asoció con daño microvascular en pacientes con grandes infartos transmurales y en los que presentan el fenómeno de no reflujo tras la reperfusión27-29. Otro método que ha mostrado similar eficacia es el estudio de la reserva del flujo en respuesta a la vasodilatación coronaria11.
Pocos estudios han empleado el Doppler transtorácico para evaluar el daño microvascular. En nuestro estudio demostramos que este método es factible: obtuvimos flujos adecuados en 64 de los 68 pacientes inicialmente evaluados, lo que supone una tasa de éxito del 94% y permite identificar a los pacientes que van a presentar una dilatación ventricular a corto plazo (odds ratio [OR] = 6,14; p < 0,01). En el estudio realizado por Voci et al30, ningún parámetro Doppler fue de utilidad y sólo la presencia de colaterales fue predictora de recuperación funcional de la zona infartada. Sin embargo, el estudio realizado por Hozumi et al31, en el que emplearon una metodología similar a la nuestra, se encontró una correlación significativa entre el tiempo de desaceleración de la onda diastólica y la mejoría en la contractilidad regional de la zona infartada. Estos autores emplearon como punto de corte 600 ms. Nosotros empleamos como punto de corte 500 ms siguiendo lo descrito mediante guías de Doppler intracoronario4,9,12,27. Finalmente, Iwakura et al, en un estudio reciente32 muestran que el patrón de flujo coronario evaluado mediante Doppler transtorácico es el mejor predictor del fenómeno de no reflujo y que supera a los criterios angiográficos, electrocardiográficos o enzimáticos.
En nuestro estudio, los pacientes con patrón de flujo anormal eran mayores y con mayor incidencia de diabetes. Además, el estudio basal muestra que estos pacientes parten con una FEVI ligeramente inferior. Todos estos datos coinciden con lo publicado por otros autores en estudios limitados a la fase aguda del IAM12,13,32. Nuestro trabajo aporta el valor del seguimiento de un mes y el del análisis multivariable. Este análisis permite observar que, a pesar de la inclusión de variables clínicas y del procedimiento terapéutico, el patrón de flujo coronario mantiene su valor independiente como predictor de la falta de recuperación funcional y del remodelado ventricular patológico.
Limitaciones
La obtención del flujo coronario mediante Doppler transtorácico precisa una sonda especial y cierto entrenamiento por parte del explorador. En nuestro grupo, el porcentaje de éxitos es > 80%. Algunos autores han criticado este patrón de flujo y han indicado que su presencia podría ser un artefacto debido a la proximidad de la muestra Doppler con las paredes del vaso33. Sin embargo, en los estudios realizados mediante guías de Doppler intracoronario se ha descrito con claridad este mismo patrón en el seno del IAM revascularizado4,9,27. Por tanto, esta explicación no parece posible. El punto de corte para el tiempo de deceleración de la velocidad diastólica no está bien definido en la bibliografía. Los tiempos altos se relacionan con la recuperación funcional, y a la inversa. En nuestro estudio establecimos como punto de corte 500 ms tras valorar los datos de los estudios intracoronarios. El número de pacientes es limitado y el seguimiento es corto. Aun así, el nivel de significación alcanzado es bastante aceptable, tanto en la valoración de la función ventricular global como en la dilatación ventricular. En el caso de valorar la viabilidad de la zona infartada, quizá una muestra mayor añadiría potencia al estudio. Por último, el estudio se limita a pacientes con IAM anterior, ya que la obtención del flujo coronario en otras arterias, aunque es posible, es más baja (en torno al 50% en nuestras manos). Sería necesario un seguimiento más largo para confirmar los resultados aquí apuntados.
CONCLUSIONES
Tras un IAM anterior revascularizado, el estudio del flujo coronario de la ADA mediante Doppler transtorácico permite identificar a los pacientes con daño microvascular que, a corto plazo, evolucionan hacia la dilatación ventricular sin recuperación de la función regional de la zona infartada.
Correspondencia: Dr. G. de la Morena.
Servicio de Cardiología. Hospital Universitario Virgen de la Arrixaca.
Ctra. Madrid-Cartagena, s/n. El Palmar. 30110 Murcia. España.
Correo electrónico: gdlmorena@yahoo.es
Recibido el 1 de agosto de 2005.
Aceptado para su publicación el 12 de enero de 2006.