La cirugía bariátrica es una herramienta eficaz de control metabólico para pacientes obesos diabéticos. El objetivo de este trabajo es determinar la evolución del peso y el metabolismo glucídico y lipídico en pacientes obesos diabéticos intervenidos de cirugía bariátrica, durante los primeros 4 años tras la intervención.
MétodosEstudio retrospectivo de 104 pacientes (71 mujeres; media de edad, 53,0±0,9 años; índice de masa corporal, 46,8±0,7) con diabetes mellitus tipo 2 de una mediana de 3 años de evolución, a los que se practicó bypass gástrico proximal laparoscópico.
ResultadosLa glucemia y la concentración de glucohemoglobina descendieron durante los primeros 1-3 meses y se mantuvieron estables hasta los 4 años, lo que permitió eliminar el tratamiento hipoglucemiante al 80% de los pacientes. No observamos diferencias en función del índice de masa corporal, tiempo de evolución de la diabetes mellitus o el tratamiento antidiabético previo. El peso descendió hasta los 15-24 meses, con ligera recuperación posterior. Los valores de colesterol total, triglicéridos y lipoproteínas de baja densidad mejoraron significativamente, y se había obtenido valores objetivo en alrededor del 80% de los pacientes a partir de 12 meses. Estos descensos no se correlacionaron con los cambios de peso. Las lipoproteínas de alta densidad descendieron hasta los 12 meses, con una pequeña recuperación posterior, a pesar de lo cual el 85% de los pacientes presentaban valores objetivo 24 meses tras la cirugía.
ConclusionesLa cirugía bariátrica es eficaz para el tratamiento de pacientes diabéticos obesos, mejora su control metabólico y reduce el riesgo cardiovascular.
Palabras clave
La obesidad es una enfermedad crónica y multifactorial, caracterizada por un exceso de grasa corporal que ocasiona un aumento de peso patológico. Afecta a una proporción considerable de la población y abarca todas las edades de la vida, a ambos sexos y todas las condiciones sociales. Así, se estima que la prevalencia de personas con índice de masa corporal (IMC)>30 se ha duplicado entre 1986 y 2000. Asimismo, la proporción de pacientes con IMC>35 alcanza al 15,5% de la población de Estados Unidos1,2. Del mismo modo se calcula que en España se ha producido un incremento de la obesidad mórbida de más del 200%3.
En las últimas décadas se ha observado un incremento paralelo en la incidencia de la diabetes mellitus tipo 2 (DM2). El fundamento de su patogenia es la insulinorresistencia vinculada estrechamente al sobrepeso o la obesidad que frecuentemente este tipo de pacientes presenta, hasta el punto de que la obesidad abdominal se considera el principal factor de riesgo de DM2. En un reciente estudio publicado en nuestro país, al menos el 30% de la población presentaba alguna alteración en el metabolismo de los hidratos de carbono, con una prevalencia de DM ajustada por edad y sexo del 13,8%4.
Los actuales tratamientos no invasivos para la obesidad, incluidos los farmacológicos, producen resultados discretos, con una baja tasa de mantenimiento de los resultados a largo plazo5,6. Este hecho es especialmente notable en el caso de los pacientes con DM2, en los que conseguir un control metabólico general, con disminución de la glucohemoglobina A1c (HbA1c) y la presión arterial y la mejora del perfil lípidico a largo plazo, resulta difícil, como muestran algunos estudios recientes publicados en España7,8.
La otra estrategia de tratamiento de estos síndromes es la cirugía bariátrica. Con ella se pretende modificar la anatomía del aparato digestivo para disminuir la capacidad gástrica exclusivamente o asociarla a grados variables de hipoabsorción intestinal, con el objetivo de reducir el peso corporal y mejorar las comorbilidades que conlleva9–12. Estas técnicas quirúrgicas se han ido estableciendo paulatinamente. Un avance capital se produjo en 1994, cuando Wittgrove y Clark realizaron el primer bypass gástrico por vía laparoscópica, mejorando significativamente la seguridad del procedimiento y reduciendo el traumatismo quirúrgico asociado a la intervención5. A partir de entonces, el número de intervenciones ha crecido exponencialmente; así, se estima que en 2008 se realizaron 344.000 intervenciones de este tipo en el mundo, de las que alrededor de 5.000 se llevaron a cabo en nuestro país13.
La cirugía bariátrica se ha demostrado extremadamente útil para pacientes obesos con DM2, no solo en términos de disminución del peso corporal, sino también de mejora del control glucémico. El mecanismo por el que esta se produce no está totalmente esclarecido, y hay varias teorías que intentan explicarla14. Complementariamente, los pacientes mejoran su presión arterial, el perfil lípidico y el síndrome de apneas del sueño, entre otras complicaciones frecuentemente asociadas a la obesidad15.
Este artículo describe los resultados derivados de un estudio retrospectivo llevado a cabo en un hospital general durante 4 años sobre la eficacia de la cirugía bariátrica en el control glucémico de pacientes con obesidad y DM2.
MÉTODOSSe presenta un estudio retrospectivo en el que se incluyó a 104 pacientes con IMC>35 (media, 46,8±0,7) que además padecían DM2 (71 mujeres y 33 varones; media de edad, 53,0±0,9 años; evolución: mediana, 3 años; media, 9,2±0,9 [1-23] años) según el criterio diagnóstico de la American Diabetes Association16. Todos ellos cumplían el criterio quirúrgico de los National Institutes of Health17.
A los pacientes se les practicó cirugía bariátrica entre 2002 y noviembre 2011 (11 pacientes intervenidos de banda gástrica y el resto, bypass gástrico proximal laparoscópico). Se había valorado previamente a todos ellos en la unidad de obesidad del servicio de endocrinología y nutrición, que incluye endocrinólogos, nutricionistas, cirujanos, psiquiatras y reumatólogos. La confidencialidad de los pacientes se garantizó mediante números clave, y todos ellos fueron adecuadamente informados sobre los procedimientos a emplear y dieron su consentimiento por escrito de acuerdo con las leyes nacionales y la Declaración de Helsinki actualizada en 2000 (Declaración de Edimburgo).
Del estudio se excluyó a los enfermos con DM tipo 1 o de otra etiología y a quienes presentaban características que contraindican la cirugía bariátrica: edad<18 o>60 años, enfermedades secundarias que justifiquen la obesidad, abuso de alcohol o drogas, alteraciones psiquiátricas mayores (esquizofrenia, psicosis), retraso mental, trastornos del comportamiento alimentario (bulimia nerviosa), embarazo o deseo de gestación en el año siguiente a la cirugía.
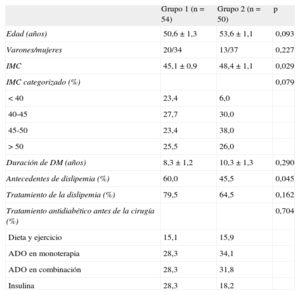
Todos los pacientes recibieron tratamiento intensivo para control de peso, siguiendo un plan de alimentación y de ejercicio físico personalizado tanto antes como tras la cirugía. Se recogieron los datos previos a la intervención y los obtenidos tras 1, 3, 6, 12, 15, 24, 36 y 48 meses. No hubo pérdidas por fallecimiento. El seguimiento de los datos fue irregular; no todos los pacientes acudieron a todas las visitas y no a todos los pacientes se les midieron todos los parámetros en las visitas a las que acudieron. Así, el seguimiento medio fue de 36,57 meses/pacientes con datos de 54 pacientes a los 4 años (solo 1 de ellos intervenido de banda gástrica). Para analizar los resultados en función del seguimiento, creamos dos grupos: grupo 1, constituido por los 54 pacientes que completaron el seguimiento a 4 años, y grupo 2, formado por 50 pacientes que no completaron dicho seguimiento. No observamos diferencias entre ambos grupos respecto a la edad, la distribución de sexos, la duración y el tratamiento de la DM. El grupo que completó el seguimiento durante 4 años presentaba menor IMC antes de la cirugía pero, al comparar su distribución en los cuatro grupos creados en función del IMC, no observamos diferencia. Además, presentaban menos dislipemia, pero la proporción de pacientes que recibían tratamiento hipolipemiante fue similar (tabla 1). Además, los pacientes recibieron tratamiento hipoglucemiante, antihipertensivo e hipolipemiante siguiendo las recomendaciones de la American Diabetes Association con el objetivo de conseguir valores de HbA1c<7%, lipoproteínas de baja densidad (LDL) <100mg/dl, lipoproteínas de alta densidad (HDL)>40mg/dl para varones y >50mg/dl para mujeres, triglicéridos <150 mg/dl, presión arterial sistólica ≤ 130 mmHg y presión arterial diastólica ≤ 80 mmHg.
Características descriptivas de la muestra en función de si completaron el seguimiento de 4 años (grupo 1) o no (grupo 2)
| Grupo 1 (n=54) | Grupo 2 (n=50) | p | |
| Edad (años) | 50,6±1,3 | 53,6±1,1 | 0,093 |
| Varones/mujeres | 20/34 | 13/37 | 0,227 |
| IMC | 45,1±0,9 | 48,4±1,1 | 0,029 |
| IMC categorizado (%) | 0,079 | ||
| <40 | 23,4 | 6,0 | |
| 40-45 | 27,7 | 30,0 | |
| 45-50 | 23,4 | 38,0 | |
| >50 | 25,5 | 26,0 | |
| Duración de DM (años) | 8,3±1,2 | 10,3±1,3 | 0,290 |
| Antecedentes de dislipemia (%) | 60,0 | 45,5 | 0,045 |
| Tratamiento de la dislipemia (%) | 79,5 | 64,5 | 0,162 |
| Tratamiento antidiabético antes de la cirugía (%) | 0,704 | ||
| Dieta y ejercicio | 15,1 | 15,9 | |
| ADO en monoterapia | 28,3 | 34,1 | |
| ADO en combinación | 28,3 | 31,8 | |
| Insulina | 28,3 | 18,2 |
ADO: antidiabético oral; DM: diabetes mellitus; IMC: índice de masa corporal.
Salvo otra indicación, los datos expresan media ± desviación estándar.
Definimos como remisión total de la DM el descenso de las concentraciones plasmáticas de glucosa en ayunas a menos de 100 mg/dl y de HbA1c por debajo del 6%. Asimismo, se consideró como remisión parcial cuando la glucemia basal en ayunas se situaba entre 100 y 125 mg/dl y la cifra de HbA1c, <6,5%.
Como variables de objetivo primario, se evaluaron: glucemia basal, HbA1c, peso e IMC (el peso en kilogramos/cuadrado de la talla en metros). Como variables secundarias, se consideraron: colesterol total, colesterol unido a LDL (cLDL) (calculado con la fórmula de Friedewald)18, colesterol unido a HDL (cHDL) y triglicéridos totales.
La muestra se dividió en función del IMC en cuatro grupos (35-40, 40-45, 45-50 y >50), el tiempo de evolución de la DM2 en dos (menos y más de 10 años de evolución) y según el tratamiento antidiabético previo a la cirugía, en cuatro categorías (dieta y ejercicio, antidiabético en monoterapia, antidiabético en combinación e insulinoterapia).
Los métodos utilizados para las diferentes determinaciones fueron los siguientes: glucemia basal, UV-hexocinasa; HbA1c, inmunoanálisis homogéneo; precipitación en ácido fosfotúngstico; iones magnesio de CHOD-PAP/colesterol total y cHDL, método enzimático colorimétrico de GPO-PAP. Todas las determinaciones bioquímicas se realizaron tras ayuno de 12 h, en un analizador Hitachi 747-734 (Boehringer Mannheim).
El análisis de datos se realizó con el paquete estadístico de libre distribución R2.1519 (www.r-project.org)19. Mediante un análisis longitudinal, se compararon las medias y las proporciones (en su caso) en cada visita con la visita anterior. La comparación de la evolución en la HbA1c en distintos grupos (IMC, evolución de la DM y tipo de tratamiento) se realizó mediante la distancia L2 entre las curvas resultantes. Todos los valores de p se calcularon por el método bootstrap general20. Este procedimiento permite el manejo de toda la información a pesar de datos faltantes21. Todos los valores de p<0,05 se consideraron estadísticamente significativos. Además se realizaron correlaciones de Spearman. Las variables numéricas se expresan como medias±error estándar. Las variables categóricas se expresan mediante frecuencias relativas.
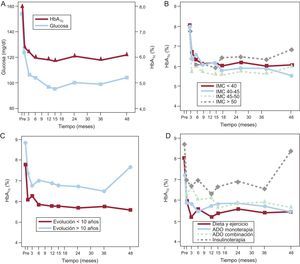
RESULTADOSControl glucémicoComo se observa en la figura 1A, los valores medios de la glucemia basal descienden desde más de 150 a unos 120 mg/dl en el primer mes postoperatorio (p<0,001) y hasta unos 105 mg/ml el tercer mes (p=0,011), y a partir de entonces se mantienen en valores totalmente normales durante el resto de los 4 años del estudio. Asimismo, las concentraciones de HBA1c disminuyen al cabo del primer mes (p<0,001), y se mantienen prácticamente estables durante el resto del tiempo de evaluación. Estas variaciones se correlacionan muy bien con la disminución acelerada de peso que ocurre durante el primer mes (r=0,473; p=0,007) para la glucemia basal, pero no en el caso de la HbA1c, pero no a partir de ese momento, ya que los valores hemáticos considerados están normalizados y, por lo tanto, no varían, mientras que el peso sigue disminuyendo. El análisis de la correlación entre la disminución de las concentraciones de HbA1c y las características patológicas previas de los pacientes reveló que no existía correspondencia con el IMC (fig. 1B). En cuanto al tiempo de evolución de la DM (más o menos de 10 años), los pacientes con más tiempo de evolución presentan mayor descenso el primer mes (p=0,029) y después ambos grupos presentan una evolución similar (fig. 1C). De igual modo, aunque en el primer mes observamos diferencias en cuanto al descenso de HbA1c en función del tratamiento antidiabético previo a la cirugía (p=0,012), la evolución posterior es similar en los cuatro grupos (fig. 1D). Sin embargo, a los 4 años de la cirugía, los pacientes con duración de la DM2>10 años y quienes previamente a la intervención precisaban tratamiento insulínico presentaron peor control metabólico, sin alcanzar significación estadística.
Evolución de la glucemia y la glucohemoglobina A durante los 4 años tras la cirugía (A) y correlación entre la evolución de la glucohemoglobina A y el índice de masa corporal (B), el tiempo de evolución de la diabetes mellitus tipo 2 (C) y el tratamiento hipoglucemiante previo a la intervención (D). ADO: antidiabético oral; HbA1c: glucohemoglobina A1c; IMC: índice de masa corporal.
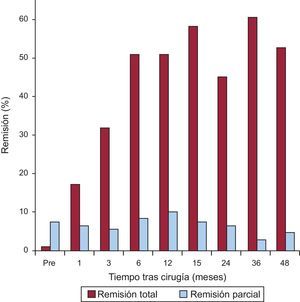
La tasa de remisión total de la DM2 aumentó significativamente desde el primer mes postoperatorio y llegó a un valor máximo de alrededor del 60% de los pacientes a los 3 años. Los pacientes con remisión parcial fueron aumentando paulatinamente hasta los 12 meses de la intervención, cuando alcanzaron el 10,3%; posteriormente los valores fueron descendiendo debido, al menos en parte, a la incorporación de muchos de ellos al grupo con remisión total (fig. 2).
En la figura 3 podemos observar que la necesidad del tratamiento hipoglucemiante se reduce de manera notable tras la intervención. Los pacientes que no precisaron medicación aumentaron progresivamente hasta que, a los 15 meses, más del 80% no necesitaba ningún tratamiento farmacológico asociado a su plan de alimentación y de ejercicio físico. A partir de ese momento se objetivó un aumento de la necesidad de administrar antidiabéticos orales solos o en combinación. El número de enfermos que pudieron prescindir del aporte de insulina externa aumentó progresivamente, y a los 4 años de la intervención no era necesario prescribirla a ninguno de nuestros pacientes.
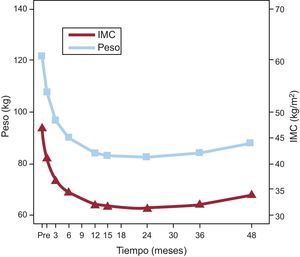
Control de pesoEste parámetro se redujo significativamente desde el primer mes hasta los 12 meses (p<0,001), hasta llegar a un mínimo a los 15-24 meses, momento tras el cual se ha mantenido estable y con descensos medios de 40 kg. El IMC disminuyó en paralelo y llegó a un valor medio compatible con obesidad de grado I a los 24 meses. En ese momento el 20,6% (n=22) de los pacientes tenían IMC<30 y el 7,5% (n=8), <25. A partir de entonces se observó una recuperación de peso moderada, 8 kg de media, lo que se tradujo en un aumento del IMC de 2,5 puntos (fig. 4).
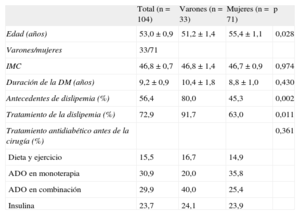
Control lipídicoEl 56,4% de los pacientes de nuestra cohorte tenían algún grado de dislipemia como complicación asociada a su cuadro, y el 72,6% de ellos recibían tratamiento hipolipemiante de algún tipo, porcentajes que eran mayores en los varones (tabla 2).
Características descriptivas de la muestra totales y en función del sexo
| Total (n=104) | Varones (n=33) | Mujeres (n=71) | p | |
| Edad (años) | 53,0±0,9 | 51,2±1,4 | 55,4±1,1 | 0,028 |
| Varones/mujeres | 33/71 | |||
| IMC | 46,8±0,7 | 46,8±1,4 | 46,7±0,9 | 0,974 |
| Duración de la DM (años) | 9,2±0,9 | 10,4±1,8 | 8,8±1,0 | 0,430 |
| Antecedentes de dislipemia (%) | 56,4 | 80,0 | 45,3 | 0,002 |
| Tratamiento de la dislipemia (%) | 72,9 | 91,7 | 63,0 | 0,011 |
| Tratamiento antidiabético antes de la cirugía (%) | 0,361 | |||
| Dieta y ejercicio | 15,5 | 16,7 | 14,9 | |
| ADO en monoterapia | 30,9 | 20,0 | 35,8 | |
| ADO en combinación | 29,9 | 40,0 | 25,4 | |
| Insulina | 23,7 | 24,1 | 23,9 |
ADO: antidiabético oral; DM: diabetes mellitus; IMC: índice de masa corporal.
Salvo otra indicación, los datos expresan media ± desviación estándar.
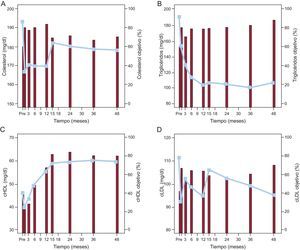
En la figura 5A se muestra la evolución de las concentraciones hemáticas de colesterol total tras el bypass gástrico. Observamos un rápido descenso desde el primer mes (p<0,001) que se mantiene estable durante el resto del primer año. Esto se tradujo en que más del 80% de los pacientes consiguieron el objetivo de normalización de las tasas de colesterol total para pacientes con DM. A los 15 meses, las concentraciones de colesterol total ascendieron ligeramente (p=0,009) y después se mantuvieron hasta los 4 años de la intervenición. A pesar de este incremento tardío, los pacientes que consiguieron el objetivo de colesterol total a los 4 años del bypass gástrico son alrededor del 70%.
Evolución de las concentraciones de colesterol total (A), triglicéridos (B), colesterol unido a lipoproteínas de alta densidad (C) y colesterol unido a lipoproteínas de baja densidad (D) durante los 4 años posteriores a la cirugía (líneas) y del porcentaje de pacientes (histogramas) que cumplían o superaban los valores objetivo para diabéticos respecto a cada uno de los parámetros analizados. cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad.
La concentración de triglicéridos en sangre sufrió un descenso acusado a lo largo del primer año (p=0,008) y después se estabilizó en torno a los 100 mg/dl (media a los 4 años, 106,5±8,7 mg/dl) es decir, muy por debajo de los 150mg/dl, que es el valor objetivo máximo para pacientes con DM. Correspondientemente, se observó un rápido incremento no significativo de la proporción de pacientes que lograron alcanzar el objetivo, que a los 6 meses de la intervención ya estaba en torno al 80% y llegó al 88,9% a los 4 años (fig. 5B).
Las concentraciones de cHDL en plasma descendieron durante el primer mes postoperatorio (p<0,001) y aumentaron progresivamente después hasta los 15 meses (p=0,004). Después se produjo una estabilización en torno a los 60 mg/dl. Esto se refleja en la proporción de pacientes que alcanzan el objetivo de HDL (> 40mg/dl los varones y>50mg/dl las mujeres) que pasa del 42,2% antes de la intervención a menos del 30% a los 3 meses, desde ese momento hasta los 15 meses aumenta paulatinamente (p=0,026) y se estabiliza en torno a un 80-85% (fig. 5C).
Las concentraciones medias de cLDL fluctuaron bastante, aunque siempre con concentraciones menores a las previas a la cirugía. El primer mes tras la cirugía se produjo un descenso significativo que se mantuvo hasta los 15 meses. En ese momento los valores aumentan (p=0,027) para mantenerse así hasta el final del segumiento. Como consecuencia, tras la operación los pacientes que consiguieron mantener sus valores por debajo del objetivo para diabéticos (< 100mg/dl) aumentaron del 30% a valores entre el 55 y el 60%, con un máximo a los 4 años del 68%, cambios en los porcentajes que no alcanzan significación estadística (fig. 5D).
Las variaciones de colesterol total, triglicéridos y cLDL no parecen correlacionarse con la reducción de peso que los pacientes sufrieron tras la cirugía. Sin embargo, sí que se observó una relación con las concentraciones de cHDL a partir de los 2 años (24 meses, r=−0,436; p=0,007; 36 meses, r=−0,522; p=0,004).
Como consecuencia de estos datos, el número de pacientes disminuyó de tal manera que recibían tratamiento hipolipemiante el 17,8, el 15,6, el 14,9, el 10,0, el 15,3, el 20,0, el 20,5 y el 19,0% (p<0,05) después de 1, 3, 6, 12, 15, 24, 36 y 48 meses respectivamente.
DISCUSIÓNLa introducción de la cirugía bariátrica aportó, además de los beneficios esperados a los pacientes, uno que aparentemente no tiene relación con ellos, como es la resolución de la DM2. Aunque los primeros datos se obtuvieron en los años setenta del pasado siglo, la confirmación del efecto es bastante más reciente. Mención especial merece el análisis retrospectivo publicado por Pories et al, en el que se presentaban datos de resolución de DM en pacientes intervenidos de cirugía bariátrica a lo largo de 10 años. En ese trabajo quedaba patente, además, que el efecto sobre la glucemia aparecía en los primeros días tras la cirugía, es decir, antes de que se iniciara la pérdida de peso22.
A pesar de ello, los estudios controlados y aleatorizados dirigidos a valorar el efecto de la cirugía bariátrica como tratamiento de la DM2 son escasos. En este trabajo, observamos que desde el primer mes tras la cirugía se producía un descenso marcado en la glucemia y en las concentraciones de HbA1c, lo que permitió reducir significativamente los tratamientos hipoglucemiantes de los pacientes intervenidos. Además, la mejora en el metabolismo glucídico no se correlacionaba con la pérdida de peso, salvo en el primer mes, aunque en ese periodo podrían intervenir otras variables relacionadas con el acto quirúrgico (ayunos, dieta por fase, pérdidas sanguíneas tras la cirugía). Por otro lado, la mejora de los valores hemáticos continúa durante parte del primer año tras la intervención y se mantiene durante el resto del periodo estudiado. No observamos relación entre la tasa de disminución de la HbA1c y el IMC previo a la cirugía y solo los grupos con una mayor duración de la DM2 o con tratamiento insulínico previo a la intervención mostraron cierto empeoramiento, aunque, al ser exclusivamente en el último punto muestreado, no queda clara su significación. Aun así, incluso en estos pacientes el manejo es más sencillo que antes de la cirugía, como se desprende del dato de que ninguno de ellos precisaba tratamiento insulínico a los 4 años de la intervención.
Estos resultados concuerdan con los de otros estudios observacionales como, por ejemplo, el de Dixon et al23 (2008), que encontraron que los pacientes a los que se implantaba una banda gástrica ajustable presentaban mejor control glucémico que los que seguían el tratamiento convencional (cambios en el estilo de vida y tratamiento hipoglucemiante). Igualmente, Mingrone et al24, al estudiar la evolución de pacientes que se habían sometido a bypass gástrico proximal, derivación biliopancreática o tratamiento convencional, encontraron que los tres grupos habían mejorado sus cifras de HbA1c al año de seguimiento, aunque los componentes de los dos grupos intervenidos quirúrgicamente presentaron descensos mayores, especialmente los de derivación biliopancreática. Correspondientemente, la tasa de remisión de la DM fue 0 en el grupo de tratamiento convencional, el 75% en el de bypass gástrico y el 95% en el colectivo de derivación biliopancreática. Además observaron, al igual que nosotros, que la edad, el sexo, el IMC previo, la duración de la DM y los cambios en el peso corporal no son factores predictores de resolución de la DM2. Por último, Schauer et al25 observaron que la tasa de resolución de DM2 de los pacientes sometidos a tratamiento convencional fue del 12%, frente al 42 y el 37% de los sometidos a bypass gástrico o gastrectomía tubular respectivamente. Tampoco pudieron relacionar la mejora del control glucémico con la pérdida de peso.
Los datos de control glucémico se acompañan de una corrección del perfil lipídico que logra que un porcentaje elevado de los pacientes alcancen o mejoren las cifras objetivo de triglicéridos, cLDL y cHDL. Nuestros datos concuerdan con los de estudios previos que han encontrado normalización de la dislipemia en hasta el 96,9% de los pacientes tras bypass gástrico14, que se acompaña de una disminución significativa del riesgo de sufrir un evento cardiovascular, al reducirse la dislipemia aterogénica asociada.
Los cambios observados tras la cirugía son consecuencia de una cascada de acontecimientos que se inician con un aumento de la sensibilidad a la insulina de hasta 4-5 veces, en parte debido al incremento de las concentraciones de adiponectina que acompaña a la disminución del tejido adiposo, especialmente en hígado y músculo. En el músculo aumentan el número de receptores de insulina y el metabolismo lipídico, lo que causa reducción de la concentración de lípidos intramiocitarios y aumento de la captación de glucosa. Paralelamente, se reduce el contenido de ácidos grasos en el hígado, con lo que disminuye la insulinorresistencia asociada a la esteatosis hepática. Todo ello se acompaña de un incremento de la secreción de insulina, y se ha postulado que la recuperación del tono incretínico podría ser fundamental26–31.
LimitacionesEl presente trabajo tiene varias limitaciones derivadas del diseño de estudio retrospectivo, como es el seguimiento irregular y los valores perdidos. Además, no se recogen datos sobre estancia hospitalaria, reintervención o morbilidad posquirúrgica, lo que incluye el fenómeno de dumping, por no considerarlos objetivos del presente trabajo, y ello podría afectar al resultado final. Por otro lado, la mayoría de los pacientes se intervinieron de bypass gástrico proximal laparoscópico, y solo había 11 con banda gástrica ajustable, por lo que, para conocer el efecto total de la cirugía, sería necesario incluir a pacientes intervenidos con otras técnicas quirúrgicas: gastrectomía tubular, derivación biliopancréatica, etc.
CONCLUSIONESPresentamos datos que demuestran que el bypass gástrico es una técnica efectiva para el tratamiento de pacientes obesos y con antecedentes de DM2. Se ha observado no solo una disminución significativa del peso, sino también un control glucémico que es mayor de lo esperado y se manifiesta antes que aquella. La intervención ayuda además a controlar las alteraciones lipídicas frecuentemente asociadas a la obesidad mórbida, lo que mejora el perfil cardiometabólico general del paciente y ayuda a conseguir objetivos de buen control.
CONFLICTO DE INTERESESNinguno.