Están demostradas la eficacia y la efectividad tanto de los antagonistas de la vitamina K (AVK) como de los anticoagulantes orales de acción directa (ACOD) en la profilaxis de accidentes cardioembólicos en la fibrilación auricular no valvular (FANV). Diversas publicaciones describen que los ACOD podrían ser coste-efectivos respecto a los AVK1. Sin embargo, existe poca información con datos de vida real sobre el impacto en el gasto sanitario, el cual debe considerar, además del gasto farmacoterapéutico, los gastos derivados de hospitalización y seguimiento.
En este estudio se hace un análisis de costes con datos poblacionales para calcular el coste sanitario directo, con horizonte temporal de 1 año en pacientes con FANV tratados con anticoagulación oral en Cataluña, comparando AVK y ACOD con análisis por intención de tratar. Se incluyó a todos los pacientes atendidos en atención primaria del Servei Català de la Salut con diagnóstico de FANV de más de 1 año en tratamiento con AVK (warfarina o acenocumarol) o ACOD (dabigatrán, rivaroxabán, apixabán o edoxabán) desde al menos 2 meses antes del inicio del análisis.
La base de datos poblacional proviene del Sistema de Información para el Desarrollo de la Investigación en Atención Primaria; el coste del fármaco, de las facturas reales de la base de datos de medicamentos dispensados en las oficinas de farmacia del Servei Català de la Salut; la fuente de datos hospitalarios, del conjunto mínimo básico de datos de las altas hospitalarias; el coste de visitas médicas, de enfermería y pruebas complementarias se obtuvo del Diari Oficial de la Generalitat de Catalunya y el coste de ingresos hospitalarios se estimó utilizando la fórmula que emplea el Servei Català de la Salut para el pago en la compra de servicios sanitarios2.
Mediante un modelo de emparejamiento por puntuación de propensión 1:1 sin reemplazo, se seleccionó al azar a 1.500 pacientes con ACOD y se les asignó una pareja de iguales características con AVK. Se realizó un análisis de sensibilidad actualizando los costes al año 2022 y capitalizando los costes al año 2024 con las tasas de descuento correspondientes.
En 2017 había en Cataluña 82.034 pacientes con FANV en tratamiento anticoagulante en atención primaria. De ellos, 64.732 (79%) estaban tratados con AVK y 17.302 (21%), con ACOD.
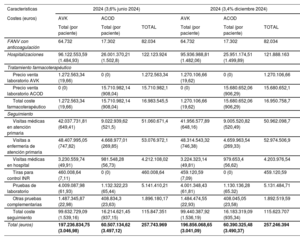
La tabla 1 muestra los resultados poblacionales y de la muestra emparejada al año 2017. El gasto sanitario de los pacientes con FANV en tratamiento anticoagulante (incluidos hospitalizaciones, tratamiento y seguimiento) fue de 207.067.314,34 euros en 1 año. Las hospitalizaciones supusieron la mayor parte del coste (98.112.374,77 euros), seguidas de los costes de seguimiento (93.069.877,87 euros) y farmacoterapéutico (15.885.061,70 euros). Hubo mayor proporción de pacientes que cambiaron de grupo de AVK a ACOD que de ACOD a AVK: 3.899 frente a 157 respectivamente. En estos, el coste por paciente se duplicó, y fue mayor en los que cambiaron de AVK a ACOD, con una diferencia de 74,02 euros.
Resultados de seguimiento, hospitalizaciones y costes en población y muestra emparejada de AVK y ACOD y de los que cambiaron de anticoagulante
| Población | Emparejamiento | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Características | AVK | ACOD | Total | Cambio(AVK-ACOD) | Cambio (ACOD-AVK) | AVK | ACOD | Total | ||
| FANV con anticoagulación | 64.732 | 17.302 | 82.034 | 3.899 | 157 | 1.500 | 1.500 | 3.000 | ||
| Seguimiento | Total(por paciente) | Total(por paciente) | TOTAL | Total(por paciente) | Total(por paciente) | n(por paciente) | n(por paciente) | Razón de tasas (95%CI) | pa | |
| Visitas médicas en atención primaria | 728.325 (11,25) | 156.327 (9,03) | 884.652 | 53.941 (13,83) | 1.975 (12,58) | 15.563 (10,38) | 13.403 (8,94) | 1,16(1,13-1,18) | <0,001 | 28.966 |
| Visitas a enfermería de atención primaria | 1.198.096 (18,50) | 115.557 (6,67) | 1.313.653 | 66.817 (17,13) | 2.352 (14,98) | 22.441 (14,96) | 9.624 (6,42) | 2,33(2,27-2,38) | <0,001 | 32.065 |
| Visitas médicas en Hospital | 18.553 (0,28) | 5.637 (0,32) | 24.19 | 1.949 (0,5) | 85 (0,54) | 373 (0,25) | 516 (0,34) | 0,72(0,63-0,83) | <0,001 | 889 |
| Tiras para control INR | 879.913 (13,59) | 0 (0) | 879.913 | 34.057 (8,73) | 1.735 (11,05) | 14.200 (9,47) | (0.00) | 0 | 0 | 14,2 |
| Hospitalizaciones | 32.435 (0,50) | 8.463 (0,48) | 40.898 | 3.528 (0,90) | 148 (0,94) | 1.087 (0,72) | 757 (0,50) | 1,44(1,31-1,58) | <0,001 | 1.844 |
| COSTES (euros, 2017) | Total(por paciente) | Total(por paciente) | TOTAL | Total(por paciente) | Total(por paciente) | Total(por paciente) | Total(por paciente) | Razón de tasas (95%CI) | Pb | Total |
| Coste hospitalizaciones | 77.223.296,7 (1.192,96) | 20.889.078,07 (1.207,32) | 98.112.375 | 8.863.303,88 (2.273,22) | 388.399,2 (2.473,88) | 2.532.475,44 (1.688,32) | 1.860.952,56 (1.240,64) | 0,33(0,32-0,33) | <0,001 | 4.393.428 |
| Total coste hospitalización | 77.223.296,7 (1.192,96) | 20.889.078,07 (1.207,32) | 98.112.375 | 8.863.303,88 (2.273,22) | 388.399,2 (2.473,88) | 2.532.475,44 (1.688,32) | 1.860.952,56 (1.240,64) | 0,33(0,32-0,33) | <0,001 | 4.393.428 |
| Precio venta laboratorio del anticoagulante oral | 1.190.254,84 (18,38) | 14.694.806,86 (849,31) | 15.885.062 | 1.927.435,21 (494.340,91) | 48.600,63 (309,56) | 18.786,73 (12,52) | 1.265.694,33 (843,80) | 0,01(0,01-0,02) | <0,001 | 1.284.481,06 |
| Total coste farmacoterapéutico | 1.190.254,84 (18,38) | 14.694.806,86 (849,31) | 15.885.062 | 1.927.435,21 (494.340,91) | 48.600,63 (309,56) | 18.786,73 (12,52) | 1.265.694,33 (843,80) | 0,01(0,01-0,02) | <0,001 | 1.284.481,06 |
| Visitas médicas en atención primaria | 33.772.430,25 (521,72) | 7.248.882,99 (418,96) | 41.021.313 | 2.501.244,17 (641,50) | 91.580,75 (583,31) | 721.656,31 (481,10) | 621.497.11 (414,33) | 1,16(1,15-1,16) | <0,001 | 1.343.153,42 |
| Visitas a enfermería de atención primaria | 38.890.196,16 (600,78) | 3.750.980,22 (216,79) | 42.641.176 | 2.168.879,82 (556,26) | 76.345,92 (486,28) | 728.434,86 (485,62) | 312.395.04 (208,26) | 2,33(2,32-2,34) | <0,001 | 1.040.829,9 |
| Visitas médicas en hospital | 2.595.379,17 (40,09) | 788.559,93 (45,57) | 3.383.939 | 272.645,61 (69,92) | 11.890,65 (75,73) | 52.178,97 (34,79) | 72.183.24 (48,12) | 0,72(0,71-0,73) | <0,001 | 124.362,21 |
| Tiras para control INR | 369.563,46 (5,70) | 369.563 | 14.303,94 (3,66) | 728.7 (4,64) | 5.964 (3,98) | 0 (0) | 0 (0) | 0 | 5.964 | |
| Pruebas de laboratorio | 3.220.836,1 (49,75) | 909.689,27 (52,57) | 4.130.525 | 274.043,67 (70,28) | 16.431,1 (104,65) | 70.093,72 (46,73) | 81.646,81 (54,43) | 0,86(0,85-0,87) | <0,001 | 151.740,53 |
| Otras pruebas complementarias | 1.194.909,49 (18,45) | 328.450,83 (18,98) | 1.523.360 | 102.818,5 (26,37) | 36.61,47 (23,32) | 21.882,82 (14,59) | 26.317,85 (17,55) | 0,83(0,82-0,85) | <0,001 | 48.200,67 |
| Total seguimiento | 80.043.314,63 (1.236,53) | 13.026.563,24 (752,89) | 93.069.878 | 5.333.935,71 (1.368,02) | 200.638,59 (1.277,95) | 1.600.210,68 (1.066,81) | 1.114.040,05 (742,69) | 1,43(1,43-1,44) | <0,001 | 2.714.250,73 |
| Total (euros) | 158.456.866,17 (2.447,89) | 48.610.448,17 (2.809,52) | 207.067.314 | 16.124.674,8 (4.135,59) | 637.638,42 (4.061,39) | 4.151.472,85 (2.767,65) | 4.240.686,94 (2.827,12) | 0,97(0,97-0,98) | <0,001 | 8.392.159,79 |
ACOD: anticoagulante oral de acción directa, AVK: antagonista de la vitamina K, INR: índice internacional normalizado.
En la muestra emparejada se observó mayor coste de AVK frente a ACOD en hospitalizaciones (1.688,32 frente a 1.240,64 euros; p<0,001) y en seguimiento (1.066,81 frente a 742,69 euros; p<0,001) y un menor coste farmacoterapéutico (12,52 frente a 843,80 euros; p<0,001). En total, el coste por paciente/año fue de 2.767,65 euros con AVK y 2.827,12 euros con ACOD (una diferencia de 59,47 euros por paciente/año; p<0,001).
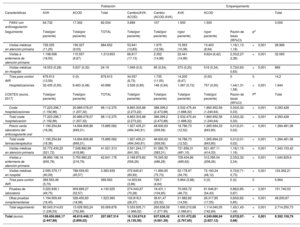
En la tabla 2 se muestran los resultados estimados para 2024. El coste sanitario directo oscilará entre 257.743.969 y 257.246.394 euros (3.041,09 y 3.046,98 euros para AVK y 3.490,37 y 3.497,12 euros para ACOD).
Análisis de sensibilidad
| Características | 2024 (3,6% junio 2024) | 2024 (3,4% diciembre 2024) | ||||
|---|---|---|---|---|---|---|
| Costes (euros) | AVK | ACOD | AVK | ACOD | ||
| Total (por paciente) | Total (por paciente) | TOTAL | Total (por paciente) | Total (por paciente) | TOTAL | |
| FANV con anticoagulación | 64.732 | 17.302 | 82.034 | 64.732 | 17.302 | 82.034 |
| Hospitalizaciones | 96.122.553,59 (1.484,93) | 26.001.370,21 (1.502,8) | 122.123.924 | 95.936.988,81 (1.482,06) | 25.951.174,51 (1.499,89) | 121.888.163 |
| Tratamiento farmacoterapéutico | ||||||
| Precio venta laboratorio AVK | 1.272.563,34 (19,66) | 0 (0) | 1.272.563,34 | 1.270.106,66 (19,62) | 0 (0) | 1.270.106,66 |
| Precio venta laboratorio ACOD | 0 (0) | 15.710.982,14 (908,04) | 15.710.982,1 | 0 (0) | 15.680.652,06 (906,29) | 15.680.652,1 |
| Total coste farmacoterapéutico | 1.272.563,34 (19,66) | 15.710.982,14 (908,04) | 16.983.545,5 | 1.270.106,66 (19,62) | 15.680.652,06 (906,29) | 16.950.758,7 |
| Seguimiento | ||||||
| Visitas médicas en atención primaria | 42.037.731,81 (649,41) | 9.022.939,62 (521,5) | 51.060.671,4 | 41.956.577,89 (648,16) | 9.005.520,82 (520,49) | 50.962.098,7 |
| Visitas a enfermería de atención primaria | 48.407.995,05 (747,82) | 4.668.977,01 (269,85) | 53.076.972,1 | 48.314.543,32 (746,38) | 4.659.963,54 (269,33) | 52.974.506,9 |
| Visitas médicas en hospital | 3.230.559,74 (49,91) | 981.548,28 (56,73) | 4.212.108,02 | 3.224.323,14 (49,81) | 979.653,4 (56,62) | 4.203.976,54 |
| Tiras para control INR | 460.008,64 (7,11) | 0 (0) | 460.008,64 | 459.120,59 (7,09) | 0 (0) | 459.120,59 |
| Pruebas de laboratorio | 4.009.087,98 (61,93) | 1.132.322,23 (65,44) | 5.141.410,21 | 4.001.348,43 (61,81) | 1.130.136,28 (65.32) | 5.131.484,71 |
| Otras pruebas complementarias | 1.487.345,87 (22,98) | 408.834,3 (23,63) | 1.896.180,17 | 1.484.474,55 (22,93) | 408.045,05 (23,58) | 1.892.519,59 |
| Total coste seguimiento | 99.632.729,09 (1.539,16) | 16.214.621,45 (937,15) | 115.847.351 | 99.440.387,92 (1.536,19) | 16.183.319,09 (935,34) | 115.623.707 |
| Total (euros) | 197.236.834,75 (3.046,98) | 60.507.134,62 (3.497,12) | 257.743.969 | 196.856.068,65 (3.041,09) | 60.390.325,48 (3.490,37) | 257.246.394 |
ACOD: anticoagulante oral de acción directa; AVK: antagonista de la vitamina K; FANV: fibrilación auricular no valvular; INR: índice internacional normalizado.
Según nuestros resultados, los costes sanitarios directos del uso de AVK y ACOD en profilaxis cardioembólica de la FANV son similares. A pesar de que los ACOD se utilizan en pacientes con mayor riesgo cardiovascular basal, tienen menor coste en seguimiento y hospitalizaciones, pero mayor coste farmacéutico. Los pacientes con mayor coste fueron los que cambiaron de anticoagulante, que fue superior para los que cambiaron de AVK a ACOD a expensas de los costes por hospitalización. Una de las limitaciones de la comparación de estudios de costes realizados en diferentes países es la diversidad de costes asignados a los distintos elementos analizados, como los costes del fármaco y de las hospitalizaciones3,4. Nuestro estudio tendría relevancia en las recomendaciones sobre anticoagulantes en España, considerando que son datos de la vida real y no simulación de costes; además, el inicio de la comercialización de genéricos se acompañará de una reducción del precio de estos medicamentos, lo que podría generar una diferencia significativa de costes a favor de los ACOD e implicaciones de política sanitaria.
Como limitaciones, nuestros datos no permiten discernir el motivo del ingreso, y se ha calculado el coste hospitalario como ingresos por cualquier causa. Tampoco se analizó el efecto de la mala dosificación de los ACOD ni del mal control de los AVK. Por último, no se ha podido evaluar los costes sanitarios indirectos, como pérdida de productividad o costes no sanitarios relacionados con el cuidado de pacientes con secuelas tras un ictus, que podrían repercutir en unos menores costes globales para los ACOD.
Como conclusión, existe escasa diferencia de costes sanitarios directos entre AVK y ACOD. Los AVK se relacionan con mayor coste de seguimiento y hospitalización, mientras que los ACOD implican mayor coste farmacoterapéutico. Dado que la diferencia radica en menores costes de seguimiento y hospitalización con ACOD, su consideración debería beneficiar a los ACOD.
FINANCIACIÓNLa base de datos se obtuvo a través de una beca SIDIAP (Convocatoria Competitiva 2017, expediente SIDIAP 17/02; fecha de resolución, 27-4-2018). El proyecto se desarrolló en el marco de Doctorados Industriales 2018 a través de la Agència de Gestió d’Ajuts Universitaris i de Recerca de la Generalitat de Catalunya, con el número de expediente 2018-DI-044 y recibió una beca económica Fundació Dr. Ferran (convocatoria 2018), otorgada el 17-5-2018. Las mencionadas instituciones no han tenido participación en ninguna de las fases del estudio.
CONSIDERACIONES ÉTICASEl estudio se realizó de acuerdo con las normas éticas establecidas en la Declaración de Helsinki y fue aprobado por el Comité Ético de Investigación Clínica de la Fundació Institut Universitari per a la Recerca a l’Atenció Primària de Salut Jordi Gol i Gurina el 30 de mayo de 2018 (código P18/080). En lo que respecta a los datos contenidos en las bases de datos del Sistema de Información para el Desarrollo de la Investigación en Atención Primaria (SIDIAP), están anonimizados y se ajustan a la legislación española sobre confidencialidad y protección de datos (Ley Orgánica 15/1999, de 13 de diciembre, de Protección de Datos de Carácter Personal), por lo que no fue necesario solicitar el consentimiento informado a los participantes.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALDurante la preparación de este trabajo los autores no utilizaron inteligencia artificial.
CONTRIBUCIÓN DE LOS AUTORESConcepción y diseño del estudio: Z. Hernández Rojas, M.R. Dalmau Llorca, C. Aguilar Martín, E. Castro Blanco, M. García-Goñi M, J.M. Alegret. Adquisición de financiación: Z. Hernández Rojas, M.R. Dalmau Llorca, C. Aguilar Martín C. Metodología: Z. Hernández Rojas, M.R. Dalmau Llorca, C. Aguilar Martín, J.M. Alegret. Adquisición y análisis de datos: Z. Hernández Rojas, M.R. Dalmau Llorca, E. Castro Blanco. Interpretación de datos: Z. Hernández Rojas, M.R. Dalmau Llorca, E. Castro Blanco, J.M. Alegret. Análisis estadístico: Z. Hernández Rojas, M.R. Dalmau Llorca, E. Castro Blanco. Análisis económico: Z. Hernández Rojas, M.R. Dalmau Llorca, M. García-Goñi, J.M. Alegret. Redacción del manuscrito: Z. Hernández Rojas, M.R. Dalmau Llorca, J.M. Alegret. Revisión y edición: Z. Hernández Rojas, M.R. Dalmau Llorca, C. Aguilar Martín, E. Castro Blanco, M. García-Goñi, J.M. Alegret. Revisión de la versión final: Z. Hernández Rojas, M.R. Dalmau Llorca, C. Aguilar Martín, E. Castro Blanco, M. García-Goñi, J.M. Alegret. Autores sénior: M.R. Dalmau Llorca, C. Aguilar Martín.
CONFLICTO DE INTERESESZ. Hernández Rojas, M.R. Dalmau Llorca y C. Aguilar Martín declaran haber participado en un estudio que recibió patrocinio parcial de Bayer. Z. Hernández Rojas declara haber recibido ayuda para formación de Boehringer y Salvat. M.R. Dalmau Llorca declara haber recibido ayuda para asistencia a congresos de Bayer. E. Castro Blanco, M. García-Goñi y J.M. Alegret declaran no tener conflictos de intereses.
AGRADECIMIENTOSLos autores agradecen la contribución de: Gerencia Territorial Terres de l’Ebre y de Atención Primaria del Institut Catalá de la Salut, Sistema d’Informació per al desenvolupament de la Investigació en Atenció Primària, Fundació Institut Universitari per a la recerca a l’Atenció Primària de Salut Jordi Gol i Gurina, Fundació Dr. Ferran y Doctorats Industrials.