Palabras clave
Distintos estudios han demostrado la asociación entre el foramen oval permeable (FOP) e ictus criptogénico. En la actualidad el tratamiento de estos pacientes es controvertido, aunque hay datos a favor del cierre percutáneo1 del FOP. El objetivo de este trabajo es estudiar los resultados inmediatos y de seguimiento a largo plazo de una serie consecutiva de pacientes con ictus criptogénico y FOP cerrado percutáneamente.
Desde enero de 2000 hasta febrero de 2006, 52 pacientes menores de 60 años diagnosticados de FOP e ictus han sido tratados con cierre percutáneo en nuestro hospital. Todos tenían diagnóstico de ictus agudo o ataque isquémico transitorio (AIT), y se realizó un estudio completo, como se recoge en la tabla 1. Se descartó cardiopatía embolígena mediante ecografía. La permeabilidad del foramen se analizó con una inyección de gelafundina al 4% sonicada desde una vía venosa periférica, en condiciones basales y tras Valsalva.
Se indicó el cierre percutáneo del foramen en los pacientes con ictus criptogénico, FOP y algunos de los siguientes criterios ecocardiográficos considerados de riesgo de nuevo evento neurológico descritos en la literatura2,3: recidiva clínica neurológica, paso amplio de contraste en reposo (más de 20 microburbujas), aneurisma de septo interauricular (ASA) definido una suma de la excursión total dentro de la aurícula izquierda y/o la derecha ³ 11 mm4, y amplia movilidad de la membrana del septum primum (> 6 mm).
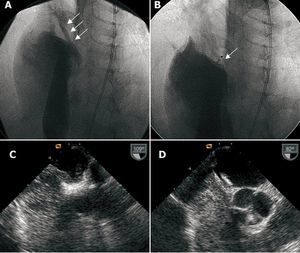
El implante se llevó a cabo con control angiográfico y anestesia general, por la dificultad para que los enfermos permanezcan en monitorización con ecocardiografía transesofágica durante el procedimiento. Antes del implante se efectuaron angiografías en arteria pulmonar y en cava inferior para valorar los pasos espontáneos izquierda-derecha y derecha-izquierda (fig. 1). Después se realizaron inyecciones de contraste ecográfico para valorar el paso de burbujas derecha-izquierda por ETE, en condiciones basales y tras maniobras respiratorias de espiración forzada, que se repitieron tras el implante (fig. 1).
Fig. 1. A: angiografía basal con inyección de contraste en aurícula derecha que muestra el paso derecha-izquierda. B: angiografía del dispositivo implantado, sellando el foramen oval, con inyección de contraste en aurícula derecha. C: ecografía transesofágica del paso de contraste derecha-izquierda. D: ecografía transesofágica del dispositivo implantado, sin paso derecha-izquierda.
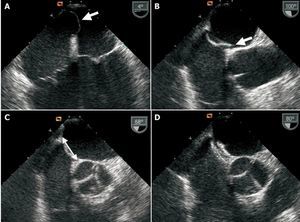
De entre las medidas existentes para cada modelo, se eligió el dispositivo cuyo diámetro mayor fuera menor que la longitud total del septo interauricular en proyección retroaórtica por ETE (fig. 2). En los casos con aneurisma del septo, se eligió un dispositivo algo mayor que la medida de la base del aneurisma. Se dejó a criterio del operador el uso de dispositivos Amplatzer (AGA Medical, Minnesota, Estados Unidos), Intra-sept (Cardia Inc., Minnesota) o Helex (W.L. Gore, Arizona, Estados Unidos), salvo en los casos con aneurisma del septo, en los que se utilizó siempre Amplatzer. Las medidas disponibles en cada dispositivo fueron 18, 25 y 35 mm en el dispositivo Amplatzer y 20, 25 y 30 mm en el dispositivo Helex.
Fig. 2. Ecografía transesofágica. A: aneurisma del septo interauricular. B: foramen oval permeable anatómico (flecha). C: medición del septo para selección del tamaño del dispositivo (flecha). D: imagen del dispositivo implantado.
Todos los pacientes recibieron tratamiento antibiótico profiláctico tras el implante, así como tratamiento antitrombótico con dalteparina (10.000 UI/día durante 1 mes) y aspirina (150 mg/día indefinidamente)5,6.
Se realizaron estudio con ecografía transtorácica (ETT) con segundo armónico y contraste antes del alta y seguimiento clínico y ecográfico con contraste a los 6 meses y al año, y después, seguimiento clínico anual.
En las variables cuantitativas, se presentan la media y la desviación estándar. En las variables cualitativas se presenta el porcentaje respecto del total. Los datos han sido analizados con el programa SPSS 8.0.
Se ha realizado el cierre percutáneo de FOP en un total de 52 pacientes menores de 60 años. En la tabla 2 se recogen las características clínicas y ecográficas. En todos los casos se pudo implantar el dispositivo, que fue Amplatzer en 40 (76%) pacientes, Helex en 11 (22%) e Intrasept en 1. En 4 pacientes se utilizó un dispositivo Amplatzer para cierre de comunicación interauricular cribiforme, por presentar una membrana multiperforada. El tamaño del dispositivo fue de 35 mm en el 25% de los pacientes, 30 mm en el 12%, 25 mm en el 54% y £ 20 mm en el 10%.
Todos los pacientes con ASA presentaron un tamaño de la base > 25 mm, por ello se utilizó un dispositivo Amplatzer de 35 mm. Al final del procedimiento hubo paso residual de burbujas, en 12 casos (24%) en situación basal y en 25 (48%) tras espiración forzada, que se consideró leve en 11 pacientes.
No hubo complicaciones mayores ni embolización del dispositivo. En el ETT con contraste al alta, se evidenció cortocircuito residual en 2 (4%) pacientes.
Se ha realizado seguimiento de 49 pacientes una mediana de 26 (intervalo, 2-72; percentiles 25-75, 8-39) meses. El seguimiento no fue posible en 3 pacientes.
No hubo eventos clínicos neurológicos ni de otro tipo atribuibles al procedimiento ni al dispositivo (endocarditis, embolización, fractura). En el estudio con ETT tardío, ya a los 6 meses no se evidenció cortocircuito residual en ningún caso.
Desde el metaanálisis de Overell et al7, la asociación entre FOP e ictus criptogénico es clara, y el método más adecuado para su diagnóstico es el ETE con contraste8. En varios estudios3 se han descrito, en el grupo de pacientes con FOP, unos factores de riesgo de ictus como los utilizados por nosotros para indicar el cierre9.
A falta de estudios aleatorizados que comparen el tratamiento médico con el cierre percutáneo, la alta tasa de recidiva con tratamiento médico, hasta del 13%10, y la existencia de estudios que respaldan firmemente el tratamiento con cierre percutáneo11 hacen que ésta sea una opción ampliamente utilizada. En España, en 2005 se han realizado 182 cierres percutáneos de FOP12.
La incidencia de recidiva tras el cierre descrita es variable y oscila entre el 0,6 y el 7,8%11. En nuestro estudio no ha habido recidivas. Ello pudiera obedecer al régimen antitrombótico utilizado, no descrito en otros estudios, que podría favorecer un adecuado y rápido cubrimiento del dispositivo sin agregación trombótica. A pesar de la existencia de cortocircuito residual tras el alta en un 4%, en el seguimiento ecocardiográfico a los 6 meses no había ningún paciente con cortocircuito, lo que concuerda con lo descrito en otros estudios13. Por otro lado, las complicaciones mayores descritas con el cierre percutáneo, que alcanzan una tasa del 1,5% en las series descritas1, no se presentaron en nuestro estudio.
Si bien el procedimiento se ha realizado con control con ETE, es posible evitar la anestesia utilizando la ecografía intracavitaria.
Según nuestra experiencia, en pacientes jóvenes con ictus criptogénico y FOP, el cierre percutáneo es una opción segura, sin recidivas o eventos a largo plazo.
La ausencia de un grupo control de pacientes con ictus criptogénico y FOP tratados médicamente nos impide comparar ambas opciones terapéuticas, pero la tasa de recidiva de eventos neurológicos en pacientes con tratamiento médico nos impulsó decididamente al cierre percutáneo. La evolución tardía de éstos parece avalar esta decisión. La finalización de estudios aleatorizados en curso, así como una prolongación en el tiempo de seguimiento, puede llegar a ratificar estos hallazgos de forma más definitiva.
Full English text available from: www.revespcardiolo.org
Correspondencia: Dr. F. Mazuelos Bellido.
Servicio de Cardiología. Hospital Reina Sofía.
Avda. Menéndez Pidal, s/n. 14004 Córdoba. España. Correo electrónico: franciscomazuelos@gmail.com
Recibido el 12 de septiembre de 2007.
Aceptado para su publicación el 7 de noviembre de 2007.