La hipertensión es un importante factor de riesgo de infarto de miocardio, insuficiencia cardiaca e ictus. El control de la presión arterial (PA) de los pacientes hipertensos es de capital importancia, pero demasiado pocos pacientes lo alcanzan, a pesar de la disponibilidad de múltiples estrategias terapéuticas seguras y efectivas1. En consecuencia, la introducción de nuevas estrategias para mejorar y optimizar el control de la PA de los pacientes hipertensos es una necesidad no satisfecha.
La identificación de nuevos biomarcadores con un valor predictivo probado en la estimación del riesgo cardiovascular (RCV), como son las variantes genéticas recientemente identificadas mediante estudios de asociación de genoma completo, permite una mejor estratificación de la estimación del RCV cuando se formula mediante una puntuación de riesgo genético multilocus (GRS)2 incluso en relación con la ateroesclerosis subclínica3. La aplicación de una GRS, basada en variantes genéticas asociadas a la cardiopatía coronaria y en factores de riesgo clásicos independientes, a pacientes incluidos en 2 estudios de cohorte, el estudio REGICOR y el Framingham Heart Study, mejoró la clasificación del riesgo, en especial el de los pacientes con un riesgo coronario intermedio4.
Teniendo en cuenta que la mayoría de los eventos coronarios se producen en individuos clasificados como de riesgo bajo o intermedio según las puntuaciones de RCV tradicionales, se plantea la hipótesis de que la incorporación de la GRS a la evaluación clínica podría ser útil para mejorar la percepción del RCV real de cada paciente, y que este conocimiento podría aportar un mayor estímulo para que el paciente alcance una buena adherencia al tratamiento antihipertensivo y a los cambios de estilo de vida, con la consiguiente mejora en el control de la PA. El objetivo de este estudio piloto es evaluar la hipótesis de que el conocimiento de la GRS de pacientes hipertensos no controlados podría mejorar el control de la PA, evaluada mediante monitorización ambulatoria de la presión arterial (MAPA) de 24 h.
Se llevó a cabo un estudio de cohortes de 16 semanas, prospectivo, aleatorizado y ciego simple, en 2 grupos paralelos. Se incluyó a 80 pacientes consecutivos con PA ambulatoria no controlada (MAPA de 24 h ≥ 130/80mmHg), a los que se aleatorizó en proporción 1:1 a 1 de los 2 grupos siguientes: a) el grupo de GRS, en el que se realizó una prueba genética adicional (Cardio inCode Score, Ferrer inCode; Barcelona, España) para determinar la presencia de variantes genéticas con objeto de mejorar la estimación del RCV (grupo de GRS), y b) el grupo de control, para el que se utilizó la asistencia habitual. Se calculó el RCV basal según la puntuación del REGICOR5. Se llevó a cabo una MAPA de 24 h en situación basal y al cabo de 16 semanas. Se utilizó un diseño ciego para los investigadores en cuanto al riesgo genético al hacer las exploraciones y los ajustes del tratamiento.
De los 80 pacientes aleatorizados, se incluyó en el análisis final a 31 del grupo de GRS y 36 controles. Las características basales de los 67 pacientes que completaron el estudio estaban bien igualadas en los 2 grupos (tabla 1). La media edad fue 54,5±9,3 años, el 74,3% eran varones y las proporciones de pacientes con diabetes mellitus y con dislipemia fueron similares. Más del 80% de los pacientes habían estado tomando medicación antihipertensiva en los 3 meses previos a la inclusión en el estudio, sin que hubiera diferencias significativas entre el grupo de intervención y el de control (el 83,6 frente al 78,6%).
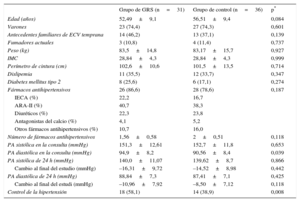
Características basales de los participantes que completaron el estudio
| Grupo de GRS (n=31) | Grupo de control (n=36) | p* | |
|---|---|---|---|
| Edad (años) | 52,49±9,1 | 56,51±9,4 | 0,084 |
| Varones | 23 (74,4) | 27 (74,3) | 0,601 |
| Antecedentes familiares de ECV temprana | 14 (46,2) | 13 (37,1) | 0,139 |
| Fumadores actuales | 3 (10,8) | 4 (11,4) | 0,737 |
| Peso (kg) | 83,5±14,8 | 83,17±15,7 | 0,927 |
| IMC | 28,84±4,3 | 28,84±4,3 | 0,999 |
| Perímetro de cintura (cm) | 102,6±10,6 | 101,5±13,5 | 0,714 |
| Dislipemia | 11 (35,5) | 12 (33,7) | 0,347 |
| Diabetes mellitus tipo 2 | 8 (25,6) | 6 (17,1) | 0,274 |
| Fármacos antihipertensivos | 26 (86,6) | 28 (78,6) | 0,187 |
| IECA (%) | 22,2 | 16,7 | |
| ARA-II (%) | 40,7 | 38,3 | |
| Diuréticos (%) | 22,3 | 23,8 | |
| Antagonistas del calcio (%) | 4,1 | 5,2 | |
| Otros fármacos antihipertensivos (%) | 10,7 | 16,0 | |
| Número de fármacos antihipertensivos | 1,56±0,58 | 2±0,51 | 0,118 |
| PA sistólica en la consulta (mmHg) | 151,3±12,61 | 152,7±11,8 | 0,653 |
| PA diastólica en la consulta (mmHg) | 94,9±8,2 | 90,56±8,4 | 0,039 |
| PA sistólica de 24 h (mmHg) | 140,0±11,07 | 139,62±8,7 | 0,866 |
| Cambio al final del estudio (mmHg) | –16,31±9,72 | –14,52±8,98 | 0,442 |
| PA diastólica de 24 h (mmHg) | 88,84±7,3 | 87,41±7,1 | 0,425 |
| Cambio al final del estudi (mmHg) | –10,96±7,92 | –8,50±7,12 | 0,118 |
| Control de la hipertensión | 18 (58,1) | 14 (38,9) | 0,008 |
ARA-II: antagonistas del receptor de la angiotensina II; ECV: enfermedad cardiovascular; GRS: puntuación de riesgo genético; IECA: inhibidores de la enzima de conversión de la angiotensina; PA: presión arterial.
Salvo otra indicación, los datos expresan n (%) o media±desviación estándar.
No se observaron diferencias significativas en la distribución basal según el RCV individual, en función del riesgo de enfermedad coronaria previsto a 10 años. Menos del 10% de los pacientes tenían un RCV intermedio-alto o alto según la escala del REGICOR, un 27% tenía un riesgo intermedio-bajo y un 65%, bajo. En la tabla 2 se muestra la reclasificación del RCV basada en el riesgo de enfermedad cardiovascular predicho a 10 años, con y sin la adición de la GRS. Se reclasificó a un grupo de riesgo superior a 11 (35%) pacientes y a un grupo de riesgo inferior por lo que respecta a la escala REGICOR basal, a 1 paciente.
Reclasificación según el riesgo de enfermedad coronaria predicho a 10 años, con o sin la puntuación de riesgo genético
Los valores basales de MAPA de 24 h eran similares en los dos grupos, sin diferencias en los periodos diurno y nocturno. Los cambios ajustados respecto a la situación basal fueron de –16,31 (intervalo de confianza del 95% [IC95%], –6,61 a –26,01) mmHg por lo que respecta a la media de PAS de 24 h en el grupo de GRS y de –14,52 (IC95%, –5,62 a –23,42) mmHg en el grupo de control (p=0,442), sin diferencias de ajustes terapéuticos entre los grupos (). Las tasas de control de la hipertensión definidas por los valores de corte de la MAPA mejoraron en mayor medida en los pacientes del grupo de GRS que en los controles (el 58,1 frente al 38,9%; p=0,008).
Al analizar el control de la MAPA teniendo en cuenta la puntuación del RCV según la información de la GRS, se alcanzó el control de la PA según los criterios de MAPA en todos los pacientes a los que se asignó un RCV alto y el 75% de los pacientes a los que se asignó un RCV intermedio-alto, mientras que solamente se alcanzó en un 66% de los pacientes de riesgo intermedio-alto asignados al grupo control. Tan solo un 40% de los pacientes con RCV intermedio-bajo y un 42% de los pacientes con RCV bajo alcanzaron unos valores de MAPA normales al final del estudio, sin diferencias significativas entre los 2 grupos. No se observaron diferencias en el tratamiento antihipertensivo entre el grupo de GRS y el de control al final del estudio (número de fármacos antihipertensivos; 2,0; IC95%, 1,52-2,48 frente a 2,33; IC95%, 1,8-2,86; p=0,142).
Los resultados de este estudio piloto indican que el conocimiento de los pacientes sobre la repercusión de la genética en su RCV mejora las tasas de control de la hipertensión definida con los valores de corte estándares de la MAPA (MAPA de 24 h<130/80mmHg), en especial los pacientes con RCV alto o muy alto. Es imposible determinar si la mayor reducción de la PA observada y el mayor porcentaje de control de la PA en el grupo de GRS fueron consecuencia de conocer el riesgo genético en sí o simplemente de la mayor concienciación respecto al RCV general de los pacientes. Lo importante es que un mejor conocimiento del riesgo condujo a una mejora del control de la PA, probablemente secundaria a un aumento de la adherencia al tratamiento antihipertensivo. Serán necesarios estudios más amplios para confirmar estos resultados y respaldar la importancia de mejorar el conocimiento del RCV personal para obtener un mejor control de la PA y una reducción de la morbilidad y la mortalidad de los pacientes con hipertensión.
CONFLICTO DE INTERESESEste trabajo fue financiado por Ferrer. E. Salas fue miembro de Gendiag.exe, S.L. propietario de una licencia de Cardio In Core Score. R. Elosua y J. Marrugat han recibido pagos de Ferrer inCode.