Palabras clave
CASO CLÍNICO
Varón de 68 años, hipertenso, fumador y diabético que, tras reposo en cama por un cuadro gripal, consultó en urgencias por angina, disnea y palpitaciones por pequeños esfuerzos. Su presión arterial era 105/85 mmHg y la frecuencia cardíaca, 110 lat/min; presentaba taquipnea sin estertores, y un leve soplo tricuspídeo regurgitante. El electrocardiograma mostró un bloqueo de la rama izquierda. La radiografía de tórax fue normal. Las analíticas evidenciaron hipoxemia (pO2 50 mmHg), hipocapnia (pCO2 31 mmHg), hiposaturación (90%), y elevación del dímero-D (3,1 ng/ml) y la troponina T (0,4 ng/ml). Una tomografía computarizada con contraste confirmó el diagnóstico de embolia pulmonar (EP), mediante la demostración de trombos en la bifurcación del tronco pulmonar y en sus ramas principales (fig. 1). En el ecocardiograma se apreciaba un ventrículo derecho (VD) dilatado con discinesia del segmento medio de la pared libre (fig. 2), y una presión arterial pulmonar de 55 mmHg. La fuente embólica fue una trombosis venosa femoral derecha (se detectaron restos de coágulos en el eco-Doppler).
Fig. 1. Tomografía computarizada helicoidal torácica con contraste (angio-TC). Plano axial del tronco y las arterias pulmonares. Se aprecian trombos tanto en la bifurcación del tronco pulmonar (flecha negra curva) como en sus ramas principales (flecha negra recta).
Fig. 2. Ecocardiograma transtorácico. Plano apical de 4 cámaras. Se aprecia abombamiento sistólico paradójico (discinesia) de la pared libre del ventrículo derecho (flechas negras). AD: aurícula derecha; AI: aurícula izquierda; VD: ventrículo derecho; VI: ventrículo izquierdo.
Se aplicó trombólisis periférica con activador tisular del plasminógeno. Un ecocardiograma a las 72 h demostró mejoría de las anomalías segmentarias del VD, así como de la presión pulmonar (35 mmHg). Tras una evolución satisfactoria, se procedió al alta y se indicó tratamiento con acenocumarol y bisoprolol.
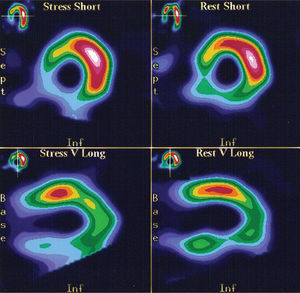
Un mes después, el paciente refería angina de grandes esfuerzos. El control ecocardiográfico resultó normal. Una gammagrafía miocárdica (con dipiridamol) evidenció un extenso defecto de perfusión inferoposterior (fig. 3). Tras 6 meses de anticoagulación, se realizó una coronariografía, donde se apreció una oclusión segmentaria proximal de la coronaria derecha, con abundante circulación colateral. Fue tratado con aspirina, estatinas y bloqueadores beta, y al año de seguimiento no presentó complicaciones.
Fig. 3. Gammagrafía de perfusión miocárdica con talio-201 y estrés farmacológico con dipiridamol. Planos axiales del eje corto y sagitales del eje largo. Se aprecia un extenso defecto de perfusión compatible con isquemia severa inferoposterior.
DISCUSIÓN
LA EP aguda masiva (20%) cursa con hipoxemia grave e inestabilidad hemodinámica, y la mortalidad es elevada sin tratamiento (hasta el 30%). Su evolución inicial parece ser mejor con trombólisis que sólo con heparina, por lo que, en general, se recomienda su uso en estos casos1-4.
Sin embargo, la mayoría de los pacientes con EP se encuentra estable en el momento del diagnóstico, lo que no siempre implica una evolución benigna. Actualmente, sabemos que el pronóstico es diferente según haya o no afección del VD, valorada mediante ecocardiografía. Así, los enfermos normotensos que no presentan alteraciones ecográficas (60%) presentan un riesgo de complicaciones serias prácticamente nulo. En cambio, los inicialmente estables que presentan disfunción VD, tienen mayor riesgo de deterioro clínico y recurrencia de la embolia, y una mortalidad del 5%. En ausencia de ensayos clínicos amplios, algunos autores sugieren que en estos casos de disfunción del VD subclínica, la trombólisis también puede ser beneficiosa (mejoría de función del VD, posible disminución de la morbimortalidad), por lo que tal vez deba considerarse su uso individualizado, en ausencia de riesgo hemorrágico aumentado o de enfermedades cardiorrespiratorias con hipertensión pulmonar previa1-5.
El ecocardiograma, además de ser útil en el diagnóstico diferencial, puede aportar datos importantes directamente relacionados con la EP2-6. Además de los hallazgos clásicos (dilatación e hipocinesia del VD con abombamiento septal a la izquierda, dilatación de las arterias pulmonares, dilatación de la cava inferior sin colapso, velocidad de regurgitación tricuspídea > 3 m/s, eyección del VD con tiempo de aceleración < 90 ms), se ha descrito un patrón de disfunción regional del VD en la EP aguda, que se considera más específico para su diagnóstico, y consiste en hipocinesia o acinesia de los segmentos medios de la pared libre (plano apical de 4 cámaras), quedando preservada la movilidad apical7-9. Los mecanismos propuestos para explicar estas anomalías incluyen el arrastre que ejerce el ventrículo izquierdo hiperdinámico sobre el ápex derecho, la morfología esferoidal adoptada por el VD para igualar la tensión de la pared ante un incremento agudo en la poscarga, y la isquemia provocada por el aumento súbito del estrés parietal.
En el cor pulmonale agudo tromboembólico, la asociación de un descenso de la perfusión coronaria (por caída del gasto cardíaco y la presión aórtica) con un aumento de la poscarga del VD provoca isquemia miocárdica, que puede agravar la disfunción del VD y perpetuar la inestabilidad hemodinámica. Se han descrito claros estigmas de isquemia miocárdica en la EP: elevación de las troponinas cardíacas, defectos de perfusión del VD en gammagrafías con 201Tl, e incluso infartos aislados del VD en necropsias de enfermos con embolias masivas, sin lesiones coronarias10,11.
En el caso que presentamos, la disfunción del VD afectó a la pared libre, pero en forma de discinesia, una anomalía segmentaria más acusada que las descritas previamente, y que se explica, además de por los mecanismos citados, por la coexistencia de una lesión coronaria que comprometía la perfusión del VD. Concluimos que la disfunción del VD en pacientes con cor pulmonale agudo tromboembólico puede estar agravada por una enfermedad coronaria subyacente.
Correspondencia: Dr. A. Rubio Alcaide.
Urbanización Montesol, 53. 29730 Rincón de la Victoria. Málaga. España.
Correo electrónico: alvaro13@terra.com