En la práctica habitual, solamente 1 de cada 3 pacientes con infarto agudo de miocardio (IAM) alcanza cifras de colesterol unido a lipoproteínas de baja densidad (cLDL) <55mg/dl en el primer año. El presente estudio pretende evaluar el impacto de un tratamiento intensivo precoz para el control lipídico tras un IAM.
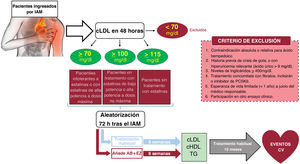
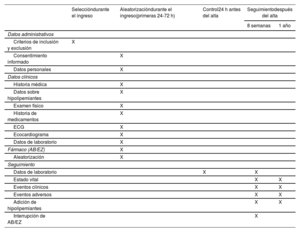
MétodosEnsayo clínico independiente, prospectivo, pragmático, controlado, aleatorizado, abierto, ciego para el evaluador (diseño PROBE), que analiza la eficacia y la seguridad de un tratamiento hipolipemiante oral triple: estatina de alta potencia+ácido bempedoico [AB] 180 mg+ezetimiba [EZ] 10 mg frente a la estrategia basada en las vigentes recomendaciones (estatina de alta potencia±EZ 10 mg) en pacientes con IAM. Se determina el cLDL en las primeras 48 h tras el IAM. Se aleatoriza 1:1 a AB+EZ o estatina±EZ sin AB a los pacientes con cifras, entre las 24 y las 72 h tras el IAM, de cLDL ≥ 115mg/dl sin estatinas previas, ≥ 100mg/dl tras estatina de baja potencia o alta potencia a dosis no máxima o ≥ 70mg/dl tras estatina de alta potencia a dosis máxima. El objetivo primario es el porcentaje de pacientes con cLDL <55mg/dl tras 8 semanas del tratamiento.
ResultadosEstos resultados aportarán información novedosa para el control del cLDL tras el IAM evaluando la utilidad de una estrategia hipolipemiante oral intensiva y precoz.
ConclusionesEl tratamiento hipolipemiante oral triple precoz frente al tratamiento recomendado por las guías de práctica clínica podría facilitar la optimización del cLDL en los primeros 2 meses tras el IAM (periodo de alto riesgo).
Número de identificaciónEudraCT 2021-006550-31.
Palabras clave
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Precio: 19,34 €
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h