Se revisan las posibles estrategias de reperfusión en el síndrome coronario agudo con elevación del segmento ST contempladas en las guías contemporáneas de forma general, y se hace especial hincapié en los conceptos que describen estas estrategias. Del mismo modo, se describe cuál es la situación de la reperfusión general y farmacológica en España.
Palabras clave
Es bien conocido y está estandarizado, desde hace años, que en la evaluación inicial del paciente con dolor torácico de características isquémicas el electrocardiograma de 12 derivaciones sigue siendo el centro del algoritmo terapéutico de los pacientes con síndrome coronario agudo. La elevación persistente del segmento ST en el electrocardiograma es sinónimo de obstrucción completa del flujo coronario y, por lo tanto, en estos pacientes debe instaurarse un tratamiento de reperfusión. Es importante tener presente que la terapia de reperfusión ha de ser proporcionada con carácter urgente, de la forma más precoz posible, dado que el retraso en su administración se relaciona con peor evolución clínica, mayor tamaño del infarto y mayor mortalidad a corto y largo plazo. Por ello, ante un paciente que se presente con un dolor torácico prolongado compatible con origen coronario de menos de 12h de evolución y se evidencie elevación persistente del segmento ST o bloqueo completo de rama izquierda o incluso tenga ritmo de marcapasos, nuestra actuación ha de ir encaminada a proporcionar una terapia de reperfusión urgente con la finalidad de conseguir la reapertura de la arteria coronaria ocluida de la manera más rápida, efectiva y definitiva posible y conseguir la restauración del flujo epicárdico y microvascular1,2.
Hay dos formas de tratamiento bien establecidas para conseguir restaurar de forma precoz la perfusión epicárdica y miocárdica tras un síndrome coronario agudo con elevación del segmento ST (SCACEST): la administración de fármacos fibrinolíticos intravenosos y la realización de una angioplastia primaria. Ambas tienen ventajas e inconvenientes. En condiciones óptimas, la angioplastia primaria parece ser más eficaz que la fibrinolisis en el objetivo de restaurar el flujo coronario y mejorar la evolución clínica de los pacientes con SCACEST. Sin embargo, debido a las limitaciones logísticas y técnicas inherentes a la angioplastia, este tratamiento es sólo aplicable, en condiciones óptimas, a una pequeña proporción de pacientes con infarto. Por el contrario, la fibrinolisis por vía intravenosa reduce la mortalidad a corto y largo plazo y puede aplicarse a la inmensa mayoría de los pacientes con SCACEST. Sin embargo, la utilidad de la fibrinolisis tiene varias limitaciones importantes: conlleva riesgo hemorrágico, con una incidencia de hemorragia cerebral del 0,5-1%; su beneficio clínico depende mucho de la precocidad de la aplicación, por lo que se reduce sustancialmente cuando la evolución del infarto supera las 6h; hay una alta incidencia de fallo de repermeabilización, y entre el 5 y el 25% de los pacientes con reapertura inicial satisfactoria sufren una reoclusión por persistencia de una estenosis residual significativa3.
Las ventajas y los inconvenientes de ambas terapias han dado lugar a un hecho bien recogido en las guías de práctica clínica, y es que hoy en día en lugar de tratamiento de reperfusión, debemos hablar de estrategia de reperfusión. Así, la utilización de fibrinolisis o angioplastia primaria dependerá fundamentalmente de tres hechos: a) la situación geográfica donde se encuentre el paciente en el momento del primer contacto médico; b) el tiempo de evolución del infarto, y c) la disponibilidad inmediata de recursos de intervencionismo coronario percutáneo. Asimismo, estas premisas, fundamentales, han dado lugar a que fibrinolisis y angioplastia puedan ser complementarias en un mismo paciente, lo que indica el concepto de la reperfusión farmacomecánica con diferentes opciones, como veremos.
ESTRATEGIAS DE REPERFUSIÓN EN EL IAM CON ELEVACIÓN DEL SEGMENTO ST. VISIÓN GENERAL Y DESCRIPCIÓN DE CONCEPTOSComo hemos comentado anteriormente, el facultativo responsable de poner en marcha la estrategia más adecuada de reperfusión en un paciente concreto con SCACEST debe tener en cuenta la localización del paciente, el tiempo de evolución del dolor y la disponibilidad inmediata de recursos de intervencionismo coronario percutáneo.
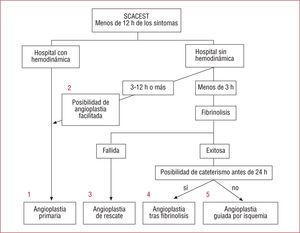
Las guías de práctica clínica de la Sociedad Europea de Cardiología sobre intervencionismo coronario percutáneo, publicadas en 2005, exponen de forma clara las diferentes estrategias de reperfusión evaluadas en los últimos años (fig. 1)4. En los pacientes con SCACEST que acuden a un hospital con servicio de cardiología intervencionista la angioplastia primaria debe ser el tratamiento de elección. Esta estrategia es, además, independiente del tiempo de infarto (o inicio de los síntomas), siempre que el paciente esté dentro de las primeras 12h del infarto. Por el contrario, en aquellos que acuden a un hospital sin hemodinámica o en los que son atendidos por los servicios de emergencias, estas guías consideran fundamental tener en cuenta el tiempo desde el inicio de los síntomas. Durante las primeras 3h de aparición de dolor torácico u otros síntomas, la fibrinolisis es una buena alternativa a la angioplastia primaria, excepto en los casos en que la fibrinolisis esté contraindicada o el paciente tenga alto riesgo, en que se recomienda el traslado inmediato del paciente para realizarle una angioplastia primaria. En las 3-12h del inicio de los síntomas, se recomienda trasladar al paciente para realizarle angioplastia primaria. Las razones fundamentales para la elección de angioplastia primaria frente a fibrinolisis durante ese periodo es salvar el miocardio, ya que el tratamiento fibrinolítico es menos eficaz en los trombos antiguos, y prevenir los ictus hemorrágicos. En todos estos casos en que el paciente es trasladado para realización de angioplastia primaria, la administración de sustancias antitrombóticas dirigidas a intentar abrir la arteria causal del infarto durante el retraso inherente al traslado y, con ello, aumentar la eficacia de la intervención coronaria percutánea (ICP) primaria podría ser atractivo. Esta estrategia farmacomecánica se conoce como angioplastia facilitada. Finalmente, en los pacientes sometidos a fibrinolisis, ésta no debe ser considerada el tratamiento final. Si la fibrinolisis no es efectiva, debe contemplarse la realización de una angioplastia de rescate, pero incluso tras la fibrinolisis efectiva se debe considerar la angiografía coronaria durante las primeras 24h e ICP si fuera preciso. Esta última estrategia se conoce como angioplastia tras trombolisis o pronóstica. Si la realización de la angiografía no fuese posible en las primeras 24h, podría considerarse realizar una estrategia guiada por isquemia con ICP, si fuese necesario, o angioplastia guiada por isquemia.
Posibles estrategias de reperfusión contempladas en las guías de práctica clínica de la Sociedad Europea de Cardiología sobre intervencionismo coronario percutáneo4. 1: angioplastia primaria; 2: angioplastia facilitada; 3: angioplastia de rescate; 4: angioplastia tras fibrinolisis o pronóstica; 5: angioplastia guiada por isquemia. SCACEST: síndrome coronario agudo con elevación del segmento ST. Explicación en el texto.
Por lo tanto, derivado de las condiciones logísticas y temporales del infarto, en los últimos años se han barajado cinco estrategias de reperfusión diferentes: a) angioplastia primaria; b) angioplastia facilitada; c) angioplastia de rescate; d) angioplastia tras fibrinolisis o pronóstica, y e) angioplastia guiada por isquemia.
A continuación, se describen los conceptos fundamentales de cada estrategia que servirán de introducción al resto de los artículos de este suplemento.
Angioplastia primariaSe define como una intervención del vaso causante del infarto durante las primeras 12h de la presentación del dolor u otros síntomas, con o sin implantación de stent, y sin utilizar previamente terapia trombolítica u otro tratamiento para la disolución de trombos. Esta estrategia debe realizarse también en los infartos de más de 12h de evolución con evidencia clínica o electrocardiográfica de isquemia e inestabilidad hemodinámica. Puede considerarse en pacientes estables cuando han transcurrido entre 12 y 24h del inicio de los síntomas y está contraindicada en infartos de más de 24h de evolución en ausencia de signos de isquemia en pacientes estables1,2.
Aunque a lo largo de este suplemento la angioplastia primaria se revisará en profundidad, es importante recordar que, en comparación con la estrategia de fibrinolisis, la angioplastia primaria ha demostrado en numerosos ensayos clínicos mayor eficacia en la normalización del flujo coronario, menor tasa de reoclusión y reinfarto, mejora de la función ventricular y mejor supervivencia5. Asimismo, la angioplastia primaria con stent disminuye la incidencia de sucesos isquémicos adversos, aunque no la mortalidad, en comparación con la utilización aislada de balón, tal y como demostró el estudio Stent PAMI6. Parece que la utilización de stents recubiertos con fármacos en este escenario es segura y se asocia a una disminución en la necesidad de futuras revascularizaciones7–9. La angioplastia primaria es superior al tratamiento fibrinolítico en pacientes con más de 3h desde el inicio de los síntomas10. Finalmente, el tiempo puerta-balón es determinante en el beneficio de la angioplastia primaria, y se consigue el mayor beneficio cuando éste es inferior a los 90 min11.
Angioplastia facilitadaLa angioplastia facilitada hace referencia a la administración de tratamiento antitrombótico y/o fibrinolítico antes de la realización de la angioplastia primaria. Debe diferenciarse de la angioplastia primaria con inhibidores de la glucoproteína IIb/IIIa durante el intervencionismo, la angioplastia de rescate y la angioplastia tras fibrinolisis. Este concepto surge con la intención de disminuir el efecto del retraso que supone la derivación de un paciente que llega a un centro sin laboratorio de hemodinámica disponible 24h y se basa en que los pacientes tienen mejor pronóstico cuando se lleva a cabo la angioplastia primaria con flujo epicárdico normal. Se han elaborado estudios con tratamiento fibrinolítico a dosis plenas, con mitad de dosis y con inhibidores de la glucoproteína IIb/IIIa en combinación con fibrinolíticos.
Los estudios contemporáneos más importantes que han evaluado la administración de tratamiento fibrinolítico antes de la angioplastia primaria son CAPITAL AMI12, ASSENT-413 y PACT14. Los dos primeros, con dosis completas de fibrinolítico y el segundo, con mitad de dosis. De todos, el más concluyente fue el estudio ASSENT-413, donde se aleatorizó finalmente a 1.667 pacientes con SCACEST a recibir tenecteplasa o placebo antes de la angioplastia primaria. La inclusión de pacientes se suspendió prematuramente al objetivarse mayor mortalidad, mayor tasa de accidentes cerebrovasculares, reinfarto y revascularización en el grupo que recibió tenecteplasa. Estos resultados fueron concordantes con el metaanálisis realizado posteriormente y que incluyó seis estudios con tratamiento fibrinolítico y dos con la combinación de fibrinolisis e inhibidores de la grucoproteína IIb/IIIa15.
También se han realizado estudios que utilizaban como fármaco un inhibidor de la glucoproteína IIb/IIIa, aislado o en combinación, antes de la angioplastia primaria. De todos ellos, el más trascendente es el recientemente publicado estudio FINESSE16. En el estudio FINESSE, se aleatorizó a 2.452 pacientes con SCACEST a tres estrategias de reperfusion: administración de abciximab y media dosis de reteplasa antes de la angioplastia (angioplastia facilitada con fibrinolíticos y IIb/IIIa), abciximab antes de la angioplastia (angioplastia facilitada con IIb/IIIa) o abciximab durante la angioplastia (angioplastia primaria). No hubo diferencias en el objetivo clínico compuesto entre los tres grupos, por el contrario la angioplastia facilitada con tratamiento farmacológico combinado conllevó una incidencia mayor de hemorragias mayores.
Con todos estos datos las guías de práctica clínica no recomiendan realizar angioplastia facilitada1,2: con fibrinolíticos se asocia a un incremento de mortalidad, infarto no fatal, revascularización coronaria urgente e ictus, y con dosis combinadas de fibrinolítico e inhibidores IIb/IIIa, o con estos últimos de forma aislada, tampoco disminuye la incidencia de complicaciones isquémicas, pero sí las hemorragias, en comparación con la administración de inhibidores de la glucoproteína IIb/IIIa durante la ICP (angioplastia primaria).
Angioplastia de rescateLa angioplastia de rescate se define como una ICP en una arteria coronaria que permanece ocluida a pesar de la terapia fibrinolítica. Hoy, se acepta como criterio para no reperfundir la falta de resolución del segmento ST > 50% en la derivación con mayor ascenso evaluada a los 60-90min del tratamiento fibrinolítico. Este criterio se basa en el estudio más significativo y actual que ha evaluado esta estrategia de reperfusión, el estudio REACT17. En este estudio la angioplastia de rescate fue superior a la repetición de la fibrinolisis o al tratamiento conservador en los pacientes que no presentaban una resolución > 50% de los cambios del segmento ST. La incidencia de cualquier tipo de eventos a los 6 meses se redujo aproximadamente a la mitad en el grupo de angioplastia de rescate, en comparación con los grupos de repetición de la fibrinolisis o terapia conservadora.
Angioplastia tras fibrinolisis o pronósticaLa angioplastia tras fibrinolisis o pronóstica se define como la realización de angiografía sistemática e ICP (cuando es preciso) poco tiempo después (entre 3 y 24h) del tratamiento fibrinolítico en los pacientes en que el fibrinolítico haya sido eficaz. La fibrinolisis, pues, aun en el caso de que sea eficaz, no debe considerarse como el tratamiento final.
Hay varios estudios que demuestran la seguridad, la aplicabilidad y los beneficios de esta estrategia. En nuestro país el grupo GRACIA demostró, en un primer ensayo aleatorizado, que realizar una ICP pasadas 6-24h de la fibrinolisis era seguro y reducía la incidencia de reinfarto y revascularización a los 12 meses respecto a la estrategia clásica guiada por isquemia18. En el ensayo GRACIA-219, al igual que en el WEST20, se demostró que la fibrinolisis seguida de ICP en 3-12h no era inferior que la angioplastia primaria. Junto con ellos, el ensayo SIAMIII21, que encontró una reducción en el número de eventos isquémicos en los pacientes que recibieron ICP pasadas de media 3,5h tras la fibrinolisis respecto a una revascularización más tardía, ha conducido a las actuales recomendaciones2.
Mientras se determina el momento idóneo para la realización de ICP tras la fibrinolisis y la terapia antiagregante adyuvante más adecuada, lo que cada vez resulta más claro, a la luz de los estudios CARESS-in-AMI22 y TRANSFER-AMI23, es la necesidad del traslado inmediato del paciente con fibrinolisis a un centro con disponibilidad de angioplastia para realizarla en las horas siguientes, lo cual ha demostrado ser seguro y disminuir el objetivo combinado de muerte, reinfarto e isquemia recurrente.
Angioplastia guiada por isquemiaLa angioplastia guiada por isquemia se define como angiografía coronaria y revascularización, si procede, que se realiza a los pacientes con SCACEST tratados con fibrinolíticos que presentan isquemia espontánea o inducible antes del alta, con independencia de que reciban tratamiento farmacológico máximo. El estudio DANAMI24 fue el primer ensayo clínico, y el único prospectivo y aleatorizado, en que se comparó una estrategia invasiva (ICP o cirugía) con una estrategia conservadora en pacientes que presentaban isquemia miocárdica inducible antes del alta hospitalaria y después de haber recibido tratamiento fibrinolítico por un primer infarto agudo de miocardio. La incidencia del objetivo primario (muerte, reinfarto e ingreso por angina inestable) se redujo significativamente a corto, medio y largo plazo.
ESTRATEGIAS DE REPERFUSIÓN EN EL IAM CON ELEVACIÓN DEL SEGMENTO ST. RECOMENDACIONES ACTUALESLas guías sobre el SCACEST, recientemente publicadas por la Sociedad Europea de Cardiología2, nuevamente ponen de manifiesto los tres requisitos a tener en cuenta a la hora de iniciar una estrategia de reperfusión en el SCACEST. En primer lugar, dónde ocurre la primera atención al paciente: en un hospital con alerta de hemodinámica, en un hospital sin esta capacidad o por los servicios de emergencia; es más, las guías incluso abogan porque la atención inicial al paciente, de forma ideal, sea por los servicios de emergencia. En segundo lugar, el tiempo de evolución del dolor debe ser clave y, finalmente, la disponibilidad inmediata o no de recursos de intervencionismo coronario percutáneo.
En los pacientes con SCACEST que acuden a un hospital con servicio de cardiología intervencionista la angioplastia primaria continúa siendo el tratamiento de elección. Por el contrario, en los pacientes que acuden a un hospital sin hemodinámica o en aquellos que son atendidos por los servicios de emergencias, es fundamental tener en cuenta la disponibilidad inmediata o no de recursos de intervencionismo coronario percutáneo y el tiempo de evolución del infarto. Así, si el tiempo entre el primer contacto médico y el inflado del balón se prevé < 2h, es preferible trasladar al paciente para realizar una angioplastia primaria (excepto durante las primeras 2h de aparición de dolor torácico u otros síntomas, en que el retraso no debe superar los 90min). Sin embargo, en caso de prever un retraso > 2h se recomienda administrar fibrinolisis. En los pacientes sometidos a fibrinolisis, no se debe considerarla el tratamiento final. Si la fibrinolisis no es efectiva, debe contemplarse la realización de una angioplastia de rescate, pero incluso tras la fibrinolisis efectiva, se debe considerar una angiografía coronaria durante las primeras 24h e ICP si fuera preciso.
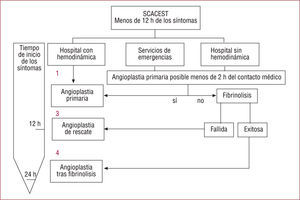
Por lo tanto, las guías europeas actuales aportan varias novedades importantes (fig. 2): a) el retraso desde el primer contacto médico al primer insuflado de balón se amplía hasta un máximo de 120min (siempre y cuando estemos fuera de las primeras 2h desde el inicio de los síntomas, en cuyo caso este retraso debe ser < 90min); b) desaparece la estrategia de angioplastia facilitada como resultado de los estudios previamente expuestos12–16. La administración de tratamiento antitrombótico y/o fibrinolítico antes de la angioplastia primaria, con la intención de disminuir el efecto del retraso que supone la derivación de un paciente que llega a un centro sin laboratorio de hemodinámica, no se ha mostrado beneficiosa, todo lo contrario; c) la fibrinolisis, aun en el caso de que sea eficaz, debe completarse con angiografía y revascularización si fuese necesario. La angioplastia tras fibrinolisis o pronóstica debe sustituir a la angioplastia guiada por isquemia como tratamiento final tras la fibrinolisis.
Posibles estrategias de reperfusión contempladas en las guías actuales de la Sociedad Europea de Cardiología sobre síndrome coronario agudo con elevación del segmento ST (SCACEST)2. 1: angioplastia primaria; 3: angioplastia de rescate; 4: angioplastia tras fibrinolisis o pronóstica. En esta figura no se representan los números 2 y 5 de la figura 1, ya que estas dos estrategias (angioplastia facilitada y angioplastia guiada por isquemia) no se contemplan en las guías actuales sobre SCACEST2.
Podemos acercarnos a conocer cuál es la realidad de la reperfusión en nuestro país gracias a los registros poblacionales que han venido realizándose de forma continuada y multidisciplinaria tanto en ámbitos provinciales como regionales o a lo largo de todo el territorio español25. A favor de estos registros está el hecho de ser mucho más representativos de la práctica clínica y traducir de forma mucho más adecuada las tasas de eventos clínicos. Los registros incluyen a pacientes no ideales y en riesgo elevado y permiten conocer si las guías se aplican de forma adecuada. Por el contrario, la valoración del impacto de un tratamiento específico mediante un registro puede ser incorrecta debido a la influencia de variables de confusión no evaluadas26.
El registro con datos más actuales y representativos en el ámbito nacional es el MASCARA. El registro MASCARA incluyó finalmente a 7.251 pacientes con SCA ingresados en 32 hospitales españoles durante 2004 y 2005. De los 3.034 pacientes con SCACEST incluidos en el MASCARA, aproximadamente un 68% de los pacientes recibieron tratamiento de reperfusión (el 43%, fibrinolisis, y el 25%, angioplastia primaria) frente a un 32% de los pacientes que todavía no reciben tratamiento alguno de reperfusión. Estos últimos son quienes muestran características basales de mayor riesgo (edad, diabetes, infarto previo, vasculopatía periférica, insuficiencia renal e insuficiencia cardiaca). La mortalidad hospitalaria bruta fue mayor en los pacientes no sometidos a ningún tipo de reperfusión (9,6%) que en los sometidos a fibrinolisis (5,6%) o angioplastia primaria (8,7%). Las diferencias de mortalidad entre los pacientes fueron aumentando a los 6 meses en los pacientes que no recibieron ningún tratamiento de reperfusión (18,7%) frente a aquellos tratados inicialmente con fibrinolisis (10,3%) o angioplastia primaria (12,7%). Aunque destaca una mayor mortalidad hospitalaria de la angioplastia primaria con respecto a la fibrinolisis, dicha diferencia probablemente esté en relación con una mayor prevalencia de factores muy relacionados con el pronóstico en ese grupo. Además, dicha diferencia en la mortalidad fue atenuándose con el tiempo, y perdió significación estadística a los 6 meses27.
Si comparamos el registro MASCARA con otros registros anteriores de ámbito nacional, como el registro PRIAMHO II28, en el año 2000 aproximadamente un 72% de los pacientes recibían tratamiento de reperfusión (el 64%, fibrinolisis, y el 8%, angioplastia primaria) frente a un 28% que no recibía tratamiento alguno de reperfusión. Estos datos evidencian que, aunque la fibrinolisis sigue siendo el tratamiento de reperfusión más utilizado, la disponibilidad de angioplastia primaria se ha incrementado notablemente en los últimos 4-5 años. Sin embargo, no se ha logrado disminuir el porcentaje tan importante de pacientes que no reciben tratamiento de reperfusión alguno.
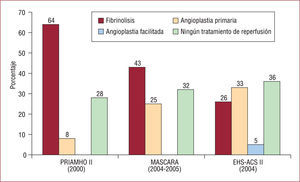
Asimismo, si comparamos el registro MASCARA con el registro europeo (Second Euro Heart Survey on Acute Coronary Syndromes) contemporáneo29, en 2004 aproximadamente un 64% de los pacientes recibían tratamiento de reperfusión (el 26%, fibrinolisis; el 5%, angioplastia facilitada, y el 33%, angioplastia primaria) frente a un 36% que no recibía tratamiento alguno de reperfusión. Lo que pone de manifiesto que el tratamiento de reperfusión más utilizado en Europa es la angioplastia primaria, pero que nuevamente el porcentaje de pacientes que no reciben reperfusión alguna es alarmante.
La figura 3 representa gráficamente los datos anteriormente expuestos, con la evolución de la reperfusión en España en comparación con Europa.
CONCLUSIONESAunque la angioplastia primaria es el tratamiento de reperfusión ideal en el SCACEST, ésta todavía no es accesible en condiciones óptimas para la mayoría de los pacientes con infarto, por ello se contemplan otras estrategias de reperfusión. A nuestro parecer la mejor estrategia de reperfusión es la aplicable a las situaciones temporales y logísticas del paciente con SCACEST.