El tratamiento con hierro carboximaltosa de pacientes con insuficiencia cardiaca crónica y deficiencia de hierro mejora los síntomas, la capacidad funcional y la calidad de vida. El propósito del estudio es evaluar el coste-efectividad del tratamiento con hierro carboximaltosa frente a no tratar a dichos pacientes.
MétodosSe realizó un modelo económico, desde la perspectiva del Sistema Nacional de Salud, con un horizonte temporal de 24 semanas. Las características de los pacientes y la efectividad del hierro carboximaltosa (años de vida ajustados por calidad) se obtuvieron del estudio Ferinject®Assessment in patients with IRon deficiency and chronic Heart Failure. El uso de recursos sanitarios y los costes unitarios provienen de fuentes españolas o del citado estudio.
ResultadosEn el caso base del análisis, para cada paciente se obtendrían 0,335 y 0,298 años de vida ajustados por calidad con y sin hierro carboximaltosa, respectivamente, con 0,037 años de vida ajustados por calidad ganados para el paciente tratado. El coste por paciente sería de 824,17 y 597,59 euros, respectivamente, conque se produce un coste adicional de 226,58 euros con hierro carboximaltosa. El coste de ganar 1 año de vida ajustado por calidad con hierro carboximaltosa sería de 6.123,78 euros. La estabilidad del resultado se confirmó en los análisis de sensibilidad. Las probabilidades de que el hierro carboximaltosa sea coste-efectivo (< 30.000 euros/año de vida ajustado por calidad) y dominante (más eficaz, con menores costes que no tratar) son del 93,0 y el 6,6% respectivamente.
ConclusionesSegún el estudio, el tratamiento con hierro carboximaltosa de pacientes con insuficiencia cardiaca crónica y deficiencia de hierro, con o sin anemia, es coste-efectivo en España.
Palabras clave
La insuficiencia cardiaca crónica (ICC) es un síndrome con alta prevalencia en España1 y un impacto muy negativo en mortalidad y morbilidad2.
El déficit de hierro es frecuente en pacientes con ICC: en pacientes ambulatorios su frecuencia ronda el 40 y el 50%3–5. En muchos casos el déficit de hierro es absoluto, asociado a pérdidas gastrointestinales ocultas (en relación con terapias anticoagulante y antiagregante), pero frecuentemente es funcional (bloqueo del hierro en el sistema reticuloendotelial) en relación con la producción de hepcidina y el estado proinflamatorio de la ICC6. Estudios recientes han demostrado que el déficit de hierro en pacientes con ICC se asocia a mayor mortalidad, peor clase funcional, peor capacidad máxima de esfuerzo y peor calidad de vida, y que este efecto es independiente de que haya anemia o no3-5,7. Estos hallazgos han permitido formular la hipótesis de que la anemia, en la mayoría de los pacientes con ICC, es secundaria a deficiencia de hierro y que esta deficiencia es en sí misma una comorbilidad con entidad propia.
En este sentido, el estudio FAIR-HF (Ferinject®Assessment in patients with IRon deficiency and chronic Heart Failure) en el que se basa el presente estudio, fue un ensayo clínico aleatorizado, a doble ciego y controlado con placebo (n = 459) en el que se evaluaron los beneficios clínicos y la calidad de vida asociados al tratamiento con hierro carboximaltosa (HCM) (mediante dosis intravenosas) en pacientes con ICC (clases funcionales de la NYHA [New York Heart Association] II o III, con fracción de eyección ventricular izquierda ≤ 40% para pacientes en clase II o ≤ 45% en clase III) que tenían deficiencia de hierro y hemoglobina en 9,5–13,5g/dl8. Las causas de la insuficiencia cardiaca en el estudio FAIR-HF fueron predominantemente isquémicas: HCM, 245 pacientes (80,6%); placebo, 123 (79,4%). Los parámetros primarios y secundarios de valoración de la eficacia fueron los cambios de clase funcional de la NYHA desde el valor basal y el cuestionario de calidad de vida relacionada con la salud EuroQol (European Quality of Life) de 5 dimensiones. El estudio FAIR-HF mostró mejores resultados con HCM que con placebo en ambos parámetros.
Más allá del impacto negativo de la insuficiencia cardiaca en la mortalidad y la calidad de vida de los pacientes, este síndrome se asocia a un elevado coste sanitario9. Esto supone una carga inasumible no solo para los pacientes, sino para cualquier sistema sanitario, pues la insuficiencia cardiaca supone cerca del 2% del presupuesto para sanidad de la mayoría de los países desarrollados9. En la coyuntura económica actual, la reducción de los costes asociados a las enfermedades crónicas y la evaluación del coste-efectividad de los nuevos tratamientos se han convertido en la piedra angular de las estrategias organizativas de los responsables de los sistemas sanitarios públicos como el español. Por ello, el presente estudio tiene por objetivo evaluar el coste-efectividad del tratamiento de la deficiencia de hierro (por vía intravenosa) utilizando HCM en pacientes con ICC, desde la perspectiva del Sistema Nacional de Salud español.
MÉTODOSModeloSe ha adaptado al entorno sanitario español un modelo de coste-efectividad, en el que se calcula el coste de ganar una unidad adicional de efectividad mediante el tratamiento de la deficiencia de hierro con HCM en comparación con la opción de no administrar hierro a pacientes con ICC, con o sin anemia. La efectividad se expresa como años de vida ajustados por calidad (AVAC), que toma un valor que oscila entre 0 o incluso valores negativos (la peor salud posible) y 1 (la mejor salud posible) según lo estimado por los pacientes y se obtiene mediante instrumentos como, por ejemplo, EuroQol10.
El modelo (entendido como un esquema teórico que permite hacer simulaciones económicas de procesos sanitarios complejos)10 se hizo mediante un árbol de decisiones y ya se describió en un análisis realizado para Reino Unido11. El modelo se realizó mediante la herramienta TreeAge Pro 2011 Suite (TreeAge Software Inc.; Williamstown, Massachusetts, Estados Unidos).
EfectividadLas características clínicas y demográficas de los pacientes modelizados son las de los pacientes del ensayo clínico FAIR-HF8,12. Los AVAC por paciente con o sin HCM se obtuvieron asimismo de los pacientes del estudio FAIR-HF, a los que se administró el cuestionario EuroQol de 5 dimensiones8,11.
La población del modelo clínico constó de 459 pacientes seleccionados por intención de tratar (304 con HCM y 155 que recibieron placebo) con deficiencia de hierro, ICC y las características indicadas en la tabla 1. El diseño y las variables de evaluación, así como los resultados clínicos, ya se han descrito previamente8,12.
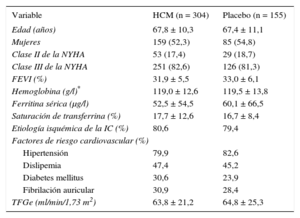
Características clínicas y demográficas de la población por intención de tratar del estudio Ferinject®Assessment in patients with IRon deficiency and chronic Heart Failure11
| Variable | HCM (n = 304) | Placebo (n = 155) |
|---|---|---|
| Edad (años) | 67,8 ± 10,3 | 67,4 ± 11,1 |
| Mujeres | 159 (52,3) | 85 (54,8) |
| Clase II de la NYHA | 53 (17,4) | 29 (18,7) |
| Clase III de la NYHA | 251 (82,6) | 126 (81,3) |
| FEVI (%) | 31,9 ± 5,5 | 33,0 ± 6,1 |
| Hemoglobina (g/l)* | 119,0 ± 12,6 | 119,5 ± 13,8 |
| Ferritina sérica (μg/l) | 52,5 ± 54,5 | 60,1 ± 66,5 |
| Saturación de transferrina (%) | 17,7 ± 12,6 | 16,7 ± 8,4 |
| Etiología isquémica de la IC (%) | 80,6 | 79,4 |
| Factores de riesgo cardiovascular (%) | ||
| Hipertensión | 79,9 | 82,6 |
| Dislipemia | 47,4 | 45,2 |
| Diabetes mellitus | 30,6 | 23,9 |
| Fibrilación auricular | 30,9 | 28,4 |
| TFGe (ml/min/1,73 m2) | 63,8 ± 21,2 | 64,8 ± 25,3 |
FEVI: fraccíon de eyección del ventrículo izquierdo; HCM: hierro carboximaltosa; NYHA: IC: insuficiencia cardiaca; NYHA: New York Heart Association; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan media ± desviación estándar o n (%).
El uso de recursos sanitarios y los costes unitarios (expresados en euros de 2013) provienen de fuentes españolas o del estudio FAIR-HF. Se consideraron los costes directos sanitarios (perspectiva del Sistema Nacional de Salud de adquisición y administración intravenosa de HCM y de la hospitalización por ICC). A partir del estudio FAIR-HF se estimaron la dosis media de HCM, el número medio de inyecciones de 200 mg de HCM, la duración y la frecuencia de la hospitalización con o sin HCM y la diferencia de AVAC con o sin HCM8,11 (tabla 2). La duración de la hospitalización del paciente con ICC se obtuvo para el GRD (grupo relacionado por el diagnóstico) 127 de la norma estatal de los GRD (AP–GRD V25) por grupos de hospitales del año 201013. El coste del hospital de día para el paciente con ICC se obtuvo de la misma fuente. El coste de la infusión intravenosa de HCM en el hospital de día, considerando 15 min de infusión, 15 min de atención de la enfermera y el coste del material fungible, se obtuvo de un reciente estudio español14. El precio de venta del laboratorio de 100 mg de HCM se tomó de la base de datos Bot Plus 2.0 del Consejo General de Colegios Oficiales de Farmacéuticos15 (tabla 2).
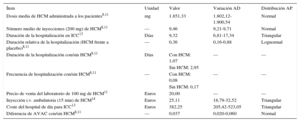
Parámetros incluidos en el modelo económico, intervalos y distribuciones utilizados en los análisis de sensibilidad
| Ítem | Unidad | Valor | Variación AD | Distribución AP |
|---|---|---|---|---|
| Dosis media de HCM administrada a los pacientes8,11 | mg | 1.851,33 | 1.802,12-1.900,54 | Normal |
| Número medio de inyecciones (200 mg) de HCM8,11 | — | 9,46 | 9,21-9,71 | Normal |
| Duración de la hospitalización en ICC13 | Días | 9,32 | 6,81-17,34 | Triangular |
| Duración relativa de la hospitalización (HCM frente a placebo)8,11 | — | 0,36 | 0,16-0,88 | Lognormal |
| Duración de la hospitalización con/sin HCM8,11 | Días | Con HCM: 1,07 | — | — |
| Sin HCM: 2,95 | ||||
| Frecuencia de hospitalización con/sin HCM8,11 | — | Con HCM: 0,08 | — | — |
| Sin HCM: 0,17 | ||||
| Precio de venta del laboratorio de 100 mg de HCM11 | Euros | 20,00 | — | — |
| Inyección i.v. ambulatoria (15 min) de HCM14 | Euros | 25,11 | 18,79-32,52 | Triangular |
| Coste del hospital de día para ICC13 | Euros | 382,25 | 205,42-523,05 | Triangular |
| Diferencia de AVAC con/sin HCM8,11 | — | 0,037 | 0,020-0,060 | Normal |
AD: análisis determinístico; AP: análisis probabilístico; AVAC: año de vida ajustado por calidad; HCM: hierro carboximaltosa; ICC: insuficiencia cardiaca crónica; i.v.: intravenosa.
El coste de la administración de HCM se calculó asumiendo que no habría pérdida de viales, al igual que en el estudio FAIR-HF. El coste de la hospitalización por ICC se calculó multiplicando el número de días de estancia hospitalaria de los pacientes con ICC por el número promedio de hospitalizaciones observadas en los pacientes del grupo placebo en el ensayo FAIR-HF, y en el caso de los pacientes tratados con HCM, multiplicado por la duración promedio de la estancia hospitalaria del grupo con HCM dividida entre la duración promedio de la estancia del grupo placebo. Los costes de los eventos adversos no se incluyeron debido a que no se encontraron diferencias clínicamente relevantes entre los grupos de tratamiento del estudio FAIR-HF11.
Horizonte temporalEl horizonte temporal (la duración del seguimiento simulado de los pacientes en el modelo) del análisis fue de 24 semanas, la misma duración del ensayo clínico FAIR-HF. La extrapolación del horizonte temporal a un plazo más largo (p. ej., a un horizonte temporal de toda la vida) no se consideró adecuada, ya que en el ensayo clínico FAIR-HF no se proporciona información sobre la supervivencia u otros efectos a largo plazo11.
Caso base, análisis de sensibilidad y presentación de los resultadosSe efectuó un análisis basal, consistente en la utilización en el modelo de los valores medios de todas las variables consideradas (uso de recursos, costes unitarios y AVAC). También se hicieron análisis de sensibilidad, cuyo objetivo es valorar la estabilidad de los resultados del análisis basal cuando se consideran los valores extremos de las variables. En concreto, se realizaron análisis de sensibilidad determinísticos univariables, modificando en cada análisis el valor basal de determinada variable e incluyendo uno de los valores extremos para esa variable indicados en los intervalos de la tabla 2. También se efectuó un análisis de sensibilidad probabilístico mediante simulación de Monte Carlo de segundo orden, en la que se realizaron 10.000 análisis modificando al azar los valores de las variables conforme a las distribuciones estadísticas de la tabla 211. Los resultados se presentan para un paciente (con o sin tratamiento con HCM) como costes por paciente, diferencia de costes, AVAC por paciente, AVAC ganados con HCM y, finalmente, como el coste de ganar 1 AVAC con HCM en comparación con la opción de no tratar al paciente (denominado RCEI [razón coste-efectividad incremental]). No se descontaron costes y beneficios debido al corto horizonte temporal del estudio11.
RESULTADOSCaso baseEn el caso base del análisis, en cada paciente se obtendrían 0,335 y 0,298 AVAC con y sin HCM, respectivamente, con una ganancia de 0,037 AVAC en el paciente tratado. El coste por paciente sería de 824,17 y 597,59 euros, respectivamente, un coste adicional de 226,58 euros con HCM. En consecuencia, el coste de ganar 1 AVAC con HCM sería de 6.123,78 euros (tabla 3).
Resultados del caso base del análisis
| Comparador | Coste/paciente (euros) | Coste incremental (euros) | AVAC/paciente | AVAC ganados | Coste de ganar 1 AVAC (euros) |
|---|---|---|---|---|---|
| Sin HCM | 597,59 | — | 0,298 | — | — |
| Con HCM | 824,17 | 226,58 | 0,335 | 0,037 | 6.123,78 |
AVAC: año de vida ajustado por calidad; HCM: hierro carboximaltosa.
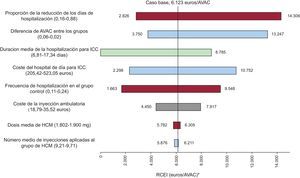
La estabilidad del resultado del caso base se confirmó en los análisis de sensibilidad. En la figura 1 se muestra el diagrama de tornado que representa los resultados del análisis de sensibilidad determinístico. Como puede observarse, la variable más sensible fue la proporción de la reducción de la estancia hospitalaria del paciente tratado con HCM respecto al no tratado, y en el peor caso se alcanza un coste por AVAC ganado de 14.306 euros. En todos los análisis, el coste de ganar 1 AVAC con HCM fue < 30.000 euros, tomado generalmente como el umbral por debajo del cual un tratamiento debe considerarse coste-efectivo en España16.
Resultados del análisis de sensibilidad determinístico. Diagrama de tornado. Cada barra indica la variabilidad del resultado del caso base cuando se utilizan los valores extremos (entre paréntesis) de la variable indicada en el texto de la izquierda. AVAC: año de vida ajustado por calidad; HCM: hierro carboximaltosa; ICC: insuficiencia cardiaca crónica; RCEI: razón coste-efectividad incremental. *Coste por año de vida ajustado por calidad ganado.
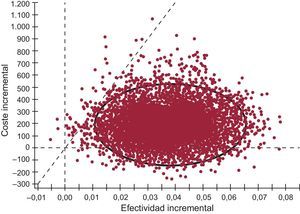
De acuerdo con la simulación de Monte Carlo, la probabilidad de que el HCM sea coste-efectivo (< 30.000 euros/AVAC) y dominante (más eficaz y con menores costes que no tratar) es del 93,0 y el 6,6% respectivamente. El 95% de los RCEI oscilaría entre 4.617 y 13.437 euros/AVAC ganado con HCM frente a la opción de no tratar (figura 2).
Resultado del análisis de sensibilidad probabilístico (simulación de Monte Carlo). Los resultados a la derecha de la línea diagonal discontinua representan los casos en que el tratamiento con hierro carboximaltosa fue coste-efectivo con cocientes de coste/año de vida ajustado por calidad ganado inferiores al umbral de 30.000 euros (lo que ocurrió en el 93,0% de los 10.000 análisis efectuados). En el 6,6% de las simulaciones, el tratamiento con hierro carboximaltosa fue dominante (más eficaz y con menores costes que la opción de no tratar). El círculo engloba el intervalo de confianza del 95% de los resultados de coste-efectividad incremental, que oscilaron entre 4.617 y 13.437 euros por año de vida ajustado por calidad ganado con hierro carboximaltosa frente a la opción de no tratar.
Según el presente estudio económico, el tratamiento con HCM de pacientes con ICC y deficiencia de hierro, con o sin anemia, es coste-efectivo en España, con un coste por AVAC ganado de 6.123,78 euros, en comparación con la opción de no tratar el déficit de hierro, netamente inferior a los 30.000 euros, tomado como el umbral por debajo del cual un tratamiento debe considerarse coste-efectivo en España16. Este resultado coincide con el del modelo originalmente publicado, según el cual el tratamiento con HCM también es coste-efectivo en Reino Unido, con un coste por AVAC ganado que oscilaría entre los 22.200 y los 33.300 euros11. La diferencia en el coste por AVAC, mayor en Reino Unido que en España, se debería principalmente a que la duración media de la hospitalización por ICC es mayor en Reino Unido (11,8 días)11 que en nuestro país (9,32 días)13.
Es de interés poner en contexto estos valores de eficiencia atribuibles al tratamiento con HCM de pacientes con ICC y deficiencia de hierro. En este sentido, según un estudio recientemente publicado17, la profilaxis primaria con implante de desfibrilador en pacientes con cardiopatía (isquémica o no) tendría en Europa un coste por AVAC ganado de 43.993 euros, en comparación con la opción de no utilizar el desfibrilador automático implantable. Por otra parte, en un estudio español se estimó que la terapia de resincronización cardiaca, en comparación con la terapia farmacológica, tendría un coste por AVAC ganado de 28.612 euros y que la resincronización con desfibrilador cuesta 53.547 euros/AVAC, respecto a la resincronización sin desfibrilador18.
LimitacionesEn la valoración de estos resultados se debe en cuenta tanto las posibles limitaciones como las consistencias del estudio. En primer lugar, debe recordarse que se trata de un modelo teórico que es, por definición, una simulación simplificada de la realidad. No obstante, el análisis de coste-efectividad es un instrumento de especial relevancia que facilita a los decisores del Sistema Nacional de Salud la toma de decisiones, ya que permite integrar y comparar la efectividad y los costes de dos opciones en una variable de eficiencia: el coste de ganar 1 AVAC con la opción más efectiva de las comparadas19. Por otra parte, los datos de eficacia a partir de los cuales se calcularon los AVAC ganados para los pacientes tratados con HCM provienen de un ensayo clínico aleatorizado, uno de cuyos objetivos fue comparar la calidad de vida entre pacientes con y sin tratamiento8,12. Este estudio se realizó administrando dosis repetidas de 200 mg de HCM hasta conseguir la repleción de los depósitos de hierro (fase de corrección), alcanzando en esta fase dosis totales medianas de 1.000 mg. En el estudio CONFIRM20,21, con un diseño similar al FAIR-HF, se administró la HCM en un esquema más rápido con dosis iniciales de hasta 1.000 mg, en la línea de lo que aparece en la ficha técnica. Este estudio, recientemente publicado, ha confirmado los resultados del FAIR-HF. Con base en ello, es posible hipotetizar que adoptar un esquema que permita reducir significativamente el número de administraciones (de las cinco que supone la fase de corrección según el esquema del FAIR-HF a una o dos en el esquema del CONFIRM) implicaría un mayor ahorro de costes asociados y, en consecuencia, una eventual reducción del coste por AVAC ganado. Es de esperar que tras la publicación del CONFIRM se pueda llevar a cabo un análisis de coste-efectividad similar al presente estudio.
Una importante limitación del presente análisis es la ausencia de información exhaustiva acerca del uso de recursos sanitarios, tales como los tratamientos concomitantes, la utilización de dispositivos como los marcapasos y los tratamientos ambulatorios, que el estudio FAIR-HF no recogió8,11,12. No obstante, no hay datos que indiquen que el uso de dichos recursos no contabilizados sea diferente entre los pacientes con y sin tratamiento con hierro, por lo que no es de esperar que —de haberse recogido— afectase a los resultados del análisis11.
La fiabilidad del resultado obtenido de coste-efectividad viene dada por los análisis de sensibilidad realizados22. Así, en todos los análisis de sensibilidad determinísticos univariables, el coste de ganar 1 AVAC con HCM fue < 30.000 euros, tomado generalmente como el umbral por debajo del cual un tratamiento debe considerarse coste-efectivo en España16. Además, según la simulación de Monte Carlo, las probabilidades de que el HCM sea coste-efectivo (< 30.000 euros/AVAC) y dominante (más eficaz y con menores costes que no tratar) son del 93,0 y el 6,6% respectivamente.
Otra de las limitaciones de este análisis es que el estudio FAIR-HF solo evaluó el efecto de HCM en pacientes estables con disfunción sistólica del ventrículo izquierdo, por lo que los resultados observados podrían no ser completamente extrapolables a otras poblaciones de pacientes con insuficiencia cardiaca con otros perfiles de estabilidad, función ventricular o comorbilidades. A pesar de ello, el análisis de subgrupos del estudio original, mostró que los resultados eran congruentes en todos los subgrupos especificados en el diseño original del ensayo23.
CONCLUSIONESSegún el presente estudio, el tratamiento con HCM puede considerarse una opción coste-efectiva para los pacientes españoles con ICC y deficiencia de hierro, con o sin anemia.
FINANCIACIÓNEstudio financiado por Vifor Pharma España S.L.
CONFLICTO DE INTERESESNinguno.
Estudio realizado con una ayuda a la investigación, sin restricciones, de Vifor Pharma.