Los stents liberadores de fármaco (farmacoactivos) de segunda generación, en comparación con los stents metálicos sin recubrimiento, reducen la tasa de eventos adversos cardiacos mayores de los pacientes con infarto agudo de miocardio con elevación del segmento ST. El objetivo es evaluar la influencia del sexo del paciente en el resultado obtenido con los stents liberadores de everolimus en comparación con los stents metálicos sin recubrimiento en pacientes con infarto agudo de miocardio con elevación del segmento ST a los 2 años de seguimiento.
MétodosSe llevó a cabo un subestudio del ensayo clínico EXAMINATION, en el que se aleatorizó a 1.498 pacientes con infarto agudo de miocardio con elevación del segmento ST tratados con intervención coronaria percutánea al grupo de stents liberadores de everolimus o al de stents metálicos sin recubrimiento. El objetivo principal fue la combinación de muerte por cualquier causa, cualquier recurrencia de infarto agudo de miocardio y cualquier revascularización. Todos los objetivos se analizaron en función del sexo del paciente en el seguimiento realizado a los 2 años.
ResultadosDe los 1.498 pacientes incluidos en el ensayo, 254 (17,0%) eran mujeres. Las mujeres eran de más edad y tenían mayor prevalencia de hipertensión arterial y menor prevalencia de tabaquismo que los varones. Respecto a los varones, el diámetro máximo del stent en las mujeres resultó menor. Tras realizar un análisis multivariable, el objetivo principal fue similar entre mujeres y varones (hazard ratio=0,95; intervalo de confianza del 95%, 0,66-1,37), y en el análisis realizado sobre las mujeres, fue similar entre tratadas con stents metálicos sin recubrimiento y tratadas con stents liberadores de everolimus (hazard ratio=2,48; intervalo de confianza del 95%, 0,95-6,46). Las mujeres presentaron una tasa de revascularización repetida menor que los varones (hazard ratio=0,55; intervalo de confianza del 95%, 0,32-0,95), a pesar de sus peores características basales. Esta diferencia se explica por un mejor resultado del stent liberador de everolimus en las mujeres.
ConclusionesPese a tener características basales peores, las mujeres con infarto agudo de miocardio con elevación del segmento ST tratadas con intervención coronaria percutánea obtuvieron resultados similares a los de los varones. El uso de stents liberadores de everolimus puede aportar un valor añadido en las mujeres, puesto que se demostró una reducción de la tasa de revascularización repetida en comparación con los varones.
Palabras clave
En Europa cada año mueren por cardiopatía isquémica más de un millón de mujeres. La mortalidad es mayor entre las mujeres que entre los varones1. El sexo del paciente puede tener influencia independiente en los resultados de la intervención coronaria percutánea (ICP)2, con una tasa de reestenosis similar o incluso menor en las mujeres a pesar de que los vasos sean más pequeños que en los varones3. Además, parece que las mujeres obtienen mayor beneficio médico con el tratamiento con stents liberadores de fármaco (farmacoactivos) (SLF)4, y más concretamente con los SLF de segunda generación5.
Los SLF, en comparación con los stents metálicos sin recubrimiento (SMSR), reducen la tasa de reestenosis y las revascularizaciones de la lesión diana en los pacientes con enfermedad coronaria crónica estable, incluidos pacientes de alto riesgo como los diabéticos6–9. En dos ensayos clínicos se ha comparado el uso de SLF de segunda generación con el de SMSR en pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST). En el ensayo clínico EXAMINATION (Evaluation of the Xience-V stent in Acute Myocardial INfarcTION), el uso de un stent liberador de everolimus (SLE) no redujo la tasa de los objetivos orientados al paciente (combinación de muerte por cualquier causa, cualquier recurrencia de infarto de miocardio y cualquier revascularización) en comparación con los SMSR; sin embargo, se observó una incidencia significativamente menor de revascularización repetida y de trombosis del stent en los pacientes con SLE, en comparación con los SMSR10 en el seguimiento a 2 años11. En el ensayo COMFORTABLE AMI, hubo una reducción de la tasa de eventos adversos cardiovasculares mayores (muerte cardiaca, reinfarto del vaso diana y revascularización de la lesión diana a causa de isquemia) al cabo de 1 año con los stents liberadores de biolimus comparados con SMSR12. La información existente sobre los resultados de los SLF de segunda generación en las mujeres con IAMCEST es escasa.
El objetivo del presente estudio es analizar la influencia del sexo del paciente en el resultado de los SLE frente a los SMSR en pacientes con IAMCEST tras 2 años de seguimiento.
MÉTODOSEste es un subestudio del ensayo clínico EXAMINATION (NCT00828087), un estudio multicéntrico, controlado y aleatorizado que incluyó a todos los pacientes consecutivamente10. El ensayo EXAMINATION aleatorizó en proporción 1:1 a un total de 1.498 pacientes con IAMCEST tratados con ICP a los grupos de SLE (Xience®, Abbott Vascular; Santa Clara, California, Estados Unidos) o SMSR (Multi-Link Vision®, Abbott Vascular). La metodología del ensayo clínico EXAMINATION se ha descrito con anterioridad13. De manera resumida, se consideró elegibles para el estudio a todos los pacientes con un IAMCEST que se presentaron en las primeras 48h siguientes al inicio de los síntomas y se sometieron a ICP primaria.
Los criterios de exclusión fueron: lesiones que requerían un tamaño del stent < 2,25 o > 4mm, IAMCEST causado por trombosis de stent, edad < 18 años, embarazo, pacientes con intolerancia conocida a ácido acetilsalicílico, clopidogrel, heparina, cobalto-cromo u otros componentes de los stents. Se excluyó también a los pacientes en tratamiento crónico con anticoagulantes orales. La ICP se llevó a cabo según la práctica médica estándar. Se utilizó heparina no fraccionada, bivalirudina o inhibidores de la glucoproteína IIb/IIIa según el criterio del operador. Antes de la ICP, se administró a los pacientes una dosis de carga de ácido acetilsalicílico (≥ 250mg) y clopidogrel (≥ 300mg). Se prescribió ácido acetilsalicílico (≥ 100mg/día) por tiempo indefinido y clopidogrel (75mg/día) durante ≥ 1 año en ambos grupos.
Todos los centros participantes solicitaron y obtuvieron la aprobación de su correspondiente comité de ética para el protocolo y para el documento de consentimiento informado. El estudio se realizó cumpliendo lo establecido en la Declaración de Helsinki, BS EN ISO 14155 parte 1 y parte 2 y las regulaciones locales aplicables. Todos los pacientes dieron su consentimiento informado por escrito.
Objetivos del estudioLos objetivos del estudio ya se han descrito13. De manera resumida, el objetivo principal es el orientado al paciente, la combinación de muerte por cualquier causa, cualquier recurrencia de infarto de miocardio y cualquier revascularización. Los objetivos secundarios incluyeron el objetivo combinado orientado al dispositivo, la combinación de muerte cardiaca, infarto de miocardio del vaso diana y revascularización de la lesión diana; la mortalidad por cualquier causa y la cardiaca; la recurrencia de infarto de miocardio (definición ampliada de la Organización Mundial de la Salud)14; la revascularización de la lesión diana; la revascularización del vaso diana; la trombosis de stent (según las definiciones del Academic Research Consortium)15; el éxito del dispositivo y de la intervención, y las hemorragias mayores y menores. Todos los eventos clínicos los validó un comité independiente de valoración de eventos clínicos (Cardialysis, Rotterdam, Países Bajos) según las definiciones del Academic Research Consortium15. Para los fines de este subestudio, todos los objetivos se analizaron según el sexo del paciente (grupo de mujeres y grupo de varones).
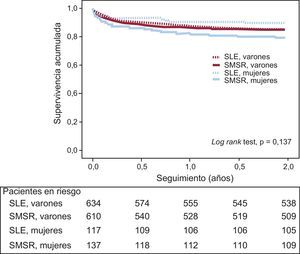
Análisis estadísticoLa cohorte de estudio se estratificó según el sexo (mujeres o varones). El análisis por grupos de sexo se había especificado a priori en el ensayo clínico EXAMINATION10. Para las variables continuas, se examinó la normalidad de la distribución con la prueba de Kolmogorov-Smirnov. Las variables de distribución normal se expresan en forma de media ± desviación estándar y las de distribución no normal, como mediana [intervalo intercuartílico]. Las variables discretas se expresan en número (porcentaje). Las características basales de cada sexo se compararon con la prueba de la t de Student para las variables continuas y la prueba de la χ2 para las variables discretas. Se elaboraron curvas de supervivencia comparativas de los cuatro grupos (SLE, varones; SMSR, varones; SLE, mujeres; SMSR, mujeres) para la evaluación del objetivo principal con los métodos de Kaplan-Meier, y se compararon mediante log rank test.
Para evaluar la posible asociación entre el sexo y los objetivos, se realizaron análisis de regresión de Cox de riesgos proporcionales. Se llevó a cabo un análisis exploratorio univariable entre el sexo y las variables de tratamiento. Las covariables para las que había una justificación clínica o un valor de p<0,10 se incluyeron en los modelos de Cox, y se incluyó también en el modelo un término de interacción entre tratamiento y sexo. Si el valor de p para el término de interacción era < 0,05, se consideraba que había una modificación del efecto. Se observó una interacción significativa entre el grupo de tratamiento y el sexo en los siguientes objetivos: a) mortalidad por cualquier causa; b) cualquier revascularización; c) revascularización de la lesión diana, y d) revascularización del vaso diana. Se realizaron análisis de regresión de Cox para cada uno de los objetivos. El modelo de Cox se eligió según el criterio de información de Akaike. El supuesto de riesgos proporcionales para el modelo de Cox se evaluó visualmente con un gráfico Log-Log para asegurar el paralelismo. Los modelos de Cox finales para cada objetivo con una medida del criterio de información de Akaike, el estadístico C y los valores de p para el término de interacción se presentan en .
Los resultados se presentaron en forma de razones de riesgos (HR), junto con los intervalos de confianza del 95% (IC95%). Se evaluó la potencia estadística para detectar diferencias entre los grupos de estudio con un error de tipo I bilateral α=0,05. Todos los valores de p fueron bilaterales, con un nivel de significación estadística de p<0,05. Los análisis estadísticos se realizaron con la versión 2.1 del programa estadístico R (R Development Core Team).
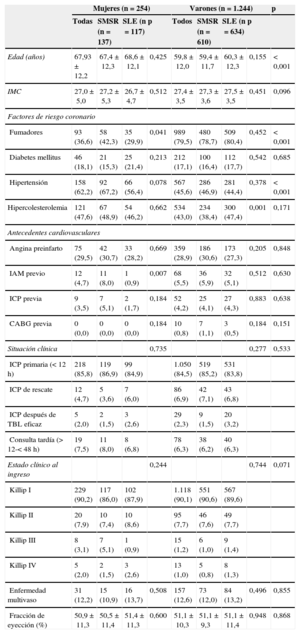
RESULTADOSCaracterísticas basales demográficas, clínicas y de la intervenciónDe los 1.498 pacientes incluidos en la asignación aleatoria del ensayo, un total de 254 (17,0%) mujeres fueron tratadas con un SMSR (n=137; 53,9%) o un SLE (n=117; 46,1%). Los 1.244 pacientes varones fueron tratados con un SMSR (n=610; 49,0%) o un SLE (n=634; 51,0%). Las características demográficas y clínicas basales de todos los pacientes se presentan en la tabla 1. Las mujeres eran de más edad, eran fumadoras en menor número y tenían mayor prevalencia de hipertensión arterial que los varones. Entre las mujeres, las asignadas a SMSR tenían mayores prevalencias de infarto de miocardio previo y de tabaquismo.
Características demográficas y clínicas basales
| Mujeres (n=254) | Varones (n=1.244) | p | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Todas | SMSR (n=137) | SLE (n=117) | p | Todos | SMSR (n=610) | SLE (n=634) | p | ||
| Edad (años) | 67,93±12,2 | 67,4±12,3 | 68,6±12,1 | 0,425 | 59,8±12,0 | 59,4±11,7 | 60,3±12,3 | 0,155 | < 0,001 |
| IMC | 27,0±5,0 | 27,2±5,3 | 26,7±4,7 | 0,512 | 27,4±3,5 | 27,3±3,6 | 27,5±3,5 | 0,451 | 0,096 |
| Factores de riesgo coronario | |||||||||
| Fumadores | 93 (36,6) | 58 (42,3) | 35 (29,9) | 0,041 | 989 (79,5) | 480 (78,7) | 509 (80,4) | 0,452 | < 0,001 |
| Diabetes mellitus | 46 (18,1) | 21 (15,3) | 25 (21,4) | 0,213 | 212 (17,1) | 100 (16,4) | 112 (17,7) | 0,542 | 0,685 |
| Hipertensión | 158 (62,2) | 92 (67,2) | 66 (56,4) | 0,078 | 567 (45,6) | 286 (46,9) | 281 (44,4) | 0,378 | < 0,001 |
| Hipercolesterolemia | 121 (47,6) | 67 (48,9) | 54 (46,2) | 0,662 | 534 (43,0) | 234 (38,4) | 300 (47,4) | 0,001 | 0,171 |
| Antecedentes cardiovasculares | |||||||||
| Angina preinfarto | 75 (29,5) | 42 (30,7) | 33 (28,2) | 0,669 | 359 (28,9) | 186 (30,6) | 173 (27,3) | 0,205 | 0,848 |
| IAM previo | 12 (4,7) | 11 (8,0) | 1 (0,9) | 0,007 | 68 (5,5) | 36 (5,9) | 32 (5,1) | 0,512 | 0,630 |
| ICP previa | 9 (3,5) | 7 (5,1) | 2 (1,7) | 0,184 | 52 (4,2) | 25 (4,1) | 27 (4,3) | 0,883 | 0,638 |
| CABG previa | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0,184 | 10 (0,8) | 7 (1,1) | 3 (0,5) | 0,184 | 0,151 |
| Situación clínica | 0,735 | 0,277 | 0,533 | ||||||
| ICP primaria (< 12 h) | 218 (85,8) | 119 (86,9) | 99 (84,9) | 1.050 (84,5) | 519 (85,2) | 531 (83,8) | |||
| ICP de rescate | 12 (4,7) | 5 (3,6) | 7 (6,0) | 86 (6,9) | 42 (7,1) | 43 (6,8) | |||
| ICP después de TBL eficaz | 5 (2,0) | 2 (1,5) | 3 (2,6) | 29 (2,3) | 9 (1,5) | 20 (3,2) | |||
| Consulta tardía (> 12-< 48 h) | 19 (7,5) | 11 (8,0) | 8 (6,8) | 78 (6,3) | 38 (6,2) | 40 (6,3) | |||
| Estado clínico al ingreso | 0,244 | 0,744 | 0,071 | ||||||
| Killip I | 229 (90,2) | 117 (86,0) | 102 (87,9) | 1.118 (90,1) | 551 (90,6) | 567 (89,6) | |||
| Killip II | 20 (7,9) | 10 (7,4) | 10 (8,6) | 95 (7,7) | 46 (7,6) | 49 (7,7) | |||
| Killip III | 8 (3,1) | 7 (5,1) | 1 (0,9) | 15 (1,2) | 6 (1,0) | 9 (1,4) | |||
| Killip IV | 5 (2,0) | 2 (1,5) | 3 (2,6) | 13 (1,0) | 5 (0,8) | 8 (1,3) | |||
| Enfermedad multivaso | 31 (12,2) | 15 (10,9) | 16 (13,7) | 0,508 | 157 (12,6) | 73 (12,0) | 84 (13,2) | 0,496 | 0,855 |
| Fracción de eyección (%) | 50,9±11,3 | 50,5±11,4 | 51,4±11,3 | 0,600 | 51,1±10,3 | 51,1±9,3 | 51,1±11,4 | 0,948 | 0,868 |
CABG: cirugía de revascularización aortocoronaria; IAM: infarto agudo de miocardio; ICP: intervención coronaria percutánea; IM: infarto de miocardio; IMC: índice de masa corporal; SLE: stents liberadores de everolimus; SMSR: stent metálico sin recubrimiento; TBL: trombolisis.
Los datos expresan n (%) o media ± desviación estándar.
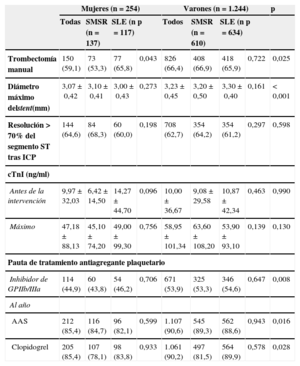
En comparación con los varones, en las mujeres se utilizaron menos trombectomía manual e inhibidores de la glucoproteína IIb/IIIa. En las mujeres asignadas a SLE se usó más la trombectomía manual que en las asignadas a SMSR. En general, los stents implantados a las mujeres eran de menor tamaño que los utilizados en los varones (tabla 2).
Características de la intervención, biomarcadores y tratamiento antiagregante plaquetario en el seguimiento a 1 año
| Mujeres (n=254) | Varones (n=1.244) | p | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Todas | SMSR (n=137) | SLE (n=117) | p | Todos | SMSR (n=610) | SLE (n=634) | p | ||
| Trombectomía manual | 150 (59,1) | 73 (53,3) | 77 (65,8) | 0,043 | 826 (66,4) | 408 (66,9) | 418 (65,9) | 0,722 | 0,025 |
| Diámetro máximo delstent(mm) | 3,07±0,42 | 3,10±0,41 | 3,00±0,43 | 0,273 | 3,23±0,45 | 3,20±0,50 | 3,30±0,40 | 0,161 | < 0,001 |
| Resolución > 70% del segmento ST tras ICP | 144 (64,6) | 84 (68,3) | 60 (60,0) | 0,198 | 708 (62,7) | 354 (64,2) | 354 (61,2) | 0,297 | 0,598 |
| cTnI (ng/ml) | |||||||||
| Antes de la intervención | 9,97±32,03 | 6,42±14,50 | 14,27±44,70 | 0,096 | 10,00±36,67 | 9,08±29,58 | 10,87±42,34 | 0,463 | 0,990 |
| Máximo | 47,18±88,13 | 45,10±74,20 | 49,00±99,30 | 0,756 | 58,95±101,34 | 63,60±108,20 | 53,90±93,10 | 0,139 | 0,130 |
| Pauta de tratamiento antiagregante plaquetario | |||||||||
| Inhibidor de GPIIb/IIIa | 114 (44,9) | 60 (43,8) | 54 (46,2) | 0,706 | 671 (53,9) | 325 (53,3) | 346 (54,6) | 0,647 | 0,008 |
| Al año | |||||||||
| AAS | 212 (85,4) | 116 (84,7) | 96 (82,1) | 0,599 | 1.107 (90,6) | 545 (89,3) | 562 (88,6) | 0,943 | 0,016 |
| Clopidogrel | 205 (85,4) | 107 (78,1) | 98 (83,8) | 0,933 | 1.061 (90,2) | 497 (81,5) | 564 (89,9) | 0,578 | 0,028 |
AAS: ácido acetilsalicílico; cTnI: troponina I cardiaca; GPIIb/IIIa: glucoproteína IIb/IIIa; ICP: intervención coronaria percutánea; SLE: stents liberadores de everolimus; SMSR: stent metálico sin recubrimiento.
Los datos expresan n (%) o media±desviación estándar.
La adherencia al tratamiento antiagregante plaquetario combinado doble a 1 año fue menor en las mujeres que en los varones (tabla 2).
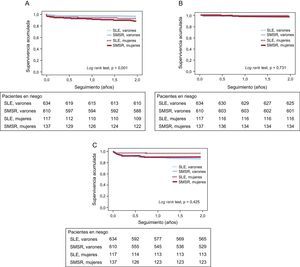
Resultados clínicosVarones frente a mujeresLos resultados clínicos comparativos entre mujeres y varones se presentan en la tabla 3. Después de 2 años de seguimiento, tanto el objetivo principal orientado al paciente (figura 1) como el orientado al dispositivo (figura 2) fueron similares entre mujeres y varones.
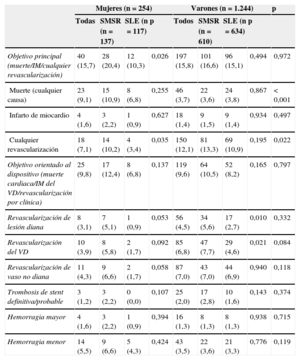
Resumen de los objetivos de valoración del estudio a los 2 años de seguimiento, con estratificación según el sexo
| Mujeres (n=254) | Varones (n=1.244) | p | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Todas | SMSR (n=137) | SLE (n=117) | p | Todos | SMSR (n=610) | SLE (n=634) | p | ||
| Objetivo principal (muerte/IM/cualquier revascularización) | 40 (15,7) | 28 (20,4) | 12 (10,3) | 0,026 | 197 (15,8) | 101 (16,6) | 96 (15,1) | 0,494 | 0,972 |
| Muerte (cualquier causa) | 23 (9,1) | 15 (10,9) | 8 (6,8) | 0,255 | 46 (3,7) | 22 (3,6) | 24 (3,8) | 0,867 | < 0,001 |
| Infarto de miocardio | 4 (1,6) | 3 (2,2) | 1 (0,9) | 0,627 | 18 (1,4) | 9 (1,5) | 9 (1,4) | 0,934 | 0,497 |
| Cualquier revascularización | 18 (7,1) | 14 (10,2) | 4 (3,4) | 0,035 | 150 (12,1) | 81 (13,3) | 69 (10,9) | 0,195 | 0,022 |
| Objetivo orientado al dispositivo (muerte cardiaca/IM del VD/revascularización por clínica) | 25 (9,8) | 17 (12,4) | 8 (6,8) | 0,137 | 119 (9,6) | 64 (10,5) | 52 (8,2) | 0,165 | 0,797 |
| Revascularización de lesión diana | 8 (3,1) | 7 (5,1) | 1 (0,9) | 0,053 | 56 (4,5) | 34 (5,6) | 17 (2,7) | 0,010 | 0,332 |
| Revascularización del VD | 10 (3,9) | 8 (5,8) | 2 (1,7) | 0,092 | 85 (6,8) | 47 (7,7) | 29 (4,6) | 0,021 | 0,084 |
| Revascularización de vaso no diana | 11 (4,3) | 9 (6,6) | 2 (1,7) | 0,058 | 87 (7,0) | 43 (7,0) | 44 (6,9) | 0,940 | 0,118 |
| Trombosis de stent definitiva/probable | 3 (1,2) | 3 (2,2) | 0 (0,0) | 0,107 | 25 (2,0) | 17 (2,8) | 10 (1,6) | 0,143 | 0,374 |
| Hemorragia mayor | 4 (1,6) | 3 (2,2) | 1 (0,9) | 0,394 | 16 (1,3) | 8 (1,3) | 8 (1,3) | 0,938 | 0,715 |
| Hemorragia menor | 14 (5,5) | 9 (6,6) | 5 (4,3) | 0,424 | 43 (3,5) | 22 (3,6) | 21 (3,3) | 0,776 | 0,119 |
IM: infarto de miocardio; SLE: stents liberadores de everolimus; SMSR: stent metálico sin recubrimiento; VD: vaso diana.
Los datos expresan n (%).
Se observó una mortalidad significativamente mayor en las mujeres que en los varones. Tras el análisis multivariable, esta diferencia deja de ser significativa (HR=1,4; IC95%, 0,75-2,72).
Las mujeres presentaron una tasa de revascularizacion repetida menor que la de los varones, incluso después de introducir un ajuste respecto a posibles factores de confusión (HR=0,55; IC95%, 0,31-0,95). La potencia estadística para detectar diferencias en la tasa de revascularización repetida, entre el 12,1% de los varones y el 7,1% de las mujeres, fue del 73,3%.
No se observaron diferencias entre mujeres y varones en la trombosis de stent definitiva/probable. Las tasas de hemorragias mayores y menores fueron similares entre ambos grupos.
Stent liberador de everolimus frente a stent metálico sin recubrimiento en las mujeresLos resultados clínicos comparativos de los SLE frente a los SMSR en las mujeres se presentan en la tabla 4. El objetivo principal fue significativamente mayor en las mujeres tratadas con SMSR que en las tratadas con SLE (HR=2,1; IC95%, 1,07-4,12). Tras el análisis multivariable, esta diferencia deja de ser significativa (HR=2,49; IC95%, 0,95-6,46). La potencia estadística —con un error de tipo I bilateral α=0,05 para la detección de una reducción en la tasa de la variable de valoración principal en las mujeres, entre el 20,4% del grupo de SMSR y el 10,3% del grupo de SLE— fue del 59,9%. Asumiendo el mismo nivel de error de tipo I bilateral, la potencia estadística fue del 20,1, el 12,0 y el 56,1%, respectivamente, para detectar una reducción de la tasa de mortalidad entre el 10,9% del grupo de SMSR y el 6,8% del grupo de SLE, una reducción del infarto de miocardio entre el 2,2% del grupo de SMSR y el 0,9% del grupo de SLE, y una reducción de cualquier revascularización entre el 10,2% del grupo de SMSR y el 3,4% del grupo de SLE.
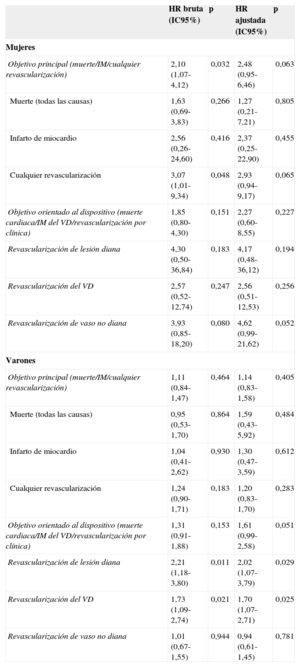
Resumen de los modelos de riesgos proporcionales de Cox (stent metálico sin recubrimiento comparado con stent liberador de everolimus por sexos) a los 2 años de seguimiento
| HR bruta (IC95%) | p | HR ajustada (IC95%) | p | |
|---|---|---|---|---|
| Mujeres | ||||
| Objetivo principal (muerte/IM/cualquier revascularización) | 2,10 (1,07-4,12) | 0,032 | 2,48 (0,95-6,46) | 0,063 |
| Muerte (todas las causas) | 1,63 (0,69-3,83) | 0,266 | 1,27 (0,21-7,21) | 0,805 |
| Infarto de miocardio | 2,56 (0,26-24,60) | 0,416 | 2,37 (0,25-22,90) | 0,455 |
| Cualquier revascularización | 3,07 (1,01-9,34) | 0,048 | 2,93 (0,94-9,17) | 0,065 |
| Objetivo orientado al dispositivo (muerte cardiaca/IM del VD/revascularización por clínica) | 1,85 (0,80-4,30) | 0,151 | 2,27 (0,60-8,55) | 0,227 |
| Revascularización de lesión diana | 4,30 (0,50-36,84) | 0,183 | 4,17 (0,48-36,12) | 0,194 |
| Revascularización del VD | 2,57 (0,52-12,74) | 0,247 | 2,56 (0,51-12,53) | 0,256 |
| Revascularización de vaso no diana | 3,93 (0,85-18,20) | 0,080 | 4,62 (0,99-21,62) | 0,052 |
| Varones | ||||
| Objetivo principal (muerte/IM/cualquier revascularización) | 1,11 (0,84-1,47) | 0,464 | 1,14 (0,83-1,58) | 0,405 |
| Muerte (todas las causas) | 0,95 (0,53-1,70) | 0,864 | 1,59 (0,43-5,92) | 0,484 |
| Infarto de miocardio | 1,04 (0,41-2,62) | 0,930 | 1,30 (0,47-3,59) | 0,612 |
| Cualquier revascularización | 1,24 (0,90-1,71) | 0,183 | 1,20 (0,83-1,70) | 0,283 |
| Objetivo orientado al dispositivo (muerte cardiaca/IM del VD/revascularización por clínica) | 1,31 (0,91-1,88) | 0,153 | 1,61 (0,99-2,58) | 0,051 |
| Revascularización de lesión diana | 2,21 (1,18-3,80) | 0,011 | 2,02 (1,07-3,79) | 0,029 |
| Revascularización del VD | 1,73 (1,09-2,74) | 0,021 | 1,70 (1,07-2,71) | 0,025 |
| Revascularización de vaso no diana | 1,01 (0,67-1,55) | 0,944 | 0,94 (0,61-1,45) | 0,781 |
HR: hazard ratio; IC95%: intervalo de confianza del 95%; IM: infarto de miocardio; VD: vaso diana.
Las mujeres tratadas con SLE presentaron una tasa de revascularización repetida menor que las tratadas con SMSR. Esta asociación no alcanza la significación estadística después de introducir un ajuste por factores de confusión (HR=2,93; IC95%, 0,94-9,17). Las mujeres tratadas con SLE presentaron tendencia a menor riesgo de trombosis de stent definitiva o probable que las tratadas con SMSR (el 2,2 frente al 0,0%; p=0,107). Todos los eventos fueron numéricamente superiores en el grupo de SMSR, sin alcanzar la significación estadística.
DISCUSIÓNLos resultados principales de este estudio pueden resumirse así: a) no se observaron diferencias en la variable de valoración principal entre varones y mujeres ni entre mujeres tratadas con SLE y tratadas con SMSR; b) las mujeres con IAMCEST presentaron una mortalidad a largo plazo superior a la de los varones; sin embargo, después de aplicar ajustes multivariables, esta diferencia dejó de ser significativa, y c) las mujeres presentaron menos riesgo de nueva revascularización tras un IAMCEST que los varones.
Aunque las mujeres con IAMCEST presentaron mayor mortalidad que los varones a los 2 años de seguimiento, tras un ajuste respecto a las diferencias en el perfil clínico y en el tratamiento, el sexo del paciente dejó de ser un factor independiente de riesgo de muerte después de un IAMCEST. Estos resultados concuerdan con los de varios estudios que describen diferencias asociadas al sexo en el perfil clínico, el tratamiento y los resultados en los pacientes con IAMCEST16–19. Las diferencias de edad, tratamiento y comorbilidades pueden explicar en parte estas observaciones20–22. Además, se ha demostrado que a las mujeres con IAMCEST se las trata menos frecuentemente mediante ICP primaria, debido al retraso en el diagnóstico como consecuencia de la presencia de síntomas atípicos23.
El menor uso en mujeres que en varones de tratamientos eficaces se ha asociado a peor pronóstico. En este estudio, fue menos frecuente el uso de trombectomía manual e inhibidores de la glucoproteína IIb/IIIa en las mujeres que en los varones. A pesar de la diferencia previa, la resolución del segmento ST tras la intervención fue similar en ambos grupos.
En el presente estudio, las mujeres presentaron una tasa de revascularización repetida menor que la de los varones. La diferencia se debía principalmente a una tasa de revascularizacion repetida menor en las mujeres tratadas con SLE. La revascularización de la lesión diana mostró una tendencia a valores inferiores, sin alcanzar significación estadística. Las mujeres tratadas con SLE tuvieron la tasa de revascularización más baja de todos los grupos. Las mujeres y los varones asignados a SMSR tuvieron tasas de revascularización similares. Se ha apuntado que las mujeres tienen mayor riesgo de deterioro luminal en respuesta a la formación de neoíntima debido a que el tamaño de los vasos es menor que en los varones4. El hecho de que las mujeres presenten menor riesgo de reestenosis a pesar de unas características basales más desfavorables se ha denominado «paradoja del sexo»2,24–26. En un estudio reciente se ha evaluado la influencia del sexo en los resultados de los SLF de primera generación, y se ha observado una reducción de la tasa de nueva revascularizacion en mujeres, en comparación con los varones, tras el uso de stents liberadores de paclitaxel27 y stents liberadores de sirolimus28. Lansky et al29 evaluaron el papel del sexo del paciente en la eficacia de los SLE en comparación con los stents liberadores de paclitaxel, en un análisis post-hoc. Tras 1 año de seguimiento, las mujeres tratadas con SLE presentaron una tasa de nueva revascularización significativamente inferior a la de las tratadas con stents liberadores de paclitaxel29. Nakatani et al26 demostraron que el sexo femenino se asocia de manera independiente a menor obstrucción por neoíntima y menor estenosis transversal máxima en los pacientes tratados con stents liberadores de zotarolimus. Por el contrario, las mujeres tratadas con SMSR presentaron mayor obstrucción por neoíntima que los varones, aunque esta observación dejaba de ser significativa tras introducir un ajuste respecto a las características basales, lo cual indica ausencia de diferencias en función del sexo por lo que respecta a la hiperplasia de neoíntima tras implante de un SMSR26. La razón de esta paradoja no se ha esclarecido por completo. Se ha propuesto la interacción entre diabetes mellitus y sexo del paciente como posible causa3. Sin embargo, las mujeres y los varones de este estudio presentaron similares prevalencias de diabetes mellitus. Se observó también una tasa inferior, que casi alcanzaba significación estadística, de las revascularizaciones de vasos distintos del vaso diana en los SLE en comparación con los SMSR en las mujeres, lo que podría haberse debido al diseño del estudio: la asignación del tratamiento no se realizó con un diseño ciego para los operadores, y podría haberse seguido una estrategia diferente en el tratamiento de las lesiones distintas de la lesión culpable.
La composición de la placa puede desempeñar un papel en las diferencias observadas en los resultados. Un estudio reciente ha confirmado una diferencia específica según el sexo en la extensión y la composición de las placas coronarias. Ruiz-García et al30 realizaron estudios de imagen de las características in vivo y la composición de las lesiones no culpables no tratadas, con ecografía intravascular de escala de grises y de radiofrecuencia, en pacientes con síndromes coronarios agudos. Las mujeres de menos de 65 años de edad presentaron una cifra inferior de lesiones no culpables, fibroateromas y longitud total de la lesión, en comparación con los varones. Se observó rotura de placa con mayor frecuencia en los varones que en las mujeres30. Las diferencias asociadas al sexo en cuanto a las características de las placas desaparecían con la edad. En estudios no controlados, el sesgo de consulta podría explicar la menor tasa de revascularizaciones de las mujeres en comparación con los varones31.
Tras la preocupación inicial generada respecto al uso de SLF en pacientes con IAMCEST, en varios ensayos se ha descrito la seguridad y la eficacia de los SLF en el IAMCEST, con similares tasas de muerte, reinfarto y trombosis de stent, y una reducción de las reestenosis angiográficas y clínicas, con máximo beneficio observado en los pacientes con riesgo elevado de reestenosis con los SMSR10,12,32. Los resultados del presente estudio son tranquilizadores y confirman que no hay problemas de seguridad asociados al sexo del paciente tras el uso de SLE en mujeres con IAMCEST.
LimitacionesLos resultados del estudio se basan en el análisis de un ensayo con resultado negativo y se debe interpretarlos como generadores de hipótesis. Además, la revascularización se decidió por motivos clínicos, lo que podría haber llevado a un menor uso en las mujeres debido a una menor solicitud de nuevos cateterismos, y no por menos reestenosis. Por otra parte, debido a la elevada tasa de error de tipo II (el 40,1% para el objetivo principal, el 79,9% para muerte, el 88% para el infarto de miocardio y el 43,9% para cualquier revascularización), estos resultados deben interpretarse con precaución.
El menor uso de la trombectomía manual en las mujeres debe tenerse en cuenta al interpretar los resultados. Por último, en este estudio no se evaluó el estado menopáusico. Sin embargo, teniendo en cuenta la edad de las mujeres incluidas en el ensayo clínico EXAMINATION, es probable que la mayoría de las participantes fueran posmenopáusicas.
CONCLUSIONESA pesar de sus peores características basales, las mujeres con IAMCEST tratadas con ICP presentaron similares resultados que los varones, con una tasa inferior de nueva revascularización.
CONFLICTO DE INTERESESNinguno.
Antonio Serra, Hospital Universitario de Sant Pau, Barcelona, España; Rosana Hernández-Antolín, Hospital Universitario San Carlos, Madrid, España; Vicente Mainar, Hospital General de Alicante, Alicante, España; Marco Valgimigli, University Hospital Ferrara, Ferrara, Italia; Maurizio Tespili, University Hospital Bolognini Seriate, Bérgamo, Italia; Pieter den Heijer, Amphia Ziekenhuis, Breda, Países Bajos; Armando Bethencourt, Hospital Son Espases, Palma de Mallorca, España; Nicolás Vázquez, Hospital A Coruña, A Coruña, España; Bianca Backx y Gerrit-Anne van Es, Cardialysis, Rotterdam, Países Bajos.