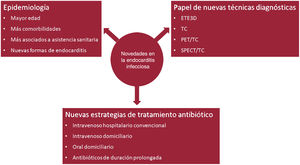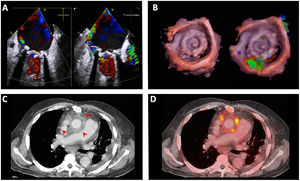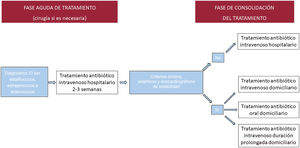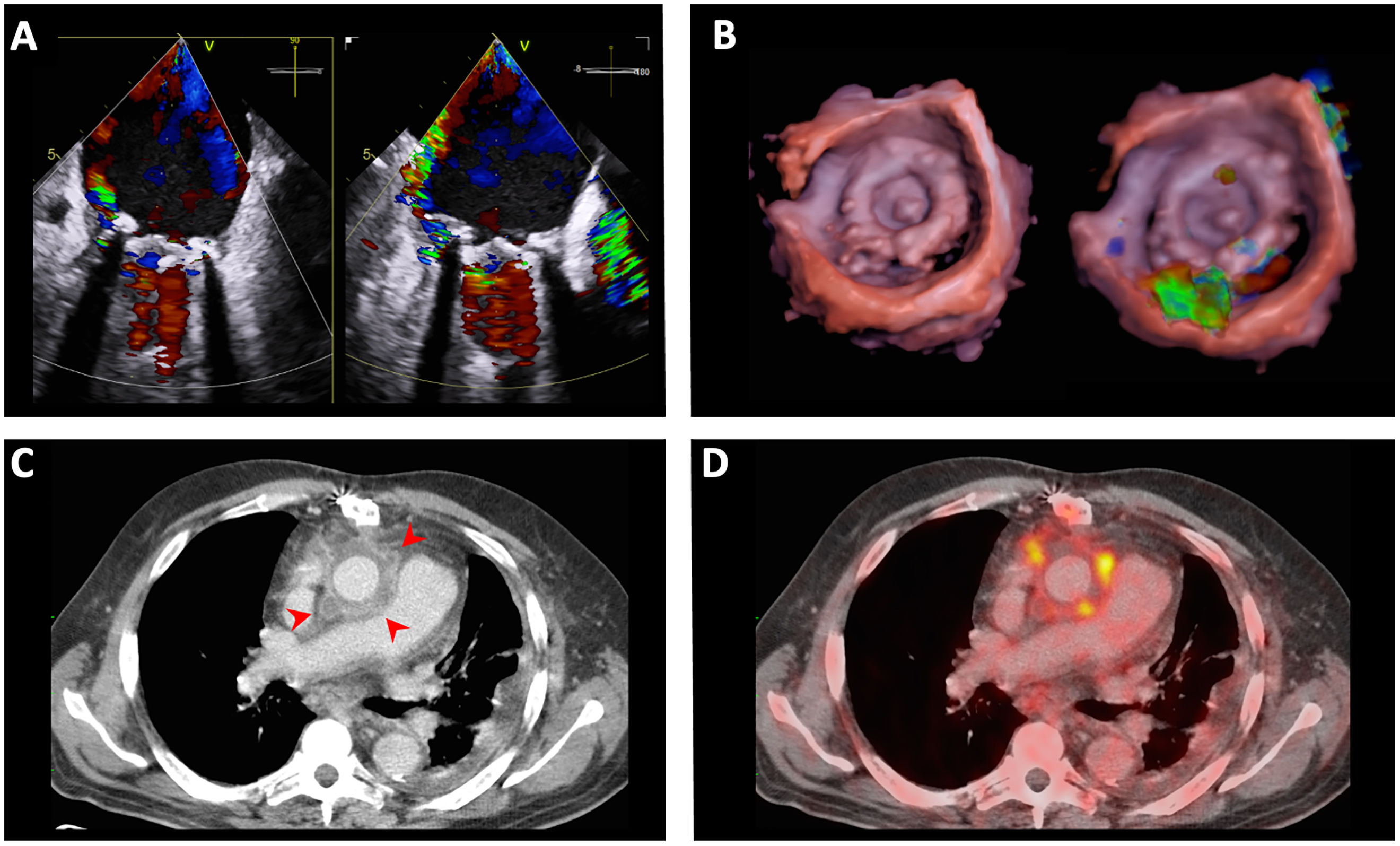
La endocarditis infecciosa es una enfermedad en continuo cambio. Los pacientes atendidos en la actualidad en nada se parecen a los de hace unas décadas: son de más edad, tienen más comorbilidades y más episodios asociados con los cuidados sanitarios. Además, han surgido nuevos grupos de pacientes con formas de endocarditis que antes no existían, como las que afectan a portadores de implantes percutáneos de prótesis valvulares. Las técnicas para el diagnóstico de la enfermedad también han cambiado. Aunque las ecocardiografías transtorácicas y transesofágicas siguen siendo las pruebas de imagen más utilizadas, cada vez son más frecuentes otras técnicas, como la ecografía transesofágica tridimensional, la tomografía computarizada cardiaca y las pruebas de medicina nuclear (PET-TC y SPECT-TC) tanto en el diagnóstico de la enfermedad como en sus complicaciones. En los últimos años también ha habido novedades muy significativas respecto al tratamiento antibiótico. En la actualidad contamos con diferentes estrategias de tratamiento para acortar la fase hospitalaria de pacientes concretos y reducir las complicaciones asociadas con el ingreso, mejorar la calidad de vida de los pacientes y sus familiares y reducir el coste sanitario relacionado con la enfermedad. En esta revisión, se comentan las principales novedades epidemiológicas, diagnósticas y terapéuticas de la endocarditis infecciosa.
Palabras clave
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Precio: 19,34 €
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h