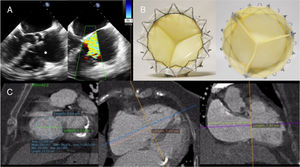
Se presenta el caso de una mujer de 76 años seguida en nuestro hospital por insuficiencia cardiaca derecha. La paciente tenía antecedentes de hipertensión arterial, diabetes mellitus, fibrilación auricular permanente y enfermedad renal crónica en diálisis. Los síntomas de insuficiencia cardiaca habían empeorado en los últimos meses y habían requerido un aumento del número de diálisis e incluso paracentesis evacuadoras. En el estudio ecocardiográfico se observó una insuficiencia tricuspídea (IT) grave debida a dilatación anular y con un importante defecto de coaptación entre los velos (figura 1A, ). La fracción de eyección del ventrículo izquierdo era normal, así como la presión pulmonar y la función del ventrículo derecho. Tras discutirlo en el equipo multidisciplinario compuesto por cardiólogos intervencionistas, cardiólogos especialistas en imagen, cardiólogos clínicos, anestesistas y cirujanos cardiacos, se decidió que la cirugía convencional tenía muy alto riesgo (EuroScore II, 8,6%), pero se le ofreció la posibilidad de implantarle vía percutánea una nueva prótesis en posición tricuspídea, bajo instancia de uso compasivo, en reemplazo de la válvula nativa. El dispositivo se denomina GATE system (NaviGate CSI; Lake Forest, California, Estados Unidos) y es una bioprótesis de velos de xenopericardio insertados en un armazón autoexpandible de nitinol (figura 1B). El stent de nitinol es más ancho en la zona ventricular, lo que le confiere una morfología troncocónica que le permite reducir el gradiente transvalvular (dicha configuración genera una entrada divergente en la cavidad ventricular derecha que permite un enlentecimiento del flujo de la sangre que entra y, por lo tanto, una reducción de la pérdida de energía y de la separación de flujo, con lo cual se optimiza el gradiente) y minimizar la obstrucción del tracto de salida, ya que el material que protruye al ventrículo es poco. Actualmente se puede implantar por vía yugular o por acceso transauricular derecho a través de minitoracotomía y se dispone de 5 tamaños (36, 40, 44, 48 y 52 mm). Para la correcta selección del tamaño, se necesita un análisis de ecocardiografía transesofágica y una tomografía computarizada cardiaca con vistas a medir el anillo tricúspide de la manera más precisa y la relación entre este y la arteria coronaria derecha (figura 1C). Se recomienda sobredimensionar ligeramente la prótesis respecto al tamaño del anillo (< 5-10%). En nuestro caso, el diámetro promedio del anillo por ambos métodos fue de 42,2 mm, por lo que se seleccionó la prótesis de 44 mm.
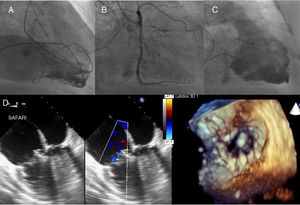
El procedimiento se realizó con anestesia general y guiado por ecocardiografía transesofágica. Se colocó un catéter guía con una guía intracoronaria en la coronaria derecha para marcar el anillo tricúspide y que sirviera de referencia en el implante. Además, se colocó una guía de alto soporte en el ventrículo izquierdo por si se precisase estimulación durante el implante (no fue necesario) y un pigtail en el ventrículo derecho para valorar la IT y el resultado final (figura 2A). En nuestro caso se optó por el acceso transauricular, ya que la vena yugular tenía un calibre límite para el introductor del dispositivo. Tras conseguir el acceso, a través del cuarto espacio intercostal, se insertó una guía de alto soporte en el ventrículo derecho, y a través de ella se colocó el introductor del dispositivo (42 Fr). Luego se avanzó el sistema de liberación de la válvula y, una vez en posición y perfectamente coaxiales al plano del anillo, se procedió a liberarla con control ecográfico y fluoroscópico. Una vez desplegada, por ecocardiografía transesofágica y ventriculografía derecha, se comprobó el resultado y la ausencia de deterioro de la coronaria derecha (figura 2B, 2C y 2D y ). El implante concluyó exitosamente con extubación a las 6 h, y se dio de alta a la paciente. En el seguimiento a los 3 meses, mostraba importante mejoría clínica, sin datos de congestión (sin edema ni ascitis), y reducción del número de sesiones de diálisis y el volumen de extracción. El ecocardiograma de control en esa fecha mostraba el normal funcionamiento de la prótesis, sin gradiente o fugas residuales significativas ().
Procedimiento. A: catéter guía y guía intracoronaria en la coronaria derecha, guía de alto soporte en el ventrículo izquierdo y pigtail en el ventrículo derecho. B: ausencia de daño en la coronaria tras el implante. C: válvula implantada, sin regurgitación residual ni obstrucción del tracto de salida. D: resultado ecográfico del implante.
Los pacientes con IT e insuficiencia cardiaca secundaria suelen estar muy sintomáticos debido al descenso en el gasto cardiaco y la congestión periférica y abdominal. Además, la presencia de IT moderada o grave se asocia con una elevada mortalidad, independientemente de la función biventricular y las presiones pulmonares1. Los datos actuales respaldan la reparación tricuspídea en el momento de las cirugías que se lleven a cabo en el corazón izquierdo; sin embargo, la reoperación por IT persistente o recurrente se asocia con una alta morbimortalidad2,3. Es por ello que, en estos casos, las técnicas percutáneas de reparación tricuspídea emergen como una alternativa a la cirugía convencional4. De todos ellos, el que acumula mayor experiencia clínica es el MitraClip en posición tricuspídea5. Sin embargo, existen condicionantes anatómicos que hacen que su uso no sea ideal, como defectos de coaptación muy grandes (> 7 mm) o presencia del chorro fuera de la zona anteroseptal. En estos casos, otros dispositivos pueden tener su lugar, como el aquí presentado. El sistema GATE es el primer sistema que consigue un reemplazo completo de la válvula en posición ortotópica y produce así la completa abolición de la IT. Este dispositivo ha mostrado buenos datos en modelo preclínico (seguridad en el implante y datos adecuados en cuanto a gradiente, ausencia de obstrucción del tracto de salida, fugas perivalvulares, daño en las arterias coronarias y trombosis o calcificación de los velos), y ya se han realizado alrededor de una treintena de casos en el mundo6. Se necesitan seguimientos más largos para confirmar estos resultados, pero es una técnica prometedora.