Palabras clave
INTRODUCCIÓN
La tomografía de coherencia óptica (OCT) es una nueva técnica de diagnóstico intracoronario, con una alta resolución, cercana a los 10-20 mm, unas 10 veces superior a otras como los ultrasonidos intravasculares (IVUS). Estudios previos han valorado la aplicación de la OCT para caracterizar los diferentes componentes de las placas ateroscleróticas tanto in vitro como in vivo1,2.
La OCT ha mostrado altas sensibilidad y especificidad respecto a la histología para clasificar los diferentes tipos de placas ateroscleróticas3. Esta técnica, dada su alta resolución, permite identificar placas con una fina cápsula fibrosa, menor de 65 mm, denominadas thin cap fibroatheroma, que son las más propensas a romperse y originar síndromes coronarios agudos4. Asimismo, la OCT se ha utilizado para valorar el contenido de colágeno y macrófagos en las placas ateroscleróticas5,6.
Por otro lado, la OCT se ha aplicado para valorar el resultado tras implante de stent en pacientes sometidos a intervencionismo coronario percutáneo (ICP)7-9.
El objetivo de este trabajo es evaluar el resultado, mediante OCT, en pacientes sometidos a ICP con una óptima imagen angiográfica en nuestro centro.
MÉTODOS
Se estudió mediante OCT a 6 pacientes sometidos a ICP que presentaban una óptima imagen angiográfica tras el implante de stent, definida como una estenosis en diámetro menor del 20%, flujo distal TIMI 3 y ausencia de imágenes anómalas mediante estimación visual. En 2 pacientes se realizó estudio previo al ICP.
El ICP se llevó a cabo según el procedimiento estándar. Se predilató con balón en 4 pacientes. El diámetro de referencia medio a nivel de la lesión medido mediante angiografía cuantitativa fue 3,01 mm, y el diámetro medio de los stents implantados, 3,3 mm (diferencias no significativas), que se implantaron a una presión media de 15 AT. No se sobredilató con balón en ningún paciente por no considerarlo necesario por la imagen angiográfica.
A continuación, se realizó el estudio mediante OCT. Sobre una guía de angioplastia, se avanzó un catéter balón coaxial (Helios OBC, Lightlab Imaging Inc., Westford, Massachusetts, Estados Unidos) hasta una zona distal al stent implantado. Después se retiró la guía y a través del balón se avanzó la sonda de OCT (ImageWire, Lightlab Imaging Inc., Westford, Massachusetts, Estados Unidos) para situarla al menos 5 mm distal al stent. Se retiró el balón hasta un segmento sano proximal al stent, se infló a una presión entre 0,5 y 0,6 AT y se comprobó que ocluyera el flujo coronario. Luego, mientras se realizaba lavado con suero salino mediante inyección manual a velocidad constante a través del balón, se realizó una retirada automática de la sonda de OCT a 1 mm/s. En los casos en que se consideró necesario, se realizó una nueva retirada, después de permanecer unos minutos con el balón desinflado. Finalmente, se desinfló el balón, se retiró éste y la sonda de OCT del árbol coronario, y se comprobó la ausencia de complicaciones.
Las imágenes se archivaron y se analizaron posteriormente en la propia consola (Lightlab, modelo M2, Lightlab Imaging Inc., Westford, Massachusetts, Estados Unidos). Se evaluó, fundamentalmente, la presencia de disecciones en los bordes del stent, protrusión de material a través de los struts del stent y zonas de mala aposición del stent, así como la presencia de placas del tipo thin cap fibroatheroma en otras zonas del vaso estudiado y la presencia de cualquier otra imagen anómala. Se consideró disección cuando la imagen dentro del stent o adyacente a éste mostraba un colgajo claramente diferenciado del resto de tejido. Se definió protrusión de tejido al prolapso de tejido a través de un arco imaginario que conectase dos struts adyacentes. Se consideró mala aposición cuando había una clara separación entre al menos un strut del stent y la pared del vaso. Se definió thin cap fibroatheroma como la zona de pared arterial de baja refringencia, homogénea, separada de la luz del vaso por una cápsula de alta refringencia < 65 mm de grosor.
RESULTADOS
Se incluyó a 6 pacientes (5 varones; media de edad, 59 años): 3 hipertensos, 2 diabéticos, 4 dislipémicos y 4 fumadores. El motivo del ICP fue síndrome coronario agudo en 4 pacientes y angina estable en 2. La arteria estudiada fue la circunfleja en 3 casos, la coronaria derecha en 2 y la descendente anterior en otro; 3 pacientes recibieron un stent recubierto.
En 3 pacientes se detectaron placas del tipo thin cap fibroatheroma, con una cápsula fibrosa entre 0,02 y 0,06 mm (en la zona de estenosis en los 2 pacientes con estudio previo al ICP y en una zona diferente al stent en el otro), sin que ello se relacionase con el motivo del ICP. Se observó protrusión de material al stent en todos los pacientes (fig. 1), microdisecciones en los bordes del stent en 4 pacientes (fig. 2) y mala aposición del stent en otros 4 pacientes (fig. 3). La mala aposición variaba desde 0,04 hasta 0,5 mm de separación máxima entre el stent y la pared arterial y hasta un máximo de 180° de la circunferencia del vaso. Dado que en el momento actual se desconoce la implicación pronóstica de estos hallazgos, no se sobredilató con balón en ninguno de los casos. En 2 pacientes se observó la formación de trombo alrededor del catéter de OCT, a pesar de anticoagulación con 70-100 UI de heparina no fraccionada por kilo de peso. Ningún paciente presento angina, alteraciones electrocardiográficas ni complicaciones durante el procedimiento. El estudio de OCT prolongó la duración total del procedimiento en menos de 5 min por paciente.
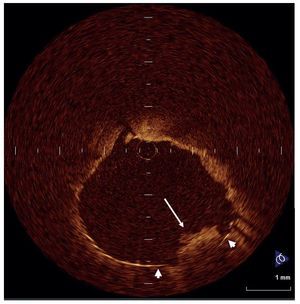
Fig. 1. Protrusión de material (flecha larga) al stent (puntas de flecha).
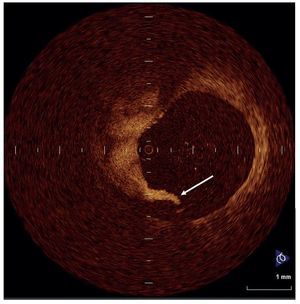
Fig. 2. Disección (flecha) observada en el borde proximal de uno de los stents.
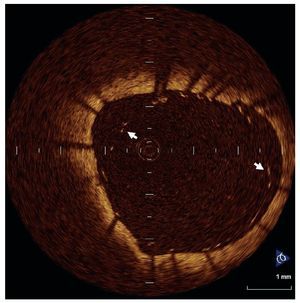
Fig. 3. Mala aposición de stent en gran parte de la pared del vaso (las flechas corresponden a algunos de los struts del stent).
DISCUSIÓN
Este trabajo muestra, gracias a la alta resolución de la OCT, la elevada frecuencia de zonas de resultado subóptimo tras el ICP a pesar de una adecuada imagen
angiográfica. Estudios previos han demostrado la superioridad de la OCT sobre la IVUS a la hora de valorar la presencia de prolapso de tejido a través de los struts del stent, microdisecciones y zonas de mala aposición después del ICP. Así, Bouma et al7 demostraron, de 42 pacientes, protrusión de tejido en 29, disecciones en 8 y mala aposición en 7 pacientes en los estudios de OCT, mientras que mediante IVUS sólo se observaron en 12, 2 y 3 pacientes, respectivamente. En nuestro trabajo, a pesar de un número más reducido de pacientes, se observan estos hallazgos en un porcentaje mucho más elevado, lo cual puede deberse a la diferencia en la técnica de obtención de imágenes de OCT, ya que, mientras que nosotros realizamos una retirada automática a 1 mm/s a lo largo de todo el stent, Bouma et al realizaban las capturas en los bordes proximal y distal del stent y la zona de mayor estenosis antes del implante de stent.
Hay discrepancias a la hora de establecer la implicación pronóstica de estos hallazgos ya que, mientras que algunos estudios han mostrado tasas de eventos adversos similares en pacientes con y sin mala aposición aguda del stent o prolapso de placa valorada por IVUS10-13, otros han demostrado la alta prevalencia de anomalías en el estudio de IVUS tras el implante de stent en pacientes que presentan una trombosis aguda de éste14. Actualmente se desconoce la implicación pronóstica de hallar zonas de resultado subóptimo mediante OCT en pacientes con una adecuada imagen angiográfica tras el ICP.
En conclusión, la OCT, gracias a su alta resolución, permite detectar zonas de resultado subóptimo tras el ICP a pesar de una adecuada imagen angiográfica. Se necesitan estudios más amplios y con seguimiento a largo plazo para valorar la implicación pronóstica de estos hallazgos.
Full English text available from: www.revespcardiol.org
Correspondencia: Dr. H. Gutiérrez.
Instituto de Ciencias del Corazón. Hospital Clínico Universitario. Avda. Ramón y Cajal, 3. 47005 Valladolid. España.
Correo electrónico: hggmaire@gmail.com
Recibido el 7 de septiembre de 2007.
Aceptado para su publicación el 19 de diciembre de 2007.