La presencia de flujos intraventriculares anómalos de alta velocidad y obstrucción dinámica a la eyección ventricular izquierda tras el reemplazo valvular aórtico, generalmente por estenosis aórtica severa, es una complicación infrecuente pero grave.El diagnóstico precoz es de crucial importancia debido a que las medidas terapéuticas habituales que se implementan para el tratamiento de la insuficiencia cardíaca postoperatoria son ineficaces y aun perjudiciales en estos casos.Incluso en pacientes con fallo severo de bomba, cuando el caso clínico es diagnosticado adecuadamente, los agentes betabloqueantes intravenosos de acción corta son de utilidad.
Palabras clave
Estenosis aórtica
Cirugía
Obstrucción intraventricular
Esmolol
INTRODUCCIÓN
La presencia de flujos intraventriculares anómalos de alta velocidad y obstrucción dinámica eyectiva del VI en el postoperatorio de reemplazo aórtico, en general por estenosis aórtica severa, es una complicación relativamente poco frecuente pero grave. Puede aparecer en pacientes con o sin gradiente subvalvular evidente en el prequirúrgico, y se evidencia por insuficiencia cardíaca con adecuada función sistólica ventricular izquierda. Debido a su baja prevalencia y a las dificultades diagnósticas, se han publicado pocas series, que sólo incluyen un limitado número de pacientes, existiendo controversia acerca de la mejor alternativa terapéutica.
CASO CLÍNICO
El paciente era un varón de 68 años de edad, que refería como único antecedente relevante un bypass aortobifemoral 15 años atrás por claudicación intermitente.
Comenzó con dolor de tipo punzante en hemitórax derecho y disnea en clase funcional II de la NYHA tres meses antes del ingreso en el hospital. Se decidió su ingreso al constatarse en el examen físico signos compatibles con estenosis valvular aórtica y lesión subendocárdica en la cara anterior en el electrocardiograma.
Al examen físico se encontraba lúcido y sin signos de fallo de bomba, con una presión arterial de 130/70 mmHg, y una frecuencia cardíaca de 80 lat/min. Presentaba un segundo ruido cardíaco abolido, sin tercer ni cuarto ruido; en el foco aórtico y el mesocardio se auscultaba un soplo sistólico eyectivo de intensidad 4/6 con acmé mesotelesistólico.
El electrocardiograma de ingreso puso de manifiesto ritmo sinusal, bloqueo completo de rama derecha, hipertrofia ventricular izquierda, y un infradesnivel descendente del segmento ST en derivaciones precordiales V3 a V6 compatible con lesión subendocárdica.
En la radiografía de tórax al ingreso y en los análisis de laboratorio no se observaron alteraciones significativas.
Un ecocardiograma Doppler evidenció: diámetro diastólico del VI de 38 mm; diámetro sistólico de 21 mm; fracción de acortamiento del 45%; espesor septal en diástole de 16 mm, y pared posterior del VI de 14 mm. La función sistólica del VI y el score de motilidad parietal eran normales. Mediante Doppler se apreció una estenosis aórtica severa con un gradiente pico de 148 mmHg, medio de 92 mmHg y un área valvular de 0,45 cm 2; la presión sistólica en la arteria pulmonar era de 44 mmHg. No se verificó incremento de la velocidad del flujo en el tracto de salida del VI.
En el estudio hemodinámico se constataron arterias coronarias angiográficamente normales; no se realizó ventriculograma izquierdo ni mediciones de gradientes aórticos por imposibilidad de trasponer el orificio valvular con el catéter.
Se decidió tratamiento quirúrgico, realizándose cirugía de reemplazo valvular aórtico, implantándose una prótesis mecánica bivalva Saint Jude número 17, sin complicaciones.
En el primer día postoperatorio presentó broncospasmo y estertores crepitantes bibasales, indicándose nebulizaciones con agonistas beta-2 y furosemida, con mejoría parcial; al día siguiente evolucionó con franco fallo de bomba, sin respuesta al tratamiento con nitroglicerina y diuréticos. Se le realizó un ecocardiograma Doppler que puso de manifiesto una función sistólica normal del VI, con hipercinesia de sus paredes, prótesis aórtica normofuncionante y un gradiente intraventricular de 133 mmHg con un flujo típico en «forma de daga» y pico telesistólico (fig. 1); no se detectó movimiento anterior sistólico mitral.
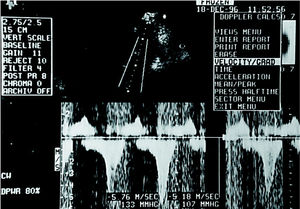
Fig. 1. Imagen con Doppler continuo en la que se observa la típica "forma de daga" de los flujos intraventriculares dinámicos, el segundo día posterior a la cirugía. La velocidad es de 5,76 m/s, con un gradiente pico de 133 mmHg.
Se inició tratamiento con diltiazem en infusión intravenosa continua, pero a las 12 h repitió el cuadro de broncospasmo e insuficiencia cardíaca, con tendencia a la hipotensión arterial, y taquicardia sinusal a 120 lat/min; se agregó amiodarona al esquema terapéutico.
Se colocó un catéter de Swan-Ganz en la arteria pulmonar, que demostró una presión en aurícula derecha de 15 mmHg, presión de enclavamiento pulmonar de 25 mmHg, índice cardíaco de 2,9 l/min/m 2 de superficie corporal, presión arterial media 68 mmHg (88/57), presión pulmonar media 31 mmHg (48/23) y resistencia vascular sistémica y pulmonar de 731 y 83 dinas/s/cm -5, respectivamente.
Ante la persistencia del deterioro clínico se realizó intubación orotraqueal y conexión a asistencia respiratoria mecánica, iniciándose infusión intravenosa de esmolol, con una dosis de carga de 500 μg/kg en 1 min y un mantenimiento creciente comenzando con 50 μg/kg/min. Se observó mejoría clínica y hemodinámica. Presentó posteriormente ritmo idioventricular con frecuencia cardíaca de 30 lat/min y descompensación hemodinámica que requirió marcapaso transitorio y suspensión del diltiazem y la amiodarona, decidiéndose mantener los betabloqueantes por vía intravenosa y posteriormente oral. Recuperó el ritmo sinusal a las 24 h. Evolucionó de manera favorable y fue dado de alta hospitalaria al séptimo día postoperatorio medicado con atenolol, 125 mg/día, aspirina y anticoagulación con acenocumarol. A los 18 meses de la operación evoluciona asintomático. DISCUSIÓN
La presencia de obstrucción intraventricular tras el reemplazo valvular aórtico ha sido atribuida a diferentes mecanismos.
Algunos autores hallaron un gradiente obstructivo telesistólico en el tracto de salida del ventrículo izquierdo 1,2, generalmente asociado a movimiento anterior sistólico de la válvula mitral; este mecanismo recuerda al que se produce en la miocardiopatía hipertrófica.
Otras series demuestran gradientes significativos medioventriculares, y no asociados a anomalías de la motilidad del aparato mitral 3,4. En este último caso, la fisiopatología de la obstrucción dinámica se asemeja a la descrita en pacientes de edad avanzada con miocardiopatía hipertrófica hipertensiva 5, en los que la marcada hipertrofia ventricular (simétrica) secundaria a hipertensión arterial da lugar, en ciertos casos, a la aparición de un flujo medioventricular de alta velocidad con ausencia de movimiento anterior sistólico mitral.
El signo clínico cardinal de los flujos intraventriculares anómalos en el postoperatorio de la estenosis aórtica es la hipotensión arterial 6. También han sido descritos disnea, angina, síncope y presencia de insuficiencia cardíaca resistente al tratamiento diurético e inotrópico. Asimismo, se ha comunicado una mayor tasa de complicaciones, generalmente asociadas a hipotensión sostenida, como disfunción renal e intubación prolongada 6. La evolución y el pronóstico de los pacientes que presentan gradientes intracavitarios anómalos son peores que la de aquellos en los cuales no se constatan 3,7. En la serie de Aurigemma et al, la mortalidad de los trece pacientes con flujos anormales fue del 38%, frente al 12% en los 40 casos restantes de reemplazo aórtico por estenosis aórtica 3.
La mayoría de los autores no ha podido correlacionar variables clínicas con la evolución, teniendo valor pronóstico solamente el ecocardiograma. La obstrucción intraventricular postoperatoria es más frecuente en pacientes con miocardiopatía hipertrófica previa, y en ventrículos pequeños y muy hipertróficos 3,7.
La terapéutica suele ser difícil, en particular si no se realiza un diagnóstico precoz. La estrategia de tratamiento suele ser exactamente la opuesta a la de la insuficiencia cardíaca producida por fallo sistólico. Las medidas a adoptar son la suspensión de fármacos inotrópicos, una cuidadosa expansión de volumen y agentes inotrópicos y cronotrópicos negativos, como los bloqueadores de los canales del calcio y betabloqueantes. En nuestro caso, la falta de respuesta al tratamiento motivó la implementación de goteo intravenoso de esmolol, bajo monitorización hemodinámica mediante catéter de Swan-Ganz. La respuesta a este agente fue hemodinámicamente muy positiva, por lo que, a pesar de producirse un bloqueo AV completo por la asociación con diltiazem y amiodarona, se decidió colocar un marcapasos transitorio y continuar con el esmolol hasta normalizar el cuadro clínico.
Uno de los motivos de la presente comunicación es destacar la importancia del reconocimiento precoz de esta entidad, hecho crucial para implementar la terapéutica adecuada, ya que las medidas habituales para tratar la insuficiencia cardíaca suelen ser ineficaces, o aun perjudiciales. Incluso en casos de insuficiencia cardíaca severa, cuando se diagnostica adecuadamente el cuadro clínico, los betabloqueantes de acción corta por vía intravenosa son de utilidad.
La presencia de flujos intraventriculares anómalos de alta velocidad y obstrucción dinámica eyectiva del VI en el postoperatorio de reemplazo aórtico, en general por estenosis aórtica severa, es una complicación relativamente poco frecuente pero grave. Puede aparecer en pacientes con o sin gradiente subvalvular evidente en el prequirúrgico, y se evidencia por insuficiencia cardíaca con adecuada función sistólica ventricular izquierda. Debido a su baja prevalencia y a las dificultades diagnósticas, se han publicado pocas series, que sólo incluyen un limitado número de pacientes, existiendo controversia acerca de la mejor alternativa terapéutica.
CASO CLÍNICO
El paciente era un varón de 68 años de edad, que refería como único antecedente relevante un bypass aortobifemoral 15 años atrás por claudicación intermitente.
Comenzó con dolor de tipo punzante en hemitórax derecho y disnea en clase funcional II de la NYHA tres meses antes del ingreso en el hospital. Se decidió su ingreso al constatarse en el examen físico signos compatibles con estenosis valvular aórtica y lesión subendocárdica en la cara anterior en el electrocardiograma.
Al examen físico se encontraba lúcido y sin signos de fallo de bomba, con una presión arterial de 130/70 mmHg, y una frecuencia cardíaca de 80 lat/min. Presentaba un segundo ruido cardíaco abolido, sin tercer ni cuarto ruido; en el foco aórtico y el mesocardio se auscultaba un soplo sistólico eyectivo de intensidad 4/6 con acmé mesotelesistólico.
El electrocardiograma de ingreso puso de manifiesto ritmo sinusal, bloqueo completo de rama derecha, hipertrofia ventricular izquierda, y un infradesnivel descendente del segmento ST en derivaciones precordiales V3 a V6 compatible con lesión subendocárdica.
En la radiografía de tórax al ingreso y en los análisis de laboratorio no se observaron alteraciones significativas.
Un ecocardiograma Doppler evidenció: diámetro diastólico del VI de 38 mm; diámetro sistólico de 21 mm; fracción de acortamiento del 45%; espesor septal en diástole de 16 mm, y pared posterior del VI de 14 mm. La función sistólica del VI y el score de motilidad parietal eran normales. Mediante Doppler se apreció una estenosis aórtica severa con un gradiente pico de 148 mmHg, medio de 92 mmHg y un área valvular de 0,45 cm 2; la presión sistólica en la arteria pulmonar era de 44 mmHg. No se verificó incremento de la velocidad del flujo en el tracto de salida del VI.
En el estudio hemodinámico se constataron arterias coronarias angiográficamente normales; no se realizó ventriculograma izquierdo ni mediciones de gradientes aórticos por imposibilidad de trasponer el orificio valvular con el catéter.
Se decidió tratamiento quirúrgico, realizándose cirugía de reemplazo valvular aórtico, implantándose una prótesis mecánica bivalva Saint Jude número 17, sin complicaciones.
En el primer día postoperatorio presentó broncospasmo y estertores crepitantes bibasales, indicándose nebulizaciones con agonistas beta-2 y furosemida, con mejoría parcial; al día siguiente evolucionó con franco fallo de bomba, sin respuesta al tratamiento con nitroglicerina y diuréticos. Se le realizó un ecocardiograma Doppler que puso de manifiesto una función sistólica normal del VI, con hipercinesia de sus paredes, prótesis aórtica normofuncionante y un gradiente intraventricular de 133 mmHg con un flujo típico en «forma de daga» y pico telesistólico (fig. 1); no se detectó movimiento anterior sistólico mitral.
Fig. 1. Imagen con Doppler continuo en la que se observa la típica "forma de daga" de los flujos intraventriculares dinámicos, el segundo día posterior a la cirugía. La velocidad es de 5,76 m/s, con un gradiente pico de 133 mmHg.
Se inició tratamiento con diltiazem en infusión intravenosa continua, pero a las 12 h repitió el cuadro de broncospasmo e insuficiencia cardíaca, con tendencia a la hipotensión arterial, y taquicardia sinusal a 120 lat/min; se agregó amiodarona al esquema terapéutico.
Se colocó un catéter de Swan-Ganz en la arteria pulmonar, que demostró una presión en aurícula derecha de 15 mmHg, presión de enclavamiento pulmonar de 25 mmHg, índice cardíaco de 2,9 l/min/m 2 de superficie corporal, presión arterial media 68 mmHg (88/57), presión pulmonar media 31 mmHg (48/23) y resistencia vascular sistémica y pulmonar de 731 y 83 dinas/s/cm -5, respectivamente.
Ante la persistencia del deterioro clínico se realizó intubación orotraqueal y conexión a asistencia respiratoria mecánica, iniciándose infusión intravenosa de esmolol, con una dosis de carga de 500 μg/kg en 1 min y un mantenimiento creciente comenzando con 50 μg/kg/min. Se observó mejoría clínica y hemodinámica. Presentó posteriormente ritmo idioventricular con frecuencia cardíaca de 30 lat/min y descompensación hemodinámica que requirió marcapaso transitorio y suspensión del diltiazem y la amiodarona, decidiéndose mantener los betabloqueantes por vía intravenosa y posteriormente oral. Recuperó el ritmo sinusal a las 24 h. Evolucionó de manera favorable y fue dado de alta hospitalaria al séptimo día postoperatorio medicado con atenolol, 125 mg/día, aspirina y anticoagulación con acenocumarol. A los 18 meses de la operación evoluciona asintomático. DISCUSIÓN
La presencia de obstrucción intraventricular tras el reemplazo valvular aórtico ha sido atribuida a diferentes mecanismos.
Algunos autores hallaron un gradiente obstructivo telesistólico en el tracto de salida del ventrículo izquierdo 1,2, generalmente asociado a movimiento anterior sistólico de la válvula mitral; este mecanismo recuerda al que se produce en la miocardiopatía hipertrófica.
Otras series demuestran gradientes significativos medioventriculares, y no asociados a anomalías de la motilidad del aparato mitral 3,4. En este último caso, la fisiopatología de la obstrucción dinámica se asemeja a la descrita en pacientes de edad avanzada con miocardiopatía hipertrófica hipertensiva 5, en los que la marcada hipertrofia ventricular (simétrica) secundaria a hipertensión arterial da lugar, en ciertos casos, a la aparición de un flujo medioventricular de alta velocidad con ausencia de movimiento anterior sistólico mitral.
El signo clínico cardinal de los flujos intraventriculares anómalos en el postoperatorio de la estenosis aórtica es la hipotensión arterial 6. También han sido descritos disnea, angina, síncope y presencia de insuficiencia cardíaca resistente al tratamiento diurético e inotrópico. Asimismo, se ha comunicado una mayor tasa de complicaciones, generalmente asociadas a hipotensión sostenida, como disfunción renal e intubación prolongada 6. La evolución y el pronóstico de los pacientes que presentan gradientes intracavitarios anómalos son peores que la de aquellos en los cuales no se constatan 3,7. En la serie de Aurigemma et al, la mortalidad de los trece pacientes con flujos anormales fue del 38%, frente al 12% en los 40 casos restantes de reemplazo aórtico por estenosis aórtica 3.
La mayoría de los autores no ha podido correlacionar variables clínicas con la evolución, teniendo valor pronóstico solamente el ecocardiograma. La obstrucción intraventricular postoperatoria es más frecuente en pacientes con miocardiopatía hipertrófica previa, y en ventrículos pequeños y muy hipertróficos 3,7.
La terapéutica suele ser difícil, en particular si no se realiza un diagnóstico precoz. La estrategia de tratamiento suele ser exactamente la opuesta a la de la insuficiencia cardíaca producida por fallo sistólico. Las medidas a adoptar son la suspensión de fármacos inotrópicos, una cuidadosa expansión de volumen y agentes inotrópicos y cronotrópicos negativos, como los bloqueadores de los canales del calcio y betabloqueantes. En nuestro caso, la falta de respuesta al tratamiento motivó la implementación de goteo intravenoso de esmolol, bajo monitorización hemodinámica mediante catéter de Swan-Ganz. La respuesta a este agente fue hemodinámicamente muy positiva, por lo que, a pesar de producirse un bloqueo AV completo por la asociación con diltiazem y amiodarona, se decidió colocar un marcapasos transitorio y continuar con el esmolol hasta normalizar el cuadro clínico.
Uno de los motivos de la presente comunicación es destacar la importancia del reconocimiento precoz de esta entidad, hecho crucial para implementar la terapéutica adecuada, ya que las medidas habituales para tratar la insuficiencia cardíaca suelen ser ineficaces, o aun perjudiciales. Incluso en casos de insuficiencia cardíaca severa, cuando se diagnostica adecuadamente el cuadro clínico, los betabloqueantes de acción corta por vía intravenosa son de utilidad.
Bibliografía
[1]
Valvular aortic stenosis and asymmetric septal hypertrophy: diagnostic considerations and clinical and therapeutic implications. Eur Heart J 1988; 9: 71-76.
[2]
Dynamic outflow obstruction after aortic valve replacement: a doppler echocardiographic study. J Am Soc Echocardiogr 1990; 3: 205-212.
[3]
Abnormal left ventricular intracavity flow acceleration in patients undergoing aortic valve replacement for aortic stenosis. A marker for high postoperative morbidity and mortality. Circulation 1992; 86: 926-936.
[4]
Systolic intra-cavitary gradients following aortic valve replacement: an echo-doppler study. Eur Heart J 1991; 12: 1098-1106.
[5]
Midventricular obstruction associated with chronic systemic hypertension and severe left ventricular hypertrophy. Am J Cardiol 1991; 68: 761-765.
[6]
John Sutton M, Plappert T, Spiegel A, Raichlen J, Douglas P, Reichek N et al. Early post-operative changes in left ventricular chamber size, architecture, and function in aortic stenosis and aortic regurgitation and their relation to intraoperative changes in afterload: a prospective two-dimensional echocardiographic study. Circulation 1987; 76: 77-89.
[7]
Left ventricular hypertrophy and mortality after aortic valve replacement for aortic stenosis. J Am Coll Cardiol 1993; 22: 1679-1683.