Recientemente se ha ofrecido el tratamiento de implantación percutánea de la válvula aórtica a pacientes seleccionados, y los resultados han sido buenos. En Europa, por ejemplo, la implantación percutánea de la válvula aórtica constituye una alternativa basada en la evidencia y claramente establecida frente a la sustitución de la válvula aórtica mediante cirugía abierta, en pacientes con estenosis aórtica en los que la cirugía cardiaca convencional comportaría un riesgo elevado. Los estudios realizados en Estados Unidos han puesto de manifiesto que, en pacientes con estenosis órtica grave que no son candidatos a cirugía, la implantación percutánea de la válvula aórtica Edwards-SAPIEN ha tenido una mortalidad significativamente inferior a la del tratamiento estándar. Sin embargo, la implantación percutánea de la válvula aórtica se asoció a una incidencia superior de ictus y complicaciones vasculares mayores, aunque sin alcanzar una diferencia significativa, en comparación con la sustitución valvular aórtica estándar. Además, al considerar conjuntamente los ictus y los accidentes isquémicos transitorios, se observó una ventaja significativa favorable a la cirugía, tanto a los 30 días como a 1 año (p=0,04). Parece claro que una selección óptima de los pacientes es crucial para el éxito de la implantación percutánea de la válvula aórtica. Además, se ha demostrado que la adopción de un enfoque multidisciplinario mejora los resultados obtenidos en intervenciones complejas como estas. Para asegurar un resultado satisfactorio de la implantación percutánea de la válvula aórtica, debe darse la colaboración de un equipo multidisciplinario de tratamiento de las valvulopatías cardiacas en todas las fases del programa: durante el examen de selección inicial, durante y después de la intervención y durante todo el periodo de seguimiento. Concretamente, los pacientes deben ser examinados con vistas a la inclusión en un programa de implantación percutánea de la válvula aórtica por un miembro del equipo multidisciplinario, y no por un especialista externo concreto. Además, la selección de los candidatos al tratamiento debe comportar una consulta entre las diferentes disciplinas (es decir, entre cardiólogos, cirujanos, especialistas en diagnóstico por la imagen, anestesiólogos, neumólogos y otros especialistas en caso necesario).
Palabras clave
La prevalencia de la estenosis aórtica está aumentando a medida que envejece la población de Estados Unidos. La incidencia de estenosis aórtica en los pacientes de edad >65 años es de un 2-7%1. En Estados Unidos son hasta 300.000 las personas que hoy sufren una estenosis aórtica sintomática. La sustitución valvular quirúrgica con prótesis valvulares biológicas o mecánicas ha sido durante muchos años el patrón de referencia para el tratamiento de las estenosis valvulares importantes, pero en algunos pacientes la cirugía comporta un riesgo elevado. No se remite a intervención quirúrgica a casi un 30% de los pacientes con valvulopatías aórticas sintomáticas que cumplen los criterios de las guías aceptadas para la sustitución valvular2. Ello es más frecuente en la población anciana con otras comorbilidades. Las mejoras de la técnica quirúrgica, el uso de válvulas protésicas duraderas y una mejor pauta de anticoagulación han conducido a excelentes supervivencia y estado funcional de los pacientes.
Resultados de los estudios de implantación percutánea de válvula aórticaRecientemente se ha ofrecido la implantación percutánea de válvula aórtica (IPVA) a pacientes seleccionados, con buenos resultados. En Europa, la IPVA es actualmente una alternativa basada en la evidencia y bien establecida frente a la sustitución de la válvula aórtica mediante cirugía abierta en pacientes con estenosis aórtica que no son candidatos a cirugía cardiaca convencional. Estudios recientes de Estados Unidos han puesto de manifiesto que, en los pacientes con estenosis aórtica grave que no son candidatos a cirugía, la implantación aórtica de la válvula Edwards-SAPIEN redujo significativamente la mortalidad en comparación con el tratamiento estándar (ensayo Partner, cohorte B)3, 4. Formaban la cohorte B del ensayo Partner 358 pacientes con estenosis aórtica sintomática grave considerada inoperable con cirugía cardiaca tradicional a corazón abierto3. Se asignó a los pacientes, aleatoriamente y en proporciones iguales, a la válvula Edwards-SAPIEN o el tratamiento estándar. Aunque las tasas a 30 días de ictus (el 3,8 frente al 2,1%; p=0,20) y de complicaciones vasculares (el 11 frente al 3,0%; p<0,001) fueron mayores en el grupo tratado con la válvula en fase de investigación, la supervivencia a 1 año de los pacientes en que se empleó esa válvula fue muy superior que la de quienes recibieron el mejor tratamiento médico (el 69,3 frente al 49,3%). Además, los pacientes tratados con la válvula tuvieron menos hospitalizaciones y mejor control de los síntomas que los tratados con la asistencia médica estándar.
Formaban la cohorte A 699 pacientes con estenosis aórtica sintomática grave, para los que se consideró que la cirugía tradicional a corazón abierto tenía un riesgo elevado4. Se incluyó a los pacientes en una asignación aleatoria en proporciones iguales al tratamiento con una válvula Edwards-SAPIEN con aplicación transfemoral o transapical o a la cirugía a corazón abierto tradicional. El estudio alcanzó su objetivo principal a 1 año, y llegó a la conclusión de que la supervivencia de los pacientes tratados percutáneamente con la válvula aórtica Edwards-SAPIEN era equivalente a la de los tratados con sustitución quirúrgica de la válvula aórtica (SVA). En esta cohorte, el estudio observó que la IPVA era no inferior a la SVA en cuanto a la mortalidad por todas las causas a 1 año, con valores del 24,2 frente al 26,8%, respectivamente; la tasa de mortalidad por cualquier causa fue del 30% con la IPVA y del 50,7% con el tratamiento estándar. Sin embargo, este método tuvo una incidencia de ictus y complicaciones vasculares mayores superior a la del tratamiento estándar. La tasa de ictus mayores fue a los 30 días del 3,8% en el grupo de IPVA frente al 2,1% en el grupo de cirugía, y a 1 año, del 5,1 frente al 2,4%, aunque la diferencia no alcanzaba significación estadística (p=0,20 a 30 días y p=0,07 a 1 año). Sin embargo, al considerar conjuntamente los ictus y los accidentes isquémicos transitorios, se observó un resultado favorable a la cirugía estadísticamente significativo, tanto a 30 días como a 1 año (p=0,04).
Selección de los pacientesUna selección óptima de los pacientes es crucial para el éxito de la intervención de IPVA. Se basa en gran parte en un enfoque de equipo multidisciplinario; es necesario un ejercicio de colaboración del equipo valvular cardiaco para alcanzar un buen resultado del programa. Este equipo multidisciplinario es esencial en el examen de selección inicial, durante la intervención, después de ella y en el seguimiento de estos pacientes. El equipo desempeña un papel fundamental al reunir a expertos en diversos campos. Un cardiólogo aportará un conocimiento sólido en relación con la intervención coronaria percutánea (ICP) que puede proporcionar un beneficio al paciente, y esta intervención se realiza siempre a través de un catéter y a menudo de manera totalmente percutánea. Por su parte, el cirujano aportará su muy buen conocimiento de la raíz aórtica y de la anatomía del lugar donde se va a desplegar la válvula. Además, el cirujano puede evaluar si el paciente es o no un buen candidato quirúrgico o puede señalar que en un paciente sería útil una intervención de IPVA, dado que su riesgo quirúrgico podría ser demasiado elevado. Además del equipo que participa en la intervención, el enfoque multidisciplinario es importante en la selección de los pacientes. El examen de selección de los pacientes para la inclusión en un programa de IPVA debe hacerlo un miembro del equipo multidisciplinario, y no cualquier especialista individual. La selección de los candidatos a la IPVA debe incluir una consulta multidisciplinaria de cardiólogos, cirujanos, especialistas en diagnóstico por la imagen, anestesiólogos, neumólogos y otros especialistas en caso necesario. Se ha demostrado que emplear un enfoque de equipo mejora los resultados obtenidos en estos tipos de intervenciones complejas5. Siempre hay que considerar dos aspectos: el del paciente (¿hay necesidad clínica en este paciente?) y el de los detalles técnicos (¿se puede implantar una válvula cardiaca a través de un catéter por vía transfemoral, apical o subclavia?).
El proceso conceptual que subyace a la selección de los pacientes puede dividirse en una evaluación de la idoneidad clínica y, luego, la idoneidad anatómica. Forman parte del equipo el coordinador del estudio, el cardiólogo intervencionista (1 o 2), el cirujano cardiaco (1 o 2), el anestesiólogo cardiaco y los ecocardiografistas (1 o 2). También hay especialistas en formación (2), enfermeras (2 o 3), técnicos cardiovasculares (2 o 3), la enfermera instrumentista de quirófano y el perfusionista de bomba circulatoria, un técnico de bomba de balón intraaórtico (BBIA) y un encargado del montaje y plegado de la válvula para su introducción.
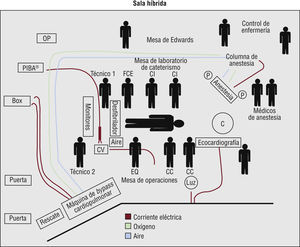
Requisitos técnicosLa SVA a través de un catéter se realiza con anestesia local o raquídea, con sedación o con anestesia general en un laboratorio de cateterismo cardiaco o en un quirófano que cuente con fluoroscopia y ecocardiografía transesofágica (ETE). La IPVA se lleva a cabo mediante abordaje transfemoral o transapical. El concepto de una sala de intervención híbrida (Figura.) se desarrolló para esta técnica y requiere un espacio de grandes dimensiones que disponga de fluoroscopia de alta resolución y cineangiografía, con TC Dyna (Siemens USA; Washington DC, Estados Unidos) y de capacidades de ETE. Requiere una circulación con doble conducto de ventilación, y disponer de máquina de bypass cardiopulmonar, BBIA y marcapasos.
Figura.. Representación esquemática de la intervención híbrida del Massachusetts General Hospital en el laboratorio de cateterismo cardiaco. C: brazo en C; CC: cirujano cardiaco; CI: cardiólogo intervencionista; CV: conexión de balón; EQ: enfermera de quirófano; FCE: fellow en cardiopatía estructural; Luz: foco de luz; OP: ordenador portátil; PIBA®: adaptador a presión.
La evaluación de los pacientes se inicia en la clínica ambulatoria. Cuando el paciente acude a la clínica, se examina cómo responde. Es preciso realizar un juicio clínico para decidir si la IPVA puede ser apropiada en ese caso. Una vez decidido esto, se pasa a una serie de exploraciones diagnósticas destinadas a examinar la idoneidad técnica de ese paciente para el uso de determinada tecnología. En la Tabla 1, Tabla 2 se presenta una relación de las pruebas que suelen ser necesarias en la evaluación de esos pacientes. A continuación, se debate de forma abierta en el grupo multidisciplinario para determinar la mejor forma de abordar el tratamiento en cada paciente individual. La estratificación del riesgo de los pacientes se establece usando métodos especiales de puntuación, como la EuroSCORE, la puntuación STS o la puntuación de fragilidad.
Tabla 1. Pasos de la selección de los pacientes para la implantación percutánea de la válvula aórtica
| Confirmar la gravedad de la estenosis aórtica (ecocardiografía transtorácica y transesofágica) |
| Evaluación clínica de los síntomas (clase funcional de la New York Heart Association, Canadian Heart Class of Angina) |
| Angiotomografía computarizada de tórax, abdomen y pelvis para evaluar la anatomía de la válvula aórtica y el acceso vascular arterial |
| Análisis del riesgo de la cirugía (EuroSCORE, puntuación STS, Fried Frailty Index) |
| Determinación de la esperanza de vida y la calidad de vida |
| Determinar la factibilidad del acceso y descartar la existencia de contraindicaciones |
Tabla 2. El Fried Frailty Index
| — Fenotipo Fried de la fragilidad |
| 1. Pérdida de peso (involuntaria)>10 libras (4,5 kg) en el último año |
| 2. Fuerza de prensión. Mínimo del 20% por sexo/IMC |
| 3. Agotamiento. Evaluado por el paciente (escala de depresión CES-D) |
| 4. Tiempo empleado para caminar 15 pies (4,6 m). Mínimo del 20% por sexo/talla |
| 5. Baja actividad |
| • Varones<383 kcal/semana |
| • Mujeres<270 kcal/semana |
Fragilidad: ≥ 3 criterios. Fragilidad intermedia/prefragilidad: 1 o 2 criterios.
Nunca se resaltará lo suficiente la importancia de las dimensiones del anillo aórtico al planificar la estrategia de IPVA, su aplicación satisfactoria y la prevención de las complicaciones. Este parámetro ha sido identificado como un factor determinante clave en la evaluación de los pacientes candidatos a la IPVA6. Actualmente se utilizan para ello diversas técnicas de diagnóstico por la imagen, como ETT, ETE y angiografía por tomografía computarizada (TC). La ETT constituye un buen método para el examen de selección inicial, la ETE se realiza a menudo inmediatamente antes de la IPVA y aporta una evaluación de confirmación, por lo que se considera el patrón de referencia actual. La TC proporciona información adicional respecto a la naturaleza no circular del anillo aórtico, que no se aprecia bien en la ecocardiografía. La válvula Edwards-SAPIEN expansible con balón fuerza una morfología circular; el diseño autoexpansivo de la Medtronic CoreValve tiende a adaptarse más a la configuración elipsoidal del anillo aórtico. La válvula Edwards-SAPIEN requiere un anillo de 18-21mm para su bioprótesis de menor tamaño, de 23mm, y un anillo de 22-25mm para su bioprótesis de mayor tamaño, de 26mm, y los valores de 21-22mm quedan en una zona gris intermedia. Un dispositivo Edwards-SAPIEN mayor, de 29mm, dispone ahora de la designación de CE para la vía transapical. La Medtronic CoreValve requiere un anillo de 20-23mm para su bioprótesis de menor tamaño, de 26mm, y un anillo de 24-27mm para su bioprótesis de mayor tamaño, de 29mm. Aunque la medida de 23-24mm está en la zona gris intermedia, generalmente se utiliza la bioprótesis de mayor tamaño en los casos que tienen estas dimensiones. La intervención de implantación comporta un acceso vascular a través de la arteria femoral, la realización de una valvuloplastia aórtica con balón y después el despliegue de la prótesis durante un marcapasos ventricular derecho rápido6.
La IPVA se realiza, la mayor parte de las veces, utilizando un abordaje transfemoral. La seguridad de esta técnica depende de una evaluación cuidadosa de los vasos iliofemorales y aortoiliacos. La determinación del tamaño de los vasos, y la evaluación de su tortuosidad y de su calcificación concéntrica son esenciales en la identificación de los candidatos ideales para este enfoque. Estas determinaciones se realizan con mayor frecuencia utilizando angio-TC, que ha pasado a ser el patrón de referencia para esta evaluación en la mayor parte de los centros. Las dimensiones femorales mínimas son de 6mm (18 Fr) para el dispositivo Medtronic CoreValve y de 7mm (22 Fr) y 8mm (24 Fr) para las prótesis Edwards-SAPIEN de 23 y 26mm respectivamente. Recientemente se ha introducido un nuevo dispositivo Edwards-SAPIEN de menor calibre, que es de 18 Fr (diámetro luminal mínimo, 6mm) y 19 Fr (diámetro luminal mínimo, 6,5mm) para las válvulas SAPIEN de 23 y 26mm respectivamente. Se ha identificado que un cociente de riesgo de acceso femoral (definido como tamaño de la vaina [Fr]/diámetro AF mínimo [mm]) de un umbral de 2,6 constituye un factor predictivo independiente para las complicaciones vasculares mayores. Además, tanto la calcificación extensa en el lugar de acceso femoral como la tortuosidad extrema han sido identificadas como factores adicionales de aparición de complicaciones vasculares mayores7.
El futuroLa IPVA es una modalidad terapéutica emergente y prometedora para el tratamiento de la estenosis aórtica grave en un grupo seleccionado de pacientes que no son buenos candidatos a cirugía. Sigue habiendo cuestiones importantes pendientes de resolver respecto a la IPVA en cuanto a su durabilidad a largo plazo y las complicaciones de la intervención. A pesar del menor grado de invasividad que tiene la IPVA en comparación con la SVA con cirugía abierta, la IPVA comporta un potencial considerable de complicaciones graves que pueden poner en peligro la vida, tanto intraoperatorias como postoperatorias. Entre ellas se encuentran lesiones vasculares, ictus, lesiones estructurales de la aorta y el corazón y sus válvulas, lesiones de la raíz o el anillo aórtico, lesiones del tejido de conducción, fugas paravalvulares, mala posición de la válvula, complicaciones coronarias como obstrucción o isquemia, derrame y taponamiento pericárdicos y depresión cardiaca en la intervención que requiere un bypass cardiopulmonar inmediato para la reanimación. La prevención, la detección y el tratamiento de estas complicaciones requieren la participación de un grupo experto, que deberá disponer de un cirujano cardiovascular con dominio de las técnicas endovasculares, un cardiólogo intervencionista, un equipo de perfusión cardiaca y anestesia cardiaca. Así pues, la asistencia óptima de los pacientes mediante IPVA requiere un enfoque multidisciplinario que aporte estos servicios.
Actualmente hay cuatro organizaciones que representan a cardiólogos y cirujanos cardiotorácicos y lideran el trabajo de articular un documento conjunto que abordará las recomendaciones para los centros que deseen desarrollar programas de IPVA. Son las siguientes: Society of Cardiac Angiography and Interventions (SCAI) conjuntamente con American Society for Thoracic Surgery (AATS), American College of Cardiology Foundation (ACCF) y Society of Thoracic Surgeons (STS). Además, estas organizaciones trabajan en el establecimiento de los requisitos necesarios para quienes pretenden desarrollar un programa de IPVA, incluidos los de acreditación de cirujanos cardiotorácicos y cardiólogos intervencionistas que llevarán a cabo las intervenciones, y también las exigencias de volumen anual de SVA quirúrgicas y de ICP para el centro y para los especialistas individuales, así como la titulación de especialidad para los cirujanos cardiotorácicos y cardiólogos intervencionistas.
En conclusión, para esta nueva técnica de IPVA es esencial un equipo multidisciplinario. Este trabajo en equipo debe incluir una consulta multidisciplinaria entre cardiólogos, cirujanos cardiacos, especialistas en diagnóstico por la imagen, anestesiólogos, neumólogos y otros especialistas en caso necesario. Con ello se asegura un adecuado examen de selección de los mejores candidatos a esta intervención y un planteamiento adecuado de la IPVA, y este enfoque es esencial en el seguimiento de estos pacientes.
Conflicto de interesesNinguno.
Autor para correspondencia. Director of Interventional Cardiology, Massachusetts General Hospital, Harvard Medical School, Boston, MA 02114, Estados Unidos. ipalacios@partners.org