La terapia de activación barorrefleja (TAB) inhibe el sistema nervioso simpático y potencia el parasimpático, lo cual ha demostrado mejorar calidad de vida, la clase funcional y la concentración de péptidos natriuréticos en pacientes con insuficiencia cardiaca (IC) con fracción de eyección reducida (IC-FEr), sin indicación de terapia de resincronización cardiaca (TRC), que siguen sintomáticos a pesar del tratamiento farmacológico1,2. Sin embargo, aún hay pocos datos de la eficacia y seguridad de la TAB en la práctica clínica real3,4 y las últimas guías europea y estadounidense de IC no establecen un nivel de recomendación para esta opción terapéutica5,6. El objetivo del presente trabajo es describir el perfil clínico de los pacientes a los que se ha implantado un dispositivo Barostim neo (CVRx, Estados Unidos) desde su introducción en España, así como la eficacia y la seguridad del procedimiento.
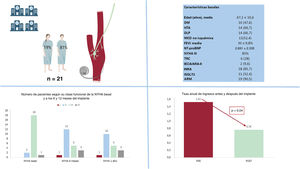
El comité de ética del centro coordinador eximió de la obtención de consentimiento informado por el carácter observacional del estudio. Se realizó un estudio de cohortes retrospectivo en el que se incluyó a 21 pacientes consecutivos procedentes de hospitales españoles, a quienes se implantó un dispositivo Barostim neo por IC-FEr entre febrero de 2017 y diciembre de 2021, con un seguimiento de 1 año. Los centros e investigadores principales se listan en el anexo. La tabla 1 muestra las características basales de los pacientes comparadas con las del grupo de intervención del ensayo clínico pivotal BeAT-HF2. El dispositivo se activó a los 17,9±8,2 días desde la cirugía. Se consiguió graduar la amplitud media del tratamiento hasta 6,6±1,3mA, con una anchura del estímulo de 129±12 μs y una frecuencia fija de 40 impulsos/s en cada paciente. La frecuencia cardiaca y la presión arterial disminuyeron tras la activación de la TAB, pero de forma no significativa. Respecto a la eficacia, se observó una reducción significativa de la tasa anual de episodios de hospitalización por IC por paciente respecto al año previo al implante (1,52 frente a 0,76; p=0,042) y una tendencia a una mejoría de la clase funcional según la clasificación de la New York Heart Association (NYHA) al año (p=0,054). Sin embargo, no se observaron diferencias en el número de visitas ambulatorias que requirieron diurético intravenoso entre el año previo y el posterior al implante (24 frente a 20; p=0,450). Tampoco se observaron diferencias entre los valores basales y al año del implante en la fracción de eyección del ventrículo izquierdo (FEVI) (del 30±9,8% frente al 31,8±11,2%; p=0,689), el diámetro telediastólico del ventrículo izquierdo (58,79±6,2 frente a 60,6±5mm; p=0,325) y la mediana de valores de la fracción aminoterminal del propéptido natriurético cerebral (tipo B) (NT-proBNP): 1.119 [intervalo intercuartílico, 450-2.763] frente a 1.149 [499-4.798] pg/ml (p=0,756) (figura 1). Respecto a la seguridad, no hubo ninguna complicación local y no se observaron diferencias en la tasa anual de terapias apropiadas del DAI por paciente entre el año previo y el posterior al implante (0,53 frente a 0,58; p=0,902). Tres pacientes (14,2%) presentaron complicaciones menores durante el año de seguimiento relacionadas con la TAB (afonía, tos seca y dolor en el cuello), que no obligaron a suspenderla y se resolvieron reprogramando la estimulación. Tres pacientes (14,2%) fallecieron durante el seguimiento, 2 por IC refractaria y 1 por ictus no relacionado con el implante del dispositivo.
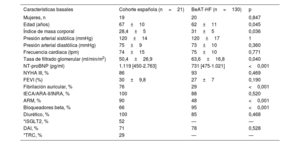
Comparación de las características basales entre la cohorte española y la del ensayo clínico BeAT-HF
| Características basales | Cohorte española (n=21) | BeAT-HF (n=130) | p |
|---|---|---|---|
| Mujeres, n | 19 | 20 | 0,847 |
| Edad (años) | 67±10 | 62±11 | 0,045 |
| Índice de masa corporal | 28,4±5 | 31±5 | 0,036 |
| Presión arterial sistólica (mmHg) | 120±14 | 120±17 | 1 |
| Presión arterial diastólica (mmHg) | 75±9 | 73±10 | 0,360 |
| Frecuencia cardiaca (lpm) | 74±15 | 75±10 | 0,771 |
| Tasa de filtrado glomerular (ml/min/m2) | 50,4±26,9 | 63,6±16,8 | 0,040 |
| NT-proBNP (pg/ml) | 1.119 [450-2.763] | 731 [475-1.021] | <0,001 |
| NYHA III, % | 86 | 93 | 0,469 |
| FEVI (%) | 30±9,8 | 27±7 | 0,190 |
| Fibrilación auricular, % | 76 | 29 | <0,001 |
| IECA/ARA-II/INRA, % | 100 | 88 | 0,520 |
| ARM, % | 90 | 48 | <0,001 |
| Bloqueadores beta, % | 66 | 95 | <0,001 |
| Diurético, % | 100 | 85 | 0,468 |
| *iSGLT2, % | 52 | — | — |
| DAI, % | 71 | 78 | 0,528 |
| *TRC, % | 29 | — | — |
ARA-II: antagonistas del receptor de la angiotensina II; ARM: antagonistas del receptor de mineralocorticoides; DAI: desfibrilador automático implantable; FEVI: fracción de eyección del ventrículo izquierdo; IECA: inhibidores de la enzima de conversión de la angiotensina; INRA: inhibidor de la neprilisina y el receptor de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral (tipo B); NYHA: clase funcional de la New York Heart Association; TRC: terapia de resincronización cardiaca.
Los valores expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
Comparación de eventos en cada sujeto 1 año antes y 1 año después del implante: tasa de ingresos por insuficiencia cardiaca y clase funcional de la NYHA. Características basales principales de la muestra del estudio. ARA-II: antagonistas del receptor de la angiotensina II; ARM: antagonistas del receptor de mineralocorticoides; DLP: dislipemia; DM: diabetes mellitus; FEVI: fracción de eyección del ventrículo izquierdo; HTA: hipertensión arterial; IECA: inhibidores de la enzima de conversión de la angiotensina; INRA: inhibidor de la neprilisina y el receptor de la angiotensina; iSGLT2: inhibidor del cotransportador de sodio-glucosa tipo 2; MCD: miocardiopatía; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral (tipo B); NYHA: clase funcional de la New York Heart Association; TRC: terapia de resincronización cardiaca.
Los resultados del presente estudio resumen por primera vez la experiencia en la práctica real en España con TAB en pacientes con IC-FEr y muestran que, en una población con IC sintomática pese a un tratamiento óptimo, su uso se asocia con una reducción de los ingresos por IC y una tendencia a la mejora de la clase funcional de la NYHA al año del implante, sin complicaciones relevantes. Nuestros datos corroboran la seguridad de la TAB en pacientes con IC-FEr comunicada en estudios previos1,2 y resaltan el beneficio pronóstico demostrado al disminuir los ingresos por IC. No se observó mejora en las cifras de péptido natriurético, clase funcional de la NYHA o la FEVI al año del implante, probablemente debido al escaso tamaño muestral y el corto periodo de seguimiento. El beneficio clínico en reducir ingresos por IC es un hallazgo importante, ya que, en comparación con la población del ensayo BeAT-HF2, los primeros pacientes con TAB en España son claramente de más edad y con peor función renal, mayor prevalencia de fibrilación auricular y concentraciones de NT-proBNP más altas, lo cual refleja en conjunto una cohorte con una IC más avanzada en un grupo de pacientes que ya se beneficiaban de un excelente tratamiento farmacológico y de dispositivos previos (aunque casi un tercio de la cohorte portaba una TRC, el implante del dispositivo a estos pacientes se realizó fuera de indicaciones previamente evaluadas). Además, este grupo considera que la TAB también podría ser una alternativa terapéutica atractiva para pacientes que no toleran los bloqueadores beta (el 34% de nuestra cohorte), cuya TAB pudo ajustarse igualmente hasta alcanzar una energía de estimulación similar a la de los pacientes que sí los toleran (6,8 frente a 6,9 mA; p=0,449); sin embargo, este potencial beneficio debería confirmarse en un trabajo dirigido a probar esta hipótesis. Otro subgrupo de especial interés clínico podría ser el de pacientes con insuficiencia renal crónica y resistencia a diuréticos, ya que en nuestra serie se observó una tendencia a una menor necesidad y en menores dosis de diuréticos del asa, con una cierta estabilización del filtrado glomerular 1 año después del implante. Desde el punto de vista mecanístico, la inhibición inmediata del sistema nervioso simpático por TAB podría conducir a un bloqueo mayor del sistema renina-angiotensina-aldosterona y, en último término, a protección cardiorrenal, lo cual deberá corroborarse en futuros estudios.
En conclusión, la experiencia en la vida real en España con TAB en pacientes con IC-FEr sintomáticos a pesar de un tratamiento médico óptimo es positiva y se asocia con una reducción de los ingresos por IC y una tendencia a la mejora de la clase funcional de la NYHA al año del implante, sin complicaciones relevantes. La comunicación de los resultados a largo plazo de los ensayos clínicos en marcha y nuevos datos en la práctica clínica ayudarán a posicionar esta prometedora técnica en el algoritmo de tratamiento de los pacientes con IC-FEr.
FINANCIACIÓNLos autores declaran no haber recibido financiación para la realización de este trabajo.
CONSIDERACIONES ÉTICASEl estudio se realizó tras la aprobación del comité de ética del centro coordinador. Se eximió de la obtención de un consentimiento informado por el carácter observacional y retrospectivo del estudio. Para el presente trabajo no se implementaron las guías SAGER, lo cual es una limitación del estudio.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALNo se empleó inteligencia artificial para el presente trabajo.
CONTRIBUCIÓN DE LOS AUTORESD. Cordero Pereda y C. de Rueda Panadero contribuyeron por igual a este trabajo como primeros autores elaborando la versión inicial del manuscrito. D. Cordero Pereda y J. Álvarez-García concibieron y diseñaron el estudio, además de analizar los datos. C. de Rueda Panadero, J. de Juan Bagudá, M. Gómez Bueno y A. Robles-Mezcua obtuvieron e interpretaron los datos y participaron en la revisión crítica y la discusión. Todos los autores dieron su aprobación final para la versión a publicar.
CONFLICTO DE INTERESESLos autores no declaran conflictos de intereses en relación con el estudio.
Los autores garantizan que los siguientes investigadores se hacen responsables de los datos contenidos en este trabajo: David Cordero Pereda, Clemencia de Rueda Panadero, Susana del Prado Díez, Marta Jiménez-Blanco Bravo, Paloma Remior Pérez, Sandra González Martín, Claudio Gandarias Zúñiga, José Luis Zamorano Gómez y Jesús Álvarez-García, del Hospital Universitario Ramón y Cajal, Madrid; Javier de Juan Bagudá y Rafael Salguero Bodes, del Hospital Universitario 12 de Octubre, Madrid; Manuel Gómez Bueno y Javier Segovia Cubero, del Hospital Universitario Puerta de Hierro, Madrid; Ainhoa Robles-Mezcua y José Manuel García Pinilla, del Hospital Universitario Virgen de la Victoria, Málaga, y José Cordero Guevara, del Instituto de Investigación Sanitaria Bioaraba, Vitoria.