En el presente artículo se hace una revisión de las publicaciones y los estudios presentados más relevantes en el ámbito de la cardiología intervencionista en el año 2012. El intervencionismo coronario en el contexto del infarto con elevación del ST ocupa un lugar destacado con estudios que confirman la importancia de reducir los tiempos de reperfusión y otros que evalúan diferentes dispositivos y estrategias farmacológicas en la angioplastia primaria. Los estudios comparativos entre stents farmacoactivos de diferentes generaciones son múltiples e indican una progresión positiva en eficacia y especialmente en seguridad. Con las nuevas generaciones de stents farmacoactivos, la trombosis tardía resulta casi equivalente a la de los stents metálicos. Los resultados con stents en la lesión del tronco común o en la enfermedad multivaso también se han abordado en importantes ensayos. Entre las técnicas de diagnóstico intracoronario, destacan los estudios de correlación entre técnicas de imagen y de presión intracoronaria. El intervencionismo cardiaco estructural y concretamente el implante de válvula aórtica y la reparación mitral continúan generando muchas publicaciones, especialmente la primera. Finalmente, la denervación renal ocupa ya un lugar destacado en la literatura médica.
Palabras clave
La importancia de las demoras en la reperfusión con intervencionismo coronario percutáneo (ICP) primario queda de nuevo bien establecida con un registro de 107.028 pacientes tratados con fibrinolisis o traslado a otro centro para ICP1. Se observó que una demora para la segunda estrategia > 120 min anulaba el beneficio de la supervivencia. El grupo PROGALIAM, pionero en nuestro país en el diseño de estos programas en red, puso de manifiesto que su aplicación ha permitido incrementar la proporción de pacientes tratados con angioplastia primaria manteniendo los resultados de esta terapia2.
StentsEn cuanto a los dispositivos empleados en ICP, concretamente los stents farmacoactivos (SFA), se ha publicado el ensayo XAMI, que comparó los stents liberadores de everolimus (SLE) con los stents liberadores de sirolimus (SLS) y muestra la no inferioridad de los primeros e incluso con tendencia a mejores resultados3.
El registro español ESTROFA-MI, comparó los SLE y los stents liberadores de paclitaxel en 734 pacientes. Se observó menor incidencia de trombosis e infarto y una fuerte tendencia a menor necesidad de revascularizaciones con los SLE4.
Otros dispositivos en este contexto son los balones liberadores de paclitaxel. En el estudio aleatorizado DEB-AMI, el uso de estos balones junto con stents metálicos (SM) presentó más reestenosis que con SFA y similar incidencia que con los SM solos5.
Acceso vascularEl acceso vascular se evaluó en el amplio estudio RIFLE, en el que se aleatorizó a 1.001 pacientes con infarto a vía radial o femoral6. El uso de la vía radial se asoció a menor incidencia de eventos adversos a 30 días (el 13,6 frente al 21%; p = 0,003).
Enfermedad multivasoEl abordaje óptimo de los pacientes con infarto agudo de miocardio y enfermedad multivaso fue objeto de un amplio metaanálisis. Se evidenció que la revascularización múltiple en el mismo procedimiento de ICP primario tenía efectos adversos y que, en cambio, la intervención diferida sobre las lesiones no causales tenía resultados favorables7.
Apoyo al intervencionismo coronario percutáneo primarioEn cuanto al tratamiento farmacológico concomitante, el estudio AIDA STEMI, con 2.065 pacientes, no demostró que la administración intracoronaria frente a la intravenosa de abciximab redujese el objetivo primario de muerte, infarto e insuficiencia cardiaca a 90 días (el 7 frente al 7,6%), pero se asoció a menor incidencia de insuficiencia cardiaca (el 2,4 frente al 4,1%; p = 0,04), por lo que, dada su seguridad, cabe recomendar su uso8.
Los dispositivos de trombectomía y el uso de abciximab intracoronario con microcatéter específico ClearWay® fueron objeto de un ensayo con aleatorización factorial (INFUSE AMI), en el que el objetivo primario era el tamaño del infarto a 30 días medido por resonancia magnética9. No se apreció beneficio con la trombectomía, pero sí con el abciximab intracoronario (reducción absoluta del 2,8%), muy especialmente si se combina con trombectomía.
Síndrome coronario agudo sin elevación del STRespecto al tratamiento antiagregante, un estudio de 302 pacientes tratados con carga de prasugrel encontró que una cuarta parte de ellos tenían una inhibición plaquetaria subóptima a las 6-12 h, hecho que se relacionó con un incremento de los eventos clínicos10.
Un subestudio del PLATO con ticagrelor encontró menos beneficio en los pacientes incluidos en Norteamérica frente a los del resto del mundo, diferencia que podría explicarse, al menos en parte, por la mayor dosis de ácido acetilsalicílico que recibieron los primeros, que redujo el impacto positivo del fármaco11.
En cuanto a los anticoagulantes, en el ensayo ATLAS, con más de 15.000 pacientes con síndrome coronario agudo, la dosis de rivaroxabán de 2,5 mg dos veces al día redujo la mortalidad a 13 meses respecto a placebo y la dosis de 5 mg, pero con un significativo incremento de hemorragias importantes y hemorragias intracraneales, sin aumento de las mortales12. Un estudio con apixabán se interrumpió prematuramente por incremento significativo de las hemorragias sin beneficio en los eventos isquémicos13.
AncianosEl ICP en el síndrome coronario agudo sin elevación del segmento ST de pacientes octogenarios fue objeto de estudio por un grupo español que encontró beneficios clínicos en su aplicación14. Los pacientes tenían en su mayoría perfil de alto riesgo y, tras ajuste por índice de propensión de tratamiento, se observó que la revascularización se asociaba a reducciones en muerte, infarto y eventos cardiacos adversos mayores en su conjunto.
DiabéticosSe comparó la cirugía con los SFA en un registro coreano de 891 pacientes diabéticos con enfermedad multivaso en seguimiento a 5 años. Tras los ajustes estadísticos, no se observaron diferencias significativas en muerte, infarto e ictus, pero la revascularización fue más frecuente con los SFA15.
TIPOS DE LESIÓN CORONARIATronco comúnSe ha publicado una segunda fase del estudio PRECOMBAT, que comparaba cirugía con el SLS. En el PRECOMBAT-2 se comparan estos dos grupos con uno tratado con SLE. Los pacientes que recibieron el SLE tuvieron una tasa general de eventos a 18 meses comparable con las de los SLS y la cirugía16. La necesidad de revascularizaciones fue menor con cirugía y similar entre los SFA. Un amplio registro internacional (DELTA), con 2.775 pacientes, comparó cirugía y SFA, y halló diferencias únicamente en la necesidad de nuevas revascularizaciones, menos frecuentes tras cirugía, a los 3 años de seguimiento17.
También se conocieron los resultados de dos estudios multicéntricos españoles. En el primero, se estudió la evolución de 226 pacientes no candidatos a cirugía18. La incidencia de eventos durante el seguimiento fue alta; los predictores adversos fueron el sexo femenino, la disfunción ventricular y el uso de SM. El otro registro es el ESTROFA-LM19, que comparó los SFA de paclitaxel con los SLE en 770 pacientes. No se encontraron diferencias clínicas significativas entre los stents aun tras ajustar por propensión de tratamiento. El uso de dos stents en lesiones distales resultó un predictor adverso.
Finalmente, un metaanálisis de los cuatro ensayos disponibles no mostró diferencias entre SFA y cirugía en los eventos totales a 1 año (el 14,5 frente al 11,8%; p = 0,1), aunque la necesidad de revascularización fue menor con cirugía y hubo menos ictus con SFA, mientras que la muerte y el infarto fueron similares20.
Enfermedad multivasoUn registro coreano, con más de 3.000 pacientes y 5 años de seguimiento, detectó incidencias similares de muerte y más necesidad de revascularización con SFA que con cirugía21.
Oclusiones crónicasLa tasa de éxito de repermeabilización de lesiones crónicas ha aumentado en los últimos años. Dos estudios han puesto de manifiesto que los pacientes tratados con éxito presentan menor tasa de eventos cardiacos mayores que aquellos con resultado fallido22,23. Un estudio español ha investigado los determinantes de éxito de la recanalización empleando tomografía computarizada; han descrito que un arco de calcificación > 50% en las porciones proximal y media de la oclusión es el único predictor de fracaso24.
El estudio CIBELES, con 207 pacientes aleatorizados en España y Portugal, comparó los SLE y los SLS en el tratamiento de las oclusiones crónicas. Los resultados muestran la no inferioridad de los primeros respecto al objetivo angiográfico con una evolución clínica comparable. No obstante, hubo una notable tendencia a menos trombosis con los SLE25.
Lesiones en bifurcacionesUn estudio aleatorizado del grupo CORPAL comparó los SLE y SLS en pacientes tratados con estrategia de implante de un solo stent en vaso principal, sin encontrar diferencias en eventos clínicos (muerte, infarto y revascularización) a 1 año26.
Venas safenasSe ha publicado recientemente un estudio aleatorizado de angioplastia en injertos de safena con SFA de primera generación frente a SM en 610 pacientes. Los resultados muestran una reducción significativa del objetivo primario (muerte, infarto y revascularización de la lesión tratada) en el grupo de pacientes tratados con SFA, a expensas principalmente de reducción de la revascularización de la lesión tratada27.
ReestenosisUn estudio coreano aleatorizó a 96 pacientes con reestenosis focales de SFA a SLS o balón de corte y 66 con reestenosis difusas a SLS o SLE. Los SLS fueron superiores para tratar las lesiones focales, mientras que los resultados de ambos stents fueron comparables en las lesiones difusas28.
El estudio español RIBS-3 evaluó el tratamiento de las reestenosis de SFA con un SFA diferente frente a otras alternativas29. Con una mediana de seguimiento de algo más de 2 años, el tratamiento con otro SFA resultó superior (muerte, infarto y revascularización de la lesión tratada, el 23 frente al 35%; p = 0,039).
STENTS FARMACOACTIVOSStents farmacoactivos de segunda generaciónEl estudio RESET incluyó a 3.197 pacientes aleatorizados a SLE o SLS30. El objetivo primario de revascularización de la lesión tratada a 1 año era muy similar (el 4,3% con SLE y el 5% con SLS), así como la trombosis definitiva (el 0,32 y el 0,38%).
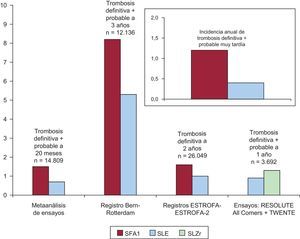
Diversos estudios, metaanálisis y revisiones han puesto de manifiesto de manera coincidente una menor incidencia de trombosis definitiva o probable con los SLE en comparación con los SFA de primera generación, en especial los de paclitaxel31–36. En un extenso metaanálisis en red, los SLE mostraron menor riesgo de trombosis a 2 años que los demás SFA e incluso que los SM36 (fig. 1).
Comparación de incidencias de trombosis entre stents farmacoactivos de primera y segunda generación. SFA1: stents farmacoactivos de primera generación; SLE: stent liberador de everolimus; SLZr: stent liberador de zotarolimus RESOLUTE. Reproducido con permiso de de la Torre Hernández y Windecker35.
El estudio TWENTE utilizó stents de zotarolimus (Resolute®) en 1.391 pacientes no seleccionados (all comers), en comparación con los SLE; se estableció la no inferioridad frente a estos37. El registro RESOLUTE US arrojó resultados excelentes en 1.402 pacientes tratados con el stent Resolute®, con trombosis a 1 año del 0,1% y revascularización de la lesión tratada del 2,8%38.
Stents farmacoactivos con polímero bioabsorbibleEl estudio LEADERS a 4 años reflejó menor incidencia de trombosis con stents de biolimus y polímero bioabsorbible que con los SLS de polímero estable39. El metaanálisis de los tres ensayos ISAR-TEST 3, ISAR-TEST 4 y LEADERS detectó menor riesgo de trombosis a 4 años con los SFA de polímero degradable que con los de polímero estable, especialmente en la fase tardía40.
Un nuevo SFA de polímero absorbible (Synergy®) con liberación abluminal de everolimus se evaluó en el estudio EVOLVE, con una pérdida luminal a 6 meses de 0,1 mm (0,13 con la mitad de dosis del fármaco)41.
Stents farmacoactivos plenamente bioabsorbiblesLa segunda generación del SLE bioabsorbible mostró a los 12 meses una pérdida luminal de 0,27 mm, manteniendo el área de soporte vascular y con un 97% de recubrimiento de los struts que terminan por disolverse totalmente en 2 años42.
BALÓN LIBERADOR DE FÁRMACOEl ensayo PEPCAD-DES aleatorizó a 110 pacientes con reestenosis tras el implante de SFA a balón de paclitaxel o balón convencional, y mostró la superioridad del primero con reestenosis del 17,2 y el 58,1% respectivamente (p < 0,001)43.
TROMBOSIS DE STENTS Y ANTIAGREGACIÓNUn estudio colaborativo de 30 estudios y con 221.066 pacientes reflejó que los más importantes factores de riesgo de trombosis del stent son la suspensión precoz de la antiagregación, la extensión de la coronariopatía y el número y la longitud de los stents44. El estudio TRIGGER PCI ha demostrado que el uso de prasugrel en pacientes con alta reactividad plaquetaria en tratamiento con clopidogrel permite lograr un nivel adecuado de inhibición plaquetaria45. Su tamaño muestral muy escaso impidió mostrar beneficio clínico con esta estrategia.
Respecto a la duración del tratamiento antiplaquetario doble, en el estudio RESET se aleatorizó a 2.117 pacientes a terapia doble durante 3 meses con stents de zotarolimus (Endeavor®) o tratamiento estándar con otros SFA de segunda generación. El estudio estableció la no inferioridad del tratamiento durante 3 meses, con trombosis al año del 0,2% (el 0,3% en el grupo estándar)46.
TÉCNICAS DE DIAGNÓSTICO INTRACORONARIOImagen intracoronariaEl tronco común sigue siendo objeto de estudios para definir los parámetros de significación de la estenosis coronaria mediante ecografía intracoronaria. Un estudio coreano identificó que un área luminal de 4,8 mm2 se correlaciona bien con la reserva fraccional de flujo (RFF)47. Sin embargo, se trata de un estudio de pequeño tamaño (55 pacientes) sin validación clínica prospectiva, ya que no hubo adherencia al protocolo (se revascularizó a un 30% de los pacientes con RFF > 0,8) y no se comunica seguimiento clínico. Además, se sabe que las diferencias poblacionales (raciales) pueden tener puntos de corte diferentes, dada las diferencias de tamaño corporal. En el ámbito del tronco común, el ya citado registro ESTROFA-LM comunicó un impacto positivo con el uso de la ecografía intracoronaria en ICP del tronco distal19.
Un estudio español de notable calidad evaluó con las tres técnicas —ecografía intracoronaria, tomografía de coherencia óptica y RFF— una serie de 61 lesiones intermedias48. Aunque la coherencia óptica mostró mayor eficiencia diagnóstica que la ecografía intracoronaria para identificar una lesión con RFF < 0,8, su utilidad para definir la gravedad de la lesión está también muy limitada por su baja especificidad. El área luminal predictora de RFF < 0,8 con esta técnica fue de 2 mm2.
Guía de presiónUn estudio español demostró que el empleo de RFF es muy útil en la evaluación de lesiones no causales en pacientes con síndrome coronario agudo. Tras 1 año, sólo el 3,7% de las lesiones no tratadas precisó ICP49.
El estudio FAME II aleatorizó a pacientes con angina estable y al menos una lesión con RFF < 0,8 a ICP más tratamiento médico óptimo o tratamiento médico solo50. Un exceso de eventos en el grupo de tratamiento médico único obligó a acabar el estudio prematuramente. Estos resultados contribuyen a explicar la ausencia de beneficio clínico observado con el ICP en ensayos como el COURAGE, estudios en que con gran probabilidad se habría incluido a una proporción notable de pacientes con lesiones angiográficamente significativas (estenosis > 50%), pero sin alteración de flujo (RFF > 0,8).
Resulta muy novedosa la obtención mediante guía de presión del índice instantaneous wave-free ratio, que muestra una excelente correlación con la RFF y podría ser una alternativa a esta, ya que además no precisa infusión de adenosina51.
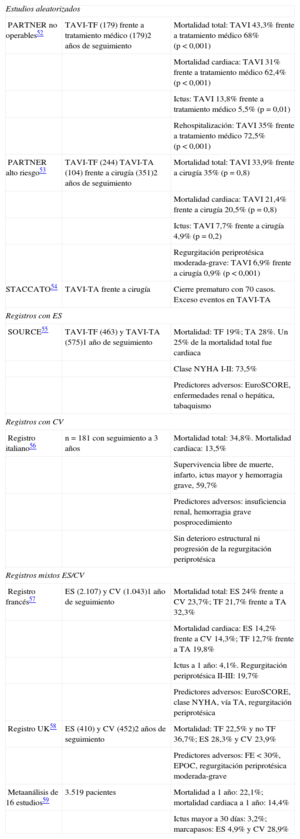
INTERVENCIONISMO CARDIACO ESTRUCTURALImplantación percutánea de prótesis valvular aórticaEste año se han publicado los resultados a 2 años de las dos partes del ensayo PARTNER, la de pacientes inoperables y la de alto riesgo quirúrgico52,53. También se publicaron diversos registros, entre los que destacan el francés, por su gran tamaño, y un amplio metaanálisis54–59. En la tabla se resumen los hallazgos principales de estos estudios.
Estudios sobre implantación transcatéter de prótesis valvulares aórticas
| Estudios aleatorizados | ||
| PARTNER no operables52 | TAVI-TF (179) frente a tratamiento médico (179)2 años de seguimiento | Mortalidad total: TAVI 43,3% frente a tratamiento médico 68% (p < 0,001) |
| Mortalidad cardiaca: TAVI 31% frente a tratamiento médico 62,4% (p < 0,001) | ||
| Ictus: TAVI 13,8% frente a tratamiento médico 5,5% (p = 0,01) | ||
| Rehospitalización: TAVI 35% frente a tratamiento médico 72,5% (p < 0,001) | ||
| PARTNER alto riesgo53 | TAVI-TF (244) TAVI-TA (104) frente a cirugía (351)2 años de seguimiento | Mortalidad total: TAVI 33,9% frente a cirugía 35% (p = 0,8) |
| Mortalidad cardiaca: TAVI 21,4% frente a cirugía 20,5% (p = 0,8) | ||
| Ictus: TAVI 7,7% frente a cirugía 4,9% (p = 0,2) | ||
| Regurgitación periprotésica moderada-grave: TAVI 6,9% frente a cirugía 0,9% (p < 0,001) | ||
| STACCATO54 | TAVI-TA frente a cirugía | Cierre prematuro con 70 casos. Exceso eventos en TAVI-TA |
| Registros con ES | ||
| SOURCE55 | TAVI-TF (463) y TAVI-TA (575)1 año de seguimiento | Mortalidad: TF 19%; TA 28%. Un 25% de la mortalidad total fue cardiaca |
| Clase NYHA I-II: 73,5% | ||
| Predictores adversos: EuroSCORE, enfermedades renal o hepática, tabaquismo | ||
| Registros con CV | ||
| Registro italiano56 | n = 181 con seguimiento a 3 años | Mortalidad total: 34,8%. Mortalidad cardiaca: 13,5% |
| Supervivencia libre de muerte, infarto, ictus mayor y hemorragia grave, 59,7% | ||
| Predictores adversos: insuficiencia renal, hemorragia grave posprocedimiento | ||
| Sin deterioro estructural ni progresión de la regurgitación periprotésica | ||
| Registros mixtos ES/CV | ||
| Registro francés57 | ES (2.107) y CV (1.043)1 año de seguimiento | Mortalidad total: ES 24% frente a CV 23,7%; TF 21,7% frente a TA 32,3% |
| Mortalidad cardiaca: ES 14,2% frente a CV 14,3%; TF 12,7% frente a TA 19,8% | ||
| Ictus a 1 año: 4,1%. Regurgitación periprotésica II-III: 19,7% | ||
| Predictores adversos: EuroSCORE, clase NYHA, vía TA, regurgitación periprotésica | ||
| Registro UK58 | ES (410) y CV (452)2 años de seguimiento | Mortalidad: TF 22,5% y no TF 36,7%; ES 28,3% y CV 23,9% |
| Predictores adversos: FE < 30%, EPOC, regurgitación periprotésica moderada-grave | ||
| Metaanálisis de 16 estudios59 | 3.519 pacientes | Mortalidad a 1 año: 22,1%; mortalidad cardiaca a 1 año: 14,4% |
| Ictus mayor a 30 días: 3,2%; marcapasos: ES 4,9% y CV 28,9% | ||
CV: CoreValve®; EPOC: enfermedad pulmonar obstructiva crónica; ES: Edwards-SAPIEN®; FE: fracción de eyección; NYHA: New York Heart Association; TA: transapical; TAVI: implante transcatéter de prótesis valvular aórtica; TF: transfemoral.
Los aspectos destacables son:
- •
Comparable incidencia de mortalidad entre los dispositivos.
- •
Mayor mortalidad con la vía transapical (relacionada en parte con un mayor riesgo basal).
- •
Una proporción importante de la mortalidad a medio-largo plazo es no cardiaca.
- •
La incidencia de ictus al año es de un 4-6%.
- •
Impacto pronóstico adverso de la regurgitación periprotésica, que es moderada o grave al año en un 7-20%.
Otros trabajos interesantes en este campo son las primeras series de implante transaórtico directo con ambos sistemas (CoreValve® y Edwards-SAPIEN®) y el implante en homoinjertos degenerados60–62.
Reparación percutánea de la válvula mitralDos subestudios del EVEREST II evaluaron los resultados en pacientes con fibrilación auricular y en pacientes de alto riesgo quirúrgico63,64. En ambos subgrupos se apreció el beneficio de la técnica en la evolución tanto clínica como ecocardiográfica.
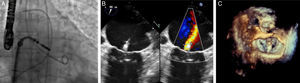
El estudio PERMIT-CARE abordó el grupo de pacientes con respuesta fallida a la resincronización. Se observó que tras la reparación mitral había una mejoría de la clase funcional de los pacientes, con reducción de los volúmenes y aumento de la función ventricular65. La figura 2 muestra imágenes de un procedimiento de implante de MitraClip®.
Foramen oval permeableRecientemente se ha publicado un metaanálisis de cierre percutáneo frente a tratamiento médico como prevención de eventos en pacientes con ictus previo debidos presumiblemente a embolias paradójicas. Se incluyen varios dispositivos de cierre. La incidencia de eventos neurológicos tras el cierre fue de 0,8 eventos/100 pacientes-año y de 5 con tratamiento médico66.
Comunicaciones interauricularesUna revisión de los casos publicados sobre erosión de aorta y aurícula izquierda asociados a los dispositivos de cierre percutáneo registró un total de 104 casos notificados con el dispositivo Amplatzer® (tasa estimada de un 0,1-0,3%) relacionados con dispositivos sobredimensionados y borde retroaórtico deficiente67.
El registro REPERA ha incluido de manera retrospectiva a 450 pacientes con defectos septales tratados con dispositivos oclusores grandes (> 26 mm) en 20 hospitales de España y Portugal68. El procedimiento se desarrolló con éxito en el 92% de los pacientes; en el 4,4% no se pudo implantar y en el 3,6% se embolizó en las primeras 24 h. Durante el seguimiento, las complicaciones serias suponen el 1,8% (embolización, 0,8%; mala aposición, 0,6%; perforación, 0,4%). Un borde inferior deficiente y un tamaño muy grande del dispositivo (≥ 38 mm) fueron los predictores del fracaso.
Orejuela izquierdaUn subanálisis del estudio PROTECT AF ha analizado la frecuencia y el impacto clínico del cierre incompleto de la orejuela tras el implante percutáneo de dispositivo. El estudio mediante ecocardiografía transesofágica mostró que el 32% de los pacientes tienen algún grado de fuga a los 12 meses del implante, pero esto no se asocia con un aumento del riesgo de embolia sintomática69.
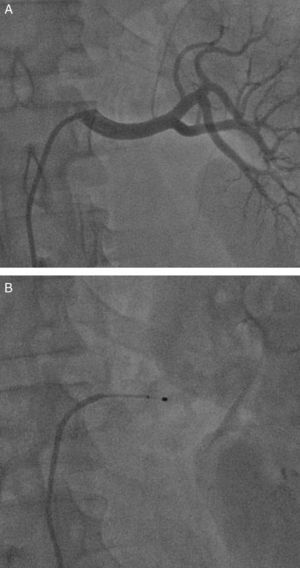
DENERVACIÓN RENALEn un estudio con 50 pacientes (37 tratados y 13 controles con seguimiento a 3 meses), además de la reducción de la presión arterial, se encontraron reducciones de glucosa en ayunas, insulina y péptido C70. En otro estudio con 64 pacientes (46 tratados y 18 controles con seguimiento a 6 meses), se observo reducción de la hipertrofia y mejoría de la función ventricular71. La figura 3 muestra imágenes angiográficas de un procedimiento de denervación renal.
TERAPIA CELULARSe presentaron los resultados del ensayo FOCUS CCTRN en el congreso 2012 del American College of Cardiology72. El estudio aleatorizó a 92 pacientes con disfunción ventricular de origen isquémico crónico a inyección trasendocárdica de células mononucleares o placebo. A los 6 meses no se observaron cambios de la función-perfusión miocárdica o clínicos.
Un metaanálisis de 50 estudios determinó que la terapia con células de la médula ósea de adulto mejora la fracción de eyección un 4% y reduce los volúmenes ventriculares de manera constante a largo plazo73. También se observó mejora en la incidencia de muerte e infarto.
CONFLICTO DE INTERESESNinguno.