La posición final de las neocomisuras en el implante percutáneo de válvula aórtica (TAVI) es aleatoria, lo que podría dificultar el acceso coronario y procedimientos futuros. Nuestro objetivo es desarrollar un método estandarizado para conseguir el alineamiento de las comisuras con ACURATE neo.
MétodosLa relación entre las comisuras nativas y las neocomisuras de la válvula se analizó en 11 pacientes con estenosis aórtica grave sometidos a TAVI. Con base en la tomografía computarizada, se desarrolló un modelo in silico para predecir la posición final de los postes comisurales. A continuación, se desarrolló una técnica modificada de implante con alineamiento comisural adecuado (ACA) y un dispositivo específico para orientar el sistema de liberación. Por último, el implante de TAVI con alineamiento comisural se simuló en modelos impresos en 3D e in vivo. Se analizó el grado de mal alineamiento y de solapamiento coronario (SC).
ResultadosEl modelo in silico predijo con precisión la posición de los postes comisurales tanto para implantes convencionales (2) como aquellos con técnica de ACA (9) (coeficiente de correlación=0,994; IC95%, 0,989-0,998; p <0,001). El TAVI con una rotación del sistema específica para cada paciente se simuló con éxito en biomodelos y en 9 pacientes (mal alineamiento comisural medio in vivo, 7,7±3,9°). Ninguno de los implantes con técnica ACA presentó SC, mientras que la simulación in silico para los mismos casos pero mediante implante convencional predijo SC en 6 de los 9 casos.
ConclusionesEl alineamiento comisural preciso del dispositivo ACURATE neo es factible mediante la inserción del sistema de liberación rotado específicamente para cada paciente basándose en el análisis de la tomografía computarizada. Este método sencillo y reproducible de alineamiento comisural podría utilizarse con todo tipo de dispositivos para TAVI.
Palabras clave
Las indicaciones del implante percutáneo de válvula aórtica (TAVI) están evolucionando para incluir a pacientes cada vez con menor riesgo1–4. Al prolongarse la esperanza de vida de los receptores de TAVI, los resultados de la intervención deben tender a igualar los beneficios a largo plazo del recambio de válvula aórtica (RVAo) mediante cirugía en todos los aspectos. El alineamiento comisural se realiza habitualmente en el RVAo quirúrgico; sin embargo, la posición de las comisuras protésicas no se tiene en cuenta durante el TAVI5. Dado que los postes comisurales pueden interferir en los ostium coronarios, preocupa bastante que estos postes puedan dificultar el acceso coronario en futuras intervenciones coronarias o favorecer la obstrucción coronaria en un eventual TAVI en TAVI6. La magnitud del problema es importante, ya que análisis anteriores han mostrado una incidencia de solapamiento coronario (SC) que oscila entre el 31 y el 51%6, y solo el 22% de los casos de TAVI presentaban un adecuado alineamiento comisural5 y, como comunicaron recientemente Barbanti et al.7, en más del 7% de los casos el acceso coronario tras un TAVI puede fracasar. En la actualidad no existen métodos para lograr el alineamiento comisural con la mayoría de los dispositivos para TAVI disponibles.
El proyecto de alineamiento comisural preciso (accurate comisural alignment [ACA]) se creó para elaborar una técnica de implante con el objetivo de lograr el alineamiento entre las comisuras nativas y las neocomisura durante el TAVI con el dispositivo ACURATE neo (Boston Scientific, Estados Unidos). El presente estudio tiene como objetivo comprobar la siguiente hipótesis: a) el comportamiento rotacional del sistema de liberación del TAVI desde el acceso femoral hasta su zona de posicionamiento final es previsible y está relacionado con la orientación final de la prótesis en la raíz aórtica; b) se puede lograr un alineamiento neocomisural controlado del dispositivo ACURATE neo para TAVI planificando una rotación del sistema de liberación específica para cada paciente antes de hacerlo avanzar por la anatomía vascular, y c) un dispositivo fácil de usar creado específicamente para este propósito puede ayudar a lograr la orientación final deseada del dispositivo para TAVI en la raíz aórtica.
MÉTODOSSe analizó la relación entre las comisuras aórticas nativas y las comisuras de las válvulas cardiacas percutáneas (VCP) de 5 pacientes con estenosis aórtica grave sometidos a TAVI con el dispositivo ACURATE neo en diferentes circunstancias. Estas se diferenciaban en: a) si se había realizado un implante de VCP convencional o modificado con el objetivo de lograr el alineamiento comisural, y b) si el implante fue simulado (por ordenador o en modelos impresos tridimensionales [3D]) o in vivo. En 2 pacientes ya se había realizado un TAVI antes del diseño del estudio (grupo de implante convencional por ordenador e in vivo) y en 3 pacientes se planificaron TAVI prospectivamente durante el transcurso del estudio (grupo de implante modificado por ordenador, en modelos impresos en 3D e in vivo). Se contó con tomografía computarizada (TC) de todos los pacientes antes y después de la intervención. Además, se obtuvo una TC después de las 3 intervenciones de implante modificado en modelos impresos en 3D. El proyecto ACA fue aprobado por el comité de ética local y los pacientes dieron su consentimiento informado.
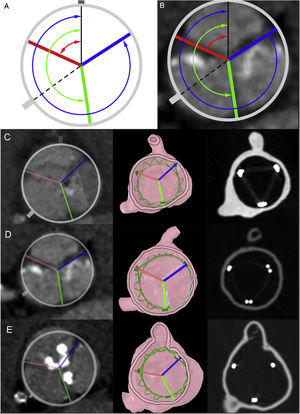
Adquisición y mediciones de tomografía computarizadaLas TC se adquirieron en un detector de 128 cortes con un grosor de corte de 0,625mm. Los estudios fueron potenciados, multifásicos y con sincronización electrocardiográfica; se seleccionó el 70% del ciclo cardiaco para su análisis. La orientación de los postes comisurales de las VCP, las comisuras de las válvulas nativas y la arteria coronaria izquierda (ACI) se midieron en una reconstrucción multiplanar perpendicular a la raíz aórtica; utilizando como punto de partida para las mediciones la arteria coronaria derecha (ACD; 0°) que se dispuso a las 12.00 asumiendo un sistema de orientación de un reloj de esfera, como se describió anteriormente5,8 y se muestra esquemáticamente en la figura 1. Las mediciones se realizaron desde el centro de la aorta o desde el centro del stent de la VCP cuando no había contacto completo de este con la aorta. Luego se midió la diferencia de ángulo de cada poste comisural respecto a la comisura nativa correspondiente y se calculó el defecto medio de alineamiento de la comisura (DAC) de cada implante como la diferencia media entre el poste de comisura protésico y la comisura nativa. El resultado se clasificó como alineado (0-15°), DAC leve (15-30°), DAC moderado (30-45°) y DAC grave (45-60°). El SC del poste comisural en relación con los ostium de la arteria coronaria se definió como un ángulo ≤ 20°.
Imágenes transversales de tomografías computarizadas previas al TAVI que resumen las medidas para la evaluación del grado de alineamiento comisural. A: la línea negra representa el ostium coronario derecho orientado a las 12 en punto; la línea discontinua representa el ostium coronario izquierdo; la línea azul representa la comisura entre el seno no coronario y el seno coronario derecho; la línea roja representa la comisura entre el seno coronario izquierdo y el seno coronario derecho; la línea verde representa la comisura entre el seno coronario izquierdo y el seno no coronario. Las flechas representan los 3 ángulos definidos por la coronaria derecha y cada comisura. B: esquema anterior superpuesto en una TC transversal previa al TAVI. C, D* y E: tomografías computarizadas previas al TAVI que muestran las comisuras de la válvula aórtica nativa (columna 1), simuladas in silico (columna 2) e in vitro (columna 3) tras el TAVI con alineamiento comisural de los casos 3, 4 y 5 respectivamente. *El stent del dispositivo ACURATE neo in silico está representado en verde. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Se utilizaron TC previas y posteriores al TAVI de los pacientes incluidos en el proyecto ACA de nuestro centro. En 2 pacientes, la posición final de la VCP implantada con la técnica estándar se simuló basándose en el análisis de la TC realizada antes y después de las intervenciones de TAVI convencional de la válvula ACURATE neo. Después se calculó prospectivamente en 3 pacientes la orientación ACA con base en la TC previa al TAVI. Los biomodelos aórticos derivados de la TC de los pacientes se obtuvieron mediante Slicer9; a continuación se calculó el eje central de la aorta, desde la aorta descendente hasta la raíz aórtica y el tracto de salida del ventrículo izquierdo. Las mallas y los ejes centrales de los biomodelos se importaron a un software de diseño asistido por ordenador (Rhinoceros, MCneel and Associates, Estados Unidos), con el que se realizaron los análisis posteriores.
Etapa 2: pruebas realizadas en modelos impresos en 3DLa necesaria rotación del sistema de liberación prevista para lograr un alineamiento correcto de las neocomisuras con las comisuras nativas se calculó mediante simulación in silico (orientación ACA). Posteriormente dicha rotación se utilizó en los implantes del dispositivo ACURATE neo realizados en modelos de impresión 3D específicos de cada paciente (impresos en nuestro Vall3DLab). Por último, se realizaron TC de los modelos 3D tras el implante de VCP para evaluar la precisión en la predicción del implante orientado. Se obtuvieron modelos impresos en 3D huecos a partir de TC previas al TAVI de 3 pacientes. Estos modelos en 3D estaban destinados a simular intervenciones de TAVI mediante guía angiográfica; para su elaboración se utilizaron múltiples materiales, incluido un material flexible con dureza similar a la silicona (formlabs elastic resin, Formlabs Inc, Estados Unidos) para permitir un comportamiento más realista de la raíz aórtica y las valvas durante el TAVI.
Se elaboró una herramienta específica para controlar con precisión la rotación axial del sistema de liberación del dispositivo (dispositivo ACA, número de solicitud de patente: P202030860). Esta herramienta simplemente permite medir los grados de rotación del sistema de liberación y consta de un elemento circular unido al manipulador. Las válvulas ACURATE neo se implantaron en los modelos impresos en 3D con la orientación ACA prevista, que se calculó utilizando los métodos por ordenador ya descritos. Después de cada implante, se grabaron las proyecciones angiográficas y se adquirieron TC del modelo impreso en 3D con la válvula implantada para comparar la orientación de los postes comisurales en la simulación por ordenador con la simulación in vitro. Se analizó el grado de desviación de los implantes por ordenador y los implantes in vitro con orientación ACA, que se presenta como la diferencia de los ángulos entre la ACD y cada poste comisural por ordenador e in vitro. El de simulación del TAVI con orientación ACA se describe en la figura 2.
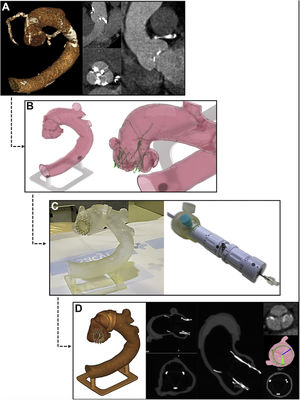
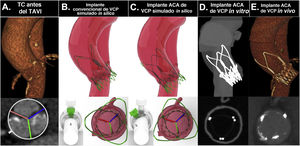
Resumen paso a paso para el cálculo de la orientación con alineamiento comisural preciso antes del procedimiento in vivo. A: imágenes de tomografía computarizada previas al TAVI. B: implante protésico simulado in silico con alineamiento comisural preciso. C: implante in vitro en un modelo del paciente impreso en 3D con alineamiento comisural preciso mediante la rotación del sistema de liberación según el ángulo de rotación calculado in silico y asistido con la herramienta de rotación específica. D: tomografía computarizada del modelo impreso en 3D después del implante de la prótesis para comprobar que se ha logrado el alineamiento comisural preciso según lo previsto.
Se realizaron implantes in vivo con orientación ACA en 9 pacientes consecutivos. En los primeros 3 pacientes se ensayó antes el TAVI en los modelos de impresión 3D obtenidos a partir de las TC previas al TAVI (implante in vitro) para después realizar las intervenciones in vivo con implementación de la orientación ACA de la válvula ACURATE neo. La rotación del sistema de liberación, facilitada por el sistema de implementación ACA, fue la misma en el modelo de impresión 3D específico de cada paciente. Una vez completado el TAVI, se grabaron las mismas proyecciones angiográficas en el modelo de impresión 3D y en los pacientes, y se comparó la orientación de los postes comisurales de la válvula con su correspondiente modelo impreso en 3D. Además, en todos los casos se realizó una TC después del TAVI para obtener una comparación precisa de la orientación de la válvula in vivo frente a simulaciones por ordenador e in vitro. Posteriormente se trató a otro 6 pacientes (casos 6-11) con implante de orientación ACA sin simulación in vitro previa. Las mediciones de la localización de los postes comisurales después del TAVI se realizaron mediante técnicas de corregistro de fluroscopia, como se ha descrito previamente6.
Análisis estadísticosLas diferencias entre las simulaciones in silico, in vitro e in vivo se calcularon tomando como referencia la orientación de la comisura nativa en cada caso y se presentan como media±desviación estándar. El grado de concordancia entre las diferentes medidas se obtuvo mediante el coeficiente de correlación de concordancia de Lin, tomando cada una de las medidas como independiente. Los análisis estadísticos se realizaron utilizando R 3.6.3 (R Foundation for Statistical Computing, Austria) y MedCalc 13.3.3 (MedCalc Software bvba, Bélgica).
RESULTADOSSimulación in silicoEn primer lugar, se demostró la hipótesis de que la rotación axial del sistema para TAVI cuando se lo hace avanzar a lo largo de la aorta está relacionada con el eje central de la aorta y permanece perpendicular al eje central de la aorta, como se muestra en la figura 3. Se identificó la orientación anatómica de los senos de Valsalva y la ubicación de los ostium coronarios. En una primera etapa, se simuló el implante comisural alineado. Para ello se importó un modelo en 3D de una válvula ACURATE neo al software de diseño asistido por ordenador y se orientó al eje central aórtico en la aorta descendente con un poste comisural alineado a las 12 en punto. A continuación, se hizo avanzar esta prótesis virtual hasta el plano de la válvula aórtica para obtener la posición previsible en su zona de posicionamiento en un implante de orientación convencional.
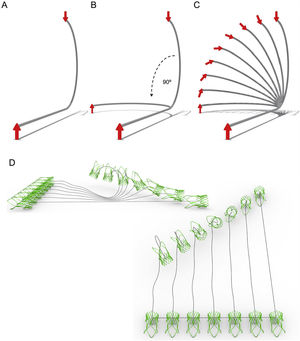
Modelo simplificado de la aorta para predecir la rotación del sistema de TAVI a lo largo de la aorta. A: simulación sin curvas latero-laterales; cuando se hace avanzar una flecha apuntando a las 12 en punto, llega al extremo distal de la curva apuntado a las 6.00. B: simulación cuando se añade una rotación de la curva de 90°. Cuando la flecha vuelva a avanzar apuntando a las 12 en punto, llegará al extremo distal apuntando a las 12.00. C: simulación del efecto de rotación del sistema con orientaciones intermedias de las curvas entre A y B. D: cuando la flecha se sustituye en el modelo por una prótesis simulada, se mantiene el mismo principio.
Luego se calculó la rotación óptima de la válvula para lograr el alineamiento comisural del implante utilizando un software de elaboración propia que permite una rotación controlada de la válvula virtual en 3D. Se realizó una rotación específica para cada paciente en sentido horario o antihorario, de modo que los postes comisurales de la prótesis coincidieran con las comisuras nativas en el biomodelo de la raíz aórtica, y esta orientación óptima del alineamiento comisural se consideró «la orientación ACA» (figura 4 y ).
La orientación prevista de la válvula se correlacionó bien con la posición final del implante convencional de la válvula ACURATE neo (con un poste comisural que apuntaba a las 12 en punto) y mostró una diferencia media entre la posición simulada y la real del poste de 6,1±5,2°. Las mediciones específicas de los casos retrospectivos se muestran en la . Además, en la tabla 1 se resumen el grado de mal alineamiento y el SC.
Grado de mal alineamiento comisural y solapamiento coronario en las simulaciones (in silico e in vitro) y después de intervenciones in vivo según el implante sea convencional o modificado (alineamiento comisural preciso)
| Implante convencional | Implante modificado (ACA) | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Caso 1 | Caso 2* | Caso 3 | Caso 4 | Caso 5 | Caso 6 | Caso 7 | Caso 8 | Caso 9 | Caso10 | Caso 11 | ||
| Simulaciones | ||||||||||||
| Por ordenador | DAC | 54,2 | 40,1 | 2,2 | 2,3 | 4,3 | 5,3 | 11,4 | 9,9 | 7,4 | 4,9 | 0,5 |
| SC | Ambas | ACI | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | |
| In vitro | DAC | - | - | 7,7 | 2,2 | 13,2 | - | - | - | - | - | - |
| SC | - | - | Ninguna | Ninguna | Ninguna | - | - | - | - | - | - | |
| Casos clínicos | ||||||||||||
| In vivo | DAC | 52,9 | 49,8 | 13,0 | 5,4 | 12,6 | 10,4 | 9,2 | 17,7 | 7,4 | 9,8 | 8,7 |
| SC | Ambas | ACI | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | Ninguna | |
DAC medio expresado en grados; SC expresado como ninguno o de ACD, ACI o ambas. ACA: alineamiento comisural preciso; ACD: arteria coronaria derecha; ACI: arteria coronaria izquierda; DAC: defecto de alineamiento de la comisura; SC: solapamiento coronario.
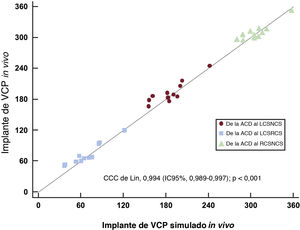
La concordancia de la orientación del poste comisural de los implantes de la VCP por simulación in silico con la orientación final del poste comisural fue elevada, tanto en implantes convencionales como en ACA (figura 5), con un coeficiente de correlación de concordancia de Lin de 0,994 (intervalo de confianza del 95% [IC95%], 0,989-0,997).
Correlación de la orientación del poste comisural por ordenador e in vivo según la tomografía computarizada posterior al TAVI. ACD: arteria coronaria derecha; CCC: coeficiente de correlación de concordancia; IC95%: intervalo de confianza del 95%; LCSNCS: poste comisural entre el seno coronario izquierdo y el seno no coronario; LCSRCS: poste comisural entre el seno coronario izquierdo y el seno coronario derecho; RCSNCS: poste comisural entre el seno coronario derecho y el seno no coronario; VCP: válvula cardiaca percutánea.
La necesaria rotación específica de cada paciente para lograr el implante con orientación ACA fue: 60, 35 y 45° en sentido antihorario en los casos 3, 4 y 5 (). Las diferencias de la orientación de las comisuras y la arteria coronaria izquierda (ACI) en la válvula nativa en las simulaciones por ordenador, in vitro e in vivo (orientación ACA) se presentan en la . El DAC medio in vitro de los 3 casos prospectivos fue de 8,2°±3,3° (caso 3), 5,2°±6,6° (caso 4) y 13,3°±1,9° (caso 5).
Validación in vivoNinguno de los 9 casos con orientación ACA presentó un solapamiento importante de los ostium coronarios; en cambio, según la simulación in silico de un implante con orientación convencional, 6 de 9 casos habrían tenido SC de 1 o las 2 arterias coronarias; en el caso 6, la válvula estaba correctamente alineada a 0° de rotación, lo que significa que el ACA y el implante convencional eran iguales. En los casos 3, 4 y 5, la rotación necesaria del sistema de liberación del implante ACA fue la misma que la del implante in vitro; en los casos 6-11, el sistema de liberación giró 0°, 55° en sentido horario, 20° en antihorario, 25° en antihorario, 60° en horario y 40° en horario respectivamente. Las VCP se giraron con precisión mediante el dispositivo ACA antes de avanzarse en el introductor. De esta forma se evitaron las fuerzas de torsión que habrían aparecido si la rotación se hubiera realizado en el interior del paciente.
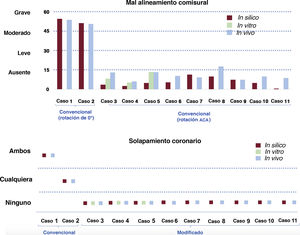
La incidencia de SC y el grado de DAC se resumen en la figura 6. El proceso desde la simulación del implante in silico en ordenador hasta el implante con orientación ACA in vivo de un dispositivo ACURATE neo se resume en la figura 7. Un total de 8 de los 9 implantes ACA presentaron alineamiento comisural; solo el caso 8 mostró un DAC leve (DAC medio de 17,7°±12,3°).
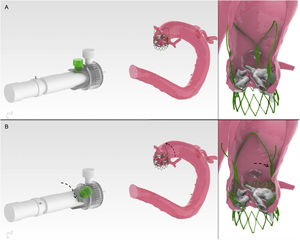
Análisis del caso y resultado tras el implante con alineamiento comisural preciso desde la simulación in silico hasta la intervención in vivo. A: válvula aórtica nativa en la tomografía computarizada de referencia. B y C: implante in silico con orientación convencional y con orientación ACA. D: tomografía computarizada de un modelo impreso en 3D e implante con orientación ACA. E: tomografía computarizada después del implante de la prótesis ACURATE neo con orientación ACA. ACA: alineamiento comisural preciso; TAVI: implante percutáneo de válvula aórtica; TC: tomografía computarizada; VCP: válvula cardiaca percutánea.
El TAVI, a diferencia del RVAo quirúrgico, en el que se extraen las valvas nativas y se implanta la válvula protésica manteniendo la orientación de las comisuras de la válvula nativa, no tiene en cuenta el alineamiento comisural del dispositivo. Se sospecha —aún se investiga— que con el alineamiento se puede obtener beneficio clínico; sin embargo, no se ha descrito ninguna estrategia estandarizada para lograrlo. Algunos autores son partidarios de la rotación del sistema de liberación en el interior de la aorta, pero esta estrategia es menos precisa y no está exenta de riesgos. Este proyecto prospectivo tenía como objetivo explorar la posibilidad de una planificación del alineamiento comisural previa a la intervención, y los principales hallazgos son los siguientes: a) la orientación rotacional del sistema de la VCP al avanzar hasta la raíz aórtica durante el TAVI con orientación convencional es predecible; b) por lo tanto, la necesaria rotación del sistema de liberación de la VCP para lograr un alineamiento comisural específico para cada paciente puede calcularse fácilmente a partir de la TC, y c) el implante ACA de la VCP ACURATE neo es factible mediante la simple rotación del sistema de liberación, que se puede realizar con precisión con el dispositivo ACA.
La evaluación del impacto clínico del alineamiento comisural respecto al TAVI convencional requiere una estrategia sistemática para ser reproducible. Esta es la primera descripción de una estrategia de este tipo y podría permitir el análisis del impacto del ACA en los resultados a corto, medio y largo plazo. Teniendo en cuenta los beneficios potenciales y la ausencia de riesgos de este sistema, es posible que esta estrategia se convierta en parte de la planificación estándar de las intervenciones de TAVI si se demuestra en series más grandes. Además, esta técnica permitiría la modificación de los diseños de los distintos dispositivos de TAVI actuales para, por ejemplo, reducir su fuerza radial en la zona adyacente al sistema de conducción, lo cual podría ayudar a disminuir la necesidad de un marcapasos permanente.
Acceso coronario en pacientes portadores de un dispositivo de implante percutáneo de válvula aórticaLa mayor esperanza de vida de los pacientes con bajo riesgo aumentará la probabilidad de que aparezca enfermedad coronaria o empeore una preexistente, lo cual hace más probable que requieran una coronariografía e intervención coronaria percutánea en el seguimiento. Aunque se dispone de guías de práctica clínica sobre el acceso coronario después del TAVI10,11, la duración de una intervención coronaria percutánea por un síndrome coronario agudo en un paciente con TAVI es mucho más larga, y en hasta un 3-9% de los pacientes, el acceso coronario puede ser imposible7,12. Las VCP de bajo perfil, como la VCP expandible con balón, facilitan más el acceso coronario que los dispositivos autoexpandibles más grandes, cuya estructura se alarga por encima de la unión sinotubular. En el registro RESOLVE, Ochiai et al.12 describieron la incidencia de características desfavorables para el acceso coronario tras un TAVI, que hallaron en el 25,8% de los casos en la ACD y el 34,8% en la ACI de pacientes portadores de un dispositivo Evolut Pro/Evolut R respecto al 8,1 y el 15,7% de los pacientes con SAPIEN-3. Curiosamente, estas características desfavorables originan una tasa considerablemente inferior de cateterización coronaria selectiva exitosa con ambos dispositivos.
En 100 implantes convencionales de ACURATE neo, Tang et al.6 comunicaron una incidencia del 51% de SC grave de 1 o las 2 arterias coronarias. Observaron que una orientación intuitiva de los postes comisurales determinada en la vista coplanar de las cúspides (orientados hacia la curva interna de la aorta) se asociaba con una reducción de la incidencia de SC a menos del 15%. En 7 casos se realizaron maniobras para orientar de este modo los postes comisurales, y aunque la tasa de obstrucción coronaria se redujo, se mantuvo en una tercera parte de los pacientes e implicó una manipulación del sistema de liberación en la aorta ascendente, lo que podría aumentar el riesgo de embolia. Estas manipulaciones del sistema de liberación destinadas a reducir la tasa de obstrucción coronaria no oclusiva también se han probado con éxito con dispositivos alternativos, como Evolut THV, pero también con un éxito moderado y posibles complicaciones. Además, estas técnicas no relacionan la orientación espacial de las estructuras anatómicas de la raíz aórtica y las arterias coronarias con el SC, si bien los pacientes con SC tendían a presentar mayor ángulo de la raíz aórtica.
La capacidad de individualizar la rotación de la VCP antes de la introducción del sistema en el paciente es una hipótesis atractiva probada con éxito en nuestra investigación y podría ser de especial interés en casos de localización anómala del ostium coronario, como los casos de válvula aórtica bicúspide con ostium coronarios separados 180°.
Pronóstico a largo plazo y resistencia de la VCPLa repetición del TAVI se convertirá en el procedimiento más frecuente, dados el número creciente de intervenciones de TAVI y la mayor esperanza de vida de los pacientes en bajo riesgo. Las maniobras para maximizar la durabilidad de las VCP son fundamentales y actualmente se centran en reducir el estrés de las valvas, con lo que mejoran los gradientes residuales y se reduce la insuficiencia aórtica residual5,8,13, junto con tratamientos específicos durante la fabricación para prevenir la calcificación de las valvas14. La deformación y el estrés de las valvas de la VCP podrían reducirse mediante un mejor alineamiento de las comisuras según investigaciones anteriores13. Además, Rogers et al.15 comunicaron que en hasta el 21% de los pacientes los velos de las VCP se encuentran por encima de la unión sinotubular, lo que aumenta el riesgo de obstrucción coronaria durante el TAVI en TAVI, ya que pueden sellar el marco del stent y dificultar el flujo a través de las celdillas hasta los ostium coronarios. Se ha descrito que el corte de las valvas de TAVI con electrocirugía percutánea (técnica BASILICA) reduce el riesgo de oclusión coronaria en intervenciones de válvula en válvula16. Sin embargo, esta compleja estrategia podría resultar ineficaz si hay mal alineamiento de las comisuras, ya que si la VCP previa no está correctamente alineada, el corte de la valva no quedaría delante del ostium de la arteria coronaria. Por lo tanto, diferentes situaciones problemáticas en el seguimiento de los pacientes podrían atajarse si se realizara sistemáticamente un alineamiento preciso de las neocomisuras de las VCP.
La principal limitación de este estudio de viabilidad es el pequeño número de casos incluidos. Sin embargo, la precisión de la mediciones realizadas sienta las bases para futuros estudios multicéntricos que reproduzcan esta metodología a mayor escala. Se necesitan estudios prospectivos con ACURATE neo y dispositivos alternativos para validar esta hipótesis. Las mediciones de TC se han realizado como se describe en la sección «Métodos»; sin embargo, si se realiza un estudio a mayor escala, la variabilidad entre observadores podría ser una fuente de sesgo. La tortuosidad extrema u otras variaciones anatómicas podrían tener impacto en la orientación final del dispositivo de TAVI y un estudio específico para estos casos está justificada.
CONCLUSIONESNuestros resultados indican que es factible un alineamiento comisural preciso del dispositivo de TAVI ACURATE neo al introducir el sistema de liberación de la VCP con una rotación específica para cada paciente (orientación ACA) basada en el análisis de la TC. Esta metodología sistemática reduce el riesgo para el paciente y permitirá una comparación segura de los resultados clínicos entre la estrategia con implante convencional y aquella con alineamiento comisural del dispositivo.
FINANCIACIÓNEl centro recibió subvenciones no condicionadas de Boston Scientific, Medtronic, Meril Life y Abbott.
CONTRIBUCIÓN DE LOS AUTORESA. Redondo, F. Valencia e I.J. Amat-Santos diseñaron el proyecto. A. Redondo e I.J. Amat-Santos recopilaron y analizaron la información y redactaron el artículo final. S. Santos-Martínez, J.R. Delgado-Arana y A. Barrero ayudaron a recopilar datos. F. Valencia, A. Serrador, H. Gutiérrez, I. Sánchez-Lite, T. Sevilla, A. Revilla, C. Baladrón, W-K. Kim, M. Carrasco-Moraleja y J.A. San Román realizaron una revisión crítica y aprobaron la versión final del artículo.
- –
La posición final de las neocomisuras no se controla durante el TAVI, lo que puede dificultar el acceso coronario y las intervenciones futuras. Se han creado varias estrategias para el alineamiento comisural. En algunos dispositivos, se recomienda una orientación estándar (no específica para cada paciente y, por lo tanto, imperfecta); en otros, la manipulación del sistema de liberación dentro del paciente puede lograr un buen alineamiento, pero a costa de aumentar el riesgo de daño vascular o embolización. Hasta la fecha, no se ha elaborado ninguna estrategia específica para cada paciente.
- –
El alineamiento comisural preciso del dispositivo ACURATE neo es posible al introducir el sistema de liberación con una rotación específica para cada paciente basada en el análisis de la TC mediante un cálculo sencillo de la posición final de la válvula. Por lo tanto, el sistema de liberación se puede orientar antes de introducirlo en el paciente y se puede lograr un buen alineamiento de las comisuras sin solapamiento coronario. Este es un método sencillo y reproducible de alineamiento comisural que podría utilizarse con cualquier tipo de dispositivos para TAVI.
I.J. Amat-Santos y W-K. Kim son supervisores de Boston Scientific.