La disfunción grave del ventrículo derecho tras cardiotomía es una complicación que se presenta tras la cirugía cardiaca tanto en el paciente pediátrico como en el adulto. La claudicación del ventrículo derecho no atribuible a una disfunción grave del corazón izquierdo puede ser tributaria de medidas terapéuticas específicas. El manejo convencional de la disfunción del ventrículo derecho incluye el tratamiento de la causa desencadenante, sea cardiaca o extracardiaca, la optimización de la precarga del ventrículo derecho, el empleo de fármacos inotrópicos inodilatadores, la manipulación de las resistencias vasculares pulmonares y estrategias específicas de ventilación mecánica orientadas a minimizar el impacto de la ventilación con presión positiva en la poscarga del ventrículo derecho. También hay opciones terapéuticas avanzadas o de rescate, como la cirugía en casos seleccionados o el empleo de soporte circulatorio mecánico en casos refractarios. Las distintas opciones terapéuticas pueden aplicarse solas o en combinación, pero siempre individualizadas a cada paciente.
Palabras clave
La evolución clínica de un paciente, niño o adulto, sometido a cirugía cardiaca está determinada por diversos factores: cardiopatía de base, estado clínico general prequirúrgico, idoneidad de la reparación quirúrgica realizada y capacidad para superar las exigencias metabólicas adicionales que la agresión quirúrgica impone al organismo1. La posibilidad de atender los requerimientos metabólicos suplementarios durante el periodo postoperatorio está directamente relacionada con la reserva cardiopulmonar. Los riesgos quirúrgicos o perioperatorios asociados a función pulmonar alterada o disfunción ventricular izquierda han sido reconocidos desde los inicios de la cirugía cardiaca. Por otro lado, el manejo de la insuficiencia respiratoria y los estados de shock circulatorio forma parte del cuerpo principal del área de conocimiento de las unidades que atienden a pacientes críticos. Sin embargo, el papel específico que la disfunción del ventrículo derecho (DVD) pueda tener en múltiples situaciones de deterioro cardiorrespiratorio, sin ser novedoso, no se ha reconocido tan ampliamente. Del mismo modo, las medidas terapéuticas orientadas a optimizar la función ventricular derecha de los pacientes críticos, en numerosas ocasiones no se consideran fundamentales en el manejo de algunos enfermos.
El objetivo de este artículo es aportar una aproximación sistemática al manejo de la DVD aguda grave en el paciente sometido a cirugía cardiaca. En primer lugar se define el concepto de DVD aislada y se revisan las medidas convencionales de tratamiento de la insuficiencia cardiaca derecha, así como las opciones de manejo avanzado.
Disfunción ventricular derecha aisladaA efectos de esta revisión, consideramos las situaciones en que se produce insuficiencia aguda de la función del ventrículo derecho (VD) o una agudización de una DVD crónica sin disfunción ventricular izquierda significativa. Es decir, no son objeto de esta revisión el manejo de la insuficiencia biventricular grave, la enfermedad cardiaca general avanzada, la DVD secundaria a disfunción ventricular izquierda grave ni la DVD secundaria a arritmias.
En la tabla 1 se resumen las principales causas de DVD agrupadas por el mecanismo etiopatogénico fundamental2. A pesar de que en muchas ocasiones está implicado más de un mecanismo etiopatogénico (p. ej., infarto agudo del VD en paciente con enfermedad pulmonar obstructiva crónica previa), la disección de la fisiopatología subyacente es fundamental para proporcionar un enfoque terapéutico apropiado3. Especial complejidad reviste el capítulo de las cardiopatías congénitas del adulto, en el que confluyen variables como la anatomía de la malformación, el tipo de reparación (anatómica-reparadora o fisiológica-paliativa), la calidad de la reparación (defectos residuales), la durabilidad de la reparación (estenosis de conductos, insuficiencias valvulares) y la viabilidad a largo plazo de reparaciones paliativas a las que se suma morbilidad propia del adulto (cardiaca o no).
Etiopatogenia de la disfunción ventricular derecha aislada
| Reducción de contractilidad | Sobrecarga de volumen | Aumento de poscarga | Mecanismo mixto |
| IAM VD | Insuficiencia tricuspídea | Estenosis pulmonar | Cortocircuito intracardiaco |
| Miocardiopatía del VD | Insuficiencia pulmonar | Embolia pulmonar | Después de trasplante cardiaco |
| Lesión perioperatoria del VD | HP primaria | Cardiopatías congénitas | |
| HP secundaria |
HP: hipertensión pulmonar; IAM: infarto agudo de miocardio; VD: ventrículo derecho.
El manejo convencional de la DVD (tabla 2) puede dividirse en: a) tratamiento de la causa subyacente o desencadenante; b) optimización de la precarga; c) tratamiento inotrópico/vasopresor; d) reducción de la poscarga del VD, y e) estrategias de ventilación mecánica.
Alternativas terapéuticas convencionales en el tratamiento de la disfunción ventricular derecha tras cardiotomía
| Optimización de la volemia | Fármacos cardiovasculares | Reducción de poscarga | Ventilación mecánica |
| PVC | Vasopresores | Vía endovenosa | Vt: 8–12ml/kg |
| < 10mmHg | Noradrenalina | PGI2-PGE1 | FR baja |
| > 15mmHg | Adrenalina | Nitratos | Relación I:E elevada |
| Oscilaciones en respiración espontánea | Dopamina | Adenosina | PEEP mínima |
| Sildenafilo | |||
| Inodilatadores | Vía inhalatoria | Extubación precoz | |
| Cambios dinámicos del volumen latido (ΔVL) | Dobutamina | Oxígeno | |
| Carga de volumen de prueba | Milrinona | Óxido nítrico | |
| Elevación pasiva de piernas | Levosimendán | Iloprost | |
| Ecocardiografía | |||
| Medición área telediastólica VD-VI |
FR: frecuencia respiratoria; PCV: presión venosa central; PEEP: presión espiratoria final positiva; PGE1: prostaglandina E1; PGI2: prostaciclina; VD: ventrículo derecho; VI: ventrículo izquierdo; Vt: volumen tidal.
El proceso de base que causa o agrava la DVD debe ser identificado y adecuadamente tratado. En el contexto de la DVD tras cardiotomía, el daño sufrido por el VD durante la cirugía no tiene tratamiento específico, pero pueden aparecer complicaciones durante el postoperatorio (infarto agudo de miocardio, sepsis, síndrome de dificultad respiratoria aguda, etc.) que requieren de tratamiento específico independientemente del manejo que se haga de la DVD. El tratamiento dirigido a la causa de la DVD puede implicar actuaciones quirúrgicas (reintervención) en el caso de que tras la cirugía se identifiquen defectos residuales hemodinámicamente significativos.
Optimización de la precargaEl primer recurso disponible para tratar un VD disfuncionante es asegurar que la precarga es adecuada. Es preciso evitar cualquier situación de hipovolemia que pueda comprometer la función ventricular. Sin embargo, la sobrecarga de fluidos puede resultar tan deletérea como la hipovolemia, y puede ocasionar sobredistensión del VD, con los consiguientes disminución de la contractilidad, aumento de la interdependencia ventricular, mal llenado ventricular izquierdo y reducción del gasto cardiaco.
La determinación de la idoneidad de la precarga del VD no es una tarea sencilla. El indicador «ideal» de la precarga óptima debería ser una medición sencilla a pie de cama, que se pudiera realizar continuamente y con una fiabilidad elevada para identificar situaciones tanto de hipovolemia como de hipervolemia. Tal indicador no existe. De todos modos, podemos recurrir a diversas medidas que pueden orientar la terapia con volumen, siempre que se tenga en cuenta las limitaciones de cada una de ellas. Dichas medidas pueden incluir: la determinación de la presión venosa central (PVC) continua o discontinua, las medidas indirectas de volemia funcional (variación de la presión arterial sistólica, variación de la presión de pulso, variación del volumen latido [ΔVL], variación del flujo aórtico), la realización de pruebas terapéuticas (elevación pasiva de piernas, administración empírica de volumen) y la medición de volúmenes ventriculares telediastólicos por ecocardiografía.
La medición de la PVC, tanto en términos del valor absoluto en milímetros de mercurio como la presentación continua en el monitor del trazado de la onda de presión, es una determinación sencilla pero con importantes limitaciones. Son numerosos los trabajos que evidencian que la determinación de la PVC no es útil para guiar la terapéutica con volumen de enfermos con deterioro hemodinámico; es decir, basándose en la PVC es muy difícil predecir si un paciente responderá o no con un incremento del gasto cardiaco a la administración de volumen4. De todos modos, conocer el valor de la PVC y disponer de su trazado pueden ser una referencia de utilidad. Así, los valores extremos de PVC (bajos o elevados) adecuadamente valorados en el contexto clínico pueden orientar la actuación inicial. En presencia de valores intermedios (10–15mmHg) con situaciones clínicas poco definidas, será prudente recurrir a otros indicadores para guiar la terapia con volumen. El paciente en respiración espontánea merece una consideración aparte5,6. En este caso particular puede resultar de utilidad la observación de los cambios en el trazado de la onda de PVC en relación con la respiración. Así, un descenso de la PVC durante la inspiración puede indicar la conveniencia de administrar volumen para optimizar la precarga, especialmente si dicho descenso es pronunciado. Alternativamente, puede hacerse la lectura contraria, la ausencia de descenso de la PVC durante la inspiración del paciente que respira a presión negativa debe considerarse, a priori, una contraindicación para la administración de volumen.
En el paciente sometido a ventilación mecánica con presión positiva, la terapia con volumen se debe guiar por las llamadas medidas funcionales de volemia7. El concepto de medida funcional de la volemia hace referencia a la valoración de los cambios dinámicos en el ΔVL en relación con el ciclo respiratorio. Así, la ΔVL elevada (> 10–15%) indica hipovolemia funcional, mientras que la ΔVL reducida (< 10%) indica volemia adecuada o, al menos, baja probabilidad de respuesta positiva a la administración de volumen. Independientemente de cómo se realice la medición o estimación de la ΔVL, directa (ecocardiografía Doppler)8 o indirecta (variación de la presión arterial sistólica, variación de la presión de pulso, análisis del contorno de la onda de pulso)9,10, son numerosos los trabajos que avalan dicha determinación como el mejor indicador disponible para guiar la administración de volumen a pacientes sometidos a ventilación mecánica. Sin embargo, la ΔVL tiene limitaciones que es preciso conocer. En primer lugar, la ΔVL está relacionada con la magnitud del volumen tidal pautado en el ventilador, es decir, a mayor volumen tidal pautado, mayor ΔVL y viceversa. De este modo, la ΔVL se debe valorar siempre en relación con el volumen tidal pautado11. En segundo lugar, y de particular interés en el entorno clínico que nos ocupa, es preciso conocer que, en presencia de DVD significativa, la ΔVL en relación con la ventilación mecánica está magnificada y tiende a sobrestimar la necesidad de administración de volumen12. Es decir que, pese a que en general la ΔVL es un buen indicador de la volemia funcional en los pacientes ventilados con presión positiva, en el contexto del paciente con DVD, dicha variabilidad se debe interpretar con mucha precaución.
Un recurso alternativo para la toma de decisiones sobre la administración de volumen es el uso de pruebas terapéuticas. Por un lado, puede ser útil la administración prudente de una carga de volumen (en 30min, 5–10ml/kg en el niño y 250–500ml en el adulto) con una valoración crítica de la respuesta obtenida, siempre que otros indicadores (signos y síntomas de congestión grave, PVC muy elevadas, ausencia de ΔVL, signos ecocardiográficos de sobredistensión del VD) no desaconsejen o contraindiquen esa maniobra de entrada13. Alternativamente, la maniobra de elevación pasiva de las extremidades inferiores es una medida sencilla de realizar, de valor contrastado y, sobre todo, con bajo riesgo de generar hipervolemia deletérea, ya que no se modifica la volemia absoluta del paciente14.
Finalmente, la estimación del volumen telediastólico del VD determinando por ecocardiografía el área telediastólica del VD comparándola con el área telediastólica del ventrículo izquierdo probablemente sea uno de los instrumentos más fiables para guiar la terapia con volumen o, al menos, identificar situaciones en que la administración de expansores de la volemia se debe considerar contraindicada (p. ej., un área telediastólica del VD mayor que el área telediastólica del VI)15,16.
Tratamiento inotrópico/vasopresorEl agente farmacológico ideal para el manejo de la DVD debería ser un inotrópico potente capaz de mejorar la función ventricular derecha, con algún efecto vasopresor sistémico que garantice la presión de perfusión coronaria del VD, pero sin efecto vasoconstrictor en la circulación pulmonar2. Tal fármaco no existe, de modo que habitualmente es necesario recurrir a combinaciones de fármacos inotrópicovasoconstrictores con fármacos inotrópico-vasodilatadores (inodilatadores)1.
En el manejo de la DVD grave es de capital importancia evitar la hipotensión sistémica, que puede originar hipoperfusión coronaria y claudicación del VD. Así, a menudo es necesario recurrir a fármacos vasoconstrictores como la noradrenalina para mantener la presión arterial, especialmente si se está empleando simultáneamente fármacos con efecto vasodilatador (inodilatadores, sedantes, opiáceos). Alternativamente, puede resultar útil emplear como inotrópico de segunda línea la adrenalina a dosis bajas, un potente inotrópico que no afecta a la presión arterial gracias a su efecto vasoconstrictor. El uso de dopamina como inotrópico es otra alternativa, pero a dosis presoras (> 10μg/kg/min) es probable que asocie un efecto vasoconstrictor significativo en la vasculatura pulmonar.
El grupo de fármacos inodilatadores tiene un perfil especialmente apropiado para la DVD, ya que, además de potenciar la función contráctil del VD, tienen el potencial de disminuir su poscarga a través de un efecto vasodilatador pulmonar. La principal limitación para su uso aislado es que también reducen las resistencias vasculares sistémicas y pueden causar hipotensión arterial. Las características de fármacos como la dobutamina y la milrinona son bien conocidas y se debe considerarlos inodilatadores de primera línea en el tratamiento de la DVD. En casos refractarios, cabe considerar el uso de levosimendán (sensibilizador al calcio), fármaco con un efecto inotrópico potente y un efecto vasodilatador que actúa también en la circulación pulmonar produciendo una reducción significativa de la poscarga del VD17–20. Por otro lado, algunos datos experimentales apuntan la posibilidad de que el levosimendán también pueda tener efectos antiproliferativos y antiinflamatorios capaces de frenar la remodelación vascular pulmonar y la progresión de una vasculopatía pulmonar21.
Reducción de la poscarga del ventrículo derechoLa reducción de las resistencias vasculares pulmonares es un punto crucial en el tratamiento de la DVD grave, dada la mala tolerancia del VD a los incrementos de poscarga. Dicha reducción puede llevarse a cabo administrando vasodilatadores pulmonares por vía endovenosa o inhalatoria.
La administración de vasodilatadores pulmonares por vía endovenosa tiene dos inconvenientes: a) la vasodilatación intrapulmonar no es selectiva, no se limita a las áreas bien ventiladas y puede incrementar el cortocircuito intrapulmonar, con lo que causaría hipoxemia al aumentar la perfusión de áreas pulmonares no ventiladas, y b) la vasodilatación tampoco es selectiva de la circulación pulmonar y afecta también a la circulación sistémica, con lo que la hipotensión arterial es el principal factor limitante a la administración de estos fármacos. De entre los fármacos disponibles, los nitratos (nitroglicerina, nitroprusiato) tienen un margen terapéutico estrecho, dado que, a las dosis que habitualmente producen vasodilatación pulmonar, inducen también una vasodilatación sistémica importante. El uso de adenosina en infusión continua como vasodilatador pulmonar es anecdótico y se limita a unos pocos casos de hipertensión pulmonar del neonato22 y la realización de test de vasodilatación pulmonar. Los fármacos de administración endovenosa más útiles para reducir las resistencias vasculares pulmonares son las prostaglandinas (PGE1, PGI2), con el epoprostenol (PGI2) como fármaco de elección, por su potente efecto vasodilatador pulmonar23. La comercialización de una formulación endovenosa de sildenafilo añade otro fármaco al arsenal terapéutico disponible24.
La administración de vasodilatadores pulmonares por vía inhalatoria es, a priori, de elección, ya que se trata de una vía de administración doblemente selectiva: a) el efecto vasodilatador tiene lugar fundamentalmente en los alvéolos ventilados, y b) el efecto vasodilatador se limita, la mayoría de las ocasiones, a la circulación pulmonar, sin afectar a la circulación sistémica. El vasodilatador pulmonar más sencillo de administrar y de disponibilidad universal es el oxígeno a alta concentración. El óxido nítrico inhalado es un potente vasodilatador pulmonar que reduce las resistencias vasculares pulmonares, mejora la relación ventilación-perfusión y apenas tiene efectos tangibles en la circulación sistémica. Su administración es relativamente sencilla y se aplica de manera continua. Existen también análogos de la PGI2 (iloprost) que pueden administrarse por vía inhalatoria25. Su administración discontinua es especialmente útil en pacientes estabilizados a quienes se pretende retirar tratamientos continuos como el óxido nítrico inhalado o el epoprostenol endovenoso. Sin embargo, la administración discontinua hace que su efecto farmacológico sea menos homogéneo en el tiempo y puede causar oscilaciones en la situación clínica del paciente. Finalmente, conviene saber que el iloprost inhalado se absorbe fácilmente a través del alvéolo y puede originar vasodilatación sistémica e hipotensión, especialmente en pacientes pediátricos (neonatos y lactantes) si se emplean dosis elevadas.
Estrategias de ventilación mecánicaLa ventilación mecánica con presión positiva, tanto invasiva como no invasiva, causa un incremento de la presión intratorácica. Dicho aumento de presión dificulta el retorno venoso al VD, limita el llenado diastólico del VD y aumenta la poscarga del VD. En situación de DVD, este aumento de poscarga es lo que puede tener un papel más relevante, por lo que es fundamental aplicar estrategias ventilatorias que minimicen el impacto en las resistencias vasculares pulmonares.
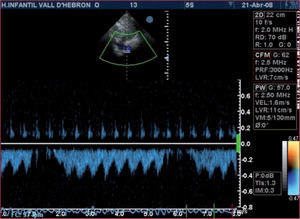
El paradigma de la fisiología de la DVD es el grupo de pacientes con cardiopatía congénita sometidos a reparaciones univentriculares en las que el flujo pulmonar fluye pasivamente, es decir, sin la presencia de un ventrículo que bombee la sangre hacia el lecho vascular pulmonar (intervención de Glenn, intervención de Fontan). En ambos casos, el flujo sanguíneo pulmonar se debe al gradiente de presión existente entre la arteria pulmonar y la aurícula izquierda. En esta situación, cualquier circunstancia que genere un aumento de las resistencias vasculares pulmonares puede afectar gravemente al flujo pulmonar. Las presiones de vía aérea en los pacientes sometidos a ventilación mecánica son máximas durante la inspiración y mínimas durante la espiración. Así, es esperable que la máxima resistencia al flujo pulmonar se produzca durante la fase inspiratoria del ciclo respiratorio y que durante la espiración el impacto de la presión positiva (PEEP) en las resistencias vasculares pulmonares sea mínimo. Dicho fenómeno queda bien reflejado en las figuras 1 y 2. Así, en pacientes con DVD o con flujo pulmonar pasivo, conviene minimizar la presión positiva aplicada y alargar al máximo posible la fase del ciclo respiratorio en que la presión de vía aérea es mínima, es decir, la espiración. Cabe proponer, pues, una ventilación con volúmenes tidales normales- elevados (8–12ml/kg) que permitan aplicar frecuencias respiratorias bajas sin incurrir en hipoventilación, tiempos inspiratorios relativamente cortos para que la relación inspiración:espiración sea lo más larga posible (1:3, 1:4), aplicando la mínima PEEP necesaria y promoviendo la extubación del paciente tan pronto como sea posible.
Ecocardiografía Doppler del flujo sanguíneo en la anastomosis cavopulmonar de un paciente que recibe ventilación con presión positiva. Obsérvese que el flujo se interrumpe durante la inspiración, momento en que la presión de la vía aérea es máxima. Durante la espiración, a pesar de la aplicación de presión positiva al final de la espiración, el flujo es constante (relación inspiración:espiración, 1:4).
En ocasiones se plantea la disyuntiva de si es apropiada o no la aplicación de PEEP a estos pacientes cuando están sometidos a ventilación mecánica. Es preciso recalcar que la aplicación de presión positiva a pacientes con DVD es beneficiosa o deletérea en función de que dicha aplicación sea apropiada a la afección/mecánica pulmonar del paciente. Así, la aplicación de PEEP inapropiadamente alta a pacientes con parénquima pulmonar sano favorece la aparición de sobredistensión pulmonar, con los consiguientes aumento de las resistencias vasculares pulmonares y agravamiento de la DVD. Sin embargo, en pacientes con enfermedad pulmonar grave de tipo restrictivo (síndrome de dificultad respiratoria aguda, neumonía grave, etc.) que cursa con colapso alveolar extenso, la aplicación juiciosa de la PEEP adecuada para conseguir un reclutamiento alveolar óptimo causa una reducción de las resistencias vasculares pulmonares que sistemáticamente están elevadas en los pacientes con áreas extensas de colapso alveolar. Obviamente, si la titulación adecuada de la PEEP no es una tarea sencilla en la mayoría de los pacientes críticos, en los pacientes con DVD debe realizarse con suma prudencia y reevaluando constantemente el efecto conseguido. Dicha reevaluación debe servir también para ser capaces de reconocer la mejoría de la función pulmonar cuando se produzca (resolución del síndrome de dificultad respiratoria aguda, curación de la neumonía) y ser diligentes en la retirada de la PEEP que ya no es necesaria.
Manejo avanzado de la disfunción ventricular derechaDenominamos manejo avanzado de la DVD al conjunto de medidas terapéuticas de rescate a las que se puede recurrir en los casos en que las medidas de manejo convencional previamente descritas no son suficientes para estabilizar y promover la recuperación del paciente (tabla 3). Así, el manejo avanzado de la DVD incluye, por un lado, tratamientos quirúrgicos como la tromboendarterectomía pulmonar, la creación de cortocircuitos intracardiacos o extracardiacos, la exclusión del VD de la circulación o, en última instancia, el trasplante cardiaco. Por otro lado, el uso de soporte mecánico de la circulación, ya sea mediante dispositivos de asistencia ventricular (DAV) o mediante oxigenación con membrana extracorpórea (ECMO), hoy es una alternativa factible.
Alternativas terapéuticas avanzadas en el tratamiento de la disfunción ventricular derecha tras cardiotomía
| Opciones quirúrgicas | Soporte circulatorio mecánico | |
| Tromboendarterectomía | DAV | ECMO |
| Creación de cortocircuito derecha-izquierda | VentajasUso prolongado, menor consumo de hemoderivados, movilización del paciente | VentajasImplante urgente no quirúrgico, proporciona sangre oxigenada, efectivo en caso de HP o enfermedad pulmonar grave |
| Exclusión del VD | ||
| Trasplante cardiaco | DesventajasImplante electivo, implante quirúrgico, precisa RVP bajas-moderamente altas, precisa pulmones «normales» | DesventajasUso a corto plazo, mayor consumo de hemoderivados, dificultad para movilizar al paciente |
DAV: dispositivo de asistencia ventricular; ECMO: oxigenación con membrana extracorpórea; HP: hipertensión pulmonar; RVP: resistencias vasculares pulmonares; VD: ventrículo derecho.
La tromboendarterectomía pulmonar puede ser útil para pacientes con hipertensión pulmonar crónica tromboembólica y DVD grave, así como la embolectomía pulmonar quirúrgica para pacientes con tromboembolia pulmonar masiva26. La creación de un cortocircuito derecha-izquierda que permita descargar la circulación pulmonar es una opción factible que permite no solo aliviar la presión en el lado derecho de la circulación, sino que es útil para evitar situaciones de bajo gasto por claudicación del VD, ya que la sangre que no puede acceder al lado izquierdo del corazón a través del lecho vascular pulmonar lo hace a través del cortocircuito creado a tal fin. En esta situación se genera una hipoxemia arterial secundaria al cortocircuito derecha-izquierda, pero normalmente se tolera bien y, en cualquier caso, mejor que la reducción crítica del gasto cardiaco que se puede producir en ausencia de dicho cortocircuito. Así, esta estrategia se ha mostrado útil tanto para el manejo de situaciones de hipertensión pulmonar crónica grave como para el manejo de DVD aguda tras cardiotomía (especialmente en el contexto de la cirugía cardiaca pediátrica). Las opciones técnicas para crear el cortocircuito derechaizquierda incluyen: a) la realización de una septostomía auricular por vía percutánea en la sala de hemodinámica27; b) la creación de una septostomía auricular o el cierre solo parcial de una comunicación interauricular/ interventricular durante la intervención quirúrgica28, y c) la creación de una fístula pulmonar-sistémica de descarga por vía quirúrgica29. La selección del procedimiento más adecuado para cada paciente debe ser individualizada.
La exclusión quirúrgica del VD es un procedimiento que implica la creación de una comunicación cavopulmonar, el cierre de la válvula tricúspide, la derivación del flujo del seno coronario hacia la aurícula izquierda y la resección/plicatura de la pared libre del VD. Se trata de una alternativa agresiva propuesta para pacientes con sobrecarga de volumen intratable del VD o enfermedad del VD intrínseca no tratable, como la displasia arritmogénica del VD o la anomalía de Ebstein. Finalmente, es posible que en algunos pacientes la única alternativa factible sea el trasplante cardiaco.
Soporte circulatorio mecánicoLas opciones para dar soporte circulatorio mecánico a la DVD refractaria son dos: DAV y ECMO30,31.
El uso de DAV univentriculares derechos no es la indicación más frecuente de estos dispositivos, dado que habitualmente la necesidad de asistir el corazón derecho surge en el contexto de una cardiopatía general que obliga a instaurar soporte biventricular. De todos modos, en casos de DVD aislada puede estar indicado este tipo de asistencia, la cual, por su sencillez de manejo comparada con otras técnicas como la ECMO, puede resultar muy atractiva. Sin embargo, la instauración de soporte con un DAV derecho implica implantación quirúrgica, con los riesgos que esto implica; del mismo modo, la retirada del DAV conlleva una nueva intervención. Por ello, la elección de este tipo de soporte debe reservarse, en principio, para pacientes cuya asistencia circulatoria se prevea de larga duración (p. ej., > 2–4 semanas32), mientras que las necesidades de soporte circulatorio más corto pueden resolverse mediante ECMO. Hay que señalar que la rápida evolución de los distintos dispositivos disponibles en el mercado hace que los criterios de selección e indicación cambien continuamente. Así, la aparición de bombas centrífugas con un perfil hemodinámico excelente, alta durabilidad (hasta 30 días) y manejo relativamente sencillo ofrece una alternativa factible para el soporte a corto plazo, especialmente en el contexto de DVD tras cardiotomía.
El uso de ECMO es una opción excelente para la asistencia circulatoria en el contexto de la DVD tras cardiotomía, siempre que el tiempo de asistencia previsto sea relativamente corto, entendiendo por tal el < 15 días en la mayoría de los supuestos y siempre menos de 30 días. Las ventajas de usar ECMO comparado con DAV son: a) la posibilidad de implantación periférica mediante la canulación (quirúrgica o percutánea) de grandes vasos, con la posibilidad de hacer una canulación central quirúrgica si se considera oportuno; b) la disponibilidad de la técnica de manera permanente en los centros que disponen de un programa de ECMO; c) la rapidez de instauración del soporte por vía periférica en situaciones de emergencia, y d) la posibilidad de aportar soporte respiratorio además del soporte circulatorio. La principal desventaja de la técnica respecto a DAV es la mayor complejidad y la mayor necesidad de anticoagulación desde el inicio. La limitación de la técnica de ECMO para dar soporte a la disfunción grave del ventrículo izquierdo debida a la dificultad para conseguir una adecuada descarga del ventrículo izquierdo no existe en el caso de la DVD, ya que la canulación venosa y el drenaje del VD son inherentes a la técnica y es sencillo realizarlo a través de los grandes vasos.
ConclusionesLas alternativas terapéuticas para el manejo de la DVD tras cardiotomía son múltiples, de modo que su aplicación racional requiere un análisis de la fisiopatología subyacente. El soporte circulatorio mecánico es una opción factible y potencialmente útil para pacientes seleccionados y se debe considerar en aquellos casos en que fracasa el tratamiento convencional.
Conflicto de interesesNinguno.