Análisis combinado basado en los datos de pacientes de los ensayos TITAX-AMI y BASE-ACS para evaluar los resultados clínicos obtenidos con stents bioactivos con recubrimiento de titanio-óxido nítrico comparados con los stents liberadores de fármacos en pacientes con infarto agudo de miocardio con elevación del segmento ST tras un seguimiento de 2 años.
MétodosEl ensayo TITAX-AMI comparó los stents bioactivos con los liberadores de paclitaxel en 425 pacientes con infarto agudo de miocardio. El ensayo BASE-ACS comparó stents bioactivos con stents liberadores de everolimus en 827 pacientes con síndrome coronario agudo. El objetivo principal para el análisis combinado fueron los eventos adversos cardiacos mayores: muerte cardiaca, infarto de miocardio recurrente o revascularización de la lesión diana por causa isquémica tras un seguimiento de 2 años.
ResultadosEl análisis combinado incluyó a 501 pacientes; se trató a 245 con stents bioactivos y se implantó stent liberador de fármacos a 256. En el análisis conjunto, el grupo de stents bioactivos presentó un cociente de riesgos de eventos adversos cardiacos mayores de 0,85 (intervalo de confianza del 95%, 0,53-1,35; p=0,49) comparado con el grupo de stents liberadores de fármacos. De igual modo, el grupo conjunto de stents bioactivos mostró un cociente de riesgos de muerte cardiaca de 0,71 (intervalo de confianza del 95%, 0,26-1,95; p=0,51); de infarto de miocardio recurrente, 0,44 (intervalo de confianza del 95%, 0,20-0,97; p=0,04), y de revascularización de la lesión diana por causa isquémica, 1,39 (intervalo de confianza del 95%, 0,74-2,59; p=0,30), en comparación con el grupo conjunto tratado con stents liberadores de fármacos. Estos resultados se confirmaron por un análisis de puntuación de propensión ajustado respecto a la serie de datos conjunta.
ConclusionesEn pacientes con infarto agudo de miocardio con elevación del segmento ST, los stents bioactivos, comparados con los stents liberadores de fármacos, se asociaron a menores tasas de infarto de miocardio recurrente tras un seguimiento de 2 años; no obstante, las tasas de muerte cardiaca y de revascularización de la lesión diana por causa isquémica fueron similares.
Palabras clave
Los stents liberadores de fármacos (SLF) de primera generación redujeron de manera efectiva la incidencia de revascularizaciones de la lesión diana (RLD) en una proporción de entre la mitad y dos tercios en un seguimiento a largo plazo1,2. Sin embargo, la evidencia reciente acumulada en registros y metanálisis pone en duda la seguridad a largo plazo de los SLF de primera generación, lo que ha despertado inquietud respecto a las posibles tasas de trombosis del stent (TS) tardía y muy tardía más altas3–5. El diseño de los SLF de segunda generación ha sido un nuevo avance. En este contexto, el stent de segunda generación liberador de everolimus ha reducido significativamente el objetivo combinado de seguridad y eficacia respecto al stent de primera generación liberador de paclitaxel tras un seguimiento de 12 meses6,7.
La seguridad del stent bioactivo (SBA) con recubrimiento de titanio-óxido nítrico se ha puesto de relieve en varios estudios observacionales en poblaciones de la práctica clínica real8,9 y en ensayos controlados y aleatorizados en pacientes con síndrome coronario agudo (SCA)10,11. En el ensayo TITAX-AMI, el SBA fue superior al stent liberador de paclitaxel por lo que respecta al objetivo de eventos adversos cardiacos mayores (MACE), muerte cardiaca, reinfarto y TS definitiva en pacientes con infarto agudo de miocardio (IAM) en un seguimiento de 5 años, con unas tasas similares de RLD a causa de isquemia10. En el ensayo BASE-ACS, el SBA no fue inferior al stent liberador de everolimus por lo que respecta al objetivo principal de MACE en pacientes con SCA tras un seguimiento de 12 meses; los IAM no mortales fueron significativamente menos con el SBA11. Sin embargo, no hay muchos datos de comparación directa de SBA con SLF en el contexto concreto del infarto agudo de miocardio con elevación del segmento ST (IAMCEST). En consecuencia, se llevó a cabo un análisis combinado basado en los datos de los pacientes de los ensayos TITAX-AMI y BASE-ACS para evaluar los resultados clínicos en los pacientes con IAMCEST tras un seguimiento de 2 años.
MÉTODOSSelección de los pacientes y diseño del estudioEl diseño de ambos ensayos se ha descrito ya con anterioridad11,12. De forma resumida, el ensayo TITAX-AMI fue un ensayo multicéntrico, prospectivo y a ciego simple llevado a cabo entre diciembre de 2005 y noviembre de 2006, en el que participaron 425 pacientes con IAM sometidos a intervención coronaria percutánea; se los distribuyó aleatoriamente en proporción 1:1 al tratamiento con un SBA (Titan-2®, Hexacath; París, Francia) o un stent liberador de paclitaxel (TAXUS Liberte®, Boston Scientific; Natick, Massachusetts, Estados Unidos). El objetivo principal fue la primera aparición de un MACE (muerte cardiaca, recurrencia del IAM o RLD a causa de isquemia) en un seguimiento de 12 meses y cuyas definiciones se han descrito ya con anterioridad12. Los objetivos secundarios fueron la muerte por cualquier causa, una combinación de muerte cardiaca y recurrencia del IAM y la TS definitiva en un seguimiento a 12 meses. El ensayo BASE-ACS fue un ensayo de no inferioridad prospectivo, multicéntrico, a ciego simple y aleatorizado llevado a cabo entre enero de 2009 y septiembre de 2010. Participaron en el ensayo 827 pacientes con SCA sometidos a intervención coronaria percutánea precoz, con una asignación aleatoria en proporción 1:1 al tratamiento con SBA o stent liberador de everolimus (Xience V®, Abbott Vascular; Santa Clara, California, Estados Unidos). El objetivo principal fue la primera aparición de un MACE (muerte cardiaca, IAM no mortal o RLD a causa de isquemia) en un seguimiento de 12 meses. Las definiciones de estos objetivos también se han descrito ya con anterioridad11. Los objetivos secundarios fueron la muerte por cualquier causa, una combinación de muerte cardiaca e IAM no mortal y la TS definitiva en un seguimiento a 12 meses. Se adoptó la categoría de TS «definitiva» según la definición del Academic Research Consortium13. En ambos ensayos, los operadores debían conocer necesariamente el tipo de stent asignado, pero se mantuvo el diseño ciego para los pacientes y el personal investigador que realizó la evaluación de los resultados clínicos. Para realizar el presente análisis, los autores tuvieron acceso sin restricciones a los datos del paciente a través de la base de datos electrónica de cada ensayo. Se seleccionó a los pacientes con IAMCEST tratados mediante intervención coronaria percutánea precoz de ambos ensayos y se combinaron sus datos para establecer dos grupos conjuntos de pacientes: los tratados con un SBA y los tratados con un SLF. Se compararon estos dos grupos en lo relativo a sus características clínicas basales, los datos angiográficos y de la intervención y los resultados clínicos a 2 años. Las variables de valoración clínicas se presentaron según lo definido por los autores en los respectivos ensayos iniciales. El análisis del objetivo primario combinado a los 2 años de seguimiento se había preespecificado en ambos ensayos.
Cuestiones éticasAmbos estudios fueron iniciados por los propios investigadores y se llevaron a cabo siguiendo las directrices éticas de la Declaración de Helsinki de 1964 revisada en 2002. Se obtuvo el consentimiento informado por escrito de cada uno de los pacientes tras una explicación detallada del protocolo del estudio. El protocolo del estudio recibió la aprobación de los comités de ética del centro de coordinación (Satakunta Central Hospital) y otros hospitales participantes. El ensayo TITAX-AMI está registrado en la base de datos ClinicalTrials14 con el número NCT00495664 y el ensayo BASE-ACS, con el número NCT00819923.
Intervenciones farmacológicasEn ambos ensayos, a los pacientes que estaban recibiendo ya un tratamiento de mantenimiento con ácido acetilsalicílico no se les administró ninguna dosis de carga adicional de este fármaco. A los pacientes que no recibían tratamiento de mantenimiento con ácido acetilsalicílico, se los pretrató con ácido acetilsalicílico en dosis de carga de 250mg por vía oral o 250-500mg por vía intravenosa durante la intervención coronaria percutánea, y se continuó después con dosis diarias de al menos 75-150mg indefinidamente. Se inició la administración de clopidogrel oral con una dosis de carga de al menos 300mg antes o inmediatamente después de la intervención, y se continuó con una dosis diaria de 75mg. Según lo establecido en el protocolo, a los pacientes de uno u otro grupo se les prescribió clopidogrel oral durante un mínimo de 6 meses y luego durante periodos más largos (máximo 12 meses), a criterio del operador. Durante la intervención, se administró por vía intravenosa heparina de bajo peso molecular (enoxaparina sódica) o heparina no fraccionada a la dosis estándar recomendada por las guías. El uso de inhibidores de la glucoproteína IIb/IIIa o bivalirudina perintervención se dejó a criterio del operador.
Análisis estadísticoEn primer lugar se combinaron las series de datos de los dos estudios aleatorizados para formar un solo conjunto de datos para el análisis sin aplicar una combinación estadística metanalítica. El análisis estadístico se llevó a cabo con el programa IBM SPSS (versión 20.0). Las variables continuas se presentaron en forma de media±error estándar y las variables dicotómicas, en forma de recuentos y porcentajes. Se utilizaron las pruebas de la χ2 de Pearson, Kolmogorov-Smirnov, análisis de la varianza de una vía, Kruskal-Wallis, exacta de Fisher y Mann-Whitney para evaluar las diferencias entre las cohortes de estudio. Aunque los datos procedían de estudios aleatorizados, se observaron algunas diferencias significativas o casi significativas entre las cohortes de estudio. En consecuencia, se optó por tener en cuenta estas diferencias mediante el desarrollo de una puntuación de propensión para los métodos de tratamiento. La puntuación de propensión se calculó mediante regresión logística, con la inclusión de variables clínicas y de intervención con alguna diferencia entre los grupos de estudio, según lo indicado por el valor de p<0,2 en el análisis univariable. Los estudios incluidos se introdujeron en el modelo de regresión logística en forma de una covariable dicotómica, con objeto de tener en cuenta toda posible diferencia relativa a las características de los pacientes y de la intervención. La puntuación de propensión se añadió al modelo de regresión en forma de covariable. Se utilizó la prueba de Hosmer-Lemeshow para evaluar el ajuste del modelo de regresión. Se utilizó un análisis de curva de características operativas del receptor para evaluar la probabilidad esperada. La puntuación de propensión obtenida tenía un área bajo la curva de 0,65 (intervalo de confianza del 95% [IC95%], 0,60-0,69; Hosmer-Lemeshow, p=0,35). La puntuación de propensión se utilizó solamente para el análisis ajustado, con objeto de estimar la influencia del tipo de stent en los resultados clínicos tras la intervención. El análisis combinado de los datos agregados se llevó a cabo con el programa Review Manager 5.2 (RevMan; Copenhague: The Nordic Cochrane Centre, The Cochrane Collaboration, 2012). El riesgo general de eventos adversos se expresó mediante el cociente de riesgos con su IC95%. Se evaluó la heterogeneidad entre los dos ensayos mediante la prueba de I2. Cuando el valor de I2 era <40%, la heterogeneidad se consideró no significativa. Se optó por utilizar el método de efectos aleatorios, ya que la potencia estadística de la prueba de I2 es pequeña cuando el número de estudios combinados es bajo. Además, algunos factores clínicos apuntan a la heterogeneidad. Por ejemplo, el grupo de SLF incluye dos tipos de stent diferentes y la definición del IAM como criterio de evaluación del resultado clínico fue diferente en los dos ensayos originales. Por último, se consideró estadísticamente significativo un valor de p<0,05.
RESULTADOSEn el presente análisis conjunto se incluyó a un total de 501 pacientes con IAMCEST tratados con intervención coronaria percutánea precoz; 245 pacientes recibieron un SBA (83 del ensayo TITAX-AMI y 162 del ensayo BASE-ACS) y a 256 se les implantaron SLF (97 con stents liberadores de paclitaxel en el ensayo TITAX-AMI y 159 con stents liberadores de everolimus en el ensayo BASE-ACS). Se dispuso de datos sobre los parámetros de evaluación del resultado clínico a los 2 años de seguimiento para todos los pacientes.
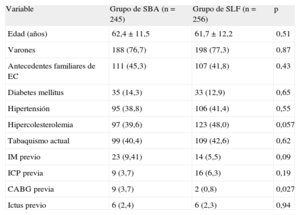
Características clínicas basales de la cohorte conjuntaLos pacientes del grupo de SBA tenían mayor probabilidad de antecedentes de cirugía de revascularización aortocoronaria que los del grupo de SLF (el 3,7 y el 0,8% respectivamente; p=0,027), mientras que los pacientes del grupo de SLF mostraron tendencia a mayor frecuencia de hipercolesterolemia. Los dos grupos estaban bien equilibrados en cuanto a las demás características clínicas basales (p>0,05 en todos los casos) (tabla 1). Las características clínicas basales de los dos subgrupos en los ensayos individuales se presentan en las tablas 1 y 2 del material suplementario.
Características clínicas basales de los dos grupos de estudio combinados
| Variable | Grupo de SBA (n=245) | Grupo de SLF (n=256) | p |
| Edad (años) | 62,4±11,5 | 61,7±12,2 | 0,51 |
| Varones | 188 (76,7) | 198 (77,3) | 0,87 |
| Antecedentes familiares de EC | 111 (45,3) | 107 (41,8) | 0,43 |
| Diabetes mellitus | 35 (14,3) | 33 (12,9) | 0,65 |
| Hipertensión | 95 (38,8) | 106 (41,4) | 0,55 |
| Hipercolesterolemia | 97 (39,6) | 123 (48,0) | 0,057 |
| Tabaquismo actual | 99 (40,4) | 109 (42,6) | 0,62 |
| IM previo | 23 (9,41) | 14 (5,5) | 0,09 |
| ICP previa | 9 (3,7) | 16 (6,3) | 0,19 |
| CABG previa | 9 (3,7) | 2 (0,8) | 0,027 |
| Ictus previo | 6 (2,4) | 6 (2,3) | 0,94 |
CABG: cirugía de revascularización aortocoronaria; EC: enfermedad coronaria; ICP: intervención coronaria percutánea; IM: infarto de miocardio; SBA: stent bioactivo; SLF: stent liberador de fármaco.
Las variables continuas se presentan en forma de media±desviación estándar; las variables dicotómicas, como n (%).
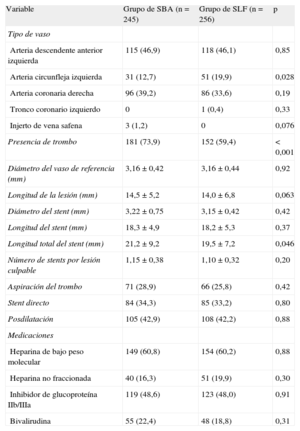
En los pacientes del grupo de SBA, la longitud total de stent era mayor que en los del grupo de SLF (21,2±9,2 frente a 19,5±7,2mm; p=0,046), y las lesiones con contenido de trombos fueron más frecuentes (el 73,9 y el 59,4%; p<0,001). Los dos grupos estaban bien equilibrados en cuanto a los demás datos angiográficos y de la intervención (p>0,05 en todos los casos) (tabla 2). Las características angiográficas y de la intervención de los dos subgrupos en los ensayos individuales se presentan en las tablas 3 y 4 del material suplementario.
Datos angiográficos y de intervención de los dos grupos de estudio combinados
| Variable | Grupo de SBA (n=245) | Grupo de SLF (n=256) | p |
| Tipo de vaso | |||
| Arteria descendente anterior izquierda | 115 (46,9) | 118 (46,1) | 0,85 |
| Arteria circunfleja izquierda | 31 (12,7) | 51 (19,9) | 0,028 |
| Arteria coronaria derecha | 96 (39,2) | 86 (33,6) | 0,19 |
| Tronco coronario izquierdo | 0 | 1 (0,4) | 0,33 |
| Injerto de vena safena | 3 (1,2) | 0 | 0,076 |
| Presencia de trombo | 181 (73,9) | 152 (59,4) | <0,001 |
| Diámetro del vaso de referencia (mm) | 3,16±0,42 | 3,16±0,44 | 0,92 |
| Longitud de la lesión (mm) | 14,5±5,2 | 14,0±6,8 | 0,063 |
| Diámetro del stent (mm) | 3,22±0,75 | 3,15±0,42 | 0,42 |
| Longitud del stent (mm) | 18,3±4,9 | 18,2±5,3 | 0,37 |
| Longitud total del stent (mm) | 21,2±9,2 | 19,5±7,2 | 0,046 |
| Número de stents por lesión culpable | 1,15±0,38 | 1,10±0,32 | 0,20 |
| Aspiración del trombo | 71 (28,9) | 66 (25,8) | 0,42 |
| Stent directo | 84 (34,3) | 85 (33,2) | 0,80 |
| Posdilatación | 105 (42,9) | 108 (42,2) | 0,88 |
| Medicaciones | |||
| Heparina de bajo peso molecular | 149 (60,8) | 154 (60,2) | 0,88 |
| Heparina no fraccionada | 40 (16,3) | 51 (19,9) | 0,30 |
| Inhibidor de glucoproteína IIb/IIIa | 119 (48,6) | 123 (48,0) | 0,91 |
| Bivalirudina | 55 (22,4) | 48 (18,8) | 0,31 |
SBA: stent bioactivo; SLF: stent liberador de fármaco.
Las variables continuas se presentan en forma de media±desviación estándar; las dicotómicas, como n (%).
La duración media del tratamiento con clopidogrel en el grupo de SBA en comparación con el de SLF fue 7,4±3,1 frente a 10,4±2,7 meses (p<0,001) en el ensayo TITAX-AMI, 8,8±3,6 frente a 10,1±2,9 meses (p<0,001) en el ensayo BASE-ACS y 8,3±3,4 frente a 10,3±2,8 meses (p<0,001) en la serie combinada.
Resultados clínicos ajustados mediante puntuación de propensión en el seguimiento a 2 añosEn el seguimiento realizado a los 2 años, en el grupo de estudio de SBA frente al grupo de SLF, las tasas de MACE fueron del 11,4 frente al 13,7% (p=0,50; ajustado por puntuación de propensión, odds ratio [OR]=0,78; IC95%, 0,45-1,35); muerte cardiaca, el 2,4 frente al 3,5% (p=0,60; ajustado por puntuación de propensión, OR=0,65; IC95%, 0,22-1,91); recurrencia del IAM, el 3,3 frente al 7,4% (p=0,032; ajustado por puntuación de propensión, OR=0,36; IC95%, 0,15-0,88); RLD a causa de isquemia, el 8,6 frente al 6,3% (p=0,39; ajustado por puntuación de propensión, OR=1,41; IC95%, 0,70-2,83), y TS definitiva, el 0,8 frente al 5,1% (p=0,007; ajustado por puntuación de propensión, OR=0,31; IC95%, 0,03-0,67).
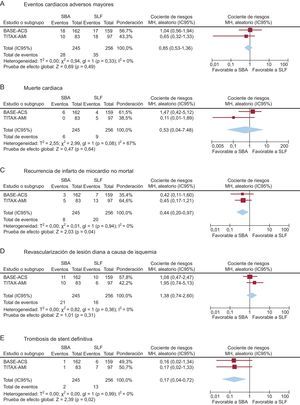
Resultados de evolución clínica conjuntos en el seguimiento a 2 añosEn la figura se presentan los gráficos de Forest de las tasas absolutas de eventos clínicos en los dos grupos combinados a los 2 años de seguimiento, con los cocientes de riesgos para el grupo combinado y en los dos ensayos individuales. En ninguno de los ensayos se observó evidencia de heterogeneidad (I2=0% para todos los eventos evaluados, excepto muerte cardiaca, I2=67%). En el grupo de SBA conjunto, se obtuvo para los MACE un cociente de riesgos de 0,85 (IC95%, 0,53-1,36; p=0,49) en comparación con el grupo de SLF conjunto. De igual modo, el grupo conjunto de SBA obtuvo para la muerte cardiaca un cociente de riesgos de 0,53 (IC95%, 0,04-7,48; p=0,63); para recurrencia del IAM, un cociente de riesgos de 0,44 (IC95%, 0,20-0,97; p=0,04); para la RLD por causa isquémica, un cociente de riesgos de 1,38 (IC95%, 0,74-2,60; p=0,31), y para la TS definitiva, un cociente de riesgos de 0,17 (IC95%, 0,04-0,72; p=0,02) en comparación con el grupo combinado de SLF (figura).
Análisis combinado de los cocientes de riesgo de eventos adversos cardiacos mayores (conjunto de muerte cardiaca, recurrencia de infarto de miocardio no mortal y revascularización de lesión diana por isquemia) (A), muerte cardiaca (B), recurrencia de infarto de miocardio no mortal (C), revascularización de lesión diana por isquemia (D) y trombosis definitiva del stent (E), asociados a los stents bioactivos frente a los stents liberadores de fármacos a los 2 años de seguimiento. gl: grados de libertad; IC95%: intervalo de confianza del 95%; MH: Mantel-Haenszel; SBA: stents bioactivos; SLF: stents liberadores de fármacos.
El presente análisis conjunto de los ensayos TITAX-AMI y BASE-ACS a los 2 años de seguimiento puso de manifiesto que, en los pacientes con IAMCEST sometidos a intervención coronaria percutánea precoz, el implante de un SBA, en comparación con SLF, se asoció a unas tasas significativamente inferiores de recurrencia del IAM (p=0,04) y de TS definitiva (p=0,02). Las tasas de muerte cardiaca, RLD a causa de isquemia y del conjunto de todos los MACE fueron estadísticamente similares (p>0,05 en todos los casos). Hasta donde saben los autores, el estudio que se presenta es el primer análisis conjunto de ensayos aleatorizados publicado hasta la fecha en el que se presentan resultados clínicos obtenidos con el SBA frente al SLF en el contexto del IAMCEST.
Variables de valoración de eficacia y de seguridadEn el presente análisis combinado, el implante de SBA en pacientes con IAMCEST se asoció a una leve reducción (15%) del riesgo relativo de la variable de valoración clínica combinada de eficacia y seguridad a los 2 años de seguimiento, en comparación con un grupo de pacientes tratados con SLF (stents liberadores de paclitaxel y liberadores de everolimus) (p=0,49). No es de extrañar que hubiera un aumento del 39% en el riesgo relativo del objetivo de eficacia específica del dispositivo, la RLD a causa de isquemia (p=0,30). El hecho de que no se realizara un seguimiento angiográfico sistemático puede haber influido en las tasas relativas de RLD entre los dos grupos de stents. Es bien sabido que el seguimiento angiográfico aumenta las diferencias absolutas entre los stents en cuanto a la RLD más allá de lo que se observaría con un seguimiento tan solo clínico. No obstante, con la adopción de un seguimiento exclusivamente clínico, los resultados reflejarían lo que sucede en la práctica clínica real, y evita reintervenciones en las lesiones angiográficas clínicamente «silentes». El aumento del riesgo relativo de RLD asociado al SBA fue compensado por una reducción del 56% en el riesgo relativo de recurrencia del IAM (p=0,04) y una reducción del 29% en el riesgo relativo de muerte cardiaca (p=0,51) (objetivos de seguridad). La reducción del riesgo de recurrencia del IAM fue muy probablemente consecuencia de la reducción del 83% en el riesgo relativo de TS definitiva que se asociaba al uso de SBA en comparación con SLF a los 2 años (p=0,02).
Perspectiva en la literatura médica actualEn el análisis post-hoc de 12 meses del ensayo BASE-ACS basado en el tipo de SCA, el cociente de riesgo relativo asociado al uso de un SBA en comparación con un stent liberador de everolimus en los pacientes con IAMCEST fue 1,06 para los MACE, 1,1 para la RLD a causa de isquemia, 0,27 para la recurrencia de IAM, 1,95 para la muerte cardiaca y 0,16 para la TS definitiva15. En dicho análisis post-hoc, las tasas de recurrencia del IAM y de muerte cardiaca a 12 meses asociadas al uso de stents liberadores de everolimus fueron del 4,4 y el 1,9%, respectivamente; la de la TS definitiva fue del 3,8%. La tasa combinada de MACE fue del 8,8%15. Sin embargo, las tasas de eventos asociadas a los SLF en el presente análisis conjunto son comparativamente superiores a las descritas en otros ensayos aleatorizados. En un análisis a 2 años de los datos conjuntos de los ensayos SPIRIT y COMPARE, las tasas de eventos asociadas a los stents liberadores de everolimus en los pacientes con SCA fueron: MACE, 8,7%; muerte cardiaca, 1,4%; IAM no mortal, 4%; RLD a causa de isquemia, 4,7%, y TS definitiva, 0,4%16. La inclusión de pacientes de todo el espectro del SCA, en comparación con la inclusión de solo pacientes con IAMCEST en el presente estudio, y el hecho de que en este análisis conjunto se incluyeran los resultados clínicos obtenidos tanto con stents liberadores de paclitaxel como con los liberadores de everolimus podrían explicar las diferencias observadas entre los dos análisis combinados por lo que respecta a los resultados a 2 años. La evidencia obtenida en el programa de ensayo SPIRIT y en el ensayo COMPARE subraya que los resultados obtenidos con los stents liberadores de paclitaxel y de everolimus no son comparables: los stents liberadores de everolimus mostraron una eficacia superior (reducción de la pérdida luminal tardía en el stent y en el segmento) y mayor seguridad (reducción de IAM y TS)7,17–19. En el ensayo EXAMINATION, que comparó los stents liberadores de everolimus con los stents metálicos sin recubrimiento en pacientes con IAMCEST, las tasas de recurrencia del IAM relacionado con el vaso diana y de muerte cardiaca a los 12 meses con los stents liberadores de everolimus fueron del 1,1 y el 3,2% respectivamente; la de la TS definitiva fue del 0,5%20. Las menores tasas de eventos pueden explicarse por el periodo de seguimiento más corto que el del presente análisis conjunto. Además, el ensayo adoptó la definición de IAM ampliada de la Organización Mundial de la Salud, que se basa en la elevación de la creatincinasa total a >2 veces el límite de superior de la normalidad (LSN), la fracción MB de la creatincinasa >3 veces el LSN o la troponina >3 veces el LSN, en orden jerárquico21. Estos criterios son menos sensibles que la definición utilizada tanto en el ensayo BASE-ACS (fracción MB de la creatincinasa o troponina >2 veces el LSN) como en el ensayo TITAX-AMI (troponina>percentil 99 del LSN)11,12. Además, la menor incidencia de TS podría atribuirse a la mayor frecuencia de trombectomías en el ensayo EXAMINATION (66%)20. De igual manera, el ensayo XAMI comparó los stents liberadores de everolimus con los stents liberadores de sirolimus en el contexto de la intervención coronaria percutánea primaria para el IAMCEST. Las tasas de recurrencia de IAM y muerte cardiaca asociadas a los stents liberadores de everolimus a los 12 meses fueron del 0,5 y el 1,5% respectivamente; la tasa de TS definitiva o probable fue del 1,2%22. Las menores tasas de recurrencia de IAM podrían interpretarse de nuevo teniendo en cuenta el periodo de seguimiento más breve. Además, la definición utilizada en el ensayo se basó en un valor total de creatincinasa>3 veces el LSN. La menor tasa de TS observada podría atribuirse posiblemente a la mayor frecuencia de aspiración del trombo (61,9%) y la administración de un inhibidor de la glucoproteína IIb/IIIa (74,5%) en el ensayo XAMI22. Por último, el ensayo PASSION comparó los stents liberadores de paclitaxel con los metálicos sin recubrimiento en la intervención coronaria percutánea primaria por IAMCEST. Las tasas a 2 años de recurrencia del IAM, muerte cardiaca y TS definitiva asociadas a los stents liberadores de paclitaxel fueron del 3,1, el 5,6 y el 2,1%23. Nuevamente, la definición de IAM fue diferente de la utilizada en el ensayo TITAX-AMI; la recurrencia del IAM se definió en función de la aparición de ondas Q patológicas o de una creatincinasa total >2 veces el LSN con elevación de la fracción MB de la creatincinasa23.
Angioplastia primaria en el infarto agudo de miocardio con elevación del segmento STLos ensayos aleatorizados de comparación de eficacia y seguridad de los SLF frente a los stents metálicos sin recubrimiento en el contexto del IAMCEST han puesto de relieve de manera uniforme que los SLF redujeron la necesidad de nuevas intervenciones de revascularización, sin que hubiera diferencias estadísticamente significativas en la incidencia de TS24. El ensayo más grande realizado hasta el momento, el HORIZONS-AMI (n=3.006), mostró la superioridad de los stents liberadores de paclitaxel por lo que respecta a la valoración primaria de la eficacia consistente en la RLD a causa de isquemia (p=0,002), y se mostró no inferior para la variable de valoración combinada de seguridad (p=0,92; no inferioridad, p=0,01), en comparación con los stents metálicos sin recubrimiento25. En un análisis conjunto de 389 pacientes diabéticos de siete ensayos controlados y aleatorizados en los que se compararon los SLF con los stents metálicos sin recubrimiento en el IAMCEST, la tasa de RLD fue significativamente inferior entre los tratados con los SLF (hazard ratio=0,44; p=0,02), sin que hubiera diferencias significativas en el objetivo combinado de seguridad de muerte o IAM (hazard ratio=0,64; p=0,12)26.
Limitaciones del estudioAunque el presente análisis conjunto se llevó a cabo para aumentar la potencia estadística de los grupos de comparación para detectar una posible diferencia en los parámetros de valoración de los resultados clínicos, la tasa de aparición de los eventos adversos individuales puede limitar la capacidad de detección de una diferencia entre las dos estrategias de tratamiento. Así pues, este análisis conjunto puede no tener la potencia estadística suficiente para abordar el análisis de los componentes individuales de la evaluación de la seguridad y la eficacia; en consecuencia, dichos resultados deben considerarse generadores de hipótesis y no concluyentes. Concretamente, las diferencias en el IAM y la TS, favorables a los SBA en comparación con los stents liberadores de everolimus, deben interpretarse con precaución. Además, solo se dispuso de dos ensayos aleatorizados para el análisis conjunto. El hecho de que los dos ensayos combinados utilizaran dos SLF diferentes con características específicas de fármaco y polímero, comportamiento biológico diferente y resultados clínicos distintos podría constituir otra limitación importante. Además, aunque las definiciones utilizadas para los eventos adversos individuales fueron bastante uniformes en los dos ensayos, la definición de la recurrencia del IAM fue ligeramente diferente: en el ensayo TITAX-AMI se incluyeron todos los infartos recurrentes, mientras que en el ensayo BASE-ACS se incluyeron solo los relacionados con el vaso diana. Los datos no disponibles sobre el resultado agudo de la intervención, como el grado de flujo TIMI (Thrombolysis In Myocardial Infarction) y la resolución del segmento ST tras la intervención y, de forma similar, la falta de datos sobre el momento de aparición de los eventos como IAM y TS son otras limitaciones del estudio. Las limitaciones de un análisis agregado de los datos para resumir unos pocos estudios son la consideración inadecuada de la heterogeneidad, la notificación selectiva y el sesgo de publicación. Por último, el hecho de que la RLD fuera motivada por la isquemia puede haber subestimado las tasas reales de reestenosis en el stent; sin embargo, evitaría las reintervenciones innecesarias en las lesiones de reestenosis limítrofes a causa del «reflejo oculoestenótico» y la indebida ansiedad del paciente.
CONCLUSIONESEste análisis conjunto de los ensayos TITAX-AMI y BASE-ACS a los 2 años de seguimiento puso de manifiesto que, en los pacientes con IAMCEST tratados con intervención coronaria percutánea precoz, el implante de un SBA se asoció a menores tasas de recurrencia del IAM y de TS definitiva, en comparación con los SLF; no obstante, las tasas de muerte cardiaca y de RLD a causa de isquemia fueron similares.
CONFLICTO DE INTERESESNinguno.