La reciente propuesta del Academic Research Consortium for High Bleeding Risk (ARC-HBR), por consenso, no considera el síndrome coronario agudo (SCA) un criterio de hemorragia per se a pesar de tratarse de una situación de alto riesgo hemorrágico (ARH). En este artículo, se investiga la aplicabilidad de la clasificación y los criterios del ARC-HBR a los pacientes con SCA.
MétodosSe clasificó retrospectivamente a los pacientes con SCA sometidos a implante de stent coronario entre 2012 y 2018 en un hospital terciario como ARH si cumplían al menos 1 criterio mayor o 2 o más criterios menores del ARC-HBR. El objetivo primario fue la incidencia acumulada a 1 año de hemorragias de grado Bleeding Academic Research Consortium (BARC) 3-5.
ResultadosDe los 4.412 pacientes incluidos, el 29,5% estaba en ARH. La incidencia de hemorragias fue mayor en el grupo con ARH que en el de no ARH (el 9,4 frente al 1,3%; p < 0,01). Las tasas de hemorragias hospitalarias periprocedimiento y tras el alta también fueron mayores en el grupo con ARH (el 4,3 frente al 0,5% y el 5,3 frente al 0,9% respectivamente; p < 0,01). El riesgo hemorrágico se incrementó gradualmente a medida que aumentaban los criterios ARC-HBR: el 1,8, el 5,0, el 9,4, el 16,8, el 25,2 y el 25,9% con, respectivamente: solo 1 criterio menor, 2 o más criterios solo menores, 1 criterio mayor (solo o sumado a 1 criterio menor), 1 criterio mayor con 2 o más criterios menores, 2 o más criterios mayores (solos o sumados a 1 criterio menor) y 2 o más criterios mayores con 2 o más criterios menores. De los 20 criterios del ARC-HBR, 16 (80%) cumplieron los cortes predefinidos del riesgo hemorrágico BARC 3-5.
ConclusionesEste estudio respalda la aplicación de la clasificación y los criterios del ARC-HBR en el contexto del SCA. La clasificación ARC-HBR proporciona una estimación precisa del riesgo de hemorragia mayor y parece adecuada para la identificación y el tratamiento de los pacientes con ARH.
Palabras clave
La hemorragia es un objetivo de seguridad crítico en los pacientes con síndrome coronario agudo (SCA)1–6. La identificación precisa de los pacientes con SCA y alto riesgo hemorrágico (ARH) es esencial para maximizar los beneficios del tratamiento antitrombótico y los procedimientos invasivos mientras se minimizan los eventos hemorrágicos1,2,6–9. Hasta hace poco, no había consenso sobre la definición de ARH en pacientes tratados mediante intervención coronaria percutánea (ICP). En mayo de 2019, el Academic Research Consortium for High Bleeding Risk (ARC-HBR) se propuso como objetivo estandarizar la definición y los criterios indicativos de ARH3. Específicamente, se definió como ARH o riesgo hemorrágico 3-5 del Bleeding Academic Research Consortium (BARC) el riesgo hemorrágico ≥ 4% al año o el riesgo de hemorragia intracraneal (HIC) ≥ 1% al año4. El consenso ARC-HBR identificó 20 criterios clínicos y analíticos mayores y menores y propuso considerar a los pacientes con ARH si cumplían al menos 1 criterio mayor o 2 criterios menores3.
El campo de acción del ARC-HBR fue toda la población con ICP y, por consenso, el SCA no se consideró un criterio del ARC-HBR per se. Sin embargo, los pacientes con SCA generalmente tienen prescrito un tratamiento antiagregante plaquetario doble (TAPD) más intensivo y de mayor duración y presentan características clínicas y quirúrgicas bastante diferentes que los pacientes sometidos a una ICP programada por enfermedad coronaria estable1,2,5,9–13. Es probable que estos aspectos afecten a los valores de corte predefinidos del ARC-HBR para la hemorragia y a la aplicabilidad de los criterios del ARC-HBR en la situación concreta del SCA.
En consecuencia, en este estudio de pacientes con SCA no seleccionados, se analizó la aplicabilidad de la propuesta del ARC-HBR en el contexto del SCA y se comparó la capacidad de predecir eventos hemorrágicos mayores de la nueva clasificación ARC-HBR con la del sistema de clasificación PRECISE-DAPT14.
MÉTODOSPoblación de pacientesSe trata de un estudio observacional retrospectivo basado en el registro (NCT03664388) de SCA de CardioCHUVI (Cardiología del Complejo Hospitalario Universitario de VIgo), en el cual participaron todos los pacientes con diagnóstico primario y final de SCA consecutivos ingresados en nuestro servicio entre enero de 2012 y septiembre de 2018. No se incluyeron en el registro los SCA secundarios durante un ingreso hospitalario por otra causa. Los cardiólogos del servicio recogieron prospectivamente las variables demográficas, clínicas y angiográficas, así como las relacionadas con el tratamiento y las complicaciones. Se trató a los pacientes al criterio de su médico responsable.
Se incluyó a todos los pacientes en las bases de datos administrativas del sistema regional de historias clínicas electrónicas, tanto hospitalarias como ambulatorias. Este sistema permitió el registro de datos clínicos y de resultados de análisis de laboratorio, tratamiento farmacológico, eventos hemorrágicos y situación vital. Dos médicos revisaron meticulosamente las historias clínicas electrónicas de manera independiente en el momento de validar los eventos de interés.
Para este estudio, se revisaron exhaustivamente las variables relacionadas con los criterios del ARC-HBR y se recuperaron datos retrospectivos sobre algunos criterios del ARC-HBR que inicialmente no se encontraban en la base de datos (). Este enfoque permitió aplicar los 20 criterios del ARC-HBR (14 mayores y 6 menores) como se describió originalmente11, excepto el criterio menor «toma de antiinflamatorios no esteroideos orales o toma de corticoides», que se definió como crónico en lugar de una toma diaria esperada durante 4 semanas o más11.
La cohorte inicial del presente estudio estaba compuesta por 5.959 pacientes. Algunos pacientes fueron excluidos de este estudio por los siguientes motivos: a) no se les realizó implante hospitalario de stent coronario (1.436 pacientes); b) no recibieron TAPD (69 pacientes); c) faltaban datos sobre los criterios del ARC-HBR (18 pacientes) o para el cálculo de la puntuación PRECISE-DAPT (11 pacientes), y d) no había datos disponibles sobre hemorragia o sobre si el paciente seguía vivo (13 pacientes). Se utilizó heparina para la anticoagulación durante el procedimiento y los inhibidores de la glucoproteína IIb/IIIa periprocedimiento se dejaron a criterio del operador. La duración del TAPD quedó a criterio de los médicos responsables.
El estudio se ajustó a los principios recogidos en la Declaración de Helsinki y fue aprobado por el comité de ética local (Galicia; código HAC-2017-05, registro 2017/290).
Objetivos, definición y seguimientoLos objetivos primarios fueron las incidencias a 1 año de la primera hemorragia BARC 3-5 y la primera HIC. Se tomó como hemorragia la ocurrida peri-ICP, la hemorragia hospitalaria y la hemorragia después del alta. El objetivo secundario fue la incidencia a 1 año de la combinación de muerte cardiovascular, infarto de miocardio o accidente cerebrovascular isquémico.
La muerte cardiovascular y el infarto de miocardio se definieron según Hicks et al.15 y la clasificación Third Universal Definition16 respectivamente. El diagnóstico de accidente cerebrovascular isquémico requirió un déficit neurológico agudo ≥ 24 h con al menos 1 prueba de diagnóstico por la imagen y confirmación neurológica.
Se clasificó a los pacientes como en ARH según la clasificación del ARC-HBR con al menos 1 criterio mayor o al menos 2 criterios menores. Dado que la puntuación PRECISE-DAPT de 5 elementos (hemoglobina, edad, leucocitos, aclaramiento de creatina sérico y hemorragia previa) es el sistema recomendado actualmente (clase IIb) para la clasificación de ARH por la Sociedad Europea de Cardiología2, se utilizó la clasificación PRECISE-DAPT para ARH (≥ 25 frente a <25 puntos) como sistema comparativo para evaluar el rendimiento relativo de la nueva clasificación del ARC-HBR.
Dos cardiólogos entrenados revisaron y establecieron por separado los eventos de interés entre diciembre de 2019 y febrero de 2020.
Métodos estadísticosLos datos cuantitativos se presentan como media ±desviación estándar o mediana [intervalo intercuartílico] según corresponda. Las variables cualitativas se presentan como n (%). Las variables cualitativas se compararon mediante la prueba de la χ2 o la prueba exacta de Fisher; las variables cuantitativas se compararon mediante la prueba de la t de Student o la prueba de la U de Mann-Whitney. Ambas clasificaciones, ARC y PRECISE-DAPT, se introdujeron en modelos de riesgo competitivos de Fine-Gray diferentes (con la muerte no relacionada con la hemorragia como riesgo competitivo) para probar su asociación con los objetivos primarios. La capacidad de cada clasificación de separar a los pacientes con ARH de aquellos sin ARH se comprobó mediante curvas de incidencia acumulada y se comparó mediante la prueba de Fine-Gray. La capacidad de discriminación de las 2 clasificaciones para predecir eventos hemorrágicos se estimó mediante el estadístico C.
Para evaluar el valor pronóstico de los criterios del ARC-HBR, se generó y se graficó la incidencia acumulada del objetivo primario por el número de criterios del ARC-HBR y se comprobó que cada criterio mayor o menor del ARC-HBR por sí solo cumpliera el valor de corte predefinido del ARC para el riesgo de hemorragia BARC 3-5. Por último, el riesgo del objetivo secundario por grupos con ARH y sin ARH del ARC se valoró mediante el método de Fine-Gray (con muerte no cardiovascular como evento competitivo). También se calculó el estadístico C como medida de discriminación para predecir el evento isquémico con ARC-HBR.
Todos los análisis fueron en bruto, ya que tanto la clasificación binaria del ARC-HBR como sus criterios individuales se establecieron utilizarlos sin ninguna adaptación estadística. La asociación entre las clasificaciones del HBR con los resultados se expresó como subhazard ratio (sHR) con sus intervalos de confianza del 95% (IC95%). Se utilizó el método Bootstrap (500 iteraciones) para calcular la significación estadística, las sHR y los valores del estadístico C, así como los IC95%. Los análisis estadísticos fueron de 2 colas y se realizaron principalmente con STATA/MP 15.1. Se utilizó R 3.6.3 para calcular los valores del estadístico C mediante el paquete «pec». La significación estadística se estableció en p <0,05.
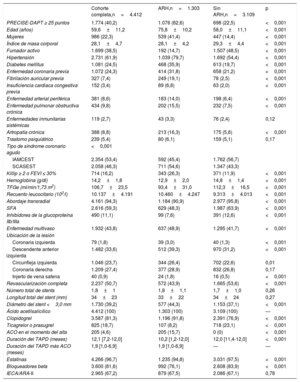
RESULTADOSCaracterísticas de referencia por estado de ARHLa cohorte del presente estudio estuvo compuesta por 4.412 pacientes con SCA tratados con TAPD e implante de stent coronario. La tabla 1 resume las diferencias en las características clínicas y quirúrgicas entre los grupos de pacientes según el estado de ARH mediante la clasificación del ARC-HBR.
Características basales de los pacientes y sus medicamentos
| Cohorte completa,n=4.412 | ARH,n=1.303 | Sin ARH,n=3.109 | p | |
|---|---|---|---|---|
| PRECISE-DAPT ≥ 25 puntos | 1.774 (40,2) | 1.076 (82,6) | 698 (22,5) | <0,001 |
| Edad (años) | 59,6±11,2 | 75,8±10,2 | 58,0±11,1 | <0,001 |
| Mujeres | 986 (22,3) | 539 (41,4) | 447 (14,4) | <0,001 |
| Índice de masa corporal | 28,1±4,7 | 28,1±4,2 | 29,3±4,4 | <0,001 |
| Fumador activo | 1.699 (38,5) | 192 (14,7) | 1.507 (48,5) | <0,001 |
| Hipertensión | 2.731 (61,9) | 1.039 (79,7) | 1.692 (54,4) | <0,001 |
| Diabetes mellitus | 1.081 (24,5) | 468 (35,9) | 613 (19,7) | <0,001 |
| Enfermedad coronaria previa | 1.072 (24,3) | 414 (31,8) | 658 (21,2) | <0,001 |
| Fibrilación auricular previa | 327 (7,4) | 249 (19,1) | 78 (2,5) | <0,001 |
| Insuficiencia cardiaca congestiva previa | 152 (3,4) | 89 (6,8) | 63 (2,0) | <0,001 |
| Enfermedad arterial periférica | 381 (8,6) | 183 (14,0) | 198 (6,4) | <0,001 |
| Enfermedad pulmonar obstructiva crónica | 434 (9,8) | 202 (15,5) | 232 (7,5) | <0,001 |
| Enfermedades inmunitarias sistémicas | 119 (2,7) | 43 (3,3) | 76 (2,4) | 0,12 |
| Artropatía crónica | 388 (8,8) | 213 (16,3) | 175 (5,6) | <0,001 |
| Trastorno psiquiátrico | 239 (5,4) | 80 (6,1) | 159 (5,1) | 0,17 |
| Tipo de síndrome coronario agudo | <0,001 | |||
| IAMCEST | 2.354 (53,4) | 592 (45,4) | 1.762 (56,7) | |
| SCASEST | 2.058 (46,3) | 711 (54,6) | 1.347 (43,3) | |
| Killip ≥ 2 o FEVI ≤ 30% | 714 (16,2) | 343 (26,3) | 371 (11,9) | <0,001 |
| Hemoglobina (g/dl) | 14,2±1,8 | 12,9±2,0 | 14,8±1,4 | <0,001 |
| TFGe (ml/min/1,73 m2) | 106,7±23,5 | 93,4±31,0 | 112,3±16,5 | <0,001 |
| Recuento leucocitario (103/l) | 10.137±4.191 | 10.460±4.247 | 9.313±4.013 | <0,001 |
| Abordaje transradial | 4.161 (94,3) | 1.184 (90,9) | 2.977 (95,8) | <0,001 |
| SFA | 2.616 (59,3) | 629 (48,3) | 1.987 (63,9) | <0,001 |
| Inhibidores de la glucoproteína IIb/IIIa | 490 (11,1) | 99 (7,6) | 391 (12,6) | <0,001 |
| Enfermedad multivaso | 1.932 (43,8) | 637 (48,9) | 1.295 (41,7) | <0,001 |
| Ubicación de la lesión | ||||
| Coronaria izquierda | 79 (1,8) | 39 (3,0) | 40 (1,3) | <0,001 |
| Descendente anterior izquierda | 1.482 (33,6) | 512 (39,3) | 970 (31,2) | <0,001 |
| Circunfleja izquierda | 1.046 (23,7) | 344 (26,4) | 702 (22,6) | 0,01 |
| Coronaria derecha | 1.209 (27,4) | 377 (28,9) | 832 (26,8) | 0,17 |
| Injerto de vena safena | 40 (0,9) | 24 (1,8) | 16 (0,5) | <0,001 |
| Revascularización completa | 2.237 (50,7) | 572 (43,9) | 1.665 (53,6) | <0,001 |
| Número total de stents | 1,8±1 | 1,8±1,1 | 1,7±1,0 | 0,26 |
| Longitud total del stent (mm) | 34±23 | 33±22 | 34±24 | 0,27 |
| Diámetro del stent <3,0 mm | 1.730 (39,2) | 577 (44,3) | 1.153 (37,1) | <0,001 |
| Ácido acetilsalicílico | 4.412 (100) | 1.303 (100) | 3.109 (100) | — |
| Clopidogrel | 3.587 (81,3) | 1.196 (91,8) | 2.391 (76,9) | <0,001 |
| Ticagrelor o prasugrel | 825 (18,7) | 107 (8,2) | 718 (23,1) | <0,001 |
| ACO en el momento del alta | 205 (4,6) | 205 (15,7) | 0 (0) | <0,001 |
| Duración del TAPD (meses) | 12,1 [7,2-12,0] | 10,2 [1,2-12,0] | 12,0 [11,4-12,0] | <0,001 |
| Duración del TAPD más ACO (meses) | 1,9 [1,0-6,9] | 1,9 [1,0-6,9] | — | — |
| Estatinas | 4.266 (96,7) | 1.235 (94,8) | 3.031 (97,5) | <0,001 |
| Bloqueadores beta | 3.600 (81,6) | 992 (76,1) | 2.608 (83,9) | <0,001 |
| IECA/ARA-II | 2.965 (67,2) | 879 (67,5) | 2.086 (67,1) | 0,78 |
ACO: anticoagulantes orales; ARA-II: antagonistas del receptor de la angiotensina II; ARH: alto riesgo hemorrágico; FEVI: fracción de eyección del ventrículo izquierdo; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; SFA: stent farmacoactivo; IECA: inhibidores de la enzima de conversión de la angiotensina; SCASEST: síndrome coronario agudo sin elevación del ST; TAPD: tratamiento antiagregante plaquetario doble; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
Hubo 1.303 pacientes (29,5%) en el grupo de ARC-ARH y 3.109 en el de ARC sin ARH. Hubo un mayor porcentaje de pacientes clasificados como ARH al aplicar PRECISE-DAPT (n=1.774; 40,2%) (prueba de McNemar, p <0,001).
En comparación con el grupo de ARC sin ARH, los pacientes del grupo ARC-ARH eran mayores, tenían mayores prevalencias de mujeres y comorbilidades cardiovasculares y no cardiovasculares. También utilizaron con menos frecuencia el abordaje transradial, hubo mayor proporción de enfermedad multivaso y recibieron ticagrelor o prasugrel con menos frecuencia. La duración media del TAPD fue más corta en el grupo de ARC-ARH (10,2 meses) que en el de ARC sin ARH (12,0 meses; p <0,001) (tabla 1).
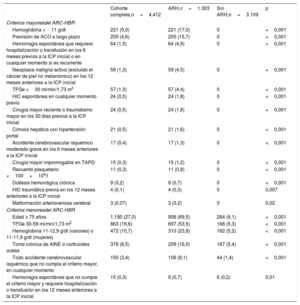
Prevalencia de los criterios del ARC-HBRLa tabla 2 muestra la prevalencia de los criterios del ARC-HBR. Los criterios mayores más frecuentes fueron hemoglobina <11 g/dl (5,0%), toma de anticoagulantes orales (4,6%), hemorragia espontánea (1,5%), neoplasia maligna activa (1,3%) y tasa de filtrado glomerular estimada <30ml/min/1,73 m2 (1,3%). Los 11 criterios mayores restantes apenas se observaron (≤ 0,5%).
Por orden decreciente, prevalencias de los criterios mayores y menores del Academic Research Consortium for High Bleeding Risk (ARC-HBR)
| Cohorte completa,n=4.412 | ARH,n=1.303 | Sin ARH,n=3.109 | p | |
|---|---|---|---|---|
| Criterios mayoresdel ARC-HBR | ||||
| Hemoglobina <11 g/dl | 221 (5,0) | 221 (17,0) | 0 | <0,001 |
| Previsión de ACO a largo plazo | 205 (4,6) | 205 (15,7) | 0 | <0,001 |
| Hemorragia espontánea que requiere hospitalización o transfusión en los 6 meses previos a la ICP inicial o en cualquier momento si es recurrente | 64 (1,5) | 64 (4,9) | 0 | <0,001 |
| Neoplasia maligna activa (excluido el cáncer de piel no melanómico) en los 12 meses anteriores a la ICP inicial | 59 (1,3) | 59 (4,5) | 0 | <0,001 |
| TFGe <30 ml/min/1,73 m2 | 57 (1,3) | 57 (4,4) | 0 | <0,001 |
| HIC espontánea en cualquier momento previo | 24 (0,5) | 24 (1,8) | 0 | <0,001 |
| Cirugía mayor reciente o traumatismo mayor en los 30 días previos a la ICP inicial | 24 (0,5) | 24 (1,8) | 0 | <0,001 |
| Cirrosis hepática con hipertensión portal | 21 (0,5) | 21 (1,6) | 0 | <0,001 |
| Accidente cerebrovascular isquémico moderado-grave en los 6 meses anteriores a la ICP inicial | 17 (0,4) | 17 (1,3) | 0 | <0,001 |
| Cirugía mayor improrrogable en TAPD | 15 (0,3) | 15 (1,2) | 0 | <0,001 |
| Recuento plaquetario <100×109/l | 11 (0,3) | 11 (0,8) | 0 | <0,001 |
| Diátesis hemorrágica crónica | 9 (0,2) | 9 (0,7) | 0 | <0,001 |
| HIC traumática previa en los 12 meses anteriores a la ICP inicial | 4 (0,1) | 4 (0,3) | 0 | 0,007 |
| Malformación arteriovenosa cerebral | 3 (0,07) | 3 (0,2) | 0 | 0,02 |
| Criterios menoresdel ARC-HBR | ||||
| Edad ≥ 75 años | 1.190 (27,0) | 906 (69,5) | 284 (9,1) | <0,001 |
| TFGe 30-59 ml/min/1,73 m2 | 863 (19,6) | 697 (53,5) | 166 (5,3) | <0,001 |
| Hemoglobina 11-12,9 g/dl (varones) o 11-11,9 g/dl (mujeres) | 472 (10,7) | 310 (23,8) | 162 (5,2) | <0,001 |
| Toma crónica de AINE o corticoides orales | 376 (8,5) | 209 (16,0) | 167 (5,4) | <0,001 |
| Todo accidente cerebrovascular isquémico que no cumpla el criterio mayor, en cualquier momento | 150 (3,4) | 106 (8,1) | 44 (1,4) | <0,001 |
| Hemorragia espontánea que no cumple el criterio mayor y requiere hospitalización o transfusión en los 12 meses anteriores a la ICP inicial | 15 (0,3) | 9 (0,7) | 6 (0,2) | 0,01 |
ACO: anticoagulantes orales; AINE: antiinflamatorios no esteroideos; ARC-HBR: Academy Research Consortium for High Bleeding Risk; ARH: alto riesgo hemorrágico; HIC: hemorragia intracraneal; ICP: intervención coronaria percutánea; TAPD: tratamiento antiagregante plaquetario doble; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan n (%).
Los criterios menores más comunes fueron la edad ≥ 75 años (27,0%), una tasa de filtrado glomerular estimada de 30-59ml/min/1,73 m2 (19,6%), una anemia leve (10,7%), la toma de antiinflamatorios no esteroideos orales o corticoides (8,5%) y accidente cerebrovascular isquémico previo (3,4%). Rara vez se observó hemorragia espontánea (0,3%).
Hemorragia BARC 3-5 al añoTras una media de 11,6±1,7 meses, 162 pacientes sufrieron un evento hemorrágico BARC 3-5; de ellos, 70 sufrieron hemorragia hospitalaria periprocedimiento.
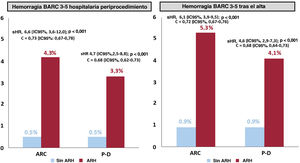
Por grupos del ARC, la incidencia general de hemorragia BARC 3-5 fue considerablemente mayor en el grupo de ARH que en el grupo sin ARH (el 9,4 frente al 1,3%; p <0,001; sHR=7,3; IC95%, 5,1-10,4) (figura 1). La tasa de hemorragia hospitalaria periprocedimiento fue del 4,3% en el grupo de ARH (frente al 0,5%; p <0,001; sHR=6,6; IC95%, 3,6-12,0), mientras que la tasa de hemorragia después del alta fue del 5,3% (frente al 0,9%; p <0,001; sHR=6,1; IC95%, 3,9-9,5) (figura 2).
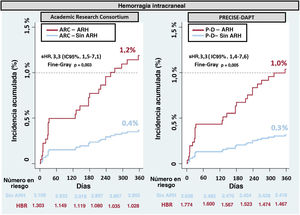
Incidencia acumulada de hemorragia BARC 3-5 por grupos con alto riesgo hemorrágico según las clasificaciones del ARC-HBR y PRECISE-DAPT. ARC-HBR: Academy Research Consortium for High Bleeding Risk; BARC: Bleeding Academy Research Consortium; IC95%: intervalo de confianza del 95%; P-D: PRECISE-DAPT (Predicting Bleeding Complication in Patients Undergoing Stent Implantation and Subsequent Dual Antiplatelet Therapy); sHR: subhazard ratio.
Incidencia acumulada de hemorragia hospitalaria periprocedimiento y después del alta por grupos con alto riesgo hemorrágico según las clasificaciones del ARC-HBR y PRECISE-DAPT. ARC: Academy Research Consortium; ARH: alto riesgo hemorrágico; BARC: Bleeding Academy Research Consortium; IC95%: intervalo de confianza del 95%; P-D: PRECISE-DAPT (Predicting Bleeding Complication in Patients Undergoing Stent Implantation and Subsequent Dual Antiplatelet Therapy); sHR: subhazard ratio.
Por grupos del PRECISE-DAPT, la incidencia general de hemorragia BARC 3-5 fue considerablemente mayor en el grupo de ARH que en el grupo sin ARH (el 7,2 frente al 1,4%; p <0,001; sHR=5,4; IC95%, 3,8-7,9) (figura 1). La tasa de hemorragia hospitalaria periprocedimiento fue del 3,3% en el grupo de ARH (frente al 0,5%; p <0,001; sHR=4,7; IC95%, 2,5-8,8), mientras que la tasa de hemorragia después del alta fue del 4,1% (frente al 0,9%; p <0,001; sHR=4,6; IC95%, 2,9-7,3) (figura 2).
Ambas clasificaciones se asociaron de manera importante con hemorragia BARC 3-5, si bien el ARC mostró una asociación general más pronunciada (sHR=7,3 frente a sHR=5,4) con hemorragia hospitalaria periprocedimiento (sHR=6,6 frente a sHR=4,7) y con hemorragia después del alta (6,1 frente a 4,6). Los valores del estadístico C también favorecieron los criterios generales del ARC (C=0,74 frente a C=0,70) para la hemorragia periprocedimiento (0,73 frente a 0,68) y para la hemorragia después del alta (0,72 frente a 0,68).
Hemorragia intracraneal al añoSufrieron HIC 26 pacientes de la población total. La incidencia de HIC fue considerablemente mayor en el grupo con ARC-HBR que en el grupo sin ARH (el 1,2 frente al 0,4%; p=0,003; sHR=3,3; IC95%, 1,5-7,1). Se observó el mismo patrón con PRECISE-DAPT (el 1,0 frente al 0,3%; p=0,005; sHR=3,3; IC95%, 1,4-7,6) (figura 3).
Incidencia acumulada de hemorragia intracraneal por grupos con alto riesgo hemorrágico según los sistemas de clasificación del ARC-HBR y PRECISE-DAPT. ARC: Academy Research Consortium; ARH: alto riesgo hemorrágico; IC95%: intervalo de confianza del 95%; P-D: PRECISE-DAPT (Predicting Bleeding Complication in Patients Undergoing Stent Implantation and Subsequent Dual Antiplatelet Therapy); sHR: subhazard ratio. .
Ambos sistemas de clasificación se asociaron de manera importante con similar riesgo de HIC (sHR=3,3 en ambos casos) y mostraron estadísticos C similares (C=0,65).
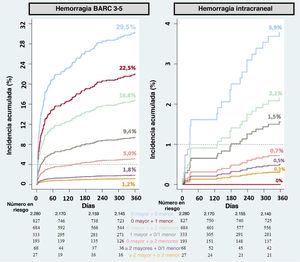
Valor pronóstico de los criterios del ARC-HBRLos resultados de riesgo hemorrágico aumentaron a mayor número de criterios mayores y menores (figura 4): para la hemorragia BARC 3-5, el riesgo fue del 1,8, el 5,0, el 9,4, el 16,8, el 22,5 y el 29,5% con solo 1 criterio menor, 2 o más criterios solo menores, 1 criterio mayor (solo o sumado a 1 criterio menor), 1 criterio mayor con 2 o más criterios menores, 2 o más criterios mayores (solos o sumados a 1 criterio menor) y 2 o más criterios mayores con 2 o más criterios menores respectivamente.
Para la HIC, el riesgo fue del 0,3, el 0,5, el 0,7, el 1,5, el 2,2 y el 3,9% con solo 1 criterio menor, 2 o más criterios solo menores, 1 criterio mayor (solo o sumado a 1 criterio menor), 1 criterio mayor más 2 o más criterios menores y 2 o más criterios mayores con 2 o más criterios menores respectivamente. No se observaron eventos de HIC en pacientes con 2 criterios mayores (solos o con 1 criterio menor).
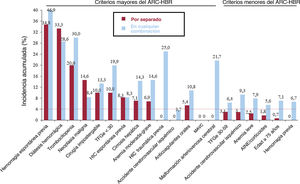
Las tasas de hemorragia BARC 3-5 a 1 año asociadas con cada criterio del ARC-HBR por separado se muestran en la figura 5. De los 20 criterios del ARC, 16 (80%) cumplieron los valores de corte predefinidos. Es decir, entre los 14 criterios mayores, 10 (71,4%) se asociaron por separado con un riesgo hemorrágico BARC 3-5 ≥ 4%. La HIC traumática previa, la cirugía/traumatismo mayor reciente, un accidente cerebrovascular isquémico moderado-grave previo y la malformación arteriovenosa cerebral por separado no se asociaron con un riesgo hemorrágico BARC 3-5 ≥ 4%. Los 6 criterios menores del ARC se asociaron por separado con un riesgo hemorrágico BARC 3-5 <4%.
Incidencia acumulada de hemorragia BARC 3-5 a 1 año de cada uno de los criterios del ARC-HBR por separado*. AINE: antiinflamatorios no esteroideos; ARC-HBR: Academy Research Consortium for High Bleeding Risk; BARC: Bleeding Academy Research Consortium; HIC: hemorragia intracraneal; MAVC: malformación arteriovenosa cerebral; TFGe: tasa de filtrado glomerular estimada. *En la tabla 2 se ofrece una descripción completa de cada criterio.
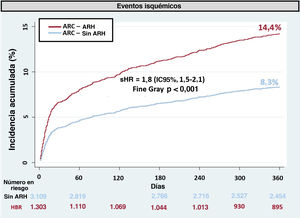
El objetivo isquémico se observó en 432 pacientes (329 infartos de miocardio, 56 accidentes cerebrovasculares isquémicos y 47 muertes cardiovasculares). La incidencia de eventos isquémicos fue 2 veces mayor en el grupo del ARC-ARH que en el del ARC sin ARH (el 14,3 frente al 8,3%; p <0,001; sHR=1,8; IC95%, 1,5-2,1) (figura 6). El estadístico C para predecir el criterio de valoración isquémico con ARC-HBR fue 0,57 (IC95%, 0,55-0,59).
DISCUSIÓNLos principales hallazgos del presente análisis son los siguientes: a) el ARC-HBR clasificó una proporción de pacientes con ARH considerablemente menor (≈30%) que el PRECISE-DAPT (≈40%); b) los pacientes con ARH según ARC-HBR y PRECISE-DAPT tenían un alto riesgo de hemorragia mayor que cumplía los umbrales predefinidos del ARC; c) el sistema del ARC mostró cualidades de un clasificador de ARH más efectivo que PRECISE-DAPT; d) hubo un efecto acumulativo por el cual el riesgo hemorrágico iba aumentando gradualmente a medida que aumentaba el número de criterios del ARC; e) la mayoría (80%) de los criterios mayores del ARC por separado cumplieron con el umbral predefinido de riesgo hemorrágico BARC 3-5, y f) los pacientes con ARH también corrían un riesgo considerablemente mayor de eventos isquémicos, pero la capacidad de predicción del ARC-HBR de estos eventos fue bastante deficiente.
Se espera que la propuesta del ARC-HBR3 ayude a los médicos a identificar correctamente a los pacientes con ARH con el fin de adaptar de manera óptima las estrategias para evitar hemorragias a los pacientes sometidos a ICP. El SCA, por consenso, no se consideró un criterio del ARC-HBR per se, pese a tratarse de una situación especial con características específicas relacionadas con el paciente y con el periprocedimiento que predisponen a un mayor riesgo de hemorragia que otras situaciones estables de ICP5,9–13. Estas consideraciones pueden afectar a la validez de los criterios y valores de corte predefinidos del ARC-HBR en el contexto del SCA. Aunque los autores del ARC-HBR afirman que el aumento del riesgo hemorrágico de los pacientes con SCA es más atribuible a un tratamiento agresivo con antiagregantes plaquetarios que al SCA per se, no se aportaron datos en el documento del ARC-HBR que respaldaran este enfoque. Además, estudios previos encontraron que el SCA es un predictor independiente de hemorragia hospitalaria o 30 días después de la ICP5,12. En consecuencia, se necesitan más datos antes de recomendar el uso de la definición y los criterios del ARC-HBR para los pacientes con SCA.
Nuestros datos indican que la aplicación de la clasificación ARC-HBR podría identificar correctamente a los pacientes que de verdad se encontraban en ARH y, por lo tanto, respaldan el uso de esa clasificación en el contexto del SCA. Además, nuestros hallazgos validan la mayoría (80%) de los criterios del ARC-HBR cuando se cumplen por separado, excepto 4 criterios mayores. Es importante destacar que la prevalencia de estos 4 criterios fue ≤ 0,5%, lo que podría haber limitado su valor pronóstico.
La validez de la propuesta del ARC-HBR se revisó recientemente en todos los pacientes sometidos a ICP17–19. Constataron que la definición del ARC-HBR identificó con éxito a los pacientes con tasas considerablemente más altas de eventos hemorrágicos después de la ICP. Sin embargo, los resultados de estudios anteriores deben interpretarse considerando la ausencia de definiciones o según las definiciones readaptadas de varios criterios del ARC-HBR y el empleo de objetivos de hemorragia distintos de la hemorragia BARC 3-5 o la HIC. Además, en estos estudios no se consideraron datos específicos sobre hemorragia en pacientes con SCA y hemorragia hospitalaria periprocedimiento, así como hemorragia después del alta en estos pacientes, ya que se incluyó a un escaso porcentaje de pacientes con SCA (menos de la mitad de la población total). Un hallazgo importante de nuestro análisis es el riesgo 7 veces mayor de hemorragia BARC 3-5 periprocedimiento observado en pacientes con SCA del grupo de ARH según el ARC-HBR. En comparación, los estudios que incluyeron a todos los pacientes sometidos a ICP comunicaron un riesgo de hemorragia 2-3 veces mayor en el grupo de ARH. Esto es importante en una población con SCA, dado el empleo de tratamientos antitrombóticos más potentes y otros aspectos de la intervención que aumentan el riesgo hemorrágico en comparación con los pacientes sometidos a una ICP programada. Por ejemplo, los factores quirúrgicos (acceso arterial y dispositivos de cierre vascular) y farmacológicos (múltiples fármacos antitrombóticos) pueden volverse menos relevantes para predecir el riesgo de hemorragia después del alta, mientras que las características del paciente y la intensidad y la duración del TAPD pueden volverse más importantes después del alta.
Los pacientes con ARH también tenían mayor carga de eventos isquémicos que los pacientes sin ARH. Este hallazgo puede explicarse por el hecho de que el riesgo isquémico está estrechamente relacionado con el riesgo hemorrágico, y los tratamientos antitrombóticos, así como los invasivos, deben equilibrar el beneficio de la prevención de eventos isquémicos con el riesgo de hemorragia grave. Cabe destacar que la clasificación dicotómica del ARC-HBR fue un predictor menos potente de eventos isquémicos (C=0,57) que del riesgo de hemorragia BARC 3-5 (C=0,74). Esto indica que la clasificación del ARC-HBR se correlaciona más estrechamente con el riesgo hemorrágico que con el riesgo isquémico. Este hallazgo probablemente sea atribuible a que los criterios del ARC-HBR están claramente orientados a la predicción de hemorragias y con pocos criterios compartidos sobre eventos isquémicos como la edad y la disfunción renal.
El PRECISE-DAPT se utilizó como comparador en este estudio. Cabe señalar que se diseñó específicamente para predecir la hemorragia después del alta, pero no la hospitalaria. Sin embargo, el sistema del ARC-HBR se comportó como un mejor clasificador de riesgo hemorrágico BARC 3-5 tanto hospitalario como después del alta de los pacientes con ARH que el sistema PRECISE-DAPT. No sorprende, ya que el PRECISE-DAPT de 5 elementos se originó a partir de una población seleccionada con bajo riesgo y no incluyó otros determinantes de hemorragia importantes en comparación con el sistema del ARC-HBR de 20 elementos. Otra ventaja del sistema del ARC-HBR es que permite clasificar a los pacientes de manera relativamente sencilla, según se cumplan al menos 1 criterio mayor o 2 criterios menores sin necesidad de hacer ningún cálculo.
Se ha demostrado que las estrategias para evitar hemorragias, como el acceso transradial, la anticoagulación periprocedimiento selectiva y los dispositivos de cierre vascular, además de acortar la duración del TAPD, son opciones terapéuticas seguras y eficaces para los pacientes con ARH6,8,9,20. El sistema de clasificación basado en los criterios del ARC-HBR puede identificar con precisión a los pacientes con una alta probabilidad de hemorragia mayor, lo que puede ayudar a los médicos a seleccionar la estrategia terapéutica más adecuada.
Fortalezas y limitacionesLas principales fortalezas de este estudio son el empleo de los criterios del ARC-HBR como se concibieron originalmente (excepto por los antiinflamatorios no esteroideos orales y los corticoides), la evaluación concomitante de la hemorragias BARC 3-5 y la HIC y la evaluación independiente de los resultados. Sin embargo, es necesario abordar algunas limitaciones importantes. Se trata de un estudio retrospectivo con las limitaciones inherentes a este tipo de diseño. El diseño unicéntrico de este estudio puede limitar la generalización de nuestros hallazgos, y el alcance del estudio se limitó a explorar adecuadamente la HIC según todos los criterios individuales del ARC-HBR.
Los hallazgos y las conclusiones de este estudio no se aplican al subgrupo de pacientes sin TAPD (n=69), ya que se los excluyó del estudio para reducir la heterogeneidad de la población estudiada y los posibles sesgos.
CONCLUSIONESDe los pacientes con SCA sometidos a implante de stent coronario, aproximadamente el 30% tiene ARH según el ARC-HBR, muchos menos que con PRECISE-DAPT (≈40%). La clasificación del ARC-HBR proporciona estimaciones de riesgo más precisas para predecir el riesgo de hemorragia mayor y parece una herramienta clínica más adecuada para la identificación y el tratamiento de los pacientes con ARH. La gran mayoría de los criterios del ARC-HBR por separado son criterios válidos para predecir el riesgo hemorrágico de los pacientes con SCA sometidos a ICP con implante de stent coronario, principalmente con acceso transradial.
- –
La identificación adecuada de los pacientes con síndrome coronario agudo (SCA) y alto riesgo hemorrágico es fundamental para optimizar el tratamiento invasivo y farmacológico.
- –
El Academic Research Consortium for High Bleeding Risk (ARC-HBR) ha estandarizado recientemente la definición de alto riesgo hemorrágico de los pacientes sometidos a ICP en el contexto de la enfermedad coronaria estable.
- –
Los pacientes con SCA suelen estar expuestos a un mayor riesgo hemorrágico, dado el tratamiento más agresivo que reciben y el propio proceso fisiopatológico subyacente.
- –
El ARC-HBR no ha considerado el SCA como un criterio per se, por lo que la aplicación del ARC-HBR en ese contexto no está clara.
- –
El sistema del ARC-HBR muestra una aplicabilidad adecuada para identificar a los pacientes con SCA y alto riesgo hemorrágico.
- –
La aplicación de los criterios del ARC-HBR fue más eficaz para identificar a los pacientes con SCA y ARH que la puntuación PRECISE-DAPT.
- –
Los criterios del ARC-HBR mostraron un efecto acumulativo en la predicción del riesgo hemorrágico: el riesgo aumenta gradualmente a medida que aumenta el número de criterios del ARC.
- –
Los pacientes con ARH también corren un riesgo considerablemente mayor de eventos isquémicos. Sin embargo, la capacidad del ARC-HBR para predecir estos eventos es bastante débil.
Ninguna.
CONTRIBUCIÓN DE LOS AUTORESEl autor para correspondencia es el responsable de garantizar que las descripciones sean precisas y sean acordadas por todos los autores. E. Abu-Assi concibió la idea presentada. Todos los autores, excepto Andrés Íñiguez Romo, participaron en la recogida y el tratamiento de los datos. E. Abu-Assi estableció los métodos y realizó los análisis. S. Raposeiras-Roubín validó el resultado de la investigación. Todos los autores discutieron los resultados y comentaron el original. Todos los autores revisaron críticamente el artículo en busca de contenido intelectual importante, estuvieron de acuerdo con todos los aspectos del trabajo y aprobaron la versión final que se publica.
CONFLICTO DE INTERESESE. Abu-Assi es Editor Asociado de Rev Esp Cardiol. Se ha seguido el procedimiento editorial de la Revista para garantizar un tratamiento imparcial del manuscrito.
Se puede consultar material adicional a este artículo en su versión electrónica disponible en https://doi.org/10.1016/j.recesp.2021.03.012.