Los dispositivos de asistencia ventricular han emergido en los últimos años como opción de rescate para pacientes con parada cardiaca y shock cardiogénico refractario1. La asistencia ventricular con membrana de oxigenación extracorpórea (AV-ECMO) venoarterial posibilita un abordaje percutáneo menos invasivo, la asistencia biventricular y una mejor oxigenación tisular, por lo que se puede utilizar como puente a la decisión para pacientes con fracaso multiorgánico grave a los que no se haya podido realizar una evaluación completa2. La experiencia con adultos publicada en España es escasísima3,4, y la mayoría de los casos publicados es tras cardiotomía5. La falta de estudios aleatorizados, el pequeño tamaño y la heterogeneidad de las series publicadas (con mortalidades elevadas en su mayor parte2) dificultan conocer con exactitud el perfil de paciente idóneo para AV-ECMO.
Nuestro objetivo es analizar características basales, indicaciones y duración de AV-ECMO, manejo y evolución intrahospitalaria y durante el seguimiento de los pacientes sometidos a AV-ECMO en nuestra unidad coronaria.
Entre diciembre de 2009 y octubre de 2012, se sometió a AV-ECMO a 16 pacientes. En todos los casos se utilizó el oxigenador Quadrox-D (Maquet; Wayne, New Jersey, Estados Unidos) y la bomba centrífuga Jostra Rotaflow (Maquet), excepto en un caso en que se utilizó la bomba centrífuga Centrimag (Thoratec; Pleasanton, California, Estados Unidos).
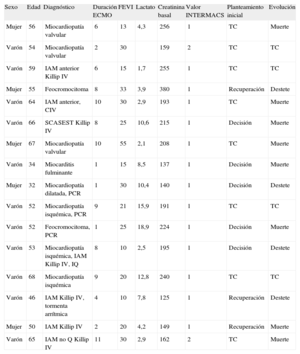
Las características de los pacientes se detallan en la tabla. La media de edad era 54,6 años y 11/16 (68,7%) eran varones. La principal indicación fue shock cardiogénico secundario a miocardiopatía dilatada (7/16, 43,7%), seguida de infarto de miocardio (6/16, 37,5%) y miocarditis (3/16, 18,7%). En 4 pacientes se había producido previamente parada cardiorrespiratoria prolongada.
Características basales, situación hemodinámica, indicaciones de asistencia ventricular con membrana de oxigenación extracorpórea y evolución clínica
| Sexo | Edad | Diagnóstico | Duración ECMO | FEVI | Lactato | Creatinina basal | Valor INTERMACS | Planteamiento inicial | Evolución |
| Mujer | 56 | Miocardiopatía valvular | 6 | 13 | 4,3 | 256 | 1 | TC | Muerte |
| Varón | 54 | Miocardiopatía valvular | 2 | 30 | 159 | 2 | TC | TC | |
| Varón | 59 | IAM anterior Killip IV | 6 | 15 | 1,7 | 255 | 1 | TC | TC |
| Mujer | 55 | Feocromocitoma | 8 | 33 | 3,9 | 380 | 1 | Recuperación | Destete |
| Varón | 64 | IAM anterior, CIV | 10 | 30 | 2,9 | 193 | 1 | TC | Muerte |
| Varón | 66 | SCASEST Killip IV | 8 | 25 | 10,6 | 215 | 1 | Decisión | Muerte |
| Mujer | 67 | Miocardiopatía valvular | 10 | 55 | 2,1 | 208 | 1 | TC | Muerte |
| Varón | 34 | Miocarditis fulminante | 1 | 15 | 8,5 | 137 | 1 | Decisión | Muerte |
| Mujer | 32 | Miocardiopatía dilatada, PCR | 1 | 30 | 10,4 | 140 | 1 | Decisión | Destete |
| Varón | 52 | Miocardiopatía isquémica, PCR | 9 | 21 | 15,9 | 191 | 1 | TC | TC |
| Varón | 52 | Feocromocitoma, PCR | 1 | 25 | 18,9 | 224 | 1 | Decisión | Muerte |
| Varón | 53 | Miocardiopatía isquémica, IAM Killip IV, IQ | 8 | 10 | 2,5 | 195 | 1 | Decisión | Destete |
| Varón | 68 | Miocardiopatía isquémica | 9 | 20 | 12,8 | 240 | 1 | TC | TC |
| Varón | 46 | IAM Killip IV, tormenta arrítmica | 4 | 10 | 7,8 | 125 | 1 | Recuperación | Destete |
| Mujer | 50 | IAM Killip IV | 2 | 20 | 4,2 | 149 | 1 | Recuperación | Muerte |
| Varón | 65 | IAM no Q Killip IV | 11 | 30 | 2,9 | 162 | 2 | TC | Muerte |
CIV: comunicación interventricular; ECMO: membrana de oxigenación extracorpórea; FEVI: fracción de eyección del ventrículo izquierdo; IAM: infarto agudo de miocardio; IQ: intervención quirúrgica; PCR: parada cardiorrespiratoria; SCASEST: síndrome coronario agudo sin elevación persistente del segmento ST; TC: trasplante cardiaco.
La gran mayoría de los pacientes (14/16, 87,5%) se encontraban en situación hemodinámica catastrófica al ingreso (categoría 1 de la clasificación INTERMACS6) a pesar de tratamiento inotrópico máximo y vasoconstrictor.
El 50% de los casos procedían de otros centros terciarios sin unidad de trasplante cardiaco. Todos los pacientes requirieron ventilación mecánica invasiva. Se utilizó catéter de Swan-Ganz en el 68,8% de los casos, contrapulsación intraaórtica en el 75% y depuración extrarrenal en el 31%.
En el 50% de los casos el planteamiento inicial fue puente a trasplante cardiaco; en el 18,7%, puente a la posible recuperación, y en el resto, puente a la decisión, en espera de evolución clínica.
De los 16 pacientes, 9 presentaron hemorragias clínicamente relevantes (deterioro hemodinámico, requerimiento de intervención o mortales) y 9 presentaron complicaciones infecciosas que requirieron antibioterapia endovenosa.
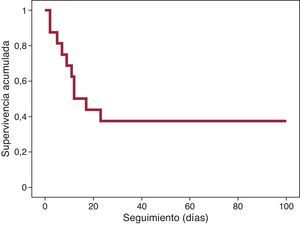
En 4 (25%) casos se consiguió un destete exitoso de AV-ACMO y en otros 4 (25%) se realizó trasplante cardiaco. Los 8 pacientes restantes fallecieron durante el soporte AV-ECMO. En 2 pacientes se sustituyó, tras cierta estabilización, la AV-ECMO por un dispositivo de asistencia biventricular central Centrimag de media duración (estrategia «puente al puente»). Un paciente trasplantado falleció por causas infecciosas y otro paciente, sometido a recambio por asistencia de media duración, falleció durante este soporte. La mortalidad intrahospitalaria fue del 62,5%. La evolución de la mortalidad se muestra en la figura. La principal causa de muerte fue la sepsis (5/10, 50%), seguida por las hemorragias (4/10, 40%) y la acidosis láctica refractaria secundaria a parada prolongada en el caso restante. Los 6 pacientes supervivientes al ingreso seguían vivos en el último seguimiento (media, 441 días).
Nuestros resultados revelan una morbimortalidad elevada, parecida a la de la mayoría de las series publicadas2. La extrema gravedad de los pacientes y que se trate de nuestra experiencia inicial permiten considerar razonables los resultados. El requerimiento de procedimientos invasivos y la tasa de complicaciones documentados hacen especialmente importante la adecuada selección de casos, y se aconseja reservar esta técnica para potenciales candidatos a trasplante cardiaco o cardiopatías agudas potencialmente reversibles en pacientes de menos de 70 años.
La principal limitación del trabajo es que se trate de un registro monocéntrico con escaso número de pacientes. Nos parece interesante recalcar la importancia de un futuro registro multicéntrico sistemático de casos que facilite un mayor tamaño muestral y una explotación más eficaz de los datos.
En conclusión, la AV-ECMO permitió el rescate del 38% de nuestros pacientes en situación catastrófica sin otras alternativas terapéuticas. Creemos que la implantación de AV-ECMO en unidades coronarias con volumen adecuado de pacientes de alta complejidad puede constituir un notable paso adelante en el manejo de pacientes críticos con insuficiencia cardiaca avanzada.Agradecimientos
Al Dr. Nicolás Manito, por su inestimable supervisión y revisión crítica del artículo.