El estudio PEACE (Performance of a sirolimus-eluting balloon strategy in acute and chronic coronary syndromes) investiga por primera vez si un balón recubierto de sirolimus (BRS) (Magic Touch, Concept Medical, India) deriva en resultados diferentes según se utilice en síndromes coronarios agudos (SCA) o crónicos (SCC).
MétodosEste es un análisis post-hoc del registro EASTBOURNE (NCT03085823). De los 2.083 pacientes inscritos, se utilizó un BRS para tratar a 968 (46,5%) pacientes con SCA y a 1.115 (53,5%) con SCC. El objetivo primario es la revascularización de la lesión diana a los 12 meses; las variables secundarias son el éxito angiográfico y los eventos cardiovasculares adversos mayores.
ResultadosLas características demográficas iniciales, el diámetro medio del vaso de referencia y la longitud media de la lesión son similares en ambos grupos. Es importante destacar que la predilatación se realiza con mayor frecuencia en SCA que en SCC (p=0,007). Los BRS se inflan a una presión estándar en ambos grupos, con una ligera tendencia hacia un tiempo de inflado más largo en SCA. El éxito angiográfico es alto en ambos grupos (el 97,4% en SCA frente al 97,7% en SCC; p=0,820) con un limitado uso de stents de rescate, y a los 12 meses la incidencia acumulada de revascularización de la lesión diana es similar en SCA y SCC (el 6,6% en SCA frente al 5,2% en SCC; p=0,258). Por el contrario, los eventos cardiovasculares adversos mayores son más frecuentes en SCA (el 10,4% frente al 8,3% en SCC; p=0,009) debido a su mayor número de recaídas. La reestenosis intrastent muestra una mayor proporción de revascularización de la lesión diana y eventos cardiovasculares adversos mayores que las lesiones nuevas, independientemente del tipo de presentación en el procedimiento inicial.
ConclusionesEste BRS muestra buenos resultados agudos y a un año, independientemente de la presentación clínica.
Palabras clave
El uso de balones recubiertos de fármaco (o balones farmacoactivos [BFA]) para tratar la enfermedad coronaria se ha ampliado progresivamente en los últimos años. La tasa no desdeñable de fallos del vaso diana en la era moderna de los stents farmacoactivos (SFA) ha generado la necesidad de estrategias de tratamiento diferentes durante la intervención coronaria percutánea (ICP)1,2.
En comparación con los SFA, los BFA no dejan ningún armazón metálico en el vaso y proporcionan una transferencia rápida y homogénea de fármacos antiproliferativos a la pared del vaso al hinchar el balón. Este tratamiento preserva la capacidad vasomotora coronaria, puede fomentar un remodelado favorable del vaso y podría traducirse en una reducción de la pérdida de luz vascular tardía en el seguimiento3.
Los ámbitos de aplicación más ampliamente aceptados para los BFA son la reestenosis en el stent (RS), los vasos pequeños y las estrategias combinadas con SFA durante las ICP complejas (como las de bifurcaciones)4-9. Los datos disponibles corresponden principalmente a plataformas que emplean paclitaxel; la introducción de nuevas tecnologías para el recubrimiento de los balones, como la de fármacos de la familia limus, solo recientemente ha llevado a realizar algunos estudios preclínicos y clínicos con plataformas que emplean sirolimus, lo cual ha abierto el camino para su uso en la práctica clínica.
En términos generales, no se suele utilizar los BFA para tratar la enfermedad en vasos grandes no tratados anteriormente, puesto que la evidencia al respecto es escasa, y los SFA de nueva generación continúan siendo el patrón de referencia en las guías internacionales. De igual modo, las oclusiones totales crónicas y los síndromes coronarios agudos (SCA) continúan siendo una zona gris para el uso de los BFA y se necesita más información basada en ensayos clínicos aleatorizados.
Por lo que respecta a este último grupo, son escasos los datos disponibles. Se ha cuestionado que la liberación del fármaco pueda verse dificultada en las lesiones que contienen un trombo10; además, la necesidad de una imprescindible preparación de la lesión antes de colocar el BFA y un hinchado prolongado del balón podrían desincentivar su uso en situaciones agudas en las que el riesgo de que no se restablezca el flujo es alto. Sin embargo, es posible que el propio trombo pueda impedir la determinación correcta del tamaño del vaso, lo que abre el camino a una mala aposición del stent; por otra parte, el medio inflamatorio en el caso del SCA puede favorecer un retraso en la cobertura tisular. En consecuencia, en estas 2 situaciones la ausencia de struts del stent puede ser beneficiosa, en especial en la enfermedad coronaria de múltiples vasos, en la que se prevén revascularizaciones múltiples.
El registro EASTBOURNE de pacientes no seleccionados (all-comers) tiene como objetivo evaluar los resultados de un nuevo balón recubierto de sirolimus en una serie amplia de pacientes (NCT03085823)11. El estudio PEACE (Performance of a sirolimus-eluting balloon strategy in acute and chronic coronary syndromes) es un análisis post hoc en el que se comparan los resultados del BFA en los contextos crónico y agudo.
MÉTODOSDescripción del dispositivoEl catéter con balón Magic Touch (Concept Medical, India) es un balón recubierto de sirolimus, semideformable, de intercambio rápido, basado en la tecnología Nanolute. El sirolimus tiene un carácter lipófilo desfavorable y puede perderse con facilidad hacia el torrente circulatorio. La tecnología Nanolute pretende superar estas limitaciones. Más concretamente, se encapsulan partículas submicrónicas de sirolimus en un portador del fármaco fosfolipídico de doble capa (el nanoportador). Un proceso de nebulización asistido por un gas inerte proporciona un recubrimiento esférico del balón con los nanoportadores de sirolimus. La concentración del fármaco llega a 1,27 μg/mm2. Tras el hinchado del balón en el lugar a tratar, se liberan los nanoportadores y, como consecuencia de la variación del pH, liberan el sirolimus, que penetra en las capas de la pared del vaso12.
Los tamaños disponibles del balón llegan a los 40 mm de longitud y 4 mm de diámetro, y todos ellos son compatibles con las guías estándares de 0,014” y con los catéteres guía de calibre 6 Fr.
Diseño del estudio EASTBOURNEEl EASTBOURNE es un registro clínico prospectivo, multicéntrico, impulsado por los investigadores, en el que se incluyó a una población de pacientes no seleccionados de la práctica clínica real, tratados con el balón liberador de sirolimus Magic Touch. El objetivo de este registro es observar y evaluar los resultados del balón recubierto de sirolimus Magic Touch en el tratamiento de cualquier tipo de lesión coronaria13. El estudio se llevó a cabo cumpliendo la Declaración de Helsinki y cada uno de los pacientes incluidos firmó un documento de consentimiento informado. Se registraron los parámetros demográficos de la población del estudio, incluida la variable sexo según lo notificado por el propio paciente.
Participaron un total de 38 centros de Europa y Asia con una experiencia suficiente en el uso del BFA (cada investigador debía certificar la utilización de un mínimo de 30 BFA al año en los últimos 5 años). Se consideró aptos para la inclusión a todos los pacientes de edad superior a 18 años con una indicación para ICP. La decisión de utilizar un BFA o cualquier otra estrategia de tratamiento se dejó a la elección del operador. La evaluación de la lesión se basó en un examen visual realizado por el operador por sí solo. Aparte de la hipersensibilidad conocida al sirolimus u otros fármacos relacionados con la intervención, los únicos criterios de exclusión fueron la presencia de calcificaciones graves o tortuosidad en el vaso diana y una carga trombótica intensa no tratable con aspiración manual.
Según se indica en el tercer informe del International DCB Consensus Group, es muy recomendable la preparación de la lesión con cualquier dispositivo que se considerara apropiado, y un intento de predilatación sin éxito se consideró un criterio de exclusión para el tratamiento con un BFA3.
Se recomendó un hinchado del BFA prolongado, durante al menos 30 s y preferiblemente 60 s. La decisión de implantar o no un stent después del BFA se dejó al criterio del operador, pero se recomendó hacerlo tan solo si había una presencia residual de una disección como mínimo de tipo C y un flujo Thrombolysis in Myocardial Infarction (TIMI) bajo.
El diseño del estudio incluyó una evaluación clínica (mediante llamada telefónica o visita presencial) al cabo de 1, 6, 24 y 36 meses y una visita en la consulta a los 12 meses de la intervención.
El objetivo principal fue la revascularización de la lesión diana (RLD) indicada clínicamente a los 12 meses. Los objetivos secundarios fueron el éxito angiográfico (estenosis residual < 50% y flujo coronario TIMI 3), el éxito de la intervención (éxito angiográfico y ausencia de eventos adversos cardiovasculares durante la hospitalización) y los eventos adversos cardiovasculares mayores (MACE), consistentes en la combinación de muerte de causa cardiaca, infarto de miocardio (IM) agudo espontáneo y necesidad de RLD a los 6, 12, 24 y 36 meses del implante. Un comité de validación de eventos centralizado, formado por cardiólogos que no participaban en el estudio, evaluó todos los eventos en los formularios de notificación de casos electrónicos, tras haber obtenido la documentación pertinente.
Subestudio PEACEEl subestudio PEACE es un análisis de cohorte post hoc en el que se compararon los resultados del dispositivo Magic Touch en los SCA con los obtenidos en los síndromes coronarios crónicos (SCC) según lo determinado por la forma de presentación clínica en la intervención índice de cualificación para el estudio. Se incluyeron en los SCA los síndromes de los pacientes con una forma de presentación de angina inestable, infarto agudo de miocardio sin elevación del segmento ST (IAMSEST) e infarto agudo de miocardio con elevación del segmento ST (IAMCEST), mientras que los SCC fueron los síndromes de los pacientes con angina estable o isquemia silente. Se incluyeron en el análisis tanto las lesiones de novo como las RS. Tras la comparación de las características basales y de la intervención en los 2 grupos, se puso el foco en los resultados hospitalarios (éxito angiográfico) y a los 12 meses (necesidad de RLD y aparición de MACE).
Análisis estadísticoLas variables cualitativas se presentan en forma de número y porcentaje y las continuas, mediante la media ± desviación estándar o la mediana [intervalo intercuartílico]. Se utilizó la prueba de la t de Student para evaluar las diferencias entre las variables continuas, la prueba de la U de Mann-Whitney para las variables no paramétricas y la prueba de la χ2 o la prueba exacta de Fisher para las variables cualitativas. El riesgo total acumulado de RLD se estimó con el método de Kaplan-Meier, y las diferencias entre los grupos se evaluaron con la prueba de orden logarítmico (log-rank). Se realizó una comparación de los resultados en el SCC con los obtenidos en el SCA, y luego se aplicó una estratificación según el tipo de lesión diana (de novo frente a RS). El efecto de la indicación clínica para la ICP en los objetivos del estudio se estimó con un modelo de riesgos proporcionales de Cox y se expresó en forma de hazard ratio (HR) con su intervalo de confianza del 95% (IC95%) y el valor de p. Se utilizaron modelos ajustados respecto a las características clínicas y de la intervención que alcanzaban significación estadística, como fueron edad, sexo, dislipemia, IM previo, ICP previa, fracción de eyección del ventrículo izquierdo, creatinina, hemoglobina, predilatación, presión de hinchado del BFA y tiempo de hinchado del BFA. Se consideró estadísticamente significativo un valor de p bilateral < 0,05; todos los análisis se llevaron a cabo con el programa informático R (R Core Team 2022, R Foundation for Statistical Computing, Austria).
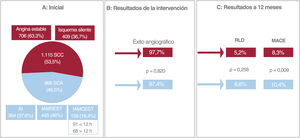
RESULTADOSEn total, se incluyó en el registro EASTBOURNE a 2.123 pacientes tratados con un BFA Magic Touch entre septiembre de 2016 y noviembre de 2020. No se había registrado la forma de presentación clínica en la intervención índice en 40 pacientes, por lo que finalmente se incluyó a 2.083 pacientes en el subestudio PEACE. En esta población había 1.115 pacientes (53,5%) con un SCC y 968 (46,5%) con un SCA que fueron tratados con el dispositivo del estudio. Hubo 364 pacientes (37,6%) con angina inestable, 445 (46%) con IAMSEST y 159 (16,4%, incluidos los pacientes con una presentación temprana o tardía de este último grupo) con IAMCEST (figura 1A). En total, el investigador consideró lesiones culpables al 79% de las lesiones incluidas en el grupo de SCA. Se dispuso de información de seguimiento completa a los 12 meses en 1.927 pacientes (92,5%).
Figura central. Población del subestudio PEACE y resultados de la intervención y a los 12 meses. A: población total en la situación basal según la forma de presentación clínica al realizar la intervención inicial. B: resultados inmediatos de la intervención por lo que respecta al éxito angiográfico (reestenosis residual inferior al 50% y flujo coronario TIMI 3) comparados entre los pacientes con SCA y con SCC. C: resultados a los 12 meses por lo que respecta a la RLD y los MACE comparados entre los pacientes con SCA y con SCC. AI: angina inestable; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; MACE: eventos adversos cardiovasculares mayores; RLD: revascularización de lesión diana; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico; TIMI: Thrombolysis in Myocardial Infarction.
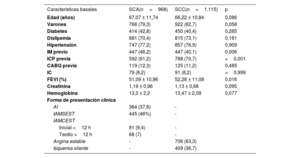
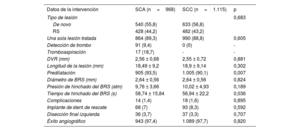
Los parámetros demográficos basales fueron comparables entre los pacientes con SCA y con SCC, excepto por la prevalencia de un IM previo, que fue mayor en los casos de presentación aguda (SCA, el 46,2% frente a SCC, el 40,1%; p=0,006) (tabla 1). Las lesiones de novo representaron más de la mitad del total de la población del estudio (56,3%) y su distribución igual en los 2 grupos (p=0,683) (figura 2A). Las características de la intervención se muestran en la tabla 2. Se aplicó una estrategia de BFA a una única lesión en la mayoría de los pacientes (el 89,3 frente al 88,8% de los pacientes con SCA y con SCC respectivamente; p=0,695), pero eventualmente se llegaron a tratar hasta 4 lesiones con BFA en unos pocos casos. Según lo indicado por la evaluación fluoroscópica, las lesiones leve y moderadamente calcificadas fueron más frecuentes en los pacientes con SCA y con SCC respectivamente, mientras que las lesiones con calcificación grave estuvieron representadas por igual en los 2 grupos (leves, el 61,2 frente al 9,4%; moderadas, el 31,8 frente al 84,4%; graves, el 7,1 frente al 6,2%; p≤0,001). La media del diámetro del vaso de referencia y la media de la longitud de la lesión fueron comparables entre los 2 grupos (diámetro, 2,56±0,68 frente a 2,55±0,72mm; p=0,881; longitud, 18,49±9,20 frente a 18,9±9,14mm; p=0,302). Es de destacar que se realizó predilatación en un alto porcentaje de los pacientes, pero no en todos, a pesar de la recomendación clara del protocolo, y que su uso fue más frecuente en los pacientes con SCA que en aquellos con SCC (el 93,5% frente al 90,1%; p=0,007). El BFA se hinchó a una presión estándar en ambos grupos (media, 9,76±3,66 frente a 10,02±4,93 atm; p=0,189) con un tiempo de hinchado moderadamente superior en los SCA (media de duración, 58,74±15,84 frente a 56,94±22,2 s; p=0,036).
Características basales comparadas del síndrome coronario agudo y el síndrome coronario crónico en la población total
| Características basales | SCA(n=968) | SCC(n=1.115) | p |
|---|---|---|---|
| Edad (años) | 67,07 ± 11,74 | 66,22 ± 10,84 | 0,086 |
| Varones | 768 (79,3) | 922 (82,7) | 0,058 |
| Diabetes | 414 (42,8) | 450 (40,4) | 0,285 |
| Dislipemia | 681 (70,4) | 815 (73,1) | 0,181 |
| Hipertensión | 747 (77,2) | 857 (76,9) | 0,909 |
| IM previo | 447 (46,2) | 447 (40,1) | 0,006 |
| ICP previa | 592 (61,2) | 788 (70,7) | <0,001 |
| CABG previa | 119 (12,3) | 125 (11,2) | 0,485 |
| IC | 79 (8,2) | 91 (8,2) | >0,999 |
| FEVI (%) | 51,09 ± 10,96 | 52,28 ± 11,08 | 0,016 |
| Creatinina | 1,19 ± 0,96 | 1,13 ± 0,68 | 0,095 |
| Hemoglobina | 13,3 ± 2,2 | 13,47 ± 2,09 | 0,077 |
| Forma de presentación clínica | |||
| AI | 364 (37,6) | - | |
| IAMSEST | 445 (46%) | - | |
| IAMCEST | |||
| Inicial <12 h | 91 (9,4) | - | |
| Tardío >12 h | 68 (7) | - | |
| Angina estable | - | 706 (63,3) | |
| Isquemia silente | - | 409 (36,7) |
AI: angina inestable; CABG: cirugía de revascularización coronaria; FEVI: fracción de eyección del ventrículo izquierdo; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; IC: insuficiencia cardiaca; ICP: intervención coronaria percutánea; IM: infarto de miocardio; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico.
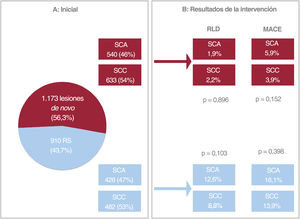
Resultados a los 12 meses de la cohorte de pacientes del estudio PEACE (SCA y SCC) según el tipo de lesión tratada (lesiones de novo o RS). A: población total en la situación basal según el tipo de lesión tratada. B: resultados a los 12 meses por lo que respecta a la RLD y los MACE según el tipo de lesión tratada y comparación entre los pacientes con SCA y con SCC. MACE: eventos adversos cardiovasculares mayores; RLD: revascularización de la lesión diana; RS: reestenosis en el stent; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico.
Datos de la intervención comparados entre síndrome coronario agudo y síndrome coronario crónico en la población total
| Datos de la intervención | SCA (n=968) | SCC (n=1.115) | p |
|---|---|---|---|
| Tipo de lesión | 0,683 | ||
| De novo | 540 (55,8) | 633 (56,8) | |
| RS | 428 (44,2) | 482 (43,2) | |
| Una sola lesión tratada | 864 (89,3) | 990 (88,8) | 0,605 |
| Detección de trombo | 91 (9,4) | 0 (0) | - |
| Tromboaspiración | 17 (18,7) | - | - |
| DVR (mm) | 2,56 ± 0,68 | 2,55 ± 0,72 | 0,881 |
| Longitud de la lesión (mm) | 18,49 ± 9,2 | 18,9 ± 9,14 | 0,302 |
| Predilatación | 905 (93,5) | 1.005 (90,1) | 0,007 |
| Diámetro de BRS (mm) | 2,64 ± 0,56 | 2,64 ± 0,56 | 0,824 |
| Presión de hinchado del BRS (atm) | 9,76 ± 3,66 | 10,02 ± 4,93 | 0,189 |
| Tiempo de hinchado del BRS (s) | 58,74 ± 15,84 | 56,94 ± 22,2 | 0,036 |
| Complicaciones | 14 (1,4) | 18 (1,6) | 0,895 |
| Implante de stent de rescate | 68 (7) | 93 (8,3) | 0,592 |
| Disección final izquierda | 36 (3,7) | 37 (3,3) | 0,707 |
| Éxito angiográfico | 943 (97,4) | 1.089 (97,7) | 0,820 |
BRS: balón cubierto de sirolimus; DVR: diámetro del vaso de referencia; RS: reestenosis en el stent.
Las características de la lesión corresponden a la lesión principal en caso de tratamiento de lesiones múltiples. Los valores expresan n (%) o media ± desviación estándar.
El éxito angiográfico fue elevado en ambos grupos (SCA, el 97,4% frente a SCC, el 97,7%; p=0,820) (figura 1B) y el implante de stents se limitó a un pequeño porcentaje de los pacientes (SCA, n=68 [7%] frente a SCC, n=93 [8,3%]; p=0,592) y se debió a un retroceso agudo del vaso o a una disección limitante del flujo. En total, se detectó una disección final en la angiografía en 73 pacientes (36 SCA [3,7%] frente a 37 SCC [3,3%]; p=0,707).
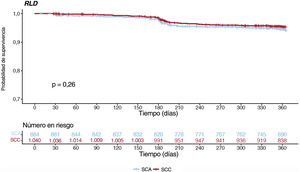
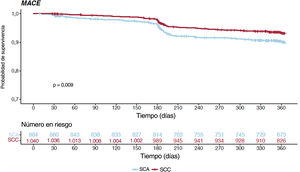
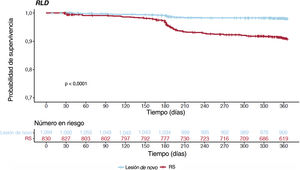
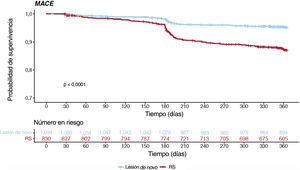
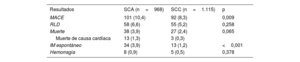
En la tabla 3 y la figura 1C se presentan los resultados globales sin ajustar a 1 año. A los 12 meses, la incidencia acumulada de RLD fue comparable, con independencia de que la intervención índice se hubiera realizado en un síndrome agudo o crónico (el 6,6 frente al 5,2% respectivamente; hazard ratio [HR] = 0,792; intervalo de confianza del 95% [IC95%], 0,528-1,186; p=0,258) (figura 3); en cambio, la incidencia acumulada de MACE fue mayor en los pacientes con una forma de presentación de SCA (el 10,4 frente al 8,3%; HR = 0,656; IC95%, 0,477-0,902; p=0,009) y su aparición pareció divergir del mes 6 de seguimiento en adelante (figura 4). La diferencia en el objetivo combinado se debió principalmente a una mayor incidencia de IM espontáneos (el 3,9 frente al 1,2%; p<0,001).
Comparación de los resultados a 12 meses en pacientes con síndrome coronario agudo y con síndrome coronario crónico en la población total
| Resultados | SCA (n=968) | SCC (n=1.115) | p |
|---|---|---|---|
| MACE | 101 (10,4) | 92 (8,3) | 0,009 |
| RLD | 58 (6,6) | 55 (5,2) | 0,258 |
| Muerte | 38 (3,9) | 27 (2,4) | 0,065 |
| Muerte de causa cardiaca | 13 (1,3) | 3 (0,3) | |
| IM espontáneo | 34 (3,9) | 13 (1,2) | <0,001 |
| Hemorragia | 8 (0,9) | 5 (0,5) | 0,378 |
IM: infarto de miocardio; MACE: eventos adversos cardiovasculares mayores; RLD: revascularización de la lesión diana; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico.
Tras aplicar un ajuste respecto a los objetivos del estudio en la situación basal y respecto a las características de la intervención, se confirmaron los resultados globales del estudio (RLD, HR = 0,76; p=0,202; MACE, HR = 0,70; p=0,036).
Se llevaron a cabo también análisis por subgrupos para las lesiones con RS y las lesiones de novo (pacientes con SCA tratados por una RS, 428 [47%]; pacientes con SCC tratados por una RS, 482 [53%]). A los 12 meses de seguimiento, las RS tratadas con BFA mostraron una mayor proporción de RLD y de aparición de MACE en comparación con las lesiones de novo tratadas con una estrategia similar (figura 5 y figura 6), con independencia del tipo de presentación en la intervención índice (véase la información adicional al respecto en la tabla 4 y la figura 2B). Asimismo es de destacar que la recurrencia de un IM espontáneo (uno de los componentes del objetivo combinado) fue más frecuente en los pacientes con SCA que en aquellos con SCC tratados por una RS en comparación con las lesiones de novo (tasa acumulada de IM a los 12 meses para las lesiones de novo, SCA frente a SCC, el 1,2 frente al 0,8%; p=0,748; tasa acumulada de IM a los 12 meses para la RS, el 7,2 frente al 1,8%; p<0,001).
Comparación de los resultados a 12 meses en pacientes con síndrome coronario agudo y con síndrome coronario crónico tratados por lesiones coronarias de novo o con reestenosis en el stent
| Lesiones coronarias de novo (n=1.173) | |||
|---|---|---|---|
| Resultados | SCA (n=540) | SCC (n=633) | p |
| MACE | 32 (5,9) | 25 (3,9) | 0,152 |
| RLD | 9 (1,8) | 13 (2,2) | 0,851 |
| Muerte | 16 (3,0) | 8 (1,3) | 0,065 |
| Muerte de causa cardiaca | 3 (0,6) | 0 | |
| IM | 6 (1,2) | 5 (0,8) | 0,748 |
| Hemorragia | 3 (0,6) | 3 (0,5) | >0,999 |
| Lesiones con RS (n=910) | |||
|---|---|---|---|
| Resultados | SCA (n=428) | SCC (n=482) | p |
| MACE | 69 (16,1) | 67 (13,9) | 0,398 |
| RLD | 49 (12,6) | 42 (9,2) | 0,141 |
| Muerte | 22 (5,1) | 19 (3,9) | 0,478 |
| Muerte de causa cardiaca | 10 (2,3) | 3 (0,6) | |
| IM | 28 (7,2) | 8 (1,8) | <0,001 |
| Hemorragia | 5 (1,3) | 2 (0,4) | 0,330 |
IM: infarto de miocardio; MACE: eventos adversos cardiovasculares mayores; RLD: revascularización de la lesión diana; RS: reestenosis en el stent; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico.
Los valores expresan n (%).
Las estrategias de reperfusión percutánea han mejorado drásticamente los resultados en los pacientes que sufren un IM agudo y los implantes de stents han superado progresivamente los de la antigua angioplastia con balón simple al reducir la necesidad de RLD en el seguimiento14. No obstante, ni siquiera los SFA de nueva generación reducen significativamente la incidencia de variables de valoración «duras» como la mortalidad o la recurrencia del IM durante un seguimiento a largo plazo, lo cual se ha explicado por la posible aparición de complicaciones relacionadas con el stent (trombosis tardía y muy tardía)15.
Como alternativa, una estrategia con BFA combina las ventajas de un fármaco antiproliferativo con la ausencia de un armazón metálico permanente en el vaso sanguíneo.
Los principales resultados del presente estudio pueden resumirse como sigue: a) este es el primer estudio en el que se ha investigado el resultado de un BFA recubierto de sirolimus en los SCA, dado que en este contexto solamente se han validado hasta el momento plataformas con paclitaxel; b) el BFA con sirolimus Magic Touch muestra unos resultados agudos y a 1 año similares cuando se emplea en la ICP para un SCA o para un SCC, y c) las tasas de predilatación y los tiempos de hinchado del BFA similares en el SCA y el SCC sugieren que los tiempos de intervenciones mayores, como son de prever cuando se emplea un BFA, no impiden al operador aplicar esta estrategia, ni siquiera en el contexto agudo.
Como ya se ha mencionado, la evidencia sobre la aplicación de los BFA en pacientes con SCA se limita a algunos registros prospectivos y unos pocos ensayos aleatorizados, todos ellos basados en el empleo de balones liberadores de paclitaxel16-19. En el ensayo REVELATION (Revascularization with paclitaxel-coated balloon angioplasty vs drug-eluting stenting in acute MI) se incluyó a 120 pacientes con IAMCEST aptos para una ICP primaria, a los que se asignó aleatoriamente, en relación 1:1, el tratamiento con un BFA (Pantera Lux, Biotronik, Alemania) o con un SFA (Orsiro, Biotronik, o Xience, Abbott, Estados Unidos). El seguimiento angiográfico a los 9 meses indicó que el criterio de valoración consistente en la reserva fraccional no mostró diferencias entre los 2 grupos (p=0,27); tampoco hubo diferencias en el objetivo secundario de los MACE (p=1,0), que también incluía la RLD (el 3% con los BFA frente al 2% con los SFA)19. Se confirmó una tasa de MACE similar en los 2 grupos a los 2 años de seguimiento (HR = 2,86; IC95%, 0,30-27,53; p=0,34). Tan solo se notificó 1 evento adicional entre los seguimientos a los 9 meses y a los 2 años. Este paciente concreto había sido asignado inicialmente a la angioplastia con BFA, pero necesitó un implante de stent como tratamiento de rescate durante la intervención índice, y hubo una RLD a causa de una RS que causó un SCA a los 561 días del implante20.
En el ensayo PEP-CAD NSTEMI se incluyó a 210 pacientes con IAMSEST que presentaban lesiones coronarias de novo a los que se aleatorizó a tratamiento con un BFA recubierto de paclitaxel (SeQuent Please, B. Braun Melsungen AG, Alemania) o un stent metálico (SM) estándar. Se observó no inferioridad del BFA respecto al SM, puesto que tanto el objetivo principal, que era el fallo de la lesión diana, como el secundario, que fueron los MACE, fueron comparables en los 2 grupos (fallo de la lesión diana con el BFA y el SM, el 3,8 frente al 6,6%; p=0,53; MACE, 6,7 frente al 14,2%; p=0,11)18.
En el subanálisis preespecificado del ensayo BASKET-SMALL 2, en el que se incluyeron lesiones en vasos de diámetro <3 mm, en el seguimiento a 1 año no hubo diferencias significativas en la incidencia del objetivo principal, es decir, los MACE, según el tratamiento asignado aleatoriamente a los pacientes con un SCA (HR = 0,50; IC95%, 0,19-1,26 con el BFA en comparación con el SFA) o con un SCC (HR = 1,29; IC95%, 0,67-2,47 con el BFA en comparación con el SFA) y no se observó interacción entre la forma de presentación clínica y el efecto del tratamiento (p para la interacción = 0,088)21.
No obstante, no se prevé un efecto de clase de los BFA, dada la enorme heterogeneidad existente en las formulaciones, las dosis, la cinética de liberación y la interacción entre fármaco y tejidos. Los fármacos antiproliferativos pertenecientes a la familia de los limus suelen tener una transferencia a los tejidos más lenta que la del paclitaxel. Para superar estas limitaciones se han aplicado varias tecnologías para la liberación del sirolimus, entre ellas las que utilizan fosfolípido portador del fármaco, que es la que se emplea en la plataforma Magic Touch3.
El presente estudio muestra por primera vez el buen rendimiento de un balón liberador de sirolimus en el contexto de los SCA. Mediante una comparación directa de los pacientes con SCA frente a los pacientes con SCC, se ha puesto de manifiesto que no hubo diferencias significativas en los resultados de la intervención ni en los resultados a 1 año por lo que respecta al éxito angiográfico y la RLD, lo cual respalda su uso en ambos contextos sin distinción. La mayor incidencia de MACE observada en los pacientes con SCA se debió principalmente a la aparición de nuevos IM espontáneos (no relacionados con la intervención). Este resultado sería esperable, con independencia de cuál fuera el dispositivo utilizado, ya que las recurrencias no son infrecuentes después de un SCA (en esta serie, los pacientes con SCA también tenían una mayor tasa de IM previos en sus características basales).
Además, nuestro estudio se basa en un registro prospectivo de pacientes no seleccionados que incluye tanto vasos pequeños como vasos grandes, así como lesiones de novo y RS, y casos de enfermedad de un solo vaso o de múltiples vasos.
A pesar de esta población heterogénea, los resultados globales a los 12 meses de seguimiento tras el uso del dispositivo Magic Touch en pacientes con un SCA fueron buenos y no mostraron diferencias respecto a los pacientes con un SCC; es de destacar que, en este registro de pacientes no seleccionados, las tasas de RLD y MACE en la cohorte de pacientes con lesiones de novo (el 1,9 y el 5,9% respectivamente) son comparables a las descritas con los balones recubiertos de paclitaxel empleados en poblaciones seleccionadas en los ensayos mencionados (como la tasa de RLD del 3% en el ensayo REVELATION o la tasa de MACE del 6,7% en el PEP-CAD NSTEMI). Además, los SFA de la generación actual utilizados en el contexto agudo produjeron unos resultados similares en el seguimiento. Por ejemplo, la incidencia de RLD fue del 2,7% con un stent de polímero biodegradable liberador de sirolimus en el estudio MASTER (en el que se comparó un SFA con un SM), mientras que en el ensayo BIOSTEMI, en el que se comparó un stent de polímero biodegradable liberador de sirolimus con un stent de polímero permanente liberador de everolimus, las tasas fueron del 2 y el 3% respectivamente22,23.
De todos modos, los resultados aparentemente peores con el BFA Magic Touch utilizado en la cohorte con RS siguen siendo coherentes con los de estudios previos de balones con paclitaxel usados para tratar las RS, en los que se observó una tasa de RLD del 10-15% a los 12 meses24,25. Es de destacar que nuestros resultados son independientes de la indicación para la ICP (SCA frente a SCC) y confirman que las estrategias de tratamiento para la RS continúan planteando un verdadero reto.
Por último, nuestro estudio muestra similares tasas de predilatación y tiempo de hinchado del BFA en los SCA y los SCC. Además, se observa que ni siquiera la presencia de un trombo (que se detectó en 91 pacientes con SCA y se abordó preventivamente mediante aspiración en un pequeño porcentaje de esos casos, el 18,7%) impidió a los operadores utilizar una estrategia de BFA.
LimitacionesLas principales limitaciones de este estudio pueden resumirse como sigue: a) pese a tratarse de un registro de pacientes no seleccionados, el estudio se limitó a centros con experiencia en el uso de los BFA y, por consiguiente, no podía ser realmente representativo de la práctica clínica real respecto a los BFA; b) no se dispuso de un laboratorio centralizado, y tanto la evaluación de las lesiones en la situación basal como la valoración de los resultados finales de la intervención se dejaron al criterio de cada operador, lo cual limita la estandarización en la interpretación de las imágenes, y c) se trata de un análisis post hoc y, aunque las poblaciones de pacientes con SCC y con SCA estuvieron numéricamente equilibradas, nuestros resultados deben considerarse generadores de hipótesis; asimismo los SCA constituyen un grupo heterogéneo, en el que coexisten el IAMCEST, el IAMSEST y la angina inestable, pero es posible que estos trastornos respondan al tratamiento de manera diferente. En consecuencia, serán necesarios nuevos estudios y ensayos aleatorizados para confirmar nuestras observaciones y extraer conclusiones sólidas.
CONCLUSIONESEl BFA con sirolimus Magic Touch muestra un buen resultado por lo que respecta a los objetivos agudos y a 1 año, tanto si se usa para una ICP en el SCA como si se emplea en el SCC. Además, a pesar de que a menudo requiere tiempo, la estrategia con un BFA es viable, incluso en el contexto agudo, en el que los operadores suelen sentirse más cómodos con una intervención que requiere menos tiempo y es rápidamente resolutiva.
- -
Los datos existentes sobre el uso de balones recubiertos de fármacos en los síndromes coronarios agudos son escasos.
- -
Hasta la fecha, solo se han validado plataformas liberadoras de fármacos basadas en paclitaxel en este contexto.
- -
Por primera vez, una plataforma basada en sirolimus (el balón Magic Touch) ha mostrado unos resultados igual de buenos por lo que respecta a los objetivos agudos y a 1 año al usarla en síndromes coronarios agudos y síndromes coronarios crónicos.
- -
Las tasas de predilatación y los tiempos de hinchado fueron similares en el contexto agudo y en el contexto crónico, lo cual indica que los previsibles tiempos de intervención más largos al usar un balón farmacoactivo no impiden a los operadores aplicar esta estrategia ni siquiera en el contexto agudo.
El estudio original EASTBOURNE es un estudio independiente, impulsado por los investigadores, que recibió financiación de Envision Scientific; la sociedad no intervino en modo alguno en la definición del protocolo, la selección de los centros, la realización del estudio ni la interpretación de los resultados. El subestudio PEACE no recibió ninguna financiación.
CONSIDERACIONES ÉTICASEl estudio EASTBOURNE recibió la aprobación del comité de ética central del centro de coordinación; los datos del subestudio PEACE proceden del registro principal. Cada uno de los pacientes incluidos en el registro EASTBOURNE firmó un documento de consentimiento informado que se conserva en un archivo. La variable sexo se presenta siguiendo las directrices SAGER, y no se preveía ninguna repercusión en los resultados. Se completó el formulario STROBE.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALNo se ha utilizado inteligencia artificial en la preparación de este trabajo.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores contribuyeron por igual en la concepción y el diseño del estudio, la obtención, análisis e interpretación de los datos y la elaboración del manuscrito.
CONFLICTO DE INTERESESNo se declara ninguno.