El objetivo es evaluar la interacción entre carga de comorbilidad y beneficio de la revascularización en ancianos con síndrome coronario agudo sin elevación del ST (SCASEST).
MétodosEstudio retrospectivo que incluyó a 7.211 pacientes de edad ≥ 70 años y procedentes de 11 registros de SCASEST españoles. Se evaluaron 6 comorbilidades (diabetes mellitus, arteriopatía periférica, enfermedad cerebrovascular, enfermedad pulmonar crónica, insuficiencia renal y anemia). Se calculó una puntuación de propensión para comparar el efecto de la revascularización frente al tratamiento conservador. El objetivo fue la mortalidad a 1 año.
ResultadosAl año habían fallecido 1.090 pacientes (15%). La frecuencia de revascularización durante la hospitalización fue del 60%. La revascularización se asoció con menor mortalidad, cuya magnitud no cambió al añadir al modelo las comorbilidades (HR=0,61; IC95%, 0,53-0,69; p=0,0001). Sin embargo, los efectos de la revascularización se atenuaron en los pacientes con insuficiencia renal, arteriopatía periférica y enfermedad pulmonar crónica (para la interacción, p=0,004, p=0,007 y p=0,03 respectivamente), mientras que no se modificaron con la diabetes mellitus, la anemia o la enfermedad cerebrovascular (p=0,74, p=0,51 y p=0,28). Los beneficios de la revascularización disminuyeron gradualmente según aumentaba el número de comorbilidades (de HR=0,48; IC95%, 0,39-0,61 con 0 comorbilidades hasta HR=0,83; IC95%, 0,62-1,12 con 5 o más comorbilidades; omnibus, p=0,016). Los resultados fueron idénticos con el modelo de la puntuación de propensión o cuando se utilizó la intervención de cateterismo cardiaco como variable de exposición.
ConclusionesLa revascularización durante el ingreso mejoró independientemente de las comorbilidades la mortalidad a 1 año de una población anciana con SCASEST. No obstante, el beneficio se redujo de manera progresiva según aumentaba la carga de comorbilidades. La insuficiencia renal, la arteriopatía periférica y la enfermedad pulmonar crónica son las comorbilidades que más contrarrestaron los potenciales beneficios de la revascularización.
Palabras clave
Las guías de práctica clínica recomiendan el empleo sistemático del tratamiento invasivo y la revascularización durante la hospitalización de los pacientes con un síndrome coronario agudo sin elevación del segmento ST (SCASEST). Los pacientes ancianos con comorbilidades están infrarrepresentados en los ensayos clínicos o incluso excluidos1. No obstante, el envejecimiento de la población está llevando a un crecimiento inexorable del número de pacientes con estas características y los médicos se enfrentan a menudo con la paradoja de aplicar recomendaciones terapéuticas basadas en estudios que incluían a pacientes de cualidades distintas2.
El ensayo más grande publicado hasta el momento que se ha centrado en los pacientes de edad avanzada indicó que una estrategia invasiva es beneficiosa3. Sin embargo, este estudio se realizó en una población muy seleccionada con una carga de morbilidad baja. La prevalencia de las comorbilidades aumenta con la edad y tiene una gran repercusión en el pronóstico del SCASEST4–7. Los beneficios aportados por la revascularización tan solo pueden demostrarse mediante un ensayo clínico aleatorizado con un tamaño muestral suficiente que se haya diseñado para el estudio de los pacientes con comorbilidades; no se ha realizado ningún estudio de este tipo. No obstante, la información obtenida de registros de la práctica clínica real podría aportar algunas pistas de interés.
En el presente estudio se realiza un análisis agrupado de los datos individuales de los pacientes ancianos incluidos en 11 registros del SCASEST de España. Nuestro objetivo es evaluar la interacción entre los efectos de la revascularización en la mortalidad a 1 año y la carga de comorbilidad. Se analiza la influencia de cada comorbilidad específica, así como la de la carga total de comorbilidades.
MÉTODOSPoblación del estudioEste estudio retrospectivo incluyó datos de 11 cohortes de registros del SCASEST de España. Nuestros criterios de selección exigían que los registros obtuvieran un conjunto mínimo de características iniciales durante el ingreso hospitalario y un seguimiento de los pacientes para determinar la mortalidad por cualquier causa a 1 año. Solo se tuvo en cuenta a los pacientes de edad ≥ 70 años. Los investigadores de los registros proporcionaron los datos individuales de los pacientes para crear una base de datos agrupada de todos ellos. Se incluyó a un total de 7.211 pacientes. En la se indican los hospitales que participaron en el estudio y sus cohortes de pacientes8–17. El estudio se atuvo a lo establecido en la Declaración de Helsinki y el protocolo del estudio fue aprobado por el comité de ética de cada hospital participante. Se ha publicado con anterioridad información más detallada sobre las cohortes participantes8–17.
Se trató a los pacientes según la práctica habitual de cada hospital. Las decisiones relativas al tratamiento y la revascularización durante la hospitalización índice de cualificación para el estudio fueron a criterio del médico responsable de su tratamiento. Las variables evaluadas se enumeran en la tabla 1. Se calculó la puntuación del Global Registry of Acute Coronary Events (GRACE) para la mortalidad a 6 meses. Se registraron 6 comorbilidades identificadas como factores independientes predictivos de la mortalidad en un estudio previo5: diabetes, arteriopatía periférica, ictus previo, función renal, concentración de hemoglobina y enfermedad pulmonar crónica. La insuficiencia renal se definió como una tasa de filtrado glomerular <60 ml/min/1,73 m2 y la anemia, como una concentración de hemoglobina <11g/dl. Se eligió este valor de corte de la hemoglobina porque es el que en estudios previos ha mostrado una mayor capacidad de discriminación5,18. La carga de comorbilidad se definió como el número de comorbilidades presentes.
Características de la población de pacientes
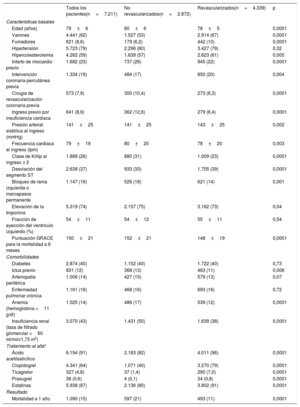
| Todos los pacientes(n=7.211) | No revascularizados(n=2.872) | Revascularizados(n=4.339) | p | |
|---|---|---|---|---|
| Características basales | ||||
| Edad (años) | 79±6 | 80±6 | 78±5 | 0,0001 |
| Varones | 4.441 (62) | 1.527 (53) | 2.914 (67) | 0,0001 |
| Fumadores | 621 (8,6) | 179 (6,2) | 442 (10) | 0,0001 |
| Hipertensión | 5.723 (79) | 2.296 (80) | 3.427 (79) | 0,32 |
| Hipercolesterolemia | 4.262 (59) | 1.639 (57) | 2.623 (61) | 0,005 |
| Infarto de miocardio previo | 1.682 (23) | 737 (26) | 945 (22) | 0,0001 |
| Intervención coronaria percutánea previa | 1.334 (19) | 484 (17) | 850 (20) | 0,004 |
| Cirugía de revascularización coronaria previa | 573 (7,9) | 300 (10,4) | 273 (6,3) | 0,0001 |
| Ingreso previo por insuficiencia cardiaca | 641 (8,9) | 362 (12,6) | 279 (6,4) | 0,0001 |
| Presión arterial sistólica al ingreso (mmHg) | 141±25 | 141±25 | 143±25 | 0,002 |
| Frecuencia cardiaca al ingreso (lpm) | 79±19 | 80±20 | 78±20 | 0,003 |
| Clase de Killip al ingreso ≥ 2 | 1.889 (26) | 880 (31) | 1.009 (23) | 0,0001 |
| Desviación del segmento ST | 2.638 (37) | 933 (33) | 1.705 (39) | 0,0001 |
| Bloqueo de rama izquierda o marcapasos permanente | 1.147 (16) | 526 (18) | 621 (14) | 0,001 |
| Elevación de la troponina | 5.319 (74) | 2.157 (75) | 3.162 (73) | 0,04 |
| Fracción de eyección del ventrículo izquierdo (%) | 54±11 | 54±12 | 55±11 | 0,54 |
| Puntuación GRACE para la mortalidad a 6 meses | 150±21 | 152±21 | 148±19 | 0,0001 |
| Comorbilidades | ||||
| Diabetes | 2.874 (40) | 1.152 (40) | 1.722 (40) | 0,73 |
| Ictus previo | 831 (12) | 368 (13) | 463 (11) | 0,006 |
| Arteriopatía periférica | 1.006 (14) | 427 (15) | 579 (13) | 0,07 |
| Enfermedad pulmonar crónica | 1.161 (16) | 468 (16) | 693 (16) | 0,72 |
| Anemia (hemoglobina <11 g/dl) | 1.025 (14) | 486 (17) | 539 (12) | 0,0001 |
| Insuficiencia renal (tasa de filtrado glomerular <60 ml/min/1,73 m2) | 3.070 (43) | 1.431 (50) | 1.639 (38) | 0,0001 |
| Tratamiento al alta* | ||||
| Ácido acetilsalicílico | 6.194 (91) | 2.183 (82) | 4.011 (96) | 0,0001 |
| Clopidogrel | 4.341 (64) | 1.071 (40) | 3.270 (79) | 0,0001 |
| Ticagrelor | 327 (4,8) | 37 (1,4) | 290 (7,0) | 0,0001 |
| Prasugrel | 38 (0,6) | 4 (0,1) | 34 (0,8) | 0,0001 |
| Estatinas | 5.938 (87) | 2.136 (80) | 3.802 (91) | 0,0001 |
| Resultado | ||||
| Mortalidad a 1 año | 1.090 (15) | 597 (21) | 493 (11) | 0,0001 |
Los valores exprersan n (%) o media ± desviación estándar.
El objetivo principal fue la mortalidad por cualquier causa a 1 año. Todos los pacientes excepto 190 (3,1%) completaron el seguimiento. La mediana de duración del seguimiento de los pacientes con alguna pérdida del seguimiento fue de 60 [intervalo intercuartílico, 7-226] días. La información relativa a la mortalidad se obtuvo de los registros hospitalarios o del registro de mortalidad regional.
Análisis estadísticoLas variables continuas se expresan en forma de media±desviación estándar y las cualitativas, mediante valores absolutos (porcentajes). Para la comparación de las características basales al ingreso en función de que se hubiera efectuado o no una revascularización, se utilizó la prueba de la t de Student para muestras independientes o la prueba de la χ2 según procediera.
En primer lugar, se determinó un modelo de base para la mortalidad mediante un análisis de regresión de Cox. Se estratificó a los pacientes según el centro hospitalario para que cada centro pudiera tener su propio valor de riesgo. Las estimaciones del riesgo se expresaron mediante los valores de hazard ratio (HR) con sus intervalos de confianza del 95% (IC95%). Para la elección del mejor modelo de base, se aplicó un método de eliminación retrógrada, en el que el modelo inicial (o saturado) incluía las características indicadas en la tabla 1, excepto por las 6 comorbilidades antes mencionadas. Este método incluía una eliminación retrógrada al tiempo que se evaluaba simultáneamente cada variable continua para determinar si se apartaba de la linealidad. En caso necesario, se transformaron las variables con los polinomios fraccionales apropiados. Se evaluó el cumplimiento de los supuestos de proporcionalidad para la función de riesgo instantáneo a lo largo del tiempo con los residuos de Schoenfeld. La capacidad de discriminación del modelo multivariante se evaluó con el estadístico C de Harrell. El modelo de base multivariante para la mortalidad incluyó: edad (años), sexo, antecedentes de infarto agudo de miocardio, antecedentes de ingreso hospitalario por insuficiencia cardiaca, frecuencia cardiaca al ingreso (lpm), presión arterial sistólica (mmHg), clase de Killip ≥ II, desviación del segmento ST, elevación de la troponina y fracción de eyección del ventrículo izquierdo. Tomando este modelo de base, se evaluó si las 6 comorbilidades tenían capacidad predictiva de mortalidad (como efecto principal) y si su inclusión modificaba el efecto de la revascularización. Dentro del modelo de Cox, los efectos de las comorbilidades se basaron en: a) un valor de p ómnibus significativo de la interacción con la revascularización, y b) el valor pronóstico añadido por una diferencia (Δ) significativa del estadístico C entre el modelo completo (que incluía la interacción) y el modelo base.
En segundo lugar, para aumentar la robustez del análisis, se determinó si las diferencias en las tasas de mortalidad corroboraban los resultados expresados en forma de HR. En consecuencia, empleando una interacción aditiva, se exploraron las diferencias en las tasas de mortalidad (expresadas como número de eventos/año-persona) a lo largo de todo el espectro de número de comorbilidades. Se llevó a cabo un análisis de la tasa de incidencia mediante una regresión de Poisson, con la inclusión del tiempo de seguimiento como un factor de compensación, y se ajustó el modelo respecto al efecto de agrupación de los centros. Estas estimaciones de medidas absolutas complementan las medidas relativas que proporcionan los valores de HR de los modelos de Cox. Dado que se debe indicar una coronariografía invasiva antes de la revascularización, también se realizó un análisis de sensibilidad utilizando el abordaje invasivo como variable de exposición, en vez de la revascularización.
Además, se utilizó un modelo de regresión logit para calcular la puntuación de propensión a la revascularización al ingreso como análisis complementario. A continuación, la puntuación de propensión se estratificó en un número óptimo de cuantiles (16 en este caso), en el que óptimo significa que no se observan diferencias significativas entre los grupos de tratamiento en ninguno de los cuantiles de la puntuación de propensión. Para emplear los datos generados por los estratos en cualquier análisis posterior, se calculó la ponderación por el inverso de la probabilidad de recibir el tratamiento. Las variables incluidas en la creación de la puntuación de propensión se indican en la .
Los valores no disponibles se atribuyeron a 5 imputaciones mediante atribución múltiple, con el método de ecuaciones encadenadas. Se calcularon también las estimaciones de los modelos mediante un conjunto de datos sin imputaciones ().
Para los análisis principales se utilizó el programa Stata Statistical Software, versión 15 (2017) (StataCorp LP, Estados Unidos). La atribución múltiple se realizó con el paquete ICE en el programa Stata.
RESULTADOSCaracterísticas basalesLas características de los pacientes se muestran en la tabla 1. La media de edad fue de 79±6 años y el 62% de los pacientes eran varones. La media de la puntuación GRACE para la mortalidad a 6 meses fue de 150±28 puntos. El cumplimiento del tratamiento recomendado en las guías fue, por lo general, alto (tabla 1). Se realizó una coronariografía invasiva durante el ingreso hospitalario a 6.032 pacientes (84%). Un total de 434 (7,2%) presentaban afección del tronco coronario izquierdo y 1.990 (33%), enfermedad de 3 vasos. Se revascularizó a 4.339 pacientes (el 60% del total) mediante intervención coronaria percutánea (n=3.848; 53%) o cirugía coronaria (n=491; 7%).
En la tabla 1 se muestran las diferencias basales entre los pacientes revascularizados y los no revascularizados. La puntuación GRACE de los pacientes no revascularizados fue ligeramente superior (152±21 frente a 148±21; p=0,0001). Las frecuencias de ictus previos, anemia e insuficiencia renal fueron mayores en el subgrupo sin revascularización, mientras que no hubo diferencias en diabetes, arteriopatía periférica o enfermedad pulmonar crónica.
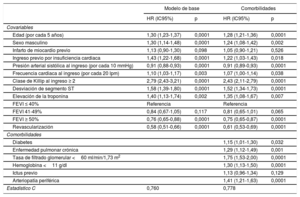
Repercusión pronóstica de las comorbilidades y la revascularizaciónEn total, 1.090 pacientes (15%) habían fallecido al cabo de 1 año. Se observaron diferencias entre los centros por lo que respecta a la revascularización realizada en el hospital (p=0,001; inervalo, 45-71%) y la mortalidad a 1 año (p=0,001; intervalo, 11-19%). En consecuencia, atenuamos el potencial de sesgo mediante una estratificación de todos los análisis de regresión de Cox según el centro hospitalario. En la tabla 2 se presentan los cálculos derivados de los modelos de regresión de Cox. Excepto por el ictus previo, que mostró una tendencia no significativa, cada comorbilidad se asociaba significativamente con la mortalidad. La Δ del estadístico C entre el modelo con las 6 comorbilidades y el modelo base fue de 0,0187 (IC95%, 0,0120-0,0254; Δ significativa con p <0,05). La exactitud discriminatoria de la puntuación GRACE (estadístico C=0,734) fue inferior a la del modelo base (estadístico C=0,760; p <0,05).
Modelos predictivos de la mortalidad a 1 año sin comorbilidades (modelo base) y con comorbilidades (modelo completo)
| Modelo de base | Comorbilidades | |||
|---|---|---|---|---|
| HR (IC95%) | p | HR (IC95%) | p | |
| Covariables | ||||
| Edad (por cada 5 años) | 1,30 (1,23-1,37) | 0,0001 | 1,28 (1,21-1,36) | 0,0001 |
| Sexo masculino | 1,30 (1,14-1,48) | 0,0001 | 1,24 (1,08-1,42) | 0,002 |
| Infarto de miocardio previo | 1,13 (0,90-1,30) | 0,098 | 1,05 (0,90-1,21) | 0,526 |
| Ingreso previo por insuficiencia cardiaca | 1,43 (1,22-1,68) | 0,0001 | 1,22 (1,03-1,43) | 0,018 |
| Presión arterial sistólica al ingreso (por cada 10 mmHg) | 0,91 (0,88-0,93) | 0,0001 | 0,91 (0,89-0,93) | 0,0001 |
| Frecuencia cardiaca al ingreso (por cada 20 lpm) | 1,10 (1,03-1,17) | 0,003 | 1,07 (1,00-1,14) | 0,038 |
| Clase de Killip al ingreso ≥ 2 | 2,79 (2,43-3,21) | 0,0001 | 2,43 (2,11-2,79) | 0,0001 |
| Desviación de segmento ST | 1,58 (1,39-1,80) | 0,0001 | 1,52 (1,34-1,73) | 0,0001 |
| Elevación de la troponina | 1,40 (1,13-1,74) | 0,002 | 1,35 (1,08-1,67) | 0,007 |
| FEVI ≤ 40% | Referencia | Referencia | ||
| FEVI 41-49% | 0,84 (0,67-1,05) | 0,117 | 0,81 (0,65-1,01) | 0,065 |
| FEVI ≥ 50% | 0,76 (0,65-0,88) | 0,0001 | 0,75 (0,65-0,87) | 0,0001 |
| Revascularización | 0,58 (0,51-0,66) | 0,0001 | 0,61 (0,53-0,69) | 0,0001 |
| Comorbilidades | ||||
| Diabetes | 1,15 (1,01-1,30) | 0,032 | ||
| Enfermedad pulmonar crónica | 1,29 (1,12-1,49) | 0,001 | ||
| Tasa de filtrado glomerular <60 ml/min/1,73 m2 | 1,75 (1,53-2,00) | 0,0001 | ||
| Hemoglobina <11 g/dl | 1,30 (1,13-1,50) | 0,0001 | ||
| Ictus previo | 1,13 (0,96-1,34) | 0,129 | ||
| Arteriopatía periférica | 1,41 (1,21-1,63) | 0,0001 | ||
| Estadístico C | 0,760 | 0,778 | ||
FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%.
La mortalidad total fue mayor entre los pacientes no revascularizados que entre los revascularizados (n=597 frente a n=493; el 21 frente al 11%; p=0,0001). Tal como se muestra en la tabla 2, la revascularización obtuvo una asociación significativa con menos mortalidad; la magnitud de la asociación no se modificó con la adición de las comorbilidades al modelo (HR=0,61; IC95%, 0,53-0,69; p=0,0001).
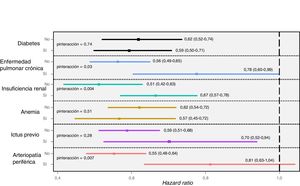
Interacción entre los efectos de la revascularización y cada una de las comorbilidadesLos efectos de la revascularización fueron diferentes en función de cada comorbilidad específica (figura 1). De hecho, la asociación entre la revascularización y la mortalidad tuvo una significación solo limítrofe en los pacientes con arteriopatía periférica o enfermedad pulmonar crónica (pinteracción=0,007 y pinteracción=0,03). Por otro lado, aunque el efecto de la revascularización fue significativo en los pacientes con y sin insuficiencia renal, su magnitud fue mayor en aquellos con una función renal normal (pinteracción=0,004). En cambio, el beneficio aportado por la revascularización no se modificó por la presencia de diabetes, anemia o un ictus previo.
Mortalidad por cualquier causa. Efectos de la revascularización en función de la comorbilidad. Los valores se expresan en forma de hazard ratio e intervalo de confianza del 95%. N=7.211. En todos los modelos se introdujo un ajuste por edad, sexo, infarto de miocardio previo, ingreso hospitalario previo por insuficiencia cardiaca, presión arterial sistólica al ingreso, frecuencia cardiaca, clase de Killip, desviación de segmento ST, elevación de la troponina y fracción de eyección del ventrículo izquierdo.
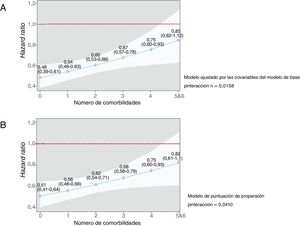
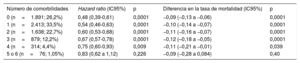
La distribución de los pacientes según el número de comorbilidades fue la siguiente: 0 (n=1.891; 26,2%), 1 (n=2.413; 33,5%), 2 (n=1.638; 22,7%), 3 (n=879; 12,2%), 4 (n=314; 4,4%), 5 (n=71; 1,0%) y 6 (n=5; 0,1%). Para el resto de los análisis, se agruparon los subgrupos 5 y 6 en un único subgrupo (n=76; 1,1%). El número de comorbilidades se asoció con la mortalidad (por cada comorbilidad, HR = 1,34; IC95%, 1,27-1,41; p=0,0001). Las estimaciones obtenidas en los modelos fueron similares al emplear el conjunto de datos sin imputaciones (). Hubo una interacción significativa entre los efectos de la revascularización y el número de comorbilidades en las escalas multiplicativas y aditivas. En la figura 2A y la tabla 3 se muestra el efecto de la revascularización en todo el espectro de la carga de comorbilidad en el análisis multiplicativo (pómnibus=0,016). La asociación entre la revascularización y la mortalidad disminuía progresivamente en función del número de comorbilidades: de HR = 0,48 (IC95%, 0,39-0,61) con 0 comorbilidades a HR=0,83 (IC95%, 0,62-1,12) con 5 o más. Los resultados fueron similares al utilizar un modelo de puntuación de propensión (figura 2B). En el análisis aditivo (pómnibus=0,007) y por lo que respecta al riesgo absoluto, las diferencias en la tasa de mortalidad a 1 año entre los pacientes revascularizados y los no revascularizados fueron significativamente favorables a la revascularización en todos los niveles de comorbilidad, excepto en el subgrupo con una carga de comorbilidad muy elevada (5 o más comorbilidades) (tabla 3). Lo mismo ocurrió en el análisis del conjunto de datos sin imputación ().
Efectos de la revascularización en la mortalidad por cualquier causa en función del número de comorbilidades. La línea continua azul indica la hazard ratio, mientras que la sombra blanca corresponde al intervalo de confianza del 95%. Los valores se expresan en forma de hazard ratio e intervalo de confianza del 95%. A: se introdujo en el modelo un ajuste por edad, sexo, infarto de miocardio previo, ingreso hospitalario previo por insuficiencia cardiaca, presión arterial sistólica al ingreso, frecuencia cardiaca, clase de Killip, desviación de segmento ST, elevación de la troponina y fracción de eyección del ventrículo izquierdo. B: modelo de puntuación de propensión. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Efectos de la revascularización en la mortalidad a 1 año según el número de comorbilidades
| Número de comorbilidades | Hazard ratio (IC95%) | p | Diferencia en la tasa de mortalidad (IC95%) | p |
|---|---|---|---|---|
| 0 (n=1.891; 26,2%) | 0,48 (0,39-0,61) | 0,0001 | −0,09 (−0,13 a −0,06) | 0,0001 |
| 1 (n=2.413; 33,5%) | 0,54 (0,46-0,63) | 0,0001 | −0,10 (−0,14 a −0,07) | 0,0001 |
| 2 (n=1.638; 22,7%) | 0,60 (0,53-0,68) | 0,0001 | −0,11 (−0,16 a −0,07) | 0,0001 |
| 3 (n=879; 12,2%) | 0,67 (0,57-0,78) | 0,0001 | −0,12 (–0,18 a −0,05) | 0,0001 |
| 4 (n=314; 4,4%) | 0,75 (0,60-0,93) | 0,009 | −0,11 (−0,21 a −0,01) | 0,039 |
| 5 o 6 (n=76; 1,05%) | 0,83 (0,62 a 1,12) | 0,226 | −0,09 (−0,28 a 0,084) | 0,40 |
IC95%: intervalo de confianza del 95%.
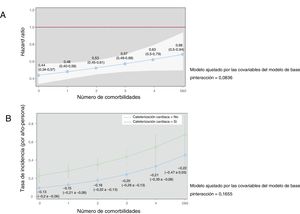
En el análisis de sensibilidad para el que se utilizó el abordaje invasivo como variable de exposición, los resultados fueron muy similares (figura 3). La asociación entre la realización de un cateterismo cardiaco y la mortalidad se redujo de HR=0,44 (IC95%, 0,34-0,57) con 0 comorbilidades a HR=0,68 (IC95%, 0,50-0,90) con 5 o más comorbilidades.
Efectos del tratamiento invasivo en la mortalidad por cualquier causa en función del número de comorbilidades. Se introdujo en los modelos un ajuste por edad, sexo, infarto de miocardio previo, ingreso hospitalario previo por insuficiencia cardiaca, presión arterial sistólica al ingreso, frecuencia cardiaca, clase de Killip, desviación de segmento ST, elevación de la troponina y fracción de eyección del ventrículo izquierdo. A: la línea continua azul indica la hazard ratio, mientras que la sombra blanca corresponde al intervalo de confianza del 95%. B: diferencia en las tasas de mortalidad (número de muertes/año-persona e intervalo de confianza del 95%) en función de que se aplicara a los pacientes un tratamiento invasivo o no.
Los principales resultados del presente estudio en pacientes ancianos hospitalizados por un SCASEST fueron: a) las comorbilidades ejercieron una potente influencia en la mortalidad a 1 año; b) la revascularización durante la hospitalización mejoró la mortalidad a 1 año con un efecto independiente de las comorbilidades; sin embargo, el beneficio aportado por la revascularización se redujo progresivamente a medida que aumentaba la carga de comorbilidades, y c) la insuficiencia renal, la arteriopatía periférica y la enfermedad pulmonar crónica fueron las comorbilidades con un mayor efecto negativo en el posible beneficio aportado por la revascularización durante la hospitalización.
Comorbilidades en pacientes ancianos con un SCASESTLas comorbilidades tienen una prevalencia elevada en los pacientes ancianos con un SCASEST y presagian una peor evolución clínica. El índice de comorbilidad de Charlson, que incluye 19 elementos, es la medida más comúnmente utilizada para la evaluación de las comorbilidades, si bien las 6 comorbilidades que mejor captan la influencia pronóstica en los pacientes hospitalizados por síndromes coronarios agudos son la insuficiencia renal, la anemia, la enfermedad pulmonar crónica, la arteriopatía periférica, la enfermedad cerebrovascular y la diabetes5,19. Varios estudios han demostrado el valor pronóstico de cada una de estas comorbilidades por separado en el síndrome coronario agudo18,20–23. La arteriopatía periférica, la enfermedad cerebrovascular y el SCASEST son trastornos cardiovasculares concordantes que reflejan una extensión sistémica amplia de la enfermedad ateroesclerótica. Asimismo la insuficiencia renal crónica y la diabetes están directamente involucradas en la aceleración del proceso ateroesclerótico. La anemia y la enfermedad pulmonar crónica son trastornos discordantes que requieren una asistencia multidisciplinaria integrada que no siempre puede coordinarse adecuadamente. En nuestro estudio, la arteriopatía periférica, la enfermedad pulmonar crónica y la insuficiencia renal fueron las comorbilidades con efectos más negativos en el beneficio aportado por la revascularización. Además, se observó un efecto aditivo de las comorbilidades: cuanto mayor es su número, peor el resultado.
Revascularización de pacientes ancianos con SCASEST y comorbilidadesDe entre las recomendaciones establecidas en la guía para el SCASEST, la revascularización coronaria durante la hospitalización es la que proporciona el mayor beneficio pronóstico, en especial a los pacientes en alto riesgo16,24. De hecho, en un reciente registro se ha observado una asociación inversa significativa entre la revascularización coronaria durante la hospitalización y la mortalidad a 2 años24. Una cuestión clave es si una gran carga de comorbilidad impide que los pacientes ancianos obtengan el beneficio proporcionado por la revascularización. El ensayo After-Eighty respaldó el empleo sistemático de una estrategia invasiva para los pacientes de edad> 80 años con un SCASEST3. Un metanálisis que incluyó a un subgrupo de pacientes de más de 75 años de ensayos clínicos aleatorizados obtuvo también resultados favorables al tratamiento invasivo25. Sin embargo, los pacientes con comorbilidades están infrarrepresentados en los ensayos clínicos aleatorizados. Un amplio registro de intervención coronaria percutánea ha puesto de manifiesto que las comorbilidades se asocian con una tasa de mortalidad hospitalaria más alta26. En consecuencia, continúa la controversia respecto a cuál es la mejor opción de tratamiento para los pacientes ancianos con SCASEST en estado grave27. En un ensayo de pequeño tamaño en el que se incluyó a pacientes ancianos con comorbilidades, el tratamiento invasivo sistemático se asoció con una tendencia no significativa a un mejor resultado28.
Nuestro análisis incluye a un gran número de pacientes de edad avanzada con SCASEST e indica la existencia de asociación entre la revascularización durante la hospitalización y una menor mortalidad a 1 año, así como la atenuación de esta asociación con el aumento de la carga de comorbilidad. La indicación de una coronariografía diagnóstica es un paso previo a la revascularización, lo que podría significar una causa de sesgo en la interpretación del pronóstico en los pacientes no revascularizados29. Después de la angiografía coronaria, algunos pacientes podrían no haber sido revascularizados debido a una anatomía muy compleja o un riesgo excesivo. Este hecho podría empeorar de por sí el pronóstico del grupo sin revascularización. Sin embargo, el análisis de sensibilidad realizado tomando como grupo de comparación a los pacientes a los que no se realizó una coronariografía diagnóstica, en vez de a los pacientes no revascularizados, mostró también una asociación entre el tratamiento invasivo y una menor mortalidad a 1 año, que se reducía al aumentar la carga de comorbilidad.
LimitacionesEn primer lugar, la limitación más importante de este estudio es que no se evaluaron la fragilidad ni la sarcopenia o las concentraciones de albúmina. La fragilidad y las comorbilidades tienen valores pronósticos complementarios y adicionales tras un síndrome coronario agudo30. Aunque nuestro estudio analizó solo la presencia de comorbilidades, y no el espectro completo de los trastornos geriátricos, la demostración de que, cuanto mayor es la carga de comorbilidad, menor es el beneficio aportado por la revascularización en cuanto a la mortalidad a 1 año podría aportar una información útil para la toma de decisiones sobre los pacientes ancianos hospitalizados por un SCASEST. En futuros estudios podrá esclarecerse el papel de la revascularización de los pacientes con fragilidad hospitalizados por un SCASEST31. En segundo lugar, el estudio tuvo los sesgos de selección inherentes a todos los registros observacionales. Hay diferencias basales entre los pacientes revascularizados y los no revascularizados, y se realizaron más intervenciones de revascularización a pacientes en menor riesgo. Para contrarrestar este sesgo, se llevaron a cabo un análisis estadístico exhaustivo y un ajuste completo de los modelos predictivos. En tercer lugar, hubo cierta heterogeneidad entre los diversos registros incluidos por lo que respecta a las características de los pacientes y del tratamiento, la definición de las variables y la calidad del seguimiento. Aunque se atenuó el potencial de sesgo mediante una estratificación de todos los análisis según el centro hospitalario, esta posible causa de sesgo limita la validez externa de los resultados. En cuarto lugar, es posible que algunas características no recogidas en la base de datos pudieran desempeñar un papel en el peor pronóstico observado en los pacientes no revascularizados.
CONCLUSIONESNuestras observaciones indican que no se debe descartar la revascularización para la mayoría de los pacientes ancianos con comorbilidades que presentan un SCASEST. Sin embargo, la carga de comorbilidad podría contrarrestar los posibles beneficios aportados por la revascularización. Por consiguiente, la decisión debe meditarse cuidadosamente ante un paciente con gran carga de morbilidad. La arteriopatía periférica, la enfermedad pulmonar crónica y la insuficiencia renal fueron las comorbilidades con las que se observó una mayor interferencia en los efectos de la revascularización.
FINANCIACIÓNEste trabajo fue financiado por subvenciones del Ministerio de Economía y Competitividad de España a través del Instituto de Salud Carlos III: CIBER-CV 16/11/00420, Madrid, España.
CONFLICTO DE INTERESESJ. Núñez ha recibido pagos personales de Novartis, Vitor Pharma y Boehringer Ingelheim y apoyo de subvenciones de Astra Zeneca y Vitor Pharma. J.A. Barrabés ha recibido pagos por actividades de formación de AstraZeneca y por consultoría de Bayer. E. Abu-Assi es editor asociado de Revista Española de Cardiología; se ha seguido el procedimiento editorial establecido en la Revista para garantizar la gestión imparcial del manuscrito. Los demás autores no tienen nada que declarar.
- –
Las guías de práctica clínica, que se basan en ensayos clínicos, recomiendan el empleo sistemático del tratamiento invasivo y la revascularización durante la hospitalización de los pacientes con un síndrome coronario agudo sin elevación del segmento ST (SCASEST).
- –
Los pacientes ancianos con comorbilidades están infrarrepresentados o excluidos en los ensayos clínicos sobre SCASEST.
- –
Sigue habiendo controversia respecto al tratamiento óptimo de los pacientes ancianos con SCASEST y comorbilidades.
- –
La carga de comorbilidad podría contrarrestar los posibles beneficios aportados por la revascularización.
- –
Hay una progresiva relación inversa entre los beneficios aportados por la revascularización y la carga de comorbilidad que tienen los pacientes.
- –
La insuficiencia renal, la arteriopatía periférica y la enfermedad pulmonar crónica son las comorbilidades que tienen una mayor influencia negativa en el efecto protector de la revascularización en los pacientes ancianos con un SCASEST.
- –
No debe descartarse la revascularización para la mayoría de los pacientes ancianos con comorbilidades que sufren un SCASEST. Sin embargo, la decisión debe meditarse cuidadosamente ante un paciente con gran carga de morbilidad.