Palabras clave
INTRODUCCION
Se denomina revascularización transmiocárdica por láser (TMLR) a la técnica cardioquirúrgica consistente en realizar perforaciones en el miocardio mediante radiación láser, empleada en pacientes con cardiopatía isquémica crónica, con el objeto de reducir la isquemia y la angina.
Esta técnica deriva del perfeccionamiento de otra más antigua consistente en realizar micropunciones del miocardio con instrumentos semejantes a los empleados en acupuntura. En dicha técnica, tras crear una vía de acceso al pericardio, el cirujano realizaba manualmente perforaciones en el miocardio por medio de una aguja que introducía desde la superficie exterior del corazón hasta la cavidad ventricular, atravesando epicardio, miocardio y endocardio. El resultado esperado era que los agujeros atravesaran en su recorrido la microvasculatura presente en todo el espesor del miocardio, de forma que la sangre progresara desde el ventrículo hacia el canal creado, y de allí a la red vascular a la que está unido, perfundiendo el miocardio.
El procedimiento original, de discutible eficacia, perdió adeptos porque los canales no permanecían permeables mucho tiempo. Al igual que cualquier lesión inducida en un tejido orgánico, la respuesta era la cicatrización y oclusión del orificio en poco tiempo, aunque se ha observado proceso de neoangiogénesis similar al de TMLR1. Se atribuyó esta evolución a que, aunque las agujas son macroscópicamente afiladas, no lo son microscópicamente, y parte del tejido es dañado durante el avance de la aguja. Por otro lado, la aguja no extrae un cilindro de tejido del miocardio, sino que, al igual que un clavo que atraviesa una superficie de caucho, en su avance comprime el tejido que atraviesa hacia el exterior, por lo que cuando se retira la aguja, éste se expande reduciendo el calibre del orificio, llegando incluso a ocluirlo.
Basándose en que la falta de éxito del procedimiento se debía a la naturaleza del mecanismo perforador, en la década de los noventa se diseñó y perfeccionó la técnica alternativa empleada en la actualidad, consistente en crear canales permeables mediante la eliminación limpia de cilindros miocárdicos. El método empleado para crear los canales fue la vaporización del tejido por medio de radiación láser.
El láser consigue la eliminación de un cilindro de tejido con poco daño del tejido circundante por la acción de un haz coherente de alta energía. El método teórico es sencillo: se genera un haz láser en una longitud de onda que tenga un índice de absorción elevado por el tejido a vaporizar, y se dirige altamente colimado a la zona objetivo.
Los láseres de uso clínico comercializados en la actualidad emplean transmisión directa de un haz de muy alta energía (láser de carbono), o la transmisión a través de fibra óptica de un haz de menor potencia, utilizando la fibra como soporte para crear el orificio (láser de Holmio:YAG).
También en el caso de orificios creados con láser los estudios anatomopatológicos han demostrado que los canales creados se ocluyen en pocos meses2. A pesar de ello, varios estudios de efectividad han demostrado la reducción de síntomas a medio plazo, aunque existe controversia respecto a la capacidad del TMLR para aumentar el flujo sanguíneo al miocardio3-6. Estos resultados han conducido a establecer hipótesis alternativas que expliquen su funcionamiento, como la dudosa destrucción de la red neuronal del miocardio7-9 o la inducción de factores de neoangiogénesis10-16.
Bases de trabajo
La comunidad científica acepta que el TMLR es un procedimiento de eficacia inferior al pontaje aortocoronario, por lo que su uso se reserva a pacientes con enfermedad coronaria en los que se excluye la posibilidad de tratamiento revascularizador convencional, entendiendo como tal la realización de pontajes o angioplastia17. Por esta razón, la mayor parte de los estudios de eficacia de TMLR se han realizado analizando sus resultados como técnica aislada18,19, y comparándolos con el de pacientes con angina refractaria sometidos únicamente a tratamiento farmacológico20-26. Como resultado, la FDA autoriza su uso como alternativa al tratamiento médico convencional en pacientes que no pueden ser sometidos a revascularización coronaria.
Sin embargo, si las hipótesis que soportan el uso de la TMLR son correctas, la acción del procedimiento debería tener efecto local27. Dicho de otro modo, demostrada la eficacia del procedimiento en el miocardio sin vasos pontables, podría aceptarse el beneficio local del TMLR en pacientes sometidos a pontaje aortocoronario en los que existan áreas no pontables que puedan ser causa de angina28. La vía de acceso para realizar el TMLR es la misma que la empleada para pontaje, por lo que restada la morbilidad que causa el acceso quirúrgico, que es el principal inconveniente del uso aislado de TMLR, los posibles perjuicios de la técnica son los debidos a la realización de perforaciones en el miocardio isquémico. Sin embargo, hay pocos estudios de eficacia y mortalidad a medio plazo29-32.
Por desgracia, es frecuente que durante una intervención de revascularización incompleta el cirujano observe la existencia de zonas amplias de miocardio no conectadas con las zonas pontadas, en la que no existen vasos epicárdicos de calibre suficiente para cirugía convencional ni para angioplastia. Se admite que estas zonas pueden ser responsables en varios casos de la persistencia de síntomas de angina en pacientes sometidos a revascularización coronaria incompleta, en los que podría ser de utilidad el uso de TMLR.
Además del uso convencional del TMLR como terapia aislada, varios grupos entre los que se encuentra nuestro centro han empleado la combinación de TMLR y cirugía convencional. En esta técnica, un procedimiento convencional de pontaje aortocoronario se complementa con TMLR en las zonas en las que no es posible realizar puentes debido a la inexistencia de vasos adecuados.
El objetivo del estudio es analizar la seguridad y resultados del procedimiento combinado de cirugía más TMLR en el primer año tras su implantación.
PACIENTES Y MÉTODO
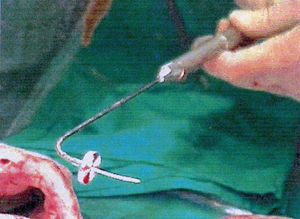
En nuestro servicio disponemos de un sistema de TMLR (Eclipse® Modelo TMR 2000, Surgical Technologies Inc.) basado en láser Holmio:YAG transmitido por fibra óptica (fig. 1). El uso del dispositivo se factura por procedimiento, por lo que no existe conflicto de intereses de los autores en el mantenimiento o abandono de la técnica. Los resultados obtenidos con nuestros pacientes durante el primer año de uso han sido sometidos a estudio.
Fig. 1. Aplicador de TMLR tipo Holmio:YAG con aplicador de fibra óptica.
Se trata de un estudio observacional de cohortes longitudinal retrospectivo, sin asignación aleatoria de casos. A pesar de ello, por el interés de los hallazgos, reproducimos nuestros resultados.
Durante el período comprendido entre el 4 de mayo de 1999 y el 25 de mayo del 2000, un total de 20 pacientes fueron sometidos a procedimiento combinado de revascularización por láser unido a revascularización por pontaje aortocoronario, y uno a revascularización por láser aislado. Como grupo control se recogió información completa de 118 pacientes intervenidos de revascularización coronaria aislada durante el mismo período. Para analizar las diferencias de tratamiento postoperatorio se obtuvo un subgrupo control constituido por los 66 pacientes del grupo control diagnosticados de angina inestable. A todos los pacientes se les hizo entrega de un consentimiento informado en el que se les comunicó su enfermedad, el procedimiento previsto y el riesgo quirúrgico, así como de la posibilidad de modificar el tipo de procedimiento en función de los hallazgos quirúrgicos.
El criterio de inclusión de pacientes no fue preestablecido por protocolo: cada cirujano decidió en cada caso según sus apreciaciones personales y su experiencia si el paciente era tributario de TMLR, en qué zona debía aplicarse, cuántos orificios se practicaban y la distribución de los mismos.
Utilizando historiales informatizados y la historia clínica convencional se traspasó la información demográfica y clínica relevante a una base de datos creada para este estudio. Los datos incluidos en la base de datos TMLR están recogidos en la tabla 1.
Definimos tres regiones de aplicación de láser en el miocardio: anterior (correspondiente a zonas irrigadas por la descendente anterior y diagonales), lateral (margen obtuso y zonas irrigadas por bisectriz y primera marginal) y posterior (irrigada por segundas y terceras marginales o por tronco posterolateral). Se registraron el número total de disparos en cada zona, la potencia y el número de orificios.
Como variables dependientes se analizaron la mortalidad y el grado funcional. Para el estudio de la mortalidad se recurrió al archivo de contabilidad del centro, en el que se registra de forma sistemática la situación del paciente al alta, de forma que no se producen pérdidas de seguimiento, aún en el caso de que el paciente fuese transferido eventualmente a otra unidad y el fallecimiento se produjese en ésta. Para el análisis de medicación antianginosa al alta se recopiló la información del informe de alta de los 66 pacientes con angina inestable del grupo control, y de los pacientes sometidos a TMLR. Para el análisis del grado funcional se recurrió a una encuesta telefónica al total de 18 pacientes con supervivencia hospitalaria, realizado entre el 19 y el 22 de junio de 2000. La encuesta fue realizada mediante un cuestionario telefónico estándar de preguntas dirigidas a conocer la máxima capacidad del paciente para realizar esfuerzos y la detección de disnea o angina. No hubo pérdidas de seguimiento.
Los datos recogidos fueron analizados con el programa estadístico SPSS® vesión 8.0 (SPSS Inc, Chicago, Illinois, EE.UU.). Los resultados fueron analizados mediante el test de la χ2 para variables cualitativas y de la t de Student de datos independientes para variables numéricas.
Técnica quirúrgica
La realización de TMLR no se realizó por intención de tratar. Todos los pacientes fueron aceptados para cirugía sobre la base de existencia de vasos epicárdicos susceptibles de revascularización. El procedimiento se realizó por técnica habitual, mediante esternotomía media y circulación extracorpórea por bomba centrífuga. Se emplearon injertos arteriales (AMI) en los pacientes que a criterio del cirujano reunían condiciones de edad y acceso adecuado.
En los pacientes en los que el calibre de los vasos epicárdicos no permitía el pontaje de áreas consideradas importantes se complementó el procedimiento mediante TMLR, realizada tras los pontajes y antes de finalizar la circulación extracorpórea, o bien preferiblemente tras finalizar ésta y revertir con protamina la heparinización precisa para el procedimiento.
La técnica es sencilla y en condiciones normales no alarga la intervención más de 10 min. No se produjo ninguna complicación hemorrágica como consecuencia de TMLR.
RESULTADOS
De los 21 pacientes sometidos a TMLR, en uno el procedimiento fue realizado de forma aislada, y en 20 de forma combinada. De ellos, en un caso se empleó conjuntamente con una sustitución valvular y en otro caso sustitución valvular y revascularización coronaria. En los 18 restantes (85%) se combinó con cirugía coronaria.
Se produjeron 3 fallecimientos, uno en el paciente sometido a láser aislado, otro en el paciente sometido además a cirugía combinada coronaria y valvular, y el último en un paciente sometido a TMLR y cirugía coronaria. Los 3 fallecimientos fueron mortalidad hospitalaria, no registrándose ninguna nueva muerte en el año de seguimiento.
Los pacientes sometidos a TMLR aislado o combinado con cirugía valvular no se compararon con grupo control por tratarse de casos aislados. Los resultados de los pacientes a los que se realizó pontaje coronario y TMLR (n = 18) se compararon con los de 118 pacientes sometidos a revascularización coronaria en el mismo período de tiempo. No hubo diferencias significativas en la edad, sexo, fracción de eyección, estimación de riesgo por método de Parsonnet o EuroSCORE, y mortalidad total. Los pacientes sometidos a procedimiento combinado presentaron preoperatoriamente una incidencia significativamente mayor de angina inestable (tabla 2).
Todos los pacientes supervivientes recibieron pontajes en la cara anterior del corazón, y el 17% recibieron dos pontajes en esa área. El 78% recibieron al menos un pontaje en la cara lateral, mientras que sólo uno de cada tres recibió un pontaje en la cara posterior.
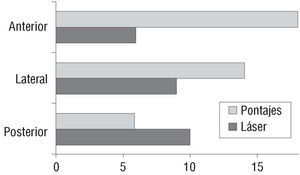
En cuanto a la aplicación de TMLR, casi la mitad de los pacientes recibieron perforaciones en la cara lateral (44%), un 56% en la cara posterior, mientras que la cara anterior fue la menos perforada, ya que sólo uno de cada 3 pacientes recibió disparos en esta zona (fig. 2).
Fig. 2. Distribución de pontajes y TMLR por regiones de miocardio.
El número medio de impulsos emitidos por paciente fue de 308. Se empleó una potencia de 6-7 vatios, y el número medio de orificios fue de 36, distribuidos de la siguiente manera (media ± desviación estándar):
- Cara anterior: 16 ± 9
- Cara lateral: 22 ± 7
- Cara inferior: 18 ± 10
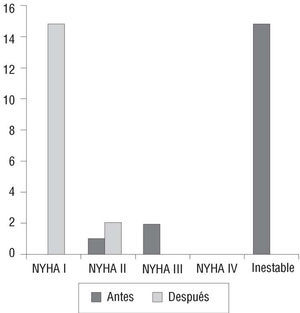
En cuanto al grado funcional, en el momento del ingreso 15 (80%) de los pacientes supervivientes presentaban angina de reposo de reciente aparición, y 2 pacientes más presentaban angina de moderados esfuerzos. Tras el procedimiento, 2 pacientes permanecían en grado funcional II y el resto en grado funcional I (fig. 3).
Fig. 3. Evolución de angina antes y después del tratamiento en pacientes sometidos a procedimiento combinado.
No hubo diferencias significativas de tratamiento antianginoso en los pacientes tratados con TMLR respecto a los que sólo recibieron cirugía convencional de pontaje aortocoronario, aunque los tratados con láser recibieron menos nitritos, bloqueadores beta y antagonistas del calcio. Del resto del tratamiento, sólo es significativo un porcentaje superior de tratamiento antidiabético oral en el grupo de los tratados con láser (tabla 3).
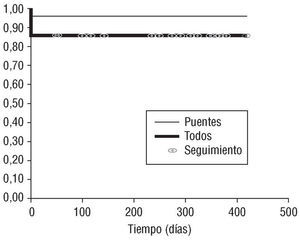
Como indica la figura 4, la supervivencia al año de los pacientes con cirugía coronaria y TMLR fue de 95%, y la supervivencia global de todos los pacientes a los que se realizó TMLR fue de 85%.
Fig. 4. Supervivencia de pacientes sometidos a TMLR.
DISCUSIÓN
Con frecuencia un cirujano tiene que enfrentarse en el quirófano al dilema del paciente cuya anatomía no permite una revascularización completa. En unas ocasiones, el plan quirúrgico prevé la imposibilidad de pontar todas las áreas isquémicas. En otras más desesperantes, el plan no puede llevarse a cabo íntegramente por falta de vasos epicárdicos viables. A pesar del empirismo que supone es difícil evitar en el cirujano, durante una intervención de revascularización incompleta, la sensación de que estas zonas conferirán un alto riesgo de hacer fracasar el objetivo de la intervención por su potencial de inducir angina.
En esta situación, es fácil que un cirujano se decante por medidas «compasivas» siempre que no incrementen el riesgo del procedimiento. La sencillez y supuesto bajo riesgo del TMLR cumple estas condiciones. Sin embargo, el nivel de seguridad y eficacia no se ha establecido convenientemente debido a que los estudios se centran en su aplicación aisla da como alternativa al tratamiento farmacológico exclusivo.
El estudio presentado debe interpretarse con cautela por ciertas restricciones en su diseño. La muestra, aunque significativa en el ámbito nacional, es reducida y, por tanto, hay riesgo de cometer error estadístico tipo II. En el corte transversal realizado sólo los primeros pacientes intervenidos desde la puesta en marcha del procedimiento acumulan un seguimiento prolongado. Y sobre todo, aunque hubiera sido deseable, la selección de casos no se realizó de modo prospectivo con aleatorización de casos, sino por criterio quirúrgico personal de cada uno de los cirujanos. En estas condiciones existe un evidente riesgo de cometer un sesgo de selección, ya que se procedió a TMLR en los casos que presentaban condiciones anatómicas más adversas a juicio del cirujano, y antecedentes de angina inestable.
Aunque esta falta de uniformidad de criterio tiene el inconveniente de reducir la efectividad respecto a un protocolo estándar de actuación, representa una situación menos artificial del entorno quirúrgico, en el que es imposible evitar cierta dosis de empirismo en la compleja interacción cirujano-paciente. El efecto negativo de la falta de uniformidad es en realidad una fuente de enriquecimiento continuo y un modo lógico de actuar cuando no hay evidencias que aseguren que una línea determinada de actuación es la correcta.
Como factor negativo del TMLR debemos considerar su coste. El precio de los equipos de TMLR oscila entre 200.000 y 500.000 euros. El coste repercutido en cada procedimiento puede llegar a ser de 2.000 euros, lo que supone un incremento del coste total del proceso en torno al 30%.
En cualquier caso, los resultados de mortalidad y clase funcional son llamativos. La ausencia de diferencias significativas en mortalidad es similar a la del grupo de pacientes sometidos a intervención coronaria aislada en el mismo período, aun cuando por el sesgo de selección los casos presentaban más dificultad de revascularizar.
Más importante es la evolución del grado funcional durante el seguimiento. Consideramos que gran parte del beneficio se debe a la eficacia del pontaje aortocoronario. Sin embargo, la ausencia de angina persistente en el grupo de pacientes tratados favorece la hipótesis de la efectividad local del procedimiento. Debe tenerse en cuenta que todos los pacientes presentaban áreas de miocardio viable con déficit de perfusión que no pudo ser solventado por revascularización. Por otro lado, comparado con el subgrupo control de pacientes con angina inestable que no recibieron TMLR, la ausencia de síntomas no puede atribuirse a un mejor control farmacológico de los síntomas, porque no existieron diferencias significativas de tratamiento. En cualquier caso, el porcentaje de uso de tratamiento antianginoso fue inferior en los tratados con láser. Por último, el mayor índice de empleo de antidiabéticos orales (significativo) e insulina (no significativo) en los pacientes tratados con TMLR es un hallazgo comprensible que refleja una situación metabólica relacionada con vasos de mala calidad, y de ahí la existencia de regiones no pontables.
A pesar del carácter compasivo con el que iniciamos su uso, la obtención de resultados satisfactorios en pacientes con un perfil desfavorable, sin aumento de mortalidad y con mejora sintomática mantenida a medio plazo, refuerza la consideración del TMLR como una alternativa a considerar, aunque su eficacia aún no puede considerarse establecida.
Varios estudios recientes corroboran estas expectativas33. En un estudio de Trehan et al en Nueva Delhi34 la mortalidad del procedimiento combinado de pontaje en la cara anterior sin bomba, y TMLR en la cara posterior o en zonas sin vasos pontables fue de sólo el 1,3%. Se trata de un estudio no controlado, originalmente diseñado para demostrar la eficacia de la cirugía mínimamente invasiva, en el que se complemente el pontaje a la descendente anterior realizado mediante la miniincisión, con TMLR en la cara posterior, ya que por esa vía se dificulta el acceso a vasos de la cara posterior. El objetivo del estudio no fue analizar la eficacia del TMLR frente a los pontajes, pero los buenos resultados de supervivencia ponen de manifiesto la bondad del método en lo que a mortalidad quirúrgica se refiere.
Por otra parte, en un estudio prospectivo, controlado, bien diseñado, realizado por Allen et al en Indianápolis35, se distribuyeron aleatoriamente 263 pacientes en un grupo de TMLR aislado (131 pacientes) frente a otro de uso combinado (132 pacientes), reduciéndose la mortalidad del 7,6 al 1,5%. El notable tamaño muestral de estos dos estudios permite confirmar los hallazgos observados en nuestro estudio: la ausencia de efectos nocivos del TMLR cuando se aplica en combinación con cirugía de pontaje aortocoronario, y la baja mortalidad hospitalaria del procedimiento combinado.
Nuestro estudio, por su parte, confirma una magnífica evolución sintomática de los pacientes a corto plazo. Queda para futuros trabajos la valoración de los efectos a plazos superiores al año, tanto en lo referente a mortalidad como al grado funcional.
CONCLUSIONES
El TMLR parece ser una técnica eficaz para evitar la reaparición de angina en pacientes en los que no es posible una revascularización completa por falta de vasos viables para el pontaje en algunas áreas del corazón. A pesar de la falta de diseño aleatorio que permita establecer una comparación real de datos, la mortalidad no difiere significativamente de la mortalidad de pacientes con revascularización completa. Teniendo en cuenta que el subgrupo de pacientes que fueron sometidos a TMLR presentan una situación vascular menos favorable que la media de los pacientes (de ahí la necesidad de usar el láser), y que los resultados son al menos similares a los obtenidos en casos más favorables con pontaje aislado, sumado a la baja mortalidad del procedimiento en nuestra casuística, consideramos el TMLR como una alternativa viable en las zonas en las que no existan vasos que revascularizar durante una operación convencional de pontaje.
Los resultados tienen importancia por la novedad, pero deben interpretarse con cautela por el tamaño reducido de la muestra y el sesgo de selección de pacientes.
ADDENDUM
Hipótesis sobre el número óptimo de canales
El procedimiento de TMLR consiste en la realización de orificios en el miocardio en número y distribución decidida de forma empírica por el cirujano. Esta subjetividad en cuanto al número óptimo de orificios que se deben realizar se debe a la ausencia de estudios orientados a determinar la existencia de un número límite de orificios a partir de la cual se reduzca el beneficio. Los diferentes estudios publicados muestran una elevada variabilidad en el número de orificios, lo que indica la falta de uniformidad de criterios. No existe ninguna recomendación oficial sobre el número óptimo de orificios que se deben realizar.
Es opinión de este autor que dicho número existe, y que puede demostrarse experimentalmente que la respuesta del corazón al número de orificios sigue una curva (respuesta/orificio) con un máximo en un número predecible de orificios por unidad de superficie, superado el cual el perjuicio de la técnica supera al beneficio.
El autor fundamenta esta opinión en las siguientes hipótesis, basadas en el conocimiento actual del funcionamiento del TMLR:
1. Se supone que las perforaciones que se realizan con TMLR producen un efecto beneficioso en la perfusión miocárdica36-38, o en la inhibición de los mecanismos desencadenantes de la angina. Este efecto puede ser por la producción de factores humorales39-41, o por el efecto físico de destrucción de la red nerviosa miocárdica. En cualquiera de los dos casos, el efecto dependerá del número de orificios, tanto en el caso de que el efecto sea local alrededor del orificio, como si es global en todo el miocardio. La primera hipótesis es que, al igual que casi todas las interacciones biológicas, el efecto no sigue un patrón lineal sino que, por la capacidad de saturación de respuesta que muestran los modelos biológicos, sigue un patrón hiperbólico o de histéresis. Esta hipótesis se fundamenta en el hecho de que no es probable que cada vez que se dobla el número de orificios continuamente, se dobla el efecto. Por el contrario, al igual que ocurre con un fármaco, es probable que a partir de un número de orificios el efecto residual de incrementar el factor humoral o la destrucción de red nerviosa apenas sea relevante, tendiendo a una asíntota en la curva de respuesta. De lo contrario, habría que admitir que si 10 orificios mejoran un 5% la perfusión miocárdica, 1.000 orificios (teóricos) deberían mejorar un 500% la perfusión, lo que desafía la plausibilidad biológica del efecto.
En el caso de que el efecto beneficioso de TMLR se deba a la producción de sustancias que estimulen el crecimiento vascular, o que inhiban la transmisión del dolor, es razonable pensar que, al igual que ocurre con todos los comportamientos farmacológicos, una vez saturados los receptores o los intermediarios, una dosis mayor apenas producirá efecto. En caso de que el efecto se produzca por interrupción o interferencia de la red nerviosa, una vez alterado un segmento de conducción e interrumpida la transmisión en ese segmento, una nueva interrupción en el mismo segmento no produce aumento del efecto, ya que el estímulo de cualquier manera no se iba a transmitir. En cualquiera de estos casos, la curva dosis/respuesta (número de orificios/efecto contra la angina analizado) probablemente siga la morfología expresada por la figura adjunta.
2. Por otro lado, la producción de orificios produce una evidente destrucción de miocitos42. A pesar del pequeño tamaño de los orificios, se produce una pérdida demostrable de masa contráctil43,44. Esta hipótesis se refuerza por los hallazgos de varios estudios en los que el uso de TMLR en pacientes con baja fracción de eyección produce un deterioro adicional de contractilidad45,46. La pérdida de miocitos es linealmente proporcional al número de orificios realizados, y a medida que avanza la destrucción, la pérdida proporcional de contractilidad es progresivamente mayor. En un modelo teórico, partiendo de 1.000 células, la pérdida de la primera reduce la contractilidad en un 0,1%, la pérdida de la célula 500 en un 0,2%, la célula 900 en 1%, y la célula 998 en un 50%.
Basándose en el efecto contrapuesto de los dos efectos y la diferente geometría de las curvas de acción, la hipótesis planteada es que en los primeros orificios la masa proporcional de tejido destruido es mínima, mientras que el efecto beneficioso del orificio mejora la contractilidad de las unidades restantes. A medida que se realizan más orificios, el beneficio se incrementa paulatinamente, pero cada vez en menor grado por un efecto de saturación. Llega un momento en el que el incremento de beneficio no compensa la reducción de masa contráctil, por lo que no mejora más la angina/contractilidad. A partir de ese momento, cada nuevo orifico reduce progresivamente la eficacia del procedimiento por pérdida de masa, pudiendo llegar a anularlo e incluso si se siguen realizando perforaciones, producir un perjuicio porque el número de unidades de miocardio disponible sean tan reducidas que, a pesar de estar estimuladas, funcionen en conjunto con menos eficacia que la masa inicial no estimulada.
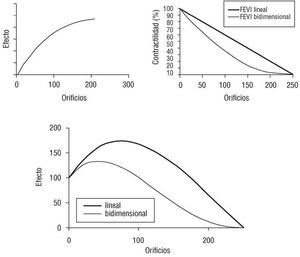
Este efecto queda reflejado en la figura 5, basada en simulación por ordenador del efecto beneficioso de cada orificio sobre el funcionamiento cardíaco, aplicado a la masa residual preservada de la destrucción de tejido por láser. Para el efecto beneficioso se genera un modelo probabilístico en el que se estima la capacidad del incremento de factor beneficioso de encontrar un lugar de acción. Se suponen dos modelos de simulación para la capacidad contráctil, uno en el que la reducción de contractilidad sigue un comportamiento lineal, reduciéndose la capacidad de contracción proporcionalmente al número de canales, y un modelo de simulación bidimensional basado en el supuesto de que la destrucción de tejido afecta a una trama contráctil bidimensional. El empleo de un modelo u otro sólo modifica el momento en el que se alcanza el efecto máximo, pero en cualquiera de los dos modelos se observa que el beneficio producido por las perforaciones sigue un patrón ascendente hasta alcanzar un máximo en el que, por cada nuevo orificio que se practica, la destrucción de tejido no compensa el incremento de contractilidad del tejido preservado.
Fig. 5. Efectos combinados de reducción de masa cardíaca y estimulación por TMLR. La gráfica superior izquierda simula el efecto estimulante producido por un disparo de TMLR en un modelo artificial con efecto de saturación. La gráfica superior derecha simula la relación entre fuerza contráctil y masa disponible, en un modelo de simulación lineal o bidimensional. La gráfica inferior es la combinación del efecto beneficioso del disparo sobre la masa contráctil residual
Este modelo necesita una verificación experimental para confirmar su validez; sin embargo, es compatible con los hallazgos clínicos descritos hasta el momento. De cumplirse este supuesto, sería útil determinar mediante un experimento protocolizado la existencia de algún índice que indique en cada caso la densidad de canales que producirá el máximo beneficio.
AGRADECIMIENTO
El seguimiento completo de todos los pacientes fue posible gracias al trabajo tenaz y meticuloso de María Teresa Llarena Cañizares.
Correspondencia: Dr. I. Díaz de Tuesta. Hospital Universitario de Canarias. 38190 La Laguna. SC Tenerife. Correo electrónico: tuesta@usa.net Recibido el 26 de diciembre de 2000. Aceptado para su publicación el 23 de abril de 2001.