Las guías de la Sociedad Europea de Cardiología (ESC) están avaladas por la Sociedad Española de Cardiología y traducidas al español para su publicación en REVISTA ESPAÑOLA DE CARDIOLOGÍA. En línea con la política iniciada en 2011, cada nueva guía va acompañada de un artículo que aporta comentarios siguiendo los objetivos y la metodología recomendados en el artículo constitucional del Comité de Guías de la SEC1.
En el presente artículo se comenta la nueva guía europea sobre el infarto agudo de miocardio con elevación del segmento ST (IAMCEST)2. El Comité de Guías formó un grupo de trabajo compuesto por miembros propuestos por las secciones de Cardiopatía Isquémica, Hemodinámica, Cardiología Clínica, Insuficiencia Cardiaca y Cardiología Geriátrica.
Como comentario general, creemos que la presente guía aporta novedades muy interesantes y es clara y detallada en la exposición de los temas. Sin embargo, también se debe resaltar que contiene 157 recomendaciones, de las cuales 69 (44%) se acompañan de un nivel de evidencia C (consenso de expertos), que predominan en los apartados de manejo intrahospitalario, insuficiencia cardiaca y complicaciones, campos en que por ello queda un amplio espacio para la individualización y el progreso en la investigación clínica. A la hora de su aplicación, merece la pena no olvidar que las propias guías nos recuerdan que sus recomendaciones de tipos A y B se basan en ensayos clínicos y que incluso estos resultados están abiertos a la interpretación. Las diferentes opciones de tratamiento que se presentan pueden estar condicionadas por los recursos disponibles. Por ello, cada vez será más necesario tener estudios de coste-eficacia que nos ayuden en la elección de las diferentes estrategias.
Con la finalidad de hacer más fácil la lectura del artículo y que queden resaltados los aspectos más relevantes o novedosos, así como los no concretados o no comentados, los hemos resumido en las tablas 1 y 2 respectivamente.
Guías ESC 2012 para el tratamiento del infarto agudo de miocardio con elevación del segmento ST. Aspectos más relevantes y/o novedososa
| Primeras medidas | • La angioplastia primaria está indicada tras muerte súbita cardiaca recuperada y elevación del segmento ST (IB) |
| • La hipotermia precoz ha demostrado buenos resultados en pacientes en coma tras parada cardiaca extrahospitalaria (IB) | |
| • Se considera al sistema de ambulancias de transporte un espacio para el diagnóstico inicial, la toma de decisiones y el tratamiento | |
| • Muy clara definición de las claves organizativas y de los criterios de calidad para evitar retrasos asistenciales en los primeros momentos | |
| Terapia de reperfusión | • La terapia de reperfusión está indicada para todos los pacientes con síntomas de evolución<12h (IA) |
| • En cuanto a la angioplastia primaria, se recomienda: | |
| − Preferirla a la fibrinolisis si se efectúa menos de 120min tras el PCM («criterio de calidad»,<90min) (IA). | |
| − El acceso radial sobre el femoral (IIa B) | |
| − Los stents farmacoactivos sobre los metálicos (IIa A) | |
| − La aspiración de trombos sistemáticamente (IIa B) | |
| − El prasugrel y el ticagrelor (ambos IB) sobre el clopidogrel (IC) | |
| − Los inhibidores de la GPIIb/IIIa sólo con indicación de rescateb (IIa C) | |
| − La bivalirudina sobre la heparina no fraccionada + inhibidores de GPIIb/IIIa (IB) | |
| • En relación con la fibrinolisis se recomienda: | |
| − Traslado de todos los pacientes inmediatamente tras la fibrinolisis a centros de ICP (IA) para apertura inmediata de la arteria causal (rescate, IA) o diferida 3-24h (IIa A) | |
| Manejo intrahospitalario y al alta | • Introducción del término «manejo estricto, pero no demasiado estricto» de la hiperglucemia en la fase aguda y evitando episodios de hipoglucemia |
| • Iniciar todas las medidas de prevención secundaria durante la fase hospitalaria | |
| • Que los centros dispongan de una unidad de deshabituación tabáquica (IB) | |
| • Beneficios derivados de una valoración y terapia cognitivo-conductual para el manejo del estrés | |
| • Cifras objetivo de presión arterial máximas menos rigurosas que en la guía previa | |
| • Poca relevancia de la resonancia magnética tanto para la valoración del tamaño del infarto como para el estudio de la viabilidad | |
| Complicaciones | • Inclusión del nitroprusiato sódico para pacientes con IC y HTA (IIa C) y de hidralazina más nitratos para los que no toleren IECA y ARA-II (IIa C) |
| • Disminución del grado de recomendación de la contrapulsación aórtica (IIb B) |
ARA-II: antagonistas de los receptores de la angiotensina II; GPIIb/IIIa: glucoproteína IIb/IIIa; HTA: hipertensión arterial; IC: insuficiencia cardiaca; ICP: intervencionismo coronario percutáneo; IECA: inhibidores de la enzima de conversión de la angiotensina; PCM: primer contacto médico.
Guías de la Sociedad Europea de Cardiología 2012 para el tratamiento del infarto agudo de miocardio con elevación del segmento ST. Aspectos no concretados y aspectos no tratados
| Primeras medidas | • Secuencia angioplastia primaria-hipotermia en caso de parada cardiaca extrahospitalaria |
| Terapia de reperfusión | • En relación con la angioplastia primaria: |
| − Eventual beneficio de los stents farmacoactivos de segunda generación | |
| − Tratamiento del fenómeno de no reflow | |
| − Cambio entre fármacos antiplaquetarios en angioplastia primaria | |
| − Reinicio del tratamiento antiplaquetario tras la cirugía coronaria | |
| • En relación con la fibrinolisis: | |
| − Tratamiento coadyuvante antitrombótico en caso de angioplastia de rescate\ | |
| Manejo intrahospitalario y al alta | • Decisiones sobre vuelta a la actividad laboral, sexual, viajes en avión, etc. |
| • Mejor estrategia para el control de la glucemia a largo plazo | |
| • Duración de la doble terapia antiagregante | |
| • Papel de los nuevos anticoagulantes orales y necesidad de más evidencia sobre su utilización en el contexto de la fibrilación auricular postinfarto | |
| Complicaciones | • Posibilidad de que las técnicas de reparación percutánea en la CIV puedan ser una alternativa o una terapia puente al tratamiento quirúrgico en casos seleccionados |
| • Recomendación de anticoagulación más doble antiagregación para pacientes con fibrilación auricular a los que se implanta un stent. La guía no ha podido tener en consideración los resultados del estudio Woest |
CIV: comunicación interventricular.
La guía hace especial énfasis en la prevención de los retrasos asistenciales. Ante la sospecha de IAMCEST, es básico facilitar el rápido acceso a la posibilidad de desfibrilación durante los primeros momentos y garantizar el acceso más temprano a la reperfusión. Lo novedoso es que para los pacientes con muerte súbita cardiaca recuperada y elevación del segmento ST, la primera opción terapéutica es la práctica de angioplastia primaria, siempre que puedan cumplirse los tiempos recomendados. Además, se resalta la evidencia de que los pacientes en coma tras una parada cardiaca extrahospitalaria recuperada se benefician del tratamiento de hipotermia siempre que se inicie precozmente.
Sigue siendo controvertido especificar el nivel de elevación del segmento ST en función de la edad (más o menos de 40 años) o el sexo del paciente. Creemos que puede ser motivo de confusión entre muchos profesionales que deben tomar decisiones basándose en el primer electrocardiograma. Se ha avanzado muy poco en el diagnóstico de pacientes con bloqueo de rama izquierda del haz de His. La única cita nueva proviene de un ensayo clínico de 2011, pero no se han publicado observaciones de registros sobre cuál es la incidencia real del diagnóstico final de IAMCEST entre los pacientes cateterizados por dolor torácico y bloqueo de rama izquierda del haz de His.
Se comentan en este apartado los casos de sospecha de oclusión coronaria sin elevación del segmento ST, que en ocasiones pueden cursar con extrema gravedad (oclusión del tronco común, de un puente de safena a circunfleja, etc.), pero otras pueden corresponder a enfermedad no coronaria. Este aspecto ya se comenta en la guía de síndrome coronario sin elevación del segmento ST, donde se destaca la importancia del cardiólogo en la realización de la historia clínica y la necesidad de un ecocardiograma urgente.
Consideramos fundamental la recomendación de que todos los hospitales que atienden a pacientes con IAMCEST registren los tiempos de atención y los revisen regularmente con el objetivo de comprobar que se están cumpliendo las recomendaciones. Más aún, la difusión pública de estos datos (hora de inicio de los síntomas, primer contacto médico, realización del electrocardiograma, momento de la reperfusión, etc.) puede ser útil para estimular la mejora en la calidad asistencial. Ni en España ni en Europa está generalizada la cultura de mostrar públicamente los resultados de los procesos asistenciales.
La guía introduce la idea novedosa de que el sistema de emergencias extrahospitalarias tiene una función esencial en todo el proceso asistencial y hay que considerarlo no sólo un instrumento de transporte, sino un espacio para el diagnóstico inicial, la toma de decisio-nes y el tratamiento. Por lo tanto, los sistemas de ambulancias deben estar capacitados para realizar un electrocardiograma, tratar el dolor, mantener la estabilidad hemodinámica, proporcionar las maniobras de reanimación en caso necesario, decidir el lugar más apropiado de traslado e iniciar el tratamiento de reperfusión en caso de fibrinolisis, así como el tratamiento coadyuvante antiplaquetario en caso de angioplastia primaria. En España, algunas comunidades tienen desde hace años protocolos de actuación que se están mostrando muy eficaces. Merece la pena recordar que dichos protocolos, aún acoplándose a las particularidades de cada territorio, deben ser fieles a las recomendaciones básicas de la ESC, especialmente en lo que a los objetivos de tiempos se refiere.
Así pues, el tratamiento óptimo del IAMCEST se basa en un sistema de emergencias extrahospitalarias eficiente y una buena red de hospi-tales de distintos niveles conectados entre sí. Las claves para que esta organización sea efectiva son:
- •
Clara definición de las áreas geográficas.
- •
Protocolos consensuados que tengan en cuenta el riesgo del paciente y el sistema de transporte disponible en cada momento.
- •
Evaluación prehospitalaria para la derivación apropiada a los diferentes centros, evitando los hospitales sin capacidad de angioplastia.
- •
Llegada directa a la unidad de hemodinámica del hospital de referencia sin pasar por el servicio de urgencias.
Una adecuada recomendación es que los pacientes con cardiopatía isquémica estable lleven siempre una copia de su electrocardiograma basal. Esto implica dar una copia del último electrocardiograma junto con el informe de alta hospitalaria.
TERAPIA DE REPERFUSIÓNLa guía actual presenta cambios importantes respecto a las previas. La sección dedicada a la terapia de reperfusión se evalúa en los siguientes seis apartados:
- 1.
Decisión de reperfusión. El aspecto más importante en la toma de esta decisión es el criterio temporal de las 12h desde el inicio de los síntomas. Se sigue manteniendo la indicación clase I para los pacientes con más de 12h de síntomas si se demuestra persistencia de la isquemia, si bien sólo con un nivel de evidencia C. No está indicada la reperfusión (clase III A) para pacientes estables con infartos de más de 24h de evolución, sin isquemia residual o viabilidad.
- 2.
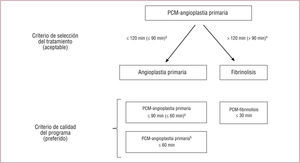
Selección de la estrategia de reperfusión. Se presenta un claro algoritmo para el uso de las terapias de reperfusión. El aspecto más importante reside en reforzar la indicación de angioplastia primaria como el tratamiento preferido siempre que se lleve a cabo en 120min por un equipo experimentado. En este sentido, se exponen claramente los objetivos en cuanto a retrasos aceptables y preferidos. El tiempo de 120min desde el primer contacto médico hasta el paso de la guía se considera el máximo retraso que podría tener la angioplastia primaria para seleccionarla como forma electiva de reperfusión. Este tiempo de preferencia sobre la fibrinolisis se reduce a 90min en el caso de infartos extensos y presentación precoz. Un aspecto novedoso es el establecimiento de unos «criterios de calidad» del tratamiento de reperfusión, con el objetivo de poder aplicarlos de manera selectiva e individualizada. Así, se considera criterio de calidad un tiempo desde el primer contacto médico al paso de la guía<90min para todos los pacientes (60min en infartos extensos y presentación precoz) y<60min para los que acuden directamente a un centro de angioplastia primaria. También se establece como criterio de calidad un tiempo máximo de 10min desde el primer contacto médico al diagnóstico de IAMCEST y de 30min como tiempo máximo desde el primer contacto médico a la fibrinolisis. Desde el punto de vista práctico, se debe considerar todos estos criterios en el momento de establecer los protocolos en los programas de IAMCEST y a la hora de evaluar los resultados de su implementación (figura). Cuando no sea posible realizar la angioplastia primaria en los primeros 120min del primer contacto médico, se debe administrar un fibrinolítico. En este caso y sin esperar al resultado, debería efectuarse un traslado inmediato a un centro con capacidad de intervencionismo urgente (de indicación IIa A, ha pasado a IA) donde se decidiría angioplastia de rescate (si no hay criterios de reperfusión) o angiografía diferida (3-24h) en caso de éxito de la fibrinolisis. Esta modificación tiene una implicación de índole práctica a la hora de definir las necesidades de traslado interhospitalario y el aumento del número de indicaciones de angioplastia.
Figura 1.Algoritmo de decisión para la selección del tipo de tratamiento basada en el retraso estimado (aceptable) y los criterios de calidad de un programa de reperfusión (preferible). Este algoritmo es válido cualquiera sea el retraso en la presentación, de manera que aun en los IAMCEST de poco tiempo de evolución se prefiere la angioplastia primaria sobre la fibrinolisis si se realiza dentro de los plazos reseñados. PCM: primer contacto médico.
aPara infartos extensos y presentación precoz.
bSi el paciente está en un centro de angioplastia primaria.
(0.29MB). - 3.
Angioplastia primaria: aspectos técnicos y farmacológicos. Lo más novedoso está en relación con la introducción del acceso radial como vía de preferencia en la mayoría de las ocasiones (clase IIa B), debido a la reducción de las hemorragias y la consiguiente reducción de la mortalidad respecto al acceso femoral. Respecto al tipo de stent, se enfatiza la importancia de una correcta selección del tamaño y se aconseja la utilización del stent farmacoactivo sobre el convencional (IIa A) si el paciente no tiene contraindicaciones a la doble terapia antiagregante y es probable el buen cumplimiento del tratamiento. Pero no se comenta el eventual beneficio de los stents farmacoactivos de segunda generación sobre los de primera o los convencionales. Tras la presentación de esta guía, se han publicado dos estudios aleatorizados (EXAMINATION3 y COMFORTABLE-AMI4) que han demostrado la eficacia y la seguridad de los stents de segunda generación en esta situación. Otra novedad es la recomendación del uso sistemático de los catéteres de aspiración durante el procedimiento. Se modifica de clase IIb a IIa B. Los resultados de los estudios de condicionamiento remoto y poscondicionamiento son poco concluyentes5. Tampoco las diferentes maniobras en el tratamiento de la falta de restablecimiento del flujo miocárdico (fenómeno de no reflow) en el laboratorio de hemodinámica han mostrado una eficacia suficiente.
Como resumen práctico, se puede proponer que la angioplastia primaria debería llevarse a cabo por acceso radial, mediante trombectomía y seguida de implantación de stent farmacoactivo.
Desde el punto de vista farmacológico, uno de los aspectos más novedosos es la introducción de prasugrel y ticagrelor como agentes antiplaquetarios de preferencia (clase IB para ambos), por delante de clopidogrel (IC), que en la guía queda relegado a las situaciones en que no se puede dar o están contraindicados prasugrel o ticagrelor y a los pacientes tratados únicamente con fibrinolisis. No se comenta en esta guía la posibilidad de cambiar fármacos para los pacientes que hayan recibido la carga de clopidogrel antes de la angioplastia primaria. Como un aspecto importante, y en caso de necesidad de cirugía coronaria con estos tratamientos, se recomienda esperar a realizarla hasta 7 días tras la retirada de prasugrel, 5 días en el caso de clopidogrel y 3-5 días en el caso de ticagrelor. En esta situación, para los pacientes a quienes sea aconsejable no suspender la terapia antiplaquetaria, se considera la posibilidad de una terapia puente (con inhibidores de la glucoproteína IIb/IIIa [GPIIb/IIIa] de semivida corta), aunque no hay evidencia clínica que lo avale.
La utilización de los inhibidores de la GPIIb/IIIa en el IAMCEST ha quedado restringida a terapia de rescate en presencia de trombo intracoronario masivo, situaciones de falta de restablecimiento del flujo miocárdico o complicaciones trombóticas (IIa C). No se recomienda su uso sistemático a la llegada al laboratorio de hemodinámica (IIb B). Como novedad, se presentan los resultados de los estudios INFUSE-AMI y AIDA-4, que comparan la administración intracoronaria con la intravenosa de abciximab, sin diferencias claras entre una y otra estrategia.
La novedad en cuanto al tratamiento anticoagulante es la recomendación de la bivalirudina como agente de elección sobre la heparina sódica asociada a inhibidores de la GPIIb/IIIa, basada en la reducción en la mortalidad observada a los 30 días y hasta los 3 años en el estudio HORIZONS-AMI. La guía comenta la interacción que pudo tener en la reducción del riesgo de trombosis de stent la administración de heparina no fraccionada antes de la aleatorización en un importante número de pacientes. No se conoce la eficacia de la bivalirudina administrada conjuntamente con prasugrel o ticagrelor, ya que el clopidogrel fue el inhibidor del receptor de ADP utilizado en dicho estudio. En el estudio ATOLL, la enoxaparina, comparada con la heparina no fraccionada, mostró una reducción del evento combinado (reducción en mortalidad a 30 días, reinfarto, fracaso del procedimiento y hemorragias), lo que respalda que se la prefiera como tratamiento coadyuvante cuando no se utilice bivalirudina. A modo de resumen práctico en cuanto al tratamiento coadyuvante a la angioplastia primaria, se recomienda pretratar al paciente con ácido acetilsalicílico y prasugrel o ticagrelor (si no hay contraindicaciones). Asimismo, el perfil favorable de seguridad y eficacia de la bivalirudina respecto a la combinación de heparinas e inhibidores de la GPIIb/IIIa indica que la bivalirudina podría ser el anticoagulante de elección. Los inhibidores de la GPIIb/IIIa se mantendrían para las situaciones más trombogénicas.
- 4.
Fibrinolisis: tratamientos coadyuvantes antitrombótico e invasivo. En caso de no disponerse de la angioplastia en tiempo óptimo, el beneficio de la fibrinolisis prehospitalaria es cada vez más evidente, sobre todo para los pacientes a los que se puede tratar en los primeros 60min tras el inicio de los síntomas. La novedad más relevante, ya comentada, es la indicación de traslado inmediatamente tras el tratamiento a un centro con capacidad de realizar angioplastia, con las implicaciones organizativas que ello conlleva. Como terapia adyuvante antiplaquetaria, se recomienda la combinación de ácido acetilsalicílico y clopidogrel, y la enoxaparina como anticoagulante de elección. Ni la bivalirudina ni los nuevos inhibidores P2Y12 se han estudiado en este contexto.
- 5.
Tratamiento para pacientes no reperfundidos. En este apartado se incluye a pacientes que acuden al hospital después de 12h sin persistencia de síntomas o isquemia o a los que no se puede reperfundir por alguna razón clínica. El tratamiento antiplaquetario recomendado incluye ácido acetilsalicílico y clopidogrel, aunque como novedad también añade ticagrelor basándose en los datos de los pacientes no revascularizados del estudio PLATO. En cuanto al tratamiento anticoagulante, se recomienda fondaparinux, enoxaparina o heparina no fraccionada a las mismas dosis que tras la fibrinolisis.
- 6.
Situaciones clínicas especiales. En pacientes con enfermedad multivaso, en el contexto del IAMCEST en la fase aguda, se recomienda tratar sólo la arteria que causa el infarto (excepto en caso de shock cardiogénico o persistencia de la isquemia tras el tratamiento de la lesión causal). En relación con el tratamiento de las otras arterias con lesiones, como recomendación práctica, se puede optar por una «estrategia conservadora», con tratamiento médico inicial y tratamiento de las otras estenosis sólo cuando haya síntomas o isquemia inducida. En caso de estenosis críticas en segmentos proximales de vasos principales, se debería optar por una estrategia de «revascularización percutánea o quirúrgica en un segundo tiempo» (según decisión multidisciplinaria) durante el ingreso o en el primer mes tras el infarto.
Es muy relevante la recomendación de no hacer diferencias en el tratamiento en función del sexo, y que la guía enfatice la necesidad del ajuste de dosis del tratamiento antitrombótico en ancianos, mujeres y pacientes con insuficiencia renal, hasta el punto de dedicarle la tabla 18 de la guía, en la que se detallan las dosis de estos fármacos para pacientes con aclaramiento de creatinina<60ml/min. No realizar este ajuste es un error frecuente que conlleva un importante incremento de las hemorragias.
La guía recomienda que todos los hospitales que participan en el cuidado inicial de pacientes con IAMCEST estén dotados de una unidad de cuidados intensivos cardiológicos o unidad coronaria. Estas unidades deberían ser capaces de ofrecer tratamiento especializado a los pacientes con síndrome coronario agudo, arritmia e insuficiencia cardiaca, y su personal debería estar familiarizado con las técnicas de soporte circulatorio mecánico, monitorización hemodinámica invasiva y no invasiva, monitorización y soporte respiratorio invasivo y no invasivo, técnicas de hipotermia terapéutica y soporte renal.
El manejo y la duración de la estancia hospitalaria difieren según el riesgo del paciente. Aunque con niveles de evidencia bajos, la guía recomienda acortar la estancia. Para los pacientes de bajo riesgo sometidos a una angioplastia primaria efectiva, considera razonable, aunque con un grado de recomendación IIb C, el traslado a otro centro sin unidad de hemodinámica el mismo día y valorar el alta hospitalaria tras 72h si es posible un seguimiento ambulatorio adecuado. La clave es a quién se considere paciente de bajo riesgo. Diferentes escalas (PAMI, Zwolle) pueden ayudar a estratificar muy precozmente el riesgo en pacientes tras la angioplastia primaria.
Se recuerda la utilidad del ecocardiograma al ingreso en caso de dudas diagnósticas. Asimismo, esta es la técnica recomendada para determinar el tamaño del infarto y la función ventricular izquierda y descartar complicaciones. La utilización de la resonancia magnética con estos fines queda relegada como alternativa cuando la ecografía no es factible (IIb C).
Se recuerda la menor importancia de los tests de isquemia sistemáticos previos al alta tras la realización de la angioplastia primaria y el conocimiento de la anatomía coronaria. Son una recomendación IA en las primeras 4-6 semanas solamente para los pacientes con enfermedad multivaso o para los que se considera la posibilidad de revascularización de vasos no tratados. La guía describe una vez más las fortalezas y debilidades de cada prueba, pero sigue sin posicionarse a favor de una u otra modalidad. Solamente, y como novedad, se muestran tajantes a la hora de descartar la utilidad de la tomografía computarizada coronaria en esta situación (III C).
Para el estudio de la viabilidad, se enumeran una vez más las técnicas disponibles (nucleares, ecocardiografía de estrés y resonancia magnética) y se deja a elección del facultativo cuál utilizar, por la escasa diferencia en los resultados obtenidos con cada una de ellas.
TratamientoPor primera vez se dedica un apartado especial para el manejo de la hiperglucemia. Se recuerda la relevancia pronóstica negativa de la hiperglucemia y se recomiendan esfuerzos diagnósticos para pacientes sin diabetes mellitus ya conocida. El mensaje más importante y novedoso se resume en la recomendación de hacer un manejo de la hiperglucemia «estricto, pero no demasiado estricto» recalcando con énfasis la necesidad de evitar la hipoglucemia. Esta estrategia se resume en mantener en la fase aguda glucemias por debajo de 20 0mg/dl (≤ 11mmol/l) y por encima de 90mg/dl (< 5mmol/l), mucho más permisivos que los aceptados hasta ahora. Están más claros los objetivos que la estrategia para conseguirlos, y se recomienda para algunos pacientes la infusión de insulina ajustada según los valores de la monitorización de glucemia (IIa B). Se rechaza la utilización de infusiones de glucosa-insulina-potasio (III A).
La actual guía presenta una diferencia fundamental respecto a la previa en cuanto al manejo médico de las fases aguda y subaguda y a largo plazo. La organización de la información se resume con gran claridad en la tabla 22 de la guía.
Todas las medidas de tratamiento y prevención secundaria deben iniciarse durante la estancia hospitalaria con el objetivo de que después tengan la máxima adherencia. Los aspectos relevantes son el énfasis en el cese del hábito tabáquico, con la recomendación de que los centros dispongan de una unidad de deshabituación, y los comentarios sobre los beneficios derivados de la valoración y la terapia cognitivo-conductual para el manejo del estrés. Es importante resaltar que la rehabilitación cardiaca, tan infrautilizada en nuestro país, sigue siendo una indicación de clase IB.
Otra novedad importante se refiere al control de la presión arterial. Con base en datos de un análisis retrospectivo del estudio PROVE-IT TIMI 22, la guía actual es menos estricta que la previa y recomienda que el objetivo de presión sistólica sea<140mmHg, pero no<110mmHg.
En terapia hipolipemiante, se recomienda el tratamiento intensivo y precoz con estatinas, independientemente de las concentraciones de colesterol, para todos los pacientes con IAMCEST. En esta ocasión, la guía se posiciona claramente a favor de la atorvastatina a dosis de 80mg. Las principales recomendaciones en este terreno y las diferencias respecto a la previa se exponen en la tabla 3.
Comparación de las recomendaciones de la Sociedad Europea de Cardiología sobre terapia hipolipemiante a largo plazo en las guías de síndrome coronario agudo con elevación del segmento ST de 2008 y 2012
| 2008 | 2012 |
| Objetivo cLDL<100mg/dl (IA) y<80mg/dl para los de alto riesgo (IIa A) | Determinacion del perfil lipidico lo antes posible en todos los pacientes (IC). Objetivo cLDL<70mg/dl para todos los pacientes. Recomendacion IIa C |
| Tratamiento con estatinas a altas dosis, sin especificar | Preferible tratamiento con atorvastatina a dosis de 80mg/dia (IA). Disminuir dosis a pacientes con riesgo aumentado de efectos adversos por estatinas |
| Tratamiento de segunda linea: fibratos y omega 3 (indicacion IIa B) | Tratamiento de segunda linea: ezetimiba |
| Suplementos de 1g de aceite de pescado para pacientes con bajo consumo | No se recomienda suplementar con acidos grasos poliinsaturados omega 3 (ensayo OMEGA) |
| Reevaluacion de concentraciones de cLDL a las 4-6 semanas de iniciarse el tratamiento (IIa C) |
cLDL: colesterol unido a lipoproteinas de baja densidad.
Respecto a la terapia antiplaquetaria, no se cuestiona la administración de ácido acetilsalicílico, y ya se ha expresado en otro apartado el papel preponderante del prasugrel o el ticagrelor sobre el clopidogrel. No cambian las recomendaciones sobre la duración del doble tratamiento antiagregante. La recomendación de mantener la duración del tratamiento con estos fármacos durante 12 meses en pacientes sin stents (IIa C) puede ser discutible.
Quedan aparcadas las dudas acerca de la interacción de los inhibidores de la bomba de protones y el clopidogrel, por la ausencia de evidencia de su significado clínico, y se mantienen sus indicaciones clásicas.
Más novedosa, y a la vez controvertida, es la posibilidad de añadir un anticoagulante oral anti-Xa (rivaroxabán) a ácido acetilsalicílico y clopidogrel como tratamiento coadyuvante a la prevención secundaria para pacientes con bajo riesgo hemorrágico (recomendación IIb B), ensayada en el estudio ATLAS-ACS TIMI 51. Se desconoce si esta estrategia es superior a la combinación de ácido acetilsalicílico con prasugrel o ticagrelor. Además de tratarse de una indicación aún no aprobada por las agencias competentes, un reciente metaanálisis6 publicado después que la guía concluye que los nuevos agentes anticoagulantes no demuestran beneficio clínico neto tras el síndrome coronario agudo.
La guía sigue recomendando (IC) la triple terapia antitrombótica (doble antiagregación y anticoagulación oral) para los pacientes con fibrilación auricular e IAMCEST. Es posible que haya que revisarla tras los resultados del estudio WOEST7, que no se pudo incluir en ella por haberse presentado simultáneamente a la propia guía en el último Congreso de la ESC. Dicho estudio demostró mayor beneficio, incluso con reducción de la mortalidad total, del tratamiento con clopidogrel y anticoagulación oral frente al que, además, añadía ácido acetilsalicílico.
Respecto al resto de los tratamientos, se recomienda posponer el inicio los bloqueadores beta hasta la estabilización del paciente, salvo cuando haya hipertensión o taquicardia y en ausencia de insuficiencia cardiaca. Su indicación pasa a IIa B, aunque mantiene incuestionablemente la recomendación al alta para pacientes con disfunción ventricular o insuficiencia cardiaca (IA). Se mantiene el nivel de recomendación IB para la utilización de antialdosterónicos en pacientes con fracción de eyección del ventrículo izquierdo (FEVI)<40% y diabetes mellitus o insuficiencia cardiaca, sin especificarse el fármaco de primera elección (eplerenona o espironolactona). Dado que la evidencia para los pacientes tras un IAMCEST se basa exclusivamente en la eplerenona, los menores efectos secundarios de ésta y sus excelentes resultados en los pacientes con insuficiencia cardiaca en estadios menos avanzados (estudio EMPHASIS HF), creemos que la eplerenona debería figurar como fármaco de primera línea dentro de este grupo farmacológico.
Siguiendo estrictamente las recomendaciones de la guía, tras un infarto el paciente será dado de alta con unos 6-10 comprimidos por término me dio. Teniendo en cuenta que la mayoría de los pacientes son ancianos, de los que muchos sufren comorbilidades que implican la toma de otros fármacos, es frecuente encontrar a pacientes con planes terapéuticos difíciles de cumplir. Si queremos pasar de la eficacia que muestran los fármacos en los ensayos clínicos a una verdadera efectividad en la vida real, son imprescindibles medidas que faciliten una toma racional de los medicamentos, como la supresión de fármacos con b enef icio marginal en un paciente determinado o el uso de presentaciones con una combinación de principios activos.
COMPLICACIONESInsuficiencia cardiaca y shockEn este apartado, la tabla 23 de la guía resume un total de 29 recomendaciones (ocho más que en las guías previas), la mayoría de las cuales son por consenso con el mínimo nivel de evidencia (C), al no disponerse de referencias bibliográficas concretas.
Aparece muy subrayado el uso de ecocardiografía utilizando el imperativo inglés must be performed.
Destaca la inclusión del nitroprusiato sódico para el tratamiento de la hipertensión, y la combinación de hidralazina y dinitrato de isosorbida para pacientes con insuficiencia cardiaca que no pueden tomar inhibidores de la enzima de conversión de la angiotensina ni antagonistas de los receptores de la angiotensina II, que no se incluían en guías previas. Recogiendo la información de dos estudios aleatorizados muy recientes, se incluye la recomendación de utilizar norepinefrina en el shock, con preferencia sobre la dopamina (IIb B). El uso de levosimendán, fármaco caro y cuya eficacia comparada con otros inotrópicos no se ha demostrado de manera fehaciente, sigue siendo muy controvertido. La guía le concede los mínimos grado de recomendación y nivel de evidencia (IIb C) posibles en la situación de Killip III, por detrás de dopamina y dobutamina. Dado su mecanismo de acción (independiente de la estimulación betaadrenérgica), se hace referencia a su posible utilidad en el caso de tratamiento previo con bloqueadores beta.
Con base en dos recientes metaanálisis, el uso de balón de contrapulsación pasa de ser una recomendación de clase I a IIb B. Casi simultáneamente a la aparición de esta guía, se ha publicado el mayor estudio aleatorizado sobre la contrapulsación hasta la fecha8. En una serie de 600 pacientes con shock cardiogénico tras infarto, en los que se planeaba revascularización, la contrapulsación no redujo la mortalidad a 30 días. Hay que considerar que el seguimiento de este estudio fue muy corto y que un 40% de los pacientes incluidos habían tenido parada cardiaca (posible shock distributivo, en el que la contrapulsación no es beneficiosa). Pese a ello, esta nueva información, que no estaba disponible cuando se redactó la guía, viene a cuestionar la utilidad de la contrapulsación de manera generalizada. En nuestra opinión, estudios en contextos generales no deberían desterrar la indicación de esta técnica para algunos pacientes individualizados, dada la amplia experiencia positiva acumulada con los años. La decisión debe tomarse bastante precozmente para evitar la aparición de fallo multiorgánico irreversible, y por cardiólogos con amplia experiencia en el cuidado de este tipo de enfermos. Es de esperar que en el futuro próximo se pueda definir los subgrupos de pacientes que pueden beneficiarse del soporte con balón de contrapulsación. Más adelante, la guía hace referencia al papel estabilizador de la contrapulsación en las complicaciones mecánicas del infarto (insuficiencia mitral aguda grave y comunicación interventricular).
El uso de la asistencia ventricular para el manejo del shock refractario también sufre una reducción en el grado de recomendación (pasa de IIa C a IIb C), basándose en un metaanálisis de los sistemas Tandem Heart e Impella 2,5. Estos sistemas, que no redujeron la mortalidad a 30 días en comparación con la contrapulsación, posiblemente no sean los más indicados actualmente.
La guía presta muy escasa atención a la ultrafiltración, aunque la respalda con un grado importante de recomendación (IIa B) en casos de sobrecarga de volumen refractaria a diuréticos, especialmente en presencia de hiponatremia.
Otras complicacionesNo hay aportaciones novedosas respecto a las arritmias. Se recuerda la necesidad de sopesar cuidadosamente la indicación de stents recubiertos en pacientes que deberán seguir tratamiento anticoagulante por fibrilación auricular. Tampoco hay importantes novedades respecto al manejo de las arritmias ventriculares. Cabe resaltar la relación entre la aparición de arritmias malignas más allá de la fase aguda (24-48h) y mal pronóstico en pacientes con FEVI muy reducida. Es improbable que en estos casos la revascularización pueda evitar la recurrencia, incluso aunque la arritmia original pudiera tener relación con un episodio de isquemia transitoria. En estos casos, la implantación de un desfibrilador automático implantable tiene una recomendación IA.
La guía sigue sin dar una recomendación específica sobre el momento más adecuado para la reparación quirúrgica de la comunicación interventricular postinfarto. Dada la mayor mortalidad en las de localización inferobasal, creemos que en este escenario se debe considerar la cirugía más precozmente, aun a falta de evidencia contrastada.
La frecuencia de trombos murales ventriculares ha disminuido significativamente con la mejora del tratamiento de reperfusión. No disponemos de datos recientes sobre la duración de la anticoagulación en estos casos. La guía propone que actualmente, teniendo en cuenta la combinación de la doble antiagregación con el tratamiento anticoagulante, el tiempo de mantenimiento de la anticoagulación puede ser<6 meses si una técnica de imagen a los 3 meses demuestra la desaparición del trombo.
CONFLICTO DE INTERESESCoordinación nacional ensayo clínico PLATO: Astra-Zeneca (MH). Clinical Commitee endpoint: Eli-Lilly (AB). Becas investigación a la institución: Abbot-Vascular (AC), Boston Cientific (AC), GSK (MH), Medtronic (AC). Consultorías: Abbott (MS), Astra-Zeneca (AB, JB, JL-S, MS, MH), Bayer (AB, AF, JB), Boheringer-Ingelheim (FW), Boston Scientific (IL), Chiesi (JB, FW), Cordis (MS), Daiichi-Sankyo (JB, AF, JL-S, FW), Eli-Lilly (AF, MS), Ferrer (AF), Medtronic (MS), MSD (AF), Rovi (AB), Sanofi (IL). Ponencias y presentaciones educativas: Abbott (AC, AF), Astra-Zeneca (AC, AF, J-LS, MH), Bayer (AC, JL-S, MP, MH), Biotronic (AC), Boheringer-Ingelheim (JL-S, FW, MH), Chiesi (AF, FW), Daiichi-Sankyo (AC,AF, JL-S, FW), Eli-Lilly (AF, MH), Ferrer (AC,AF), GSK (AF), Menarini (JL-S, MH), MSD (AF, FW), Roche (AF), Rovi (MH).
| Coordinadores: |
| Fernando Worner |
| Angel Cequier |
| Grupo de Trabajo de la Sociedad Española de Cardiología para la guía de práctica clínica sobre el síndrome coronario agudo con elevación del segmento ST: |
| Alfredo Bardají |
| Vicente Bodí |
| Ramón Bover |
| Manuel Martínez-Sellés |
| Manel Sabaté |
| Alejandro Sionis |
| José Antonio Vázquez de Prada |
| Grupo de Revisores Expertos para la guía de síndrome coronario agudo con elevación del segmento ST: |
| Fernando Arós Fernando Arribas José Barrabés |
| Oscar Díaz de Castro |
| Magda Heras |
| Ramón López Palop |
| José Luis López-Sendón |
| Nicolás Manito |
| M. Carmen de Pablo |
| Tomás Ripoll |
| Alberto San Román |
| José M. de la Torre |
| Comité de Guías de Práctica Clínica de la Sociedad Española de Cardiología: |
| Antonio Fernandez-Ortiz (presidente) |
| Ángel M. Alonso Gómez |
| Manuel Anguita |
| Angel Cequier |
| Josep Comín |
| Isabel Diaz-Buschmann |
| Ignacio Fernández Lozano |
| José Juan Gómez de Diego |
| Manuel Pan |
| Fernando Worner |