SEC 2023 - El Congreso de la Salud Cardiovascular
Introducción
Dr. Juan José Gómez Doblas
Presidente del Comité Científico del Congreso
Vicepresidente de la SEC
Comités ejecutivo, organizador y científico
Comité de evaluadores
Listado de sesiones
Índice de autores
51. Actualización en aspectos clínicos de las cardiopatías familiares
3. AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
1Cardiología. Hospital Universitari Arnau de Vilanova, Lleida, España, 2Cardiología. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 3Bioquímica clínica. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 4Neurología. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 5Medicina Nuclear. Complejo Asistencial Universitario de Salamanca, Salamanca, España y 6Salamanca. Complejo Asistencial Universitario de Salamanca, Salamanca, España.
Introducción y objetivos: La amiloidosis cardiaca (AC) es una enfermedad por depósito de proteínas mal plegadas en el espacio extracelular; la producida por transtirretina (AC-ATTR) es la forma más frecuente y su prevalencia aumenta con la edad. Actualmente se acepta el diagnóstico de forma no invasiva basado en gammagrafía con trazadores óseos y descartando la existencia de proteína monoclonal. El diagnóstico de AC-ATTR se debe completar con la secuenciación del gen TTR para la diferenciación entre las formas hereditarias (ATTRv) y las seniles (ATTRwt). Esta diferenciación puede permitir iniciar fármacos con beneficio pronóstico, así como la detección de familiares portadores o afectados y su potencial tratamiento.
Métodos: Nuestro objetivo ha sido analizar la prevalencia de ATTRv en el subgrupo de pacientes ancianos (según la OMS edad ≥ 75 años), sus características diferenciales y las implicaciones de este diagnóstico para los pacientes y familiares.
Resultados: Entre los años 2016 y 2022 se incluyeron 145 pacientes con ATTR-AC (85% varones), con una edad media al diagnóstico de 82 ± 7,4 años (rango 49-95 años); 130 de ellos (89%) tenían 75 años (figura). Se realizó secuenciación del gen TTR el 95% de los ancianos (de los 7 pacientes restantes, uno lo declinó y los otros 6 fallecieron antes de completar el estudio). En 8 pacientes el test identificó una variante patogénica (1 p.Ser97Tyr, 2 p.Val50Met y 5 Val142Ile), prevalencia de ATTRv del 6,5%. Los ancianos con ATTRv tenían una edad inferior (79,7 ± 3,7 años vs 84,3 ± 4,2 años; p = 0,003). No hubo diferencias entre varones y mujeres (5,8 vs 10,5%; p = NS) ni en el resto de las características y eventos (tabla). 5 pacientes presentaban polineuropatía y 4 iniciaron tratamiento con estabilizador de transtirretina (tafamidis) y en uno de ellos ha sido necesario el cambio a inhibidor de ARN (patisirán) por progresión de la neuropatía. Se estudiaron 14 sujetos de 4 familias, identificándose un caso de ATTRv que ha iniciado tratamiento con tafamidis y otros 6 portadores asintomáticos.
|
Características basales del total de la cohorte y comparativa dentro del subgrupo de ancianos (≥ 75 años) según el resultado del estudio genético |
||||
|
|
ATTR-AC (N = 145) |
ATTRv ancianos (n = 8) |
ATTRwt ancianos (n = 114) |
p |
|
Sexo (varones) |
124 (85%) |
6 (75%) |
98 (85%) |
NS |
|
Edad, años |
82 (± 7) |
80 (± 4) |
84 (± 4) |
0,003 |
|
Comorbilidad |
||||
|
HTA |
115 (79%) |
5 (62,5%) |
94 (82%) |
NS |
|
Diabetes |
32 (22%) |
2 (25%) |
27 (23,5%) |
NS |
|
Dislipemia |
85 (58%) |
5 (62,5%) |
68 (59%) |
NS |
|
Tabaquismo |
28 (19%) |
2 (25%) |
25 (22%) |
NS |
|
IRC (estadio 3 o más) |
88 (60%) |
4 (50%) |
72 (63%) |
NS |
|
Patología respiratoria crónica |
31 (21%) |
1 (12,5%) |
26 (23%) |
NS |
|
Cardiopatía isquémica |
29 (20%) |
1 (12,5%) |
25 (22%) |
NS |
|
Cáncer |
34 (23%) |
0 (0%) |
28 (24%) |
NS |
|
Estenosis aórtica (al menos moderada) |
17 (12%) |
2 (25%) |
14 (12%) |
NS |
|
Extracardiaco |
||||
|
STC |
55 (38%) |
3 (37,5%) |
44 (38%) |
NS |
|
Estenosis canal lumbar |
16 (11%) |
0 (0%) |
13 (11%) |
NS |
|
Rotura supraespinoso |
21 (14%) |
3 (37,5%) |
16 (14%) |
NS |
|
Polineuropatía |
25 (17%)* |
5 (83%) |
- |
- |
|
Ecocardiograma* |
n = 124 |
n = 5 |
n = 100 |
|
|
FEVI< 50% |
40 (32%) |
1 (20%) |
33 (33%) |
NS |
|
Disfunción VD |
43 (35%) |
1 (20%) |
42 (42%) |
NS |
|
Máximo grosor septal, mm |
17 ± 3,5 |
14,9 ± 1,4 |
17,1 ± 3,6 |
NS |
|
Hipertrofia VD |
81 (65%) |
4 (80%) |
65 (65%) |
NS |
|
Derrame pericárdico |
30 (24%) |
1 (20%) |
27 (27%) |
NS |
|
GLS, % |
-12,1 ± 3,6* |
-14,3 ± 3,3* |
-11,8 ± 3,9* |
NS |
|
Preservación apical |
53 (93%)* |
3 (75%)* |
39 (93%)* |
NS |
|
Resonancia cardiaca* |
n = 85 |
n = 4 |
n = 69 |
|
|
FEVI, % |
51,9 ± 11,5 |
53,7 ± 10,7 |
51,2 ± 11,2 |
NS¥ |
|
FEVD, % |
55,1 ± 11,3 |
56,5 ± 8,2 |
54,3 ± 11,4 |
NS¥ |
|
Masa VI, g/m2 |
114,4 ± 28,5 |
144 ± 37,7 |
110,6 ± 24,6 |
NS¥ |
|
VEC miocárdico, % |
48,2 ± 11,9* |
54,9 ± 3,6 |
47,8 ± 1,26* |
NS¥ |
|
Z score T1 nativo |
4,6 ± 1,6* |
5,4 ± 0,96* |
4,4 ± 1,7* |
NS¥ |
|
Bioquímica |
||||
|
Tasa de filtrado glomerular, ml/min/1,73 m2 |
54 ± 20 |
65 ± 18,7 |
52,5 ± 18,7 |
NS |
|
NTproBNP (pg/mL) |
3.477 (1.720-6.471) |
3.114 (1.878-7.170) |
3.617 (2.070-7.201) |
NS¥ |
|
Ratio troponina ultrasensible (respecto límite de laboratorio) |
3,56 (1,94-5,65) |
3,64 (1,26-6,23) |
3,79 (2,03-6,10) |
NS¥ |
|
Eventos |
||||
|
Insuficiencia cardiaca |
100 (68,5%) |
5 (62,5%) |
82 (71%) |
NS |
|
Fibrilación auricular |
91 (62%) |
6 (75%) |
72 (63%) |
NS |
|
Marcapasos |
27 (18,5%) |
3 (37,5%) |
19 (16,5%) |
NS |
|
ACV o embolia |
34 (23%) |
2 (25%) |
27 (23,5%) |
NS |
|
Fallecidos |
49 (34%) |
1 (12,5%) |
42 (36,5%) |
NS |
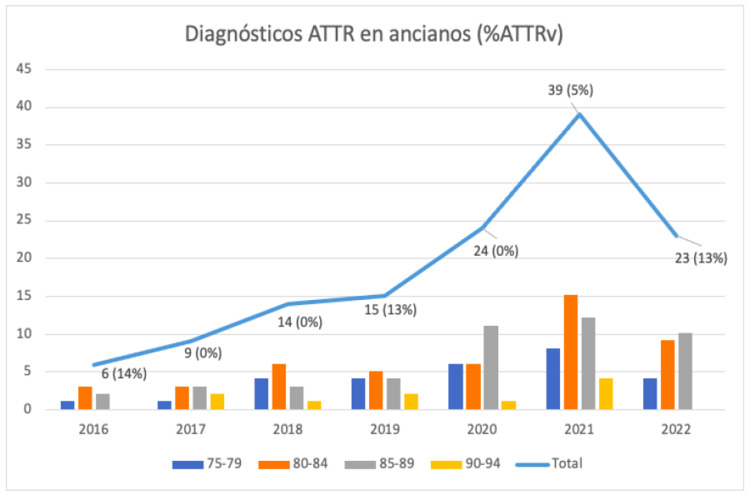
Diagnósticos de ATTR-AC en ancianos y porcentaje de ATTRv.
Conclusiones: La prevalencia de ATTRv en una cohorte independiente de pacientes ancianos con AC-ATTR fue del 6,5%, sin característica diferenciales que permitan guiar una indicación selectiva del análisis genético. Estos hallazgos apoyan la recomendación actual de realizar test genético a todos los pacientes diagnosticados con AC-ATTR independientemente de la edad.
Comunicaciones disponibles de "Actualización en aspectos clínicos de las cardiopatías familiares"
- 1. MODERA
- Esther Zorio Grima, Hospital Universitario y Politécnico La Fe, València
- 2. EVALUACIÓN DE EVENTOS HEMORRÁGICOS EN UNA COHORTE DE PACIENTES CON AMILOIDOSIS CARDIACA POR TRANSTIRRETINA
- Lucía Moreno de Redrojo Cortés1, María Gallego Delgado1, Rocío Eiros Bachiller1, Jara Gayán Ordás2, José Cañadas Salazar3, Elena Díaz Peláez1, Sara Rodríguez Diego1, Mónica García Monsalvo1, Ángel Víctor Hernández Martos4, Sara Lozano Jiménez1, Daniel Alejandro Bracho Bracchitta1, Olga Cabañas Tendero1, Juan Diego Oviedo Rodríguez1, Eduardo Villacorta Argüelles1 y Pedro Luis Sánchez Fernández1
1Cardiología, Complejo Asistencial Universitario de Salamanca, Salamanca, España, 2Cardiología. Hospital Universitari Arnau de Vilanova, Lleida, España, 3Medicina Nuclear. Complejo Asistencial Universitario de Salamanca, Salamanca, España y 4Complejo Asistencial Universitario de Salamanca, Salamanca, España.
- 3. AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- Jara Gayán Ordás1, María Gallego Delgado2, Rocío Eiros Bachiller2, Belén García Berrocal3, María Dolores Calabria Gallego4, José Cañadas Salazar5, Elena Díaz Peláez2, Ana Martín García2, Ángel Hernández Martos6, David Heredero Hansoe3, Lucía Moreno de Redrojo Cortes2, Cristina Álvarez Martínez2, María Isidoro García3, Pedro Luis Sánchez Fernández2 y Eduardo Villacorta Argüelles2
1Cardiología. Hospital Universitari Arnau de Vilanova, Lleida, España, 2Cardiología. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 3Bioquímica clínica. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 4Neurología. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 5Medicina Nuclear. Complejo Asistencial Universitario de Salamanca, Salamanca, España y 6Salamanca. Complejo Asistencial Universitario de Salamanca, Salamanca, España.
- 4. MIOCARDIOPATÍA DE TAKO-TSUBO DURANTE EL PERIPARTO: DATOS DE UN REGISTRO NACIONAL Y DE LA LITERATURA PUBLICADA
- Ravi Vazirani Ballesteros1, Emilia Blanco-Ponce2, Manuel Almendro Delia3, Agustín Martín-García4, Clara Fernández-Cordón5, Aitor Uribarri González6, Óscar Ángel Vedia Cruz1, Alessandro Sionis Green7, Jorge Salamanca Viloria8, Miguel José Corbi Pascual9, Alberto Pérez-Castellanos10, Manuel Martínez-Selles5, Sergio Raposeiras Roubín11, Javier López-País12 e Iván Núñez Gil1
1Hospital Clínico San Carlos, Madrid, España, 2Hospital Universitari Arnau de Vilanova, Lleida, España, 3Hospital Universitario Virgen Macarena, Sevilla, España, 4Complejo Asistencial Universitario de Salamanca, Salamanca, España, 5Hospital General Universitario Gregorio Marañón, Madrid, España, 6Hospital Universitari Vall d’Hebron, Barcelona, España, 7Hospital de la Santa Creu i Sant Pau, Barcelona, España, 8Hospital Universitario de La Princesa, Madrid, España, 9Complejo Hospitalario Universitario, Albacete, España, 10Hospital Son Espases, Palma de Mallorca (Illes Balears), España, 11Hospital Álvaro Cunqueiro, Vigo (Pontevedra), España y 12Complejo Hospitalario Universitario de Ourense, Ourense, España.
- 5. FENOCOPIAS EN EL SÍNDROME DE TAKO-TSUBO, EXPLORANDO UNA ENTIDAD DIFERENTE
- Pablo Carrión Montaner1, Gabriel Torres Ruiz1, Jordi Sans Roselló1, Salvatore Brugaletta2, Enrico Cerrato3, Fernando Alonso4, Nieves Gonzalo5, Jesús Ignacio Amat6, Blanca Simón Francés7, Víctor García Hernando1, Antoni Martínez Rubio1 y Héctor M. García-García7
1Cardiología. Corporació Sanitària Parc Taulí, Sabadell (Barcelona), España, 2Hospital Clínic, Barcelona, España, 3Section of Interventional Cardiology. San Luigi Gonzaga University Hospital, Turin, Italia, 4Unidad de Hemodinámica. Hospital Universitario de La Princesa, Madrid, España, 5Unidad de Hemodinámica. Hospital Clínico San Carlos, Madrid, España, 6Unidad de Hemodinámica. Hospital Clínico Universitario de Valladolid, Valladolid, España y 7Section of Interventional Cardiology. MedStar Washington Hospital Center, Washington DC Washington, Estados Unidos.
- 6. ESTRATEGIA DE CRIBADO SISTEMÁTICO DE PACIENTES CON HIPERCOLESTEROLEMIA FAMILIAR PARTIENDO DE ANALÍTICA CENTRALIZADA PREEXISTENTE Y ESTUDIO DE LAS ALTERACIONES GENÉTICAS DOCUMENTADAS
- Joaquín Sánchez-Prieto Castillo1, Joan Ramon Enseñat1, Charlotte Boillot1, Ana Díaz Rojo1, Andrea González Pigorini1, Lucía Villafáfila Martínez1, Patricia del Valle Tabernero1, Ainhoa Aguinaga Mendibil1, José Manuel Martínez Palomares1, Natalia Navarro Pelegrini1, Alejandro Cabello Rodríguez1, Esther Gigante Miravalles1, María Cristina Morante Perea1, Fernando Sabatel Pérez2 y Luis Rodríguez Padial1
1Cardiología. Hospital Universitario Toledo, Toledo, España y 2Hospital General Básico Santa Ana de Motril, Motril (Granada), España.
- 7. CARACTERIZACIÓN FENOTÍPICA Y FUNCIONAL DE LA VARIANTE L889V EN EL GEN SCN5A
- María Gallego Delgado1, Ricardo Caballero2, Beatriz Plata Izquierdo3, Belén García Berrocal4, David Hansoe Heredero Jung4, Laura de la Fuente Blanco1, Armando Oterino Manzanas1, Elena Marcos Vadillo4, Lucía Rodríguez Estévez5, Alfonso Mayorga Bajo6, Pedro Luis Sánchez Fernández1, María Isidoro García4, Eva Delpón2 y Eduardo Villacorta Argüelles1
1Cardiología. Hospital Universitario de Salamanca, Salamanca, España, 2Universidad Complutense, Madrid, España, 3Pediatría. Hospital Universitario de Salamanca, Salamanca, España, 4Bioquímica clínica y Análisis clínicos. Hospital Universitario de Salamanca, Salamanca, España, 5Cardiología. Hospital Virgen de la Concha, Zamora, España y 6Cardiología. Hospital del Bierzo, Ponferrada León, España.
- 8. VALOR DIAGNÓSTICO DEL PATRÓN DE PRESERVACIÓN APICAL DURANTE EL ECOCARDIOGRAMA DE EJERCICIO EN PACIENTES CON AMILOIDOSIS CARDIACA
- Marina Combarro Eiriz, Jesús Peteiro Vázquez, Gonzalo Barge Caballero y Alberto Bouzas Mosquera
Complexo Hospitalario Universitario de A Coruña, A Coruña, España.
- 9. REVISIÓN DE LAS CARACTERÍSTICAS E IMPACTO PRONÓSTICO DE LA FIBRILACIÓN AURICULAR EN MIOCARDIOPATÍA HIPERTRÓFICA CON GROSOR SEPTAL LEVE
- Carlos José Morales Alcázar1, Ana María Martínez Rodríguez1, Isabel Jiménez Alcántara2, Magdalena Carrillo Bailén1, José María Segura Aumente1, Juan Carlos Fernández Guerrero1 y José Ángel Urbano Moral1
1Cardiología. Complejo Hospitalario de Jaén, Jaén, España y 2Complejo Hospitalario de Jaén, Jaén, España.
- 10. PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- Milena Antúnez Ballesteros1, Eduardo Villacorta Argüelles1, Marta García Ruiz2, Manuel Barreiro Pérez3, María Gallego Delgado1, Elena Díaz Peláez1, Fabián Blanco Fernández1, Mónica García Monsalvo1, Olga Cabañas Tendero1, Cristina Álvarez Martinez1, Ana Elvira Laffond1, Lucia Moreno de Redrojo Cortes1, Juan Diego Oviedo Rodríguez1, Daniel Alejandro Bracho Bracchitta1 y Pedro Luis Sánchez Fernández1
1Cardiología. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 2Universidad de Salamanca, Salamanca, España y 3Cardiología. Hospital Álvaro Cunqueiro, Vigo (Pontevedra), España.
- 11. UTILIDAD DEL ANÁLISIS COMPUTARIZADO DEL ELECTROCARDIOGRAMA PARA PREDECIR LA PRESENCIA DE FIBROSIS EN PACIENTES CON MIOCARDIOPATÍA HIPERTRÓFICA
- Dafne Viliani1, Alberto Cecconi2, Alba Osorio Míguez3, Miguel Spínola Tena4, Pablo Martínez Vives9, Beatriz López Melgar5, Álvaro Montes5, Gianluca de Toffol5, Susana Hernández Muñiz6, Paloma Caballero Sánchez-Robles6, Fernando Alfonso Manterola7, Guillermo José Ortega8 y Luis Jesús Jiménez Borreguero5
1Ospedale Santa Chiara, Trento, Italia, 2Servicio de Cardiología. Hospital Universitario de La Princesa, Madrid, España, 3Universidad Rey Juan Carlos, Madrid, España, 4Unidad de Análisis Datos, Hospital Universitario de La Princesa, Madrid, España, 5Servicio de Cardiología. Hospital Universitario de La Princesa, Madrid, España, 6Servicio de Radiología. Hospital Universitario de La Princesa, Madrid, España, 7Servicio de Cardiología. Hospital Universitario La Princesa, Madrid, España, 8Unidad de Análisis de Datos. Hospital Universitario de La Princesa, Madrid, España, 9Servicio de Cardiología, Hospital Ramón y Caja, Madrid, España.
- 12. RESULTADOS DE UN PROGRAMA DE CRIBADO GENÉTICO POBLACIONAL DE AMILOIDOSIS POR TRANSTIRRETINA HEREDITARIA P.GLU109LYS EN UNA ZONA ENDÉMICA
- Fernando de Frutos Seminario1, Isabel Caraballo Ramos2, Victoria Martínez Chaves2, Adoración María Corral Azor2, M. Solimán Berchíd Débdi2, Daniel de Castro Campos1, Juan Pablo Ochoa Folmer1, Esther González López1, Fernando Domínguez Rodríguez1, Eva Cabrera Romero1, José Ángel Urbano Moral3 y Pablo García Pavía1
1Cardiología. Hospital Universitario Puerta de Hierro, Majadahonda (Madrid), España, 2Centro de Salud Villacarrillo, Villacarrillo (Jaén), España y 3Cardiología. Complejo Hospitalario de Jaén, Jaén, España.
- 13. ENFERMEDAD DE ANDERSON-FABRY DE INICIO INTERMEDIO ASOCIADA A LA VARIANTE P.ARG301GLN EN GLA
- Tomás Ripoll Vera1, Rocío Blanco2, Jaume Pons Linares3, Álvaro Hermida Ameijeiras4, Albina Nowak5, Peter Nordbeck6, Fiama Caimi Martínez1, Elena Fortuny Frau3, Jorge Álvarez Rubio1, Guadalupe Federik1, Carlos Miguel Veras Burgos1 y Teresa Bosch Rovira7
1Cardiología. Hospital Universitario Son Llàtzer, Palma de Mallorca (Illes Balears), España, 2Cardiología. Hospital Italiano de Buenos Aires, Buenos Aires - Argentina, 3Cardiología. Hospital Son Espases, Palma de Mallorca (Illes Balears), España, 4Medicina Interna. Complexo Hospitalario Universitario de Santiago de Compostela, Santiago de Compostela (A Coruña), España, 5Endocrinología. Universidad de Zúrich, Zúrich, Suiza, 6Cardiología. Universidad de Würzburg, Wurzburgo Nordrhein-Westfalen, Alemania y 7Hospital Son Espases, Palma de Mallorca (Illes Balears), España.
Más comunicaciones de los autores
-
Álvarez Martínez, Cristina
- 2 - VALOR PRONÓSTICO Y COMPLICACIONES SEGÚN LA CLASIFICACIÓN DE SCAI EN PACIENTES CON DIFERENTES DISPOSITIVOS DE SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 10 - PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- 9 - PRONOSTICO Y CARACTERÍSTICAS DE LOS PACIENTES CON ENDOCARDITIS INFECCIOSA CON INDICACIÓN QUIRÚRGICA TRATADOS DE FORMA CONSERVADORA
- 2 - EVENTOS INFECCIOSOS TRAS IMPLANTE DE PRÓTESIS PERCUTÁNEA AÓRTICA: ¿ESTAMOS INFRADIAGNOSTICANDO LA ENDOCARDITIS INFECCIOSA SOBRE TAVI?
- 11 - DIFERENCIAS DE GÉNERO EN PACIENTES INGRESADOS POR INSUFICIENCIA CARDIACA. REGISTRO PROSPECTIVO MULTICÉNTRICO
- 15 - MEJORÍA DE LA INSUFICIENCIA MITRAL TRAS EL IMPLANTE DE UNA TAVI: IMPACTO PRONÓSTICO E INFLUENCIA DEL MECANISMO DE LA VALVULOPATÍA
- 10 - INCIDENCIA Y PERFIL EPIDEMIOLÓGICO DE LAS COMPLICACIONES MECÁNICAS DEL INFARTO EN LA ERA ACTUAL
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 3 - TROMBOSIS VALVULAR PROTÉSICA: PRONÓSTICO Y FACTORES DE RIESGO
- Calabria Gallego, María Dolores
- Cañadas Salazar, José
-
Díaz Peláez, Elena
- 10 - PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 3 - ANÁLISIS DE LOS RESULTADOS DE LOS ESTUDIOS DE RESONANCIA MAGNÉTICA CARDIACA EN PACIENTES DEPORTISTAS CON ANTECEDENTES FAMILIARES O SÍNTOMAS CARDIOVASCULARES, ALTERACIONES ELECTROCARDIOGRÁFICAS O ECOCARDIOGRÁFICAS
-
Eiros Bachiller, Rocío
- 3 - IMPACTO DE UNA NUEVA MEDIDA DE FUNCIÓN VENTRICULAR DERECHA POR RESONANCIA MAGNÉTICA. RESULTADOS DEL REGISTRO MULTICÉNTRICO DE INSUFICIENCIA TRICUSPÍDEA GRAVE
- 3 - ANÁLISIS DE LOS RESULTADOS DE LOS ESTUDIOS DE RESONANCIA MAGNÉTICA CARDIACA EN PACIENTES DEPORTISTAS CON ANTECEDENTES FAMILIARES O SÍNTOMAS CARDIOVASCULARES, ALTERACIONES ELECTROCARDIOGRÁFICAS O ECOCARDIOGRÁFICAS
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 5 - APRENDIZAJE AUTOMÁTICO BASADO EN ELECTROCARDIOGRAFÍA Y ECOCARDIOGRAFÍA PARA DIAGNOSTICAR AMILOIDOSIS CARDIACA POR TRANSTIRRETINA
- 4 - CARACTERIZACIÓN DE LA PERFUSIÓN MIOCÁRDICA MEDIANTE TOMOGRAFÍA COMPUTARIZADA ESPECTRAL EN PACIENTES CON AMILOIDOSIS CARDIACA
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 1 - MODERA
- 2 - IMPACTO DE LOS VOLÚMENES Y LA FUNCIÓN DEL VENTRÍCULO DERECHO POR RESONANCIA MAGNÉTICA. RESULTADOS DEL REGISTRO MULTICÉNTRICO DE INSUFICIENCIA TRICUSPÍDEA GRAVE
-
Gallego Delgado, María
- 7 - CARACTERIZACIÓN FENOTÍPICA Y FUNCIONAL DE LA VARIANTE L889V EN EL GEN SCN5A
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 8 - REGISTRO NACIONAL DE MIOCARDITIS MY-SEC: EXPERIENCIA INICIAL
- 4 - CARACTERIZACIÓN DE LA PERFUSIÓN MIOCÁRDICA MEDIANTE TOMOGRAFÍA COMPUTARIZADA ESPECTRAL EN PACIENTES CON AMILOIDOSIS CARDIACA
- 2 - PREVALENCIA DE AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN PACIENTES ANCIANOS CON FIBRILACIÓN AURICULAR DE RECIENTE APARICIÓN
- 5 - APRENDIZAJE AUTOMÁTICO BASADO EN ELECTROCARDIOGRAFÍA Y ECOCARDIOGRAFÍA PARA DIAGNOSTICAR AMILOIDOSIS CARDIACA POR TRANSTIRRETINA
- 5 - IMPACTO DEL GENOTIPO EN LA RESPUESTA A TRATAMIENTO MÉDICO A LARGO PLAZO EN MIOCARDIOPATÍA DILATADA NO ISQUÉMICA
- 5 - PENETRANCIA DE LA MIOCARDIOPATÍA DILATADA EN PORTADORES GENÉTICOS
- 10 - PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 10 - EVALUACIÓN SISTEMÁTICA PROSPECTIVA DE PACIENTES JÓVENES CON IMPLANTACIÓN DE MARCAPASOS IDIOPÁTICA
- García Berrocal, Belén
-
Gayán Ordás, Jara
- 5 - ¿EXISTEN DIFERENCIAS EN EL MANEJO DE LA MIOCARDIOPATÍA HIPERTRÓFICA EN LOS CENTROS CON O SIN UNIDAD MULTIDISCIPLINAR SEGÚN EL REGISTRO DE LA MIOCARDIOPATÍA HIPERTRÓFICA EN CATALUÑA (MIHCAT)?
- 8 - INFLUENCIA DEL SEXO EN LA MIOCARDIOPATÍA HIPERTRÓFICA SEGÚN EL REGISTRO MIHCAT (MIOCARDIOPATIA HIPERTRÓFICA EN CATALUÑA)
- 5 - APRENDIZAJE AUTOMÁTICO BASADO EN ELECTROCARDIOGRAFÍA Y ECOCARDIOGRAFÍA PARA DIAGNOSTICAR AMILOIDOSIS CARDIACA POR TRANSTIRRETINA
- 3 - ALGORITMO INTEGRADO DE DETECCIÓN Y ESTABILIZACIÓN DEL SHOCK CARDIOGÉNICO INCIPIENTE POST INFARTO AGUDO DE MIOCARDIO CON ELEVACIÓN DEL SEGMENTO ST: EXPERIENCIA INICIAL DEL PROTOCOLO PRE-SHOCK
- 15 - USO DEL DESFIBRILADOR AUTOMÁTICO IMPLANTABLE EN PACIENTES CON MIOCARDIOPATÍA HIPERTRÓFICA. DATOS DEL REGISTRO MIHCAT (MIOCARDIOPATÍA HIPERTRÓFICA EN CATALUÑA)
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 12 - EFICACIA DEL CAMBIO INTRAPROCEDIMIENTO A ESTIMULACIÓN DE RAMA IZQUIERDA DESPUÉS DE FRACASO EN INTENTO DE RESINCRONIZACIÓN
- 8 - REGISTRO NACIONAL DE MIOCARDITIS MY-SEC: EXPERIENCIA INICIAL
- 3 - REGISTRO DE LA MIOCARDIOPATÍA HIPERTRÓFICA EN CATALUÑA (MIHCAT): RESULTADOS GLOBALES
- 2 - ESTUDIO VACCINE-CARDITIS: REGISTRO MULTICÉNTRICO ESPAÑOL DE ENFERMEDAD INFLAMATORIA CARDIACA TRAS VACUNACIÓN CONTRA COVID-19. SUBANÁLISIS DE LOS PACIENTES CON DISFUNCIÓN VENTRICULAR EN FASE AGUDA Y SEGUIMIENTO A 6 MESES
- 7 - ESTUDIO VACCINE-CARDITIS: REGISTRO MULTICÉNTRICO ESPAÑOL DE ENFERMEDAD INFLAMATORIA CARDIACA TRAS VACUNACIÓN CONTRA COVID-19. DIFERENCIAS ENTRE LA AFECTACIÓN MIOCÁRDICA Y LA PERICARDITIS AISLADA
- 5 - CONTROL DE LOS FACTORES DE RIESGO CARDIOVASCULAR EN UN ESTUDIO MULTICÉNTRICO DE PACIENTES CON INSUFICIENCIA CARDIACA: A CALL TO ACTION
- 5 - CONTROL DE FACTORES DE RIESGO EN PACIENTES CON ENFERMEDAD RENAL AVANZADA Y SÍNDROME CARDIORRENAL. DATOS DEL REGISTRO CARDIOREN
- 4 - ESTUDIO VACCINE-CARDITIS: REGISTRO MULTICÉNTRICO ESPAÑOL DE ENFERMEDAD INFLAMATORIA CARDIACA TRAS VACUNACIÓN CONTRA COVID-19. ACTUALIZACIÓN Y SEGUIMIENTO A 6 MESES
- Heredero Jung, David Hansoe
-
Hernández Martos, Ángel Víctor
- 11 - DIFERENCIAS EN LA PERFUSIÓN MIOCÁRDICA DE PRIMER PASO MEDIANTE TOMOGRAFÍA COMPUTARIZADA ESPECTRAL EN PACIENTES CON MIOCARDITIS AGUDA
- 2 - VALOR PRONÓSTICO Y COMPLICACIONES SEGÚN LA CLASIFICACIÓN DE SCAI EN PACIENTES CON DIFERENTES DISPOSITIVOS DE SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 14 - INFLUENCIA PRONÓSTICA DE LA INFECCIÓN PREVIA EN PACIENTES CON SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 3 - ANÁLISIS DE LOS RESULTADOS DE LOS ESTUDIOS DE RESONANCIA MAGNÉTICA CARDIACA EN PACIENTES DEPORTISTAS CON ANTECEDENTES FAMILIARES O SÍNTOMAS CARDIOVASCULARES, ALTERACIONES ELECTROCARDIOGRÁFICAS O ECOCARDIOGRÁFICAS
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 8 - ENFERMEDAD RENAL CRÓNICA EN PACIENTES SOMETIDOS A IMPLANTE DE TAVI: PREVALENCIA, PRONÓSTICO Y EVOLUCIÓN DURANTE EL SEGUIMIENTO
- 15 - MEJORÍA DE LA INSUFICIENCIA MITRAL TRAS EL IMPLANTE DE UNA TAVI: IMPACTO PRONÓSTICO E INFLUENCIA DEL MECANISMO DE LA VALVULOPATÍA
- 9 - OPTIMIZACIÓN DEL TRATAMIENTO CUÁDRUPLE EN LA INSUFICIENCIA CARDIACA CON FEVI < 50% DENTRO DE UN PROGRAMA DE REHABILITACIÓN CARDIACA, ¿QUÉ PODEMOS ESPERAR? EXPERIENCIA DE UN CENTRO
- 10 - ANÁLISIS DE LAS CARACTERÍSTICAS Y LOS RESULTADOS DEL CIERRE PERCUTÁNEO DE OREJUELA IZQUIERDA EN PACIENTES ONCOLÓGICOS
- 3 - ANÁLISIS DE LA MORTALIDAD Y DE LAS DIFERENCIAS EN TASAS DE SANGRADO EN PACIENTES ONCOLÓGICOS SOMETIDOS A CIERRE PERCUTÁNEO DE OREJUELA IZQUIERDA
- 5 - CLASIFICACIÓN DE SCAI Y SU VALOR PRONÓSTICO SEGÚN INDICACIÓN Y ETIOLOGÍA EN PACIENTES CON SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- Isidoro García, María
- Martín García, Ana
-
Moreno de Redrojo Cortes, Lucia
- 10 - PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- 10 - INCIDENCIA Y PERFIL EPIDEMIOLÓGICO DE LAS COMPLICACIONES MECÁNICAS DEL INFARTO EN LA ERA ACTUAL
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 11 - DIFERENCIAS DE GÉNERO EN PACIENTES INGRESADOS POR INSUFICIENCIA CARDIACA. REGISTRO PROSPECTIVO MULTICÉNTRICO
- 2 - EVENTOS INFECCIOSOS TRAS IMPLANTE DE PRÓTESIS PERCUTÁNEA AÓRTICA: ¿ESTAMOS INFRADIAGNOSTICANDO LA ENDOCARDITIS INFECCIOSA SOBRE TAVI?
- 9 - PRONOSTICO Y CARACTERÍSTICAS DE LOS PACIENTES CON ENDOCARDITIS INFECCIOSA CON INDICACIÓN QUIRÚRGICA TRATADOS DE FORMA CONSERVADORA
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 2 - VALOR PRONÓSTICO Y COMPLICACIONES SEGÚN LA CLASIFICACIÓN DE SCAI EN PACIENTES CON DIFERENTES DISPOSITIVOS DE SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 15 - MEJORÍA DE LA INSUFICIENCIA MITRAL TRAS EL IMPLANTE DE UNA TAVI: IMPACTO PRONÓSTICO E INFLUENCIA DEL MECANISMO DE LA VALVULOPATÍA
-
Sánchez Fernández, Pedro Luis
- 3 - ANÁLISIS DE LA MORTALIDAD Y DE LAS DIFERENCIAS EN TASAS DE SANGRADO EN PACIENTES ONCOLÓGICOS SOMETIDOS A CIERRE PERCUTÁNEO DE OREJUELA IZQUIERDA
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 7 - CARACTERIZACIÓN FENOTÍPICA Y FUNCIONAL DE LA VARIANTE L889V EN EL GEN SCN5A
- 10 - ANÁLISIS DE LAS CARACTERÍSTICAS Y LOS RESULTADOS DEL CIERRE PERCUTÁNEO DE OREJUELA IZQUIERDA EN PACIENTES ONCOLÓGICOS
- 11 - DIFERENCIAS EN LA PERFUSIÓN MIOCÁRDICA DE PRIMER PASO MEDIANTE TOMOGRAFÍA COMPUTARIZADA ESPECTRAL EN PACIENTES CON MIOCARDITIS AGUDA
- 2 - VALOR PRONÓSTICO Y COMPLICACIONES SEGÚN LA CLASIFICACIÓN DE SCAI EN PACIENTES CON DIFERENTES DISPOSITIVOS DE SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 14 - INFLUENCIA PRONÓSTICA DE LA INFECCIÓN PREVIA EN PACIENTES CON SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 5 - CLASIFICACIÓN DE SCAI Y SU VALOR PRONÓSTICO SEGÚN INDICACIÓN Y ETIOLOGÍA EN PACIENTES CON SOPORTE CIRCULATORIO MECÁNICO DE CORTA DURACIÓN
- 3 - ANÁLISIS DE LOS RESULTADOS DE LOS ESTUDIOS DE RESONANCIA MAGNÉTICA CARDIACA EN PACIENTES DEPORTISTAS CON ANTECEDENTES FAMILIARES O SÍNTOMAS CARDIOVASCULARES, ALTERACIONES ELECTROCARDIOGRÁFICAS O ECOCARDIOGRÁFICAS
- 2 - ABLACIÓN AMBULATORIA DE FIBRILACIÓN AURICULAR: COMPARACIÓN DE CRIOABLACIÓN FRENTE A RADIOFRECUENCIA
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 8 - REALIDAD DE LA TERAPIA MÉDICA NUTRICIONAL EN PACIENTES BAJO SOPORTE MECÁNICO CIRCULATORIO EN UN CENTRO DE TERCER NIVEL
- 2 - SÍNDROME CARDIORRENAL Y ASISTENCIAS VENTRICULARES DE LARGA DURACIÓN: ¿ESCRIBIENDO EL FUTURO?
- 6 - ENSAYO CLÍNICO ALEATORIZADO DE INTERVENCIÓN CON NTPROBNP EN LA TRANSICIÓN DE PACIENTES HOSPITALIZADOS POR INSUFICIENCIA CARDIACA CON FRACCIÓN DE EYECCIÓN CONSERVADA: ESTUDIO NICE
- 3 - INTOLERANCIA AL EJERCICIO EN PACIENTES CON CIRCULACIÓN DE FONTAN: PREDICTORES DE EVENTOS EN EL SEGUIMIENTO
- 10 - PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- 2 - VALOR PREDICTIVO DE LA FRECUENCIA CARDIACA PREVIA A LA TAQUIARRITMIA VENTRICULAR QUE PRODUCE TERAPIA APROPIADA EN LA HOSPITALIZACIÓN POSTERIOR POR INSUFICIENCIA CARDIACA. ANÁLISIS BASADO EN LOS ELECTROGRAMAS ALMACENADOS
- 3 - TROMBOSIS VALVULAR PROTÉSICA: PRONÓSTICO Y FACTORES DE RIESGO
- 10 - INCIDENCIA Y PERFIL EPIDEMIOLÓGICO DE LAS COMPLICACIONES MECÁNICAS DEL INFARTO EN LA ERA ACTUAL
- 8 - ENFERMEDAD RENAL CRÓNICA EN PACIENTES SOMETIDOS A IMPLANTE DE TAVI: PREVALENCIA, PRONÓSTICO Y EVOLUCIÓN DURANTE EL SEGUIMIENTO
- 15 - MEJORÍA DE LA INSUFICIENCIA MITRAL TRAS EL IMPLANTE DE UNA TAVI: IMPACTO PRONÓSTICO E INFLUENCIA DEL MECANISMO DE LA VALVULOPATÍA
- 5 - APRENDIZAJE AUTOMÁTICO BASADO EN ELECTROCARDIOGRAFÍA Y ECOCARDIOGRAFÍA PARA DIAGNOSTICAR AMILOIDOSIS CARDIACA POR TRANSTIRRETINA
- 4 - CARACTERIZACIÓN DE LA PERFUSIÓN MIOCÁRDICA MEDIANTE TOMOGRAFÍA COMPUTARIZADA ESPECTRAL EN PACIENTES CON AMILOIDOSIS CARDIACA
- 11 - CRIBADO POBLACIONAL DE DISLIPEMIA EN UNAS JORNADAS DE PREVENCIÓN REALIZADAS EN EL ÁMBITO HOSPITALARIO
- 9 - OPTIMIZACIÓN DEL TRATAMIENTO CUÁDRUPLE EN LA INSUFICIENCIA CARDIACA CON FEVI < 50% DENTRO DE UN PROGRAMA DE REHABILITACIÓN CARDIACA, ¿QUÉ PODEMOS ESPERAR? EXPERIENCIA DE UN CENTRO
- 2 - EVENTOS INFECCIOSOS TRAS IMPLANTE DE PRÓTESIS PERCUTÁNEA AÓRTICA: ¿ESTAMOS INFRADIAGNOSTICANDO LA ENDOCARDITIS INFECCIOSA SOBRE TAVI?
- 9 - PRONOSTICO Y CARACTERÍSTICAS DE LOS PACIENTES CON ENDOCARDITIS INFECCIOSA CON INDICACIÓN QUIRÚRGICA TRATADOS DE FORMA CONSERVADORA
- 2 - INFLUENCIA DEL SEXO FEMENINO EN EL PERFIL CLÍNICO-EPIDEMIOLÓGICO Y PRONÓSTICO DEL IAMCEST. ANÁLISIS DE UNA COHORTE HISTÓRICA
-
Villacorta Argüelles, Eduardo
- 7 - CARACTERIZACIÓN FENOTÍPICA Y FUNCIONAL DE LA VARIANTE L889V EN EL GEN SCN5A
- 3 - AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN EL ANCIANO, LA IMPORTANCIA DEL ESTUDIO GENÉTICO
- 10 - PREVALENCIA Y REPERCUSIÓN DE LA HIPERTROFIA DE VENTRÍCULO DERECHO ENTRE LOS PACIENTES CON DIAGNÓSTICO DE MIOCARDIOPATÍA HIPERTRÓFICA Y ESTUDIO GENÉTICO POSITIVO
- 3 - TROMBOSIS VALVULAR PROTÉSICA: PRONÓSTICO Y FACTORES DE RIESGO
- 2 - VALIDACIÓN DE LOS CRITERIOS ECOCARDIOGRÁFICOS DIAGNÓSTICOS DE AMILOIDOSIS CARDIACA EN PACIENTES CON AMILOIDOSIS POR TRASNTIRRETINA
- 2 - PREVALENCIA DE AMILOIDOSIS CARDIACA POR TRANSTIRRETINA EN PACIENTES ANCIANOS CON FIBRILACIÓN AURICULAR DE RECIENTE APARICIÓN
- 9 - PRONOSTICO Y CARACTERÍSTICAS DE LOS PACIENTES CON ENDOCARDITIS INFECCIOSA CON INDICACIÓN QUIRÚRGICA TRATADOS DE FORMA CONSERVADORA
- 2 - EL ANÁLISIS EXHAUSTIVO DE RMC MEJORA LA ESTRATIFICACIÓN PRONÓSTICA EN NO COMPACTACIÓN DEL VENTRÍCULO IZQUIERDO
- 3 - EFECTO FUNDADOR DE LA VARIANTE GENÉTICA P.ASN271ILE EN TNNT2 EN A CORUÑA ASOCIADA A MIOCARDIOPATÍA HIPERTRÓFICA DE PRONÓSTICO BENIGNO
- 5 - APRENDIZAJE AUTOMÁTICO BASADO EN ELECTROCARDIOGRAFÍA Y ECOCARDIOGRAFÍA PARA DIAGNOSTICAR AMILOIDOSIS CARDIACA POR TRANSTIRRETINA
