SEC 2024 - El Congreso de la Salud Cardiovascular
Introducción
Dr. José María de la Torre Hernández
Presidente del Comité Científico del Congreso. Vicepresidente de la SEC
Comités ejecutivo, organizador y científico
Comité de evaluadores
Listado completo de comunicaciones
Índice de autores
6019. Miocardiopatías
6019-115. Genética de la miocardiopatía hipertrófica en Andalucía
1Hospital Universitario Virgen del Rocío, Sevilla, España, 2Hospital Universitario Virgen de Valme, Sevilla, España, 3Hospital Regional Universitario de Málaga, Málaga, España, 4Hospital Universitario Virgen de las Nieves, Granada, España, 5Hospital Comarcal de Melilla, Melilla, España, 6Hospital Clínico Universitario Virgen de la Victoria, Málaga, España y 7Complejo Hospitalario Torrecárdenas, Almería, España.
Introducción y objetivos: La miocardiopatía hipertrófica (MCH) es la cardiopatía familiar más frecuente, con una morbimortalidad importante secundaria a manifestaciones clínicas graves como la insuficiencia cardiaca y la muerte súbita. Los principales genes implicados en su etiología codifican proteínas sarcoméricas. La variabilidad fenotípica y genotípica es una característica definitoria de esta enfermedad. El registro RACAGEN, como proyecto multicéntrico andaluz, pretende dar luz a las características particulares de la genética, el tratamiento y la evolución clínica y pronóstica de la MCH en nuestra comunidad. Objetivos: describir los rasgos genéticos característicos de la MCH en nuestra región.
Métodos: Estudio observacional retrospectivo multicéntrico realizado por las Unidades de Cardiopatías Familiares de 6 centros de nuestra comunidad. Se recogieron 504 pacientes con miocardiopatía hipertrófica, reclutados desde enero de 2021 a abril de 2024. Se analizaron los resultados genéticos y se identificaron variables que se asociaran con una mayor rentabilidad del estudio.
Resultados: La edad media fue de 53 ± 16 años. 207 pacientes (41%) tenían antecedentes familiares de MCH, y 128 (25%) tenían antecedentes de muerte súbita en la familia. El estudio genético fue positivo en 188 pacientes (37,3%). VUS (variantes de significado incierto) fueron detectadas en 113 pacientes (22,4%). Los principales genes afectados fueron MYBPC3 (40%), MYH7 (30,8%) seguidos por las troponinas: TNNT2 (11,4%) TNNI 3 (3,8%) y TNNC1 (2,2%). Las variantes más frecuentemente encontradas fueron (p.Asp778Glu) en MYH7 (14 pacientes) y p. Arg92Trp en TNNT2 (12). La edad menor a 45 años, los antecedentes familiares y de muerte súbita y la ausencia de factores de riesgo cardiovascular se asociaron a estudio genético positivo. El género o la presencia de síntomas no lo hicieron. En el estudio multivariante, los antecedentes familiares y la ausencia de factores de riesgo mantuvieron significación (p < 0,001 y 0,013 respectivamente).
|
Variables asociadas a rentabilidad del estudio genético |
|||||||
|
Pacientes/media |
%/DS |
Sí pos |
No neg |
p |
OR |
Multivariante p |
|
|
Antecedentes familiares |
207 |
41% |
114 (55,1%) |
64 (24%) |
< 0,001 |
3,8 (2,5-5,6) |
< 0,001 |
|
AF muerte súbita |
128 |
25,4% |
63 (49%) |
113 (32,7%) |
0,001 |
1,99 (1,3-3) |
|
|
Edad < 45 años |
79 |
29% |
79 (54%) |
109 (30,4%) |
< 0,001 |
2,7 (1,8-4) |
|
|
FRCV |
113 |
22,4% |
21 (8%) |
10 (45%) |
0,006 |
3,6 (1,3-9,5) |
0,013 |
|
Sexo mujer |
175 |
34,7% |
75 (43%) |
113 (34,3%) |
0,06 |
|
|
|
AF: antecedentes familiares; FRCV: factores de riesgo cardiovascular. |
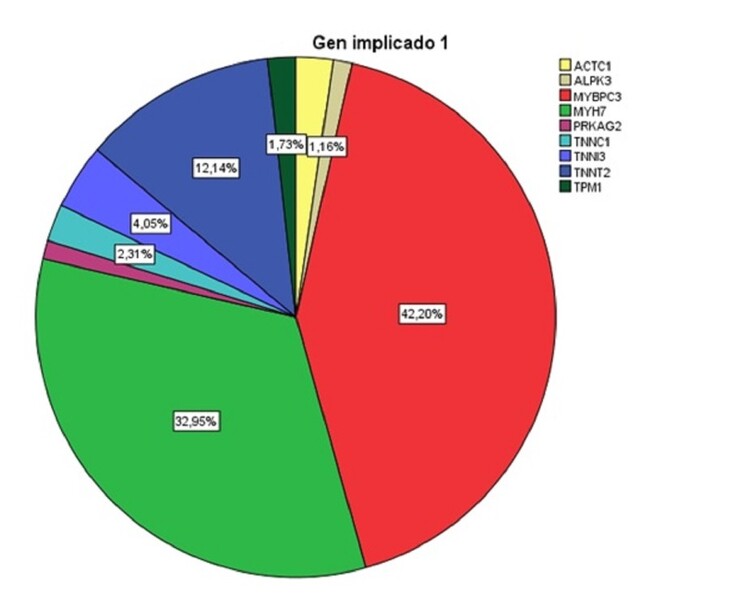
Resultados estudio genético.
Conclusiones: Las mutaciones en MYBPC3 y MYH7 fueron las predominantes, con una rentabilidad del estudio del 37%. La presencia de factores de riesgo cardiovascular y la ausencia de antecedentes familiares se asociaron a una menor rentabilidad del estudio. La evolución de nuestro registro está ayudando a optimizar el estudio familiar de la MCH y a identificar correlaciones genotipo-fenotipo propias de nuestra región.
Comunicaciones disponibles de "6019. Miocardiopatías"
- 6019-97. Uso y valor pronóstico del Holter-ECG en pacientes con miocardiopatía dilatada
- Lidia María Carrillo Mora1, José Francisco Gil Fernández2, Mario Hernández Iniesta1, Alba María García García1, Noelia Fernández Villa1, Juan Ramón Gimeno Blanes1, Beatriz Pérez Martínez3, Carmen Muñoz Esparza1, Francisca María Muñoz Franco4 y María Sabater Molina1
1Hospital Clínico Universitario Virgen de la Arrixaca, El Palmar (Murcia), España, 2Hospital Clínico Universitario de Valladolid, Valladolid, España, 3Hospital Virgen del Castillo, Yecla (Murcia), España y 4Hospital Comarcal del Noroeste, Caravaca de la Cruz (Murcia), España.
- 6019-98. Características clínicas y de imagen de la miocardiopatía dilatada no isquémica en adultos mayores: papel del bloqueo de rama izquierda como posible etiología
- Pablo Zulet Fraile, María Alejandra Restrepo Córdoba, Josebe Goirigolzarri Artaza, Iván Sánchez Izquierdo, Marcos Ferrández Escarabajal, Fabián Islas Ramírez, José Alberto de Agustín Loeches y Carmen Olmos Blanco
Instituto Cardiovascular. Hospital Clínico San Carlos, Madrid, España.
- 6019-99. Incidencia y utilidad de la disfunción del ventrículo derecho en la indicación de implante de DAI en portadores de mutaciones desmosomales
- Arancha Díaz Expósito, Amalio Ruiz Salas, M. Carmen Medina Palomo, Germán Berteli García, Javier Muñiz Sáenz-Díez, Alberto Barrera Cordero, Ainhoa Robles Mezcua, Alejandro Isidoro Pérez Cabeza, Clara Jiménez Rubio, Francisco Javier Alzueta Rodríguez y José Manuel García Pinilla
Hospital Clínico Universitario Virgen de la Victoria, Málaga, España.
- 6019-100. ¿Cómo se trata en Cataluña la obstrucción del tracto de salida del ventrículo izquierdo en la miocardiopatía hipertrófica?
- Pablo Carrión Montaner1, Laura Guillamón Torán2, Jara Gayán Ordás3, Marta Campreciós Crespo4, Eva Guillaumet2, Núria Casanovas2, Claudia Scardino5, Germán Cediel Calderón6, Montserrat Cardona Ollé7, Sonia Ruíz Bustillo8, Coloma Tiron de Llano9, Montserrat Ayats Delgado10, Paola Rojas1, Gabriel Torres Ruiz1 y Antonio Martínez Rubio1
1Cardiología. Corporació Sanitària Parc Taulí, Sabadell (Barcelona), España, 2Cardiología, Departamento de Imagen Cardiaca. Corporació Sanitària Parc Taulí, Sabadell (Barcelona), España, 3Cardiología. Hospital Universitari Arnau de Vilanova, Lleida, España, 4Cardiología. Hospital de la Santa Creu i Sant Pau, Barcelona, España, 5Cardiología. Hospital Universitario Joan XXIII, Tarragona, España, 6Cardiología. Hospital Universitari Germans Trias i Pujol, Badalona (Barcelona), España, 7Cardiología. Complex Hospitalari Moisès Broggi, Barcelona, España, 8Cardiología. Hospital del Mar, Barcelona, España, 9Cardiología. Hospital Universitario Dr. Josep Trueta, Girona, España y 10Cardiología. Hospital General de Granollers, Granollers (Barcelona), España.
- 6019-101. Fibrilación auricular en miocardiopatía hipertrófica apical ¿más prevalente y peligrosa?
- David Cordero Pereda1, Sandra González Martín2, Simón Novo Flores2 y Paloma Remior Pérez1
1Unidad de Cardiopatías Familiares. Servicio de Cardiología. Hospital Universitario Ramón y Cajal, Madrid, España y 2Servicio de Cardiología. Instituto Ramón y Cajal de Investigación Sanitaria, Madrid, España.
- 6019-102. Utilidad del ecocardiograma de esfuerzo en la valoración de pacientes con miocardiopatía hipertrófica
- Tomás Ripoll Vera1, Alba Corralejo del Peso2, Carlos Miguel Veras Burgos1, Jorge Álvarez Rubio1, Joan Torres Marqués1, Virginia Ruiz Pizarro1, Marta Alamar Cervera1, Margarita Esther Moranta Ribas1, Hugo del Castillo Carnevali1, David Cremer Luengos1, José María Gámez Martínez1 y Santiago Magnani Raganato1
1Servicio de Cardiología. Hospital Universitario Son Llàtzer, Palma de Mallorca (Illes Balears), España y 2Facultad de Medicina. Universidad de las Islas Baleares, Palma de Mallorca (Illes Balears), España.
- 6019-103. Incidencia y progresión de la afectación del ventrículo izquierdo en pacientes con miocardiopatía arritmogénica
- Arancha Díaz Expósito, Amalio Ruiz Salas, M. Carmen Medina Palomo, Germán Berteli García, Javier Muñiz Sáenz-Díez, Alberto Barrera Cordero, Ainhoa Robles Mezcua, Alejandro Isidoro Pérez Cabeza, Clara Jiménez Rubio, Francisco Javier Alzueta Rodríguez y José Manuel García Pinilla
Hospital Clínico Universitario Virgen de la Victoria, Málaga, España.
- 6019-104. Score Mayo como herramienta de acceso a consulta específica de miocardiopatía hipertrófica
- Marcos García Jambrina
Cardiología. Hospital San Pedro de Alcántara, Cáceres, España
- 6019-105. Evaluación de la incidencia de cardiopatía en pacientes con lipodistrofia familiar parcial tipo 2. Datos de un área hospitalaria en la vida real
- Carlos Perea Alfaro, Marina Fernández Aragón y Ana José Manovel Sánchez
Cardiología. Hospital Juan Ramón Jiménez, Huelva, España.
- 6019-106. Miocardiopatía HCN4: el extraordinario caso homocigoto
- José Francisco Gil Fernández1, Lidia María Carrillo Mora2, Francisco Castro García3, Santiago Escudero Cárceles3, Serena Evelina Margaretha Munteanu4, María Sabater Molina4 y Juan Ramón Gimeno Blanes2
1Cardiología. Hospital Clínico Universitario de Valladolid, Valladolid, España, 2Cardiología. Hospital Clínico Universitario Virgen de la Arrixaca, Murcia, España, 3Pediatría. Hospital Clínico Universitario Virgen de la Arrixaca, Murcia, España y 4Instituto Murciano de Investigación Biosanitaria Virgen de la Arrixaca, Murcia, España.
- 6019-107. Variantes patogénicas del gen titina y miocardiopatía dilatada: explorando vínculos genéticos y clínicos
- Mónica García Monsalvo1, Judith Calle Pérez1, Javier Muñoz Sánchez2, Lorena Martín Bartolomé2, Alba Martín Morán2, Luis Miguel Rincón Díaz1, Rocío Eiros Bachiller1, Belén García Berrocal3, David Hansoe Heredero Jung3, Sandra Milagros Lorenzo Hernández3, Fabián Blanco Fernández1, M. José Ruiz Olgado4, Pedro Luis Sánchez Fernández1, María Gallego Delgado1 y Eduardo Villacorta Argüelles1
1Cardiología. Hospital Clínico Universitario de Salamanca, Salamanca, España, 2Universidad de Salamanca, Salamanca, España, 3Bioquímica Clínica/Análisis Clínicos. Hospital Clínico Universitario de Salamanca, Salamanca, España y 4Cardiología. Hospital Virgen de la Concha, Zamora, España.
- 6019-108. Influencia de las anomalías del aparato subvalvular y de la válvula mitral sobre la eficacia del tratamiento para la obstrucción dinámica del tracto de salida en pacientes con miocardiopatía hipertrófica
- Marta Andrés Sierra, Jesús Piqueras Flores, Beatriz Jiménez Rubio, Emilio Blanco López, Pablo Soto Martín, Andrez Felipe Cubides Novoa, Maeve Soto Pérez, Laura Montesinos Vinader, Cinthya Nuez Cuartango, Daniel Águila Gordo y Cristina Mateo Gómez
Cardiología. Hospital General Universitario de Ciudad Real, Ciudad Real, España.
- 6019-109. La miocardiopatía hipertrófica en Canarias, ¿somos diferentes?
- Julio Vázquez Reguera, Aridane Cárdenes León y Eduardo Caballero Dorta
Hospital Universitario de Gran Canaria Dr. Negrín, Las Palmas de Gran Canaria (Las Palmas), España.
- 6019-110. Miocardiopatía hipertrófica y eventos cardiológicos adversos
- Charlotte Boillot1, Joaquín Sánchez-Prieto Castillo1, Belén Santos González1, José Porcel Maleno2, Andrea González Pigorini1, Ana Díaz Rojo1, Patricia del Valle Tabernero1, Natalia Navarro Pelegrini1, Ainhoa Aguinaga Mendibil1, José Manuel Martínez Palomares1, Irene Torres Chilleron1, Gabriel Rivera Saltos1, Guillermo Galeote Escalera1, Lucía Villafáfila Martínez1 y Joan Ramon Enseñat1
1Hospital Universitario de Toledo, Toledo, España y 2Hospital Universitario Puerta de Hierro, Madrid, España.
- 6019-111. Pronóstico a medio plazo de pacientes con síndrome de tako-tsubo
- Lucas Barreiro Mesa, Nerea Aguayo Caño, Álvaro Roldán Guerra, Cristina Urbano Sánchez y Rafael González Manzanares
Hospital Universitario Reina Sofía, Córdoba, España.
- 6019-112. Electrocardiograma como herramienta diagnóstica entre enfermedad Fabry y miocardiopatía hipertrófica sarcomérica
- José Gregorio Soto Rojas1, Beatriz Girela Pérez1, Carlos Gómez Navarro1, Remedios Garofano López2 y Ricardo Fajardo Molina1
1Hospital Universitario Torrecárdenas, Almería, España y 2Servicio de Nefrología. Hospital Universitario Torrecárdenas, Almería, España.
- 6019-113. Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- M. Esperanza Donoso Muñoz1, María Luisa Peña Peña1, Helena Llamas Gómez1, Miguel Barranco Gutiérrez1, Lidia Rodero Barcos1, Pablo Martín Marín1, David Grimaldos Parra1, Rosa Macías Ruíz2, María José Romero Reyes3, Ana González González4, José Gregorio Soto Rojas5, Noemí González Cruces6, Marta Martín Vélez1, Javier Azcona Sousa1 y Juan Manuel Aragón González1
1Hospital Universitario Virgen del Rocío, Sevilla, España, 2Hospital Universitario Virgen de las Nieves, Granada, España, 3Hospital Universitario Virgen de Valme, Sevilla, España, 4Hospital Regional Universitario Carlos Haya, Málaga, España, 5Complejo Hospitalario Torrecárdenas, Almería, España y 6Hospital Comarcal de Melilla, Melilla, España.
- 6019-114. Cohorte nacional de sospecha de miocarditis Pre-MYO: características basales de los 100 primeros casos
- José Javier Tercero Fajardo1, Fernando Domínguez Rodríguez2, Ana Belén Maestre Hernández3, Marcelo Sanmartín Fernández4, Ángel Manuel Iniesta Manjavacas5, Pablo Pastor Pueyo6, Silvia López Fernández7, Teresa Sola Moreno8, María Martín Fernández9, Juan Górriz Magaña10, María José Romero Reyes11, Fernando Alfonso Manterola12, Jesús Piqueras Flores13, M. José Ruiz Olgado14 y Domingo Pascual-Figal1
1Cardiología. Hospital Clínico Universitario Virgen de la Arrixaca, Murcia, España, 2Cardiología. Hospital Universitario Puerta de Hierro, Majadahonda (Madrid), España, 3Cardiología Clínica y Experimental. Instituto Murciano de Investigación Biosanitaria Virgen de la Arrixaca, Murcia, España, 4Cardiología. Hospital Universitario Ramón y Cajal, Madrid, Madrid, España, 5Cardiología. Hospital Universitario La Paz, Madrid, España, 6Cardiología. Hospital Universitari Arnau de Vilanova, Lleida, España, 7Cardiología. Hospital Universitario Virgen de las Nieves, Granada, España, 8Cardiología. Hospital Clínico Universitario Lozano Blesa, Zaragoza, España, 9Cardiología. Hospital Universitario Central de Asturias, Oviedo (Asturias), España, 10Cardiología. Hospital Militar Gómez Ulla, Madrid, España, 11Cardiología. Hospital Universitario Virgen de Valme, Sevilla, España, 12Cardiología. Hospital Universitario de la Princesa, Madrid, España, 13Cardiología. Hospital General Universitario de Ciudad Real, Ciudad Real, España y 14Cardiología. Complejo Asistencial de Zamora, Zamora, España.
- 6019-115. Genética de la miocardiopatía hipertrófica en Andalucía
- Pablo Martín Marín1, Helena Llamas Gómez1, David Grimaldos Parra1, María José Romero Reyes2, Ainhoa Robles Mezcua3, Rosa Macías Ruíz4, Noemí González Cruces5, Ana María González González6, José Gregorio Soto Rojas7 y María Luisa Peña Peña1
1Hospital Universitario Virgen del Rocío, Sevilla, España, 2Hospital Universitario Virgen de Valme, Sevilla, España, 3Hospital Regional Universitario de Málaga, Málaga, España, 4Hospital Universitario Virgen de las Nieves, Granada, España, 5Hospital Comarcal de Melilla, Melilla, España, 6Hospital Clínico Universitario Virgen de la Victoria, Málaga, España y 7Complejo Hospitalario Torrecárdenas, Almería, España.
- 6019-116. Papel del estudio genético en una cohorte de pacientes con miocardiopatía dilatada sometidos a trasplante cardiaco
- Miguel Barranco Gutiérrez1, Pablo Martín Marín1, María Luisa Peña Peña2, Helena Llamas Gómez2, José Manuel Sobrino Márquez3, Santiago Fernández-Gordón Sánchez1, Fernando Gavilán Domínguez1, Pablo Rojas Romero1, David Grimaldos Parra1 y Ernesto Ruiz Pereira1
1Servicio de Cardiología, 2Unidad de Cardiopatías Familiares. Servicio de Cardiología y 3Unidad de Trasplante Cardiaco, Servicio de Cardiología. Hospital Universitario Virgen del Rocío, Sevilla, España.
- 6019-117. Miocardiopatía de estrés en el postrasplante hepático inmediato: ¿mito o realidad?
- José Miguel Rojo Pérez, Ramón Rubí Matamoros, Eugenio Picazo Feu, Clara Nuevo Gallardo, Javier Corral Macías, Rosa Navarro Romero, Natalia Torrijos López, Andrea Alonso Campana, Miguel Ángel Vallejo Ruiz, Ana Belén Merón Pino, Ana María Martínez Carapeto, María Yuste Domínguez, Juan Manuel Durán Guerrero, Juan Manuel Nogales Asensio y M. Eugenia Fuentes Cañamero
Servicio de Cardiología. Complejo Hospitalario Universitario de Badajoz, Badajoz, España.
- 6019-118. Impacto de la no compactación ventricular en el pronóstico de la miocardiopatía hipertrófica y dilatada
- Pablo Soto Martín1, Jesús Piqueras Flores2, Jorge Martínez del Río2, Daniel Águila Gordo1, Cristina Mateo Gómez1, Maeve Soto Pérez1, Andrez Felipe Cubides Novoa1, Emilio Blanco López1, Marta Andrés Sierra1, Beatriz Jiménez Rubio1, Cynthia Nuez Cartango1 y Laura Montesinos Vinader1
1Servicio de Cardiología y 2Servicio de Cardiología. Unidad de Cardiopatías Familiares. Hospital General Universitario de Ciudad Real, Ciudad Real, España.
- 6019-119. Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- Miguel Barranco Gutiérrez1, Helena Llamas Gómez1, David Grimaldos Parra1, María Luisa Peña Peña1, Ainhoa Robles Mezcua2, Carlos Gómez Navarro3, Noemí González Cruces4, María José Romero Reyes5, Rosa Macías Ruíz6, Ana María González González7, Fátima Esteban Martínez8, Fernando Gavilán Domínguez1, Santiago Fernández-Gordón Sánchez1 y Pablo Romero Rojas1
1Servicio de Cardiología. Hospital Universitario Virgen del Rocío, Sevilla, España, 2Servicio de Cardiología. Hospital Clínico Universitario Virgen de la Victoria, Málaga, España, 3Servicio de Cardiología. Hospital Universitario Torrecárdenas, Almería, España, 4Servicio de Cardiología. Hospital Comarcal de Melilla, Melilla, España, 5Servicio de Cardiología. Hospital Universitario Virgen de Valme, Sevilla, España, 6Servicio de Cardiología. Hospital Universitario Virgen de las Nieves, Granada, España, 7Servicio de Cardiología. Hospital Regional Universitario Carlos Haya, Málaga, España y 8Servicio de Cardiología. Hospital Universitario Reina Sofía, Córdoba, España.
- 6019-120. Mejoría de FEVI en taquimiocardiopatía: predictores y su implicación
- David Grimaldos Parra, Carlos Palacios Castelló, Iris Esteve Ruiz, Antonio Aranda Dios, Antonio Grande Trillo y Diego Rangel Sousa
Hospital Universitario Virgen del Rocío, Sevilla, España.
- 6019-121. Ablación septal con alcohol. Experiencia en nuestro centro
- Diego Matellán Alonso, Ana García Martín, Paloma Remior Pérez, Sandra González Martín, José Luis Mestre Barceló, Covadonga Fernández Golfín, José Luis Zamorano Gómez, Sonia Antoñana Ugalde y David Cordero Pereda
Servicio de Cardiología. Hospital Universitario Ramón y Cajal, Madrid, España.
- 6019-122. Trasplantes cardiacos en Canarias y su relación con las miocardiopatías familiares
- Claudia Peña Saavedra, Aridane Cárdenes León, María del Val Groba Marco, Mario Galván Ruiz, Miguel Fernández de Sanmamed Girón, Paula Luján Perez, Daesub Chung Kwon, Antonio García Quintana y Eduardo Caballero Dorta
Servicio de Cardiología. Hospital Universitario de Gran Canaria Dr. Negrín, Las Palmas de Gran Canaria (Las Palmas), España.
Más comunicaciones de los autores
-
González Cruces, Noemí
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
-
González González, Ana María
- 6011-72 - Descripción de amiloidosis cardiaca TTR en Andalucía. Estudio multicéntrico
- 6011-65 - Análisis de una cohorte andaluza de amiloidosis cardiaca por transtirretina. Susceptibilidad y selección de tratamiento con tafamidis
- 6011-71 - Evaluación de las puntuaciones multiparamétricas en una cohorte de pacientes con amiloidosis cardiaca por transtirretina
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 4022-3 - Cambios morfofuncionales, tisulares y de captación cardiaca mediante imagen de resonancia magnética y gammagrafía cardiaca en amiloidosis ATTR hereditaria tras un año de tratamiento con un silenciador génico
- 6117-14 - Aspectos pronósticos y predicción de eventos adversos en el seguimiento a medio plazo tras miocarditis aguda
-
Grimaldos Parra, David
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6019-116 - Papel del estudio genético en una cohorte de pacientes con miocardiopatía dilatada sometidos a trasplante cardiaco
- 6019-120 - Mejoría de FEVI en taquimiocardiopatía: predictores y su implicación
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 5002-5 - Rentabilidad del estudio genético en la miocardiopatía hipertrófica en una unidad especializada
- 6071-448 - Taquimiocardiopatía. ¿Control de ritmo o de frecuencia?
-
Llamas Gómez, Helena
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6121-11 - Evaluación del rendimiento diagnóstico de diferentes criterios ecocardiográficos de deformación en pacientes con amiloidosis cardiaca por transtirretina
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6011-72 - Descripción de amiloidosis cardiaca TTR en Andalucía. Estudio multicéntrico
- 6113-5 - Alteraciones de la conducción, arritmias y miocardiopatía dilatada asociadas a una mutación no descrita en el gen TNNI3K
- 6113-10 - Rentabilidad del estudio genético en pacientes trasplantados por miocardiopatía dilatada
- 6113-7 - Descripción del fenotipo asociado a una nueva variante del gen MYBPC3 relacionado con la miocardiopatía hipertrófica
- 5002-5 - Rentabilidad del estudio genético en la miocardiopatía hipertrófica en una unidad especializada
- 6011-71 - Evaluación de las puntuaciones multiparamétricas en una cohorte de pacientes con amiloidosis cardiaca por transtirretina
- 6019-116 - Papel del estudio genético en una cohorte de pacientes con miocardiopatía dilatada sometidos a trasplante cardiaco
-
Macías Ruíz, Rosa
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 4030-3 - Valor predictivo del electrocardiograma y la resonancia magnética en la localización de las taquicardias ventriculares monomórficas en el estudio electrofisiológico en pacientes con miocardiopatía hereditaria con afectación del ventrículo izquierdo
- 6120-7 - Análisis de los hallazgos y la efectividad del Holter insertable para el estudio del síncope dentro de un servicio de cardiología con enfoque intervencionista en pacientes con bloqueo bifascicular y presentación cardiogénica
- 5002-11 - Caracterización y pronóstico de la amiloidosis cardiaca hereditaria por transtirretina en España
- 4016-3 - Origen de las taquicardias ventriculares monomórficas en miocardiopatía hereditaria con afectación de ventrículo izquierdo: correlación genotipo-fenotipo
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 4030-4 - Ausencia de realce tardío de gadolinio y pronóstico en pacientes con miocardiopatía dilatada no isquémica tratados con terapia de resincronización cardiaca
-
Martín Marín, Pablo
- 5002-5 - Rentabilidad del estudio genético en la miocardiopatía hipertrófica en una unidad especializada
- 6113-7 - Descripción del fenotipo asociado a una nueva variante del gen MYBPC3 relacionado con la miocardiopatía hipertrófica
- 6113-10 - Rentabilidad del estudio genético en pacientes trasplantados por miocardiopatía dilatada
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6019-116 - Papel del estudio genético en una cohorte de pacientes con miocardiopatía dilatada sometidos a trasplante cardiaco
-
Peña Peña, María Luisa
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6121-11 - Evaluación del rendimiento diagnóstico de diferentes criterios ecocardiográficos de deformación en pacientes con amiloidosis cardiaca por transtirretina
- 6011-72 - Descripción de amiloidosis cardiaca TTR en Andalucía. Estudio multicéntrico
- 5002-5 - Rentabilidad del estudio genético en la miocardiopatía hipertrófica en una unidad especializada
- 6019-116 - Papel del estudio genético en una cohorte de pacientes con miocardiopatía dilatada sometidos a trasplante cardiaco
- 6011-71 - Evaluación de las puntuaciones multiparamétricas en una cohorte de pacientes con amiloidosis cardiaca por transtirretina
- 6113-10 - Rentabilidad del estudio genético en pacientes trasplantados por miocardiopatía dilatada
- 6113-5 - Alteraciones de la conducción, arritmias y miocardiopatía dilatada asociadas a una mutación no descrita en el gen TNNI3K
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6011-65 - Análisis de una cohorte andaluza de amiloidosis cardiaca por transtirretina. Susceptibilidad y selección de tratamiento con tafamidis
- 6030-185 - Corrección de los defectos de la válvula mitral como técnica asociada a miectomía septal en pacientes con miocardiopatía hipertrófica: experiencia de un centro
- 6113-7 - Descripción del fenotipo asociado a una nueva variante del gen MYBPC3 relacionado con la miocardiopatía hipertrófica
-
Robles Mezcua, Ainhoa
- 6011-72 - Descripción de amiloidosis cardiaca TTR en Andalucía. Estudio multicéntrico
- 6104-15 - Efecto de sacubitrilo/valsartán en el remodelado cardiaco: desde los biomarcadores moleculares a las técnicas de imagen
- 4017-7 - Utilidad del análisis del vector de impedancia bioeléctrica para valoración de la hidratación y su implicación pronóstica en pacientes incluidos en nuestra reciente unidad cardiorrenal-metabólica
- 5002-7 - Genotipos de alto riesgo en miocardiopatía dilatada: más allá de las arritmias
- 5002-1 - Modera
- 6011-71 - Evaluación de las puntuaciones multiparamétricas en una cohorte de pacientes con amiloidosis cardiaca por transtirretina
- 6019-103 - Incidencia y progresión de la afectación del ventrículo izquierdo en pacientes con miocardiopatía arritmogénica
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6019-99 - Incidencia y utilidad de la disfunción del ventrículo derecho en la indicación de implante de DAI en portadores de mutaciones desmosomales
- 6121-11 - Evaluación del rendimiento diagnóstico de diferentes criterios ecocardiográficos de deformación en pacientes con amiloidosis cardiaca por transtirretina
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 4022-3 - Cambios morfofuncionales, tisulares y de captación cardiaca mediante imagen de resonancia magnética y gammagrafía cardiaca en amiloidosis ATTR hereditaria tras un año de tratamiento con un silenciador génico
-
Romero Reyes, María José
- 6062-399 - Asociación entre las características clínicas y morfológicas de la válvula aórtica bicúspide y la aortopatía
- 6110-11 - Factores clínicos y morfológicos asociados a la presencia de estenosis aórtica en pacientes con válvula aórtica bicúspide
- 6019-119 - Caracterización de una cohorte multicéntrica de pacientes con miocardiopatía hipertrófica candidatos a tratamiento con mavacamtén
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6062-400 - Características y diferencias por sexo en una cohorte amplia de pacientes con válvula aórtica bicúspide
- 6019-114 - Cohorte nacional de sospecha de miocarditis Pre-MYO: características basales de los 100 primeros casos
-
Soto Rojas, José Gregorio
- 6019-113 - Diferencias en el tratamiento y manejo de la miocardiopatía hipertrófica por edad en una cohorte multicéntrica andaluza
- 6004-4 - Fibrilación auricular de novo en pacientes jóvenes como red flag de miocardiopatía o canalopatía. Rendimiento del estudio genético
- 6019-115 - Genética de la miocardiopatía hipertrófica en Andalucía
- 6123-14 - Biomarcadores e implicaciones pronósticas en pacientes ingresados por síndrome coronario agudo
- 6064-411 - VExUS en el fenotipado de la congestión de pacientes ingresados por IC e implicaciones pronósticas
- 6019-112 - Electrocardiograma como herramienta diagnóstica entre enfermedad Fabry y miocardiopatía hipertrófica sarcomérica
