SEC 2024 - El Congreso de la Salud Cardiovascular
Introducción
Dr. José María de la Torre Hernández
Presidente del Comité Científico del Congreso. Vicepresidente de la SEC
Comités ejecutivo, organizador y científico
Comité de evaluadores
Listado completo de comunicaciones
Índice de autores
6113. Novedades en cardiogenética
6113-6. Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
1Hospital Universitario La Fe, Valencia, España, 2Cardiopatías Familiares. Hospital Universitario La Fe, Valencia, España, 3Genomic Unit. Health Research Institute Hospital La Fe (IIS La Fe), Valencia, España, 4Health in Code, A Coruña (A Coruña), España y 5Hospital Clínico Universitario de Valladolid, Valladolid, España.
Introducción y objetivos: El gen RBM20 codifica una proteína rica en serina/arginina que regula el proceso de splicing alternativo de diferentes genes relacionados con patología cardiovascular, entre los que destaca la titina. Hasta el momento casi todas las variantes causales descritas son de tipo missense, y se encuentran fundamentalmente en la región rica en Arg-Ser (exón 9) y el dominio en dedos de cinc (exón 14), estando asociadas al desarrollo de MCD en forma autosómica dominante.
Métodos: Revisión narrativa de la literatura sobre patología asociada a RBM20 y estudio de la cosegregación en una familia con MCD y mutación intrónica en este gen.
Resultados: Presentamos una familia con 17 sujetos estudiados donde 10 fueron portadores heterocigotos de la variante c.1527+1G>A en RBM20. De ellos 7 expresaban el fenotipo de MCD en mayor o menor medida, con máxima expresión en un paciente trasplantado cardiaco y su hermano con muerte súbita con 46 años, y mínima expresión en las 3 portadoras más jóvenes (18-22 años) que resultaron fenotipo negativo. Hasta la fecha, la evidencia de patogenicidad para variantes intrónicas o truncantes es muy escasa. La variante intrónica c.1527+1G>A, lo mismo que la cercana c.1528-1G>C, tienen altas Probabilidades de estar asociadas a un proceso de splicing anómalo (se encuentran en el sitio consenso de splicing), y dado que afectan a un exón asimétrico se podrían asemejar a una variante frameshift (p.Asp477Valfs*18), o nula. Aplicando los criterios ACMG 2015, podríamos clasificar la variante c.1527+1G>A como variante probablemente patogénica en caso de demostrar afectación funcional de los transcritos para sumar un PS3 a los criterios ya presentes, PM2 (ausente en controles), PP1 (cosegregación en la familia) y PP3 (in silico deletéreo).
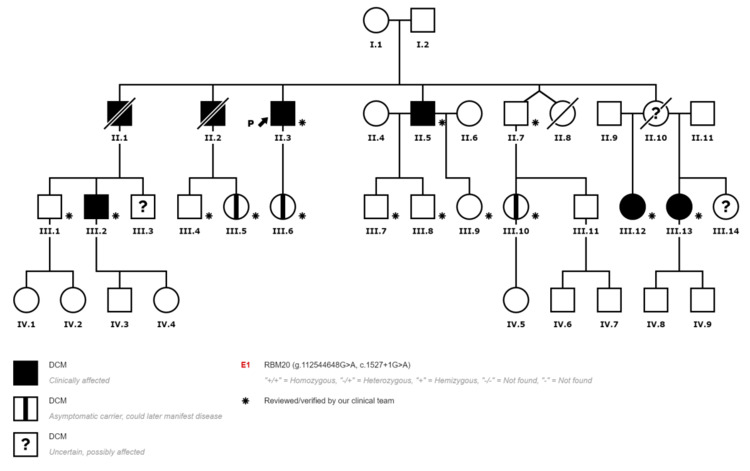
Árbol genealógico.
Conclusiones: En definitiva, el grado de evidencia disponible en la literatura no siempre es el suficiente para poder demostrar las hipótesis que nos genera la clínica. Sería deseable poder disponer de recursos suficientes para poder realizar los estudios funcionales (experimentos que demuestren la presencia de transcritos aberrantes o haploinsuficiencia por RNA-decay) necesarios a fin de poder otorgar de forma definitiva valor predictivo a determinadas variantes.
2023-1240-1 IMPULSA INNOVACIÓN.
Comunicaciones disponibles de "6113. Novedades en cardiogenética"
- 6113-1. Modera
- Luis Escobar López, Baracaldo (Guipúzcoa)
- 6113-2. Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
- Guillem Murillo Varona1, Marta Gil Molina1, María Valverde Gómez2, Franc Peris Castelló3, Francisco González Llopis3, María José Aparisi4, Cristina Cardona-Gay5, Diana Domingo Valero6, Aitana Braza Boïls7, Luis Martínez Dolz8, Juan Pablo Ochoa9 y Esther Zorio Grima10
1Cardiología. Hospital Universitario La Fe, Valencia, España, 2Health in Code. Health Research Institute Hospital La Fe (IIS La Fe), Valencia, España, 3Cardiología. Hospital General de Elda, Elda (Alicante), España, 4Unidad de Genómica, IIS La Fe de Valencia. Health Research Institute Hospital La Fe (IIS La Fe), Valencia, España, 5Unidad de Genómica, IIS La Fe de Valencia. Hospital Universitario La Fe, Valencia, España, 6Cardiopatías Familiares Hospital Universitario y Politécnico La Fe de Valencia, CAFAMUSME IIS La Fe de Valencia. Hospital Universitario La Fe, Valencia, España, 7CAFAMUSME IIS La Fe de Valencia, CIBERCV Madrid. Hospital Universitario La Fe, Valencia, España, 8Servicio de Cardiología Hospital Universitario y Politécnico La Fe de Valencia, Grupo de Investigación Traslacional en Cardiología IIS La Fe de Valencia, CIBERCV Madrid. Hospital Universitario La Fe, Valencia, España, 9Health in Code S.L. Health Research Institute Hospital La Fe (IIS La Fe), Valencia, España y 10Cardiopatías Familiares Hospital Universitario y Politécnico La Fe de Valencia, CAFAMUSME IIS La Fe de Valencia, CIBERCV Madrid. Hospital Universitario La Fe, Valencia, España.
- 6113-3. Riesgo genético poligénico en muestra de pacientes ingresados por síndrome coronario agudo
- Joaquín Sánchez-Prieto Castillo, Joan Ramon Enseñat, Charlotte Boillot, Lucía Villafáfila Martínez, José Manuel Martínez Palomares, Alejandro Cabello Rodríguez, Natalia Navarro Pelegrini, Ainhoa Aguinaga Mendibil, Patricia del Valle Tabernero, Ana Díaz Rojo, Andrea González Pigorini, Esther Gigante Miravalles, María Cristina Morante Perea y Luis Rodríguez Padial
Cardiología. Hospital Universitario de Toledo, Toledo, España.
- 6113-4. Miocardiopatía HCN4: más allá del canal de potasio
- José Francisco Gil Fernández1, Lidia María Carrillo Mora2, Francisco Castro García3, Santiago Escudero Cárceles3, Serena Evelina Margaretha Munteanu4, María Sabater Molina4 y Juan Ramón Gimeno Blanes2
1Cardiología. Hospital Clínico Universitario de Valladolid, Valladolid, España, 2Hospital Clínico Universitario Virgen de la Arrixaca, Murcia, España, 3Pediatría. Hospital Clínico Universitario Virgen de la Arrixaca, Murcia, España y 4Instituto Murciano de Investigación Biosanitaria Virgen de la Arrixaca, Murcia, España.
- 6113-5. Alteraciones de la conducción, arritmias y miocardiopatía dilatada asociadas a una mutación no descrita en el gen TNNI3K
- Marta González Quijano, Helena Llamas Gómez, María Luisa Peña Peña, Rosario Flaño Lombardo, Ángel A. Pedrote Martínez y Juan Acosta Martínez
Hospital Universitario Virgen del Rocío, Sevilla, España.
- 6113-6. Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- Guillermo Rad García1, Jorge Llau García1, Esther Zorio Grima2, Sara Huélamo Montoro1, Nerea Fernández Ortiz1, Guillem Murillo Varona1, Marta Gil Molina1, Valero Vicente Soriano Alfonso1, Enrique Robles Pérez1, Aitana Braza Boïls1, María J. Aparisi3, Soledad García Hernández4, Juan Pablo Ochoa Folmer4, Jordi Candela Ferre5 y Luis Martínez Dolz1
1Hospital Universitario La Fe, Valencia, España, 2Cardiopatías Familiares. Hospital Universitario La Fe, Valencia, España, 3Genomic Unit. Health Research Institute Hospital La Fe (IIS La Fe), Valencia, España, 4Health in Code, A Coruña (A Coruña), España y 5Hospital Clínico Universitario de Valladolid, Valladolid, España.
- 6113-7. Descripción del fenotipo asociado a una nueva variante del gen MYBPC3 relacionado con la miocardiopatía hipertrófica
- Marta González Quijano, Pablo Martín Marín, Helena Llamas Gómez y María Luisa Peña Peña
Hospital Universitario Virgen del Rocío, Sevilla, España.
- 6113-8. Análisis de los resultados genéticos en una cohorte de pacientes con miocardiopatía dilatada en función de la edad al diagnóstico
- Mónica García Monsalvo1, Sandra Riesco Sánchez2, Teresa María Romero Sillero2, María Natividad Marín Ruíz2, Luis Miguel Rincón Díaz1, Inés Toranzo Nieto1, Belén García Berrocal3, David González Calle1, Sandra Milagros Lorenzo Hernández3, Sara Lozano Jiménez1, David Hansoe Heredero Jung3, Milena Antúnez Ballesteros4, Pedro Luis Sánchez Fernández1, Eduardo Villacorta Argüelles1 y María Gallego Delgado1
1Cardiología. Hospital Clínico Universitario de Salamanca, Salamanca, España, 2Universidad de Salamanca, Salamanca, España, 3Bioquímica Clínica/Análisis Clínicos. Hospital Clínico Universitario de Salamanca, Salamanca, España y 4Cardiología. Complexo Hospitalario Universitario A Coruña, A Coruña (A Coruña), España.
- 6113-9. Interacción miRNA-mRNA: entender el enigma de la cardiomiopatía dilatada asociada al gen LMNA
- Mónica Ramos1, Maribel Quezada Feijoo1, Ignacio Pérez de Castro Insua2, José Córdoba Caballero3, Juan Antonio García Ranea3, Óscar Campuzano Larrea4, Georgia Sarquella Brugada5 y Rocío Toro Cebada6
1Unidad de Cardiología. Hospital Central de la Cruz Roja, Madrid, España, 2Instituto de Salud Carlos III, Madrid, España, 3Universidad de Málaga, Málaga, España, 4Instituto de investigación Biomédica de Girona (IdIBGi). Hospital Universitario Dr. Josep Trueta, Girona, España, 5Unidad de arritmias. Hospital Sant Joan de Déu, Barcelona, España y 6Facultad de Medicina. Universidad de Cádiz, Cádiz, España.
- 6113-10. Rentabilidad del estudio genético en pacientes trasplantados por miocardiopatía dilatada
- Pablo Martín Marín, Miguel Barranco Gutiérrez, Helena Llamas Gómez, José Manuel Sobrino Márquez y María Luisa Peña Peña
Hospital Universitario Virgen del Rocío, Sevilla, España.
- 6113-11. Características y evolución de una cohorte de pacientes con amiloidosis cardiaca por transtirretina sin insuficiencia cardiaca
- María Teresa Nogales Romo1, Verónica Suberviola Sánchez-Caballero1, Cristina de Cortina Camarero1, Cristina Beltrán Herrera1, Marta Domínguez Muñoa1, Silvia Jiménez Loeches1, Laura Mora Yagüe1, María del Mar Sarrión Catalá1, Pedro Martínez Losas1, Alejandro Cortés Beringola1, Zaira Gómez Álvarez1, Eloy Gómez Mariscal1, Gabriela Tirado Conte2, David Vaqueriza Cubillo1 y Roberto Muñoz Aguilera1
1Hospital Universitario Infanta Leonor, Madrid, España y 2Hospital Universitario Ramón y Cajal, Madrid, España.
- 6113-12. Evolución natural de la amiloidosis cardiaca: cronología de aparición de red flags y eventos en una cohorte
- Emilio Blanco López1, Jesús Piqueras Flores2, Jorge Martínez del Río2, Martín Negreira Caamaño3, Cristina Mateo Gómez1, Daniel Águila Gordo1, Maeve Soto Pérez1, Andrez Felipe Cubides Novoa1, Pablo Soto Martín1, Beatriz Jiménez Rubio1, Marta Andrés Sierra1, Cynthia Nuez Cuartango1, Laura Montesinos Vinader1 e Ignacio Sánchez Pérez1
1Servicio de Cardiología. Hospital General Universitario de Ciudad Real, Ciudad Real, España, 2Unidad de Cardiopatías Familiares, Servicio de Cardiología. Hospital General Universitario de Ciudad Real, Ciudad Real, España y 3Unidad de Arritmias, Servicio de Cardiología. Hospital Universitario 12 de Octubre, Madrid, España.
- 6113-13. Impacto del upgrade a terapia de resincronización cardiaca o estimulación de rama izquierda en pacientes con amiloidosis cardiaca por transtirretina
- Belén Peiró Aventín1, Nerea Mora Ayestarán1, Celia Gil Llopis2, Daniel Águila Gordo3, Daniel de Castro Campos1, Chinh Pham Trung4, Fernando Domínguez Rodríguez1, Víctor Castro Urda4, Esther González López1 y Pablo García Pavía1
1Unidad de Cardiopatías Familiares, Servicio de Cardiología. Hospital Universitario Puerta de Hierro, Majadahonda (Madrid), España, 2Servicio de Cardiología. Hospital Universitario Dr. Peset, Valencia, España, 3Servicio de Cardiología. Hospital General Universitario de Ciudad Real, Ciudad Real, España y 4Unidad de Electrofisiología, Servicio de Cardiología. Hospital Universitario Puerta de Hierro, Majadahonda (Madrid), España.
- 6113-14. Comparación de la presentación clínica y el pronóstico de hombres y mujeres con amiloidosis cardiaca por transtirretina. Análisis del registro de amiloidosis cardiaca de Galicia (AMIGAL)
- Fausto de Andrés Cardelle1, Mario Porto Souto2, Gonzalo Barge Caballero1, Eduardo Barge Caballero1, Andrea López López3, Manuel López Pérez4, Raquel Bilbao Quesada5, Eva González Babarro6, Mario Gutiérrez Feijoo7, Inés Gómez Otero8, Alfonso Varela Román8 y María G. Crespo Leiro1
1Complexo Hospitalario Universitario A Coruña, A Coruña, España, 2Universidad de Santiago de Compostela, Santiago de Compostela (A Coruña), España, 3Hospital Universitario Lucus Augusti, Lugo, España, 4Hospital Arquitecto Marcide, Ferrol (A Coruña), España, 5Hospital Álvaro Cunqueiro, Vigo (Pontevedra), España, 6Hospital Montecelo, Pontevedra, España, 7Complexo Hospitalario, Ourense, España y 8Complexo Hospitalario Universitario de Santiago de Compostela, Santiago de Compostela (A Coruña), España.
- 6113-15. Protocolo multidisciplinar para el cribado de hipercolesterolemia familiar heterocigota
- Gustavo Aníbal Cortez Quiroga, Marina Fernández Gárate, Saida Navarro Melero, María de la Paz Eliche Mozas, Ana Cubillas Quero y Lara Cruz Romero
Hospital Alto Guadalquivir, Andújar (Jaén), España.
- 6113-16. Diseño y justificación de la creación de una plataforma nacional multicéntrica para el estudio de la enfermedad inflamatoria del miocardio: cohorte Pre-MYO
- Fernando Domínguez Rodríguez1, Azahara M.M. García Serna2, Ángel Esteban Gil3, Ángel Manuel Iniesta Manjavacas4, José María Larrañaga Moreira5, Antonio Grande Trillo6, Belén Álvarez Álvarez7, Juan Lacalzada Almeida8, Luis Ruiz Guerrero9, Marc Llagostera Martín10, Aitor Uribarri González11, Alberto Esteban Fernández12, Ana García Álvarez13, Juan Fernández Martínez14 y Domingo Pascual-Figal15
1Cardiología. Hospital Universitario Puerta de Hierro, Majadahonda (Madrid), España, 2Cardiología Clínica y Experimental. Instituto Murciano de Investigación Biosanitaria Virgen de la Arrixaca, Murcia, España, 3Tecnologías de Modelado, Procesamiento y Gestión del Conocimiento. Instituto Murciano de Investigación Biosanitaria Virgen de la Arrixaca, Murcia, España, 4Cardiología. Hospital Universitario La Paz, Madrid, España, 5Cardiología. Complexo Hospitalario Universitario A Coruña, A Coruña, España, 6Cardiología. Hospital Universitario Virgen del Rocío, Sevilla, España, 7Cardiología. Complexo Hospitalario Universitario de Santiago de Compostela, Santiago de Compostela (A Coruña), España, 8Cardiología. Complejo Hospitalario Universitario de Canarias, San Cristóbal de La Laguna (Santa Cruz de Tenerife), España, 9Cardiología. Hospital Universitario Marqués de Valdecilla, Santander (Cantabria), España, 10Cardiología. Hospital del Mar, Barcelona, España, 11Cardiología. Hospital Universitari Vall d'Hebron, Barcelona, España, 12Cardiología. Hospital Universitario Severo Ochoa, Madrid, España, 13Cardiología. Hospital Clínic, Barcelona, España, 14Cardiología. Hospital de la Santa Creu i Sant Pau, Barcelona, España y 15Cardiología. Hospital Clínico Universitario Virgen de la Arrixaca, Murcia, España.
Más comunicaciones de los autores
- Aparisi, María José
-
Braza Boïls, Aitana
- 6113-2 - Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
- 6011-67 - ¿Podemos mejorar la detección precoz de arritmias en amiloidosis cardiaca por transtirretina?
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- Candela Ferre, Jordi
-
Fernández Ortiz, Nerea
- 4020-2 - Correlación entre la ratio de integral velocidad tiempo y el área valvular aórtica en la estenosis aórtica grave. ¿Nuevo punto de corte?
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 6053-344 - Utilidad del método Average Pixel Intensity para la detección de insuficiencia mitral moderada-grave en comparación con el área del orificio regurgitante
- 6118-12 - Análisis de recurrencias arrítmicas en pacientes sometidos a un segundo procedimiento de ablación de fibrilación auricular con electroporación vs radiofrecuencia
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- García Hernández, Soledad
-
Gil Molina, Marta
- 4020-2 - Correlación entre la ratio de integral velocidad tiempo y el área valvular aórtica en la estenosis aórtica grave. ¿Nuevo punto de corte?
- 6113-2 - Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
- 6062-401 - Dificultad en la cuantificación de la gravedad de la estenosis valvular aórtica
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
-
Huélamo Montoro, Sara
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6011-67 - ¿Podemos mejorar la detección precoz de arritmias en amiloidosis cardiaca por transtirretina?
- 6053-347 - Cuantificación y mecanismo de la insuficiencia mitral moderada-grave en la vida real: análisis de potenciales métricas de control de calidad en ecocardiografía
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
-
Llau García, Jorge
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6118-12 - Análisis de recurrencias arrítmicas en pacientes sometidos a un segundo procedimiento de ablación de fibrilación auricular con electroporación vs radiofrecuencia
- 6053-347 - Cuantificación y mecanismo de la insuficiencia mitral moderada-grave en la vida real: análisis de potenciales métricas de control de calidad en ecocardiografía
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
-
Martínez Dolz, Luis
- 4005-6 - Angina persistente en el síndrome coronario crónico con evidencia de isquemia clínica, angiográfica y mediante RMC de estrés: dinámica y pronóstico a largo plazo
- 6068-426 - Determinantes de la recuperación miocárdica tras una hospitalización en pacientes con insuficiencia cardiaca de novo y fracción de eyección ventricular izquierda reducida
- 4015-5 - Predictores de endocarditis infecciosa tras el implante de válvula pulmonar en pacientes con cardiopatías congénitas
- 4020-2 - Correlación entre la ratio de integral velocidad tiempo y el área valvular aórtica en la estenosis aórtica grave. ¿Nuevo punto de corte?
- 5004-7 - Resultados de la ablación de las venas pulmonares y de la pared posterior de la aurícula izquierda con electroporación comparada con radiofrecuencia
- 5004-3 - Eventos en blanking en el aislamiento de venas pulmonares en una población contemporánea de radiofrecuencia y electroporación. ¿Son eventos tan benignos? ¿Son todos iguales?
- 4016-2 - Electroporación frente a radiofrecuencia para el aislamiento de venas pulmonares. Análisis a un año de dos cohortes históricas. Análisis de subgrupos y búsqueda de factores predisponentes
- 6064-409 - Perspectivas actuales de la ultrafiltración en el síndrome cardiorrenal: metaanálisis de eficacia y seguridad
- 6026-134 - Modificación de la placa e impacto en la microcirculación coronaria tras angioplastia con balón farmacoactivo. Estudio PLAMI
- 6118-4 - Diferencias de sexo en la macrorreentrada auricular izquierda tras ablación de fibrilación auricular
- 6113-2 - Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
- 5004-11 - Electroporación frente a radiofrecuencia en el aislamiento de venas pulmonares en pacientes con miocardiopatía dilatada y probable taquimiocardiopatía
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 6106-8 - Strain auricular en pacientes adultos con D-TGA y corrección anatómica ¿se relaciona con la capacidad de esfuerzo?
- 6053-347 - Cuantificación y mecanismo de la insuficiencia mitral moderada-grave en la vida real: análisis de potenciales métricas de control de calidad en ecocardiografía
- 6062-401 - Dificultad en la cuantificación de la gravedad de la estenosis valvular aórtica
- 6011-63 - Estudio de amiloidosis en grasa extraída de la bolsa del generador en pacientes a los que se les va a implantar un dispositivo de estimulación cardiaca
- 6053-344 - Utilidad del método Average Pixel Intensity para la detección de insuficiencia mitral moderada-grave en comparación con el área del orificio regurgitante
- 6118-12 - Análisis de recurrencias arrítmicas en pacientes sometidos a un segundo procedimiento de ablación de fibrilación auricular con electroporación vs radiofrecuencia
- 6011-67 - ¿Podemos mejorar la detección precoz de arritmias en amiloidosis cardiaca por transtirretina?
- 5021-5 - Análisis temporal comparativo de morbilidad y mortalidad precoz en trasplante cardiaco con soporte ECMO: explorando las tendencias a lo largo del tiempo
-
Murillo Varona, Guillem
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 6062-401 - Dificultad en la cuantificación de la gravedad de la estenosis valvular aórtica
- 6113-2 - Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
-
Ochoa Folmer, Juan Pablo
- 5002-4 - Variantes missense en FLNC y miocardiopatía hipertrófica: el todo no es la suma de las partes
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6113-2 - Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
- 5002-7 - Genotipos de alto riesgo en miocardiopatía dilatada: más allá de las arritmias
-
Rad García, Guillermo
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6062-401 - Dificultad en la cuantificación de la gravedad de la estenosis valvular aórtica
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 4020-2 - Correlación entre la ratio de integral velocidad tiempo y el área valvular aórtica en la estenosis aórtica grave. ¿Nuevo punto de corte?
-
Robles Pérez, Enrique
- 5004-3 - Eventos en blanking en el aislamiento de venas pulmonares en una población contemporánea de radiofrecuencia y electroporación. ¿Son eventos tan benignos? ¿Son todos iguales?
- 5004-11 - Electroporación frente a radiofrecuencia en el aislamiento de venas pulmonares en pacientes con miocardiopatía dilatada y probable taquimiocardiopatía
- 6118-12 - Análisis de recurrencias arrítmicas en pacientes sometidos a un segundo procedimiento de ablación de fibrilación auricular con electroporación vs radiofrecuencia
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 4016-2 - Electroporación frente a radiofrecuencia para el aislamiento de venas pulmonares. Análisis a un año de dos cohortes históricas. Análisis de subgrupos y búsqueda de factores predisponentes
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 5004-7 - Resultados de la ablación de las venas pulmonares y de la pared posterior de la aurícula izquierda con electroporación comparada con radiofrecuencia
- 6053-344 - Utilidad del método Average Pixel Intensity para la detección de insuficiencia mitral moderada-grave en comparación con el área del orificio regurgitante
- 4020-2 - Correlación entre la ratio de integral velocidad tiempo y el área valvular aórtica en la estenosis aórtica grave. ¿Nuevo punto de corte?
- 6062-401 - Dificultad en la cuantificación de la gravedad de la estenosis valvular aórtica
-
Soriano Alfonso, Valero Vicente
- 4016-2 - Electroporación frente a radiofrecuencia para el aislamiento de venas pulmonares. Análisis a un año de dos cohortes históricas. Análisis de subgrupos y búsqueda de factores predisponentes
- 4015-5 - Predictores de endocarditis infecciosa tras el implante de válvula pulmonar en pacientes con cardiopatías congénitas
- 5004-7 - Resultados de la ablación de las venas pulmonares y de la pared posterior de la aurícula izquierda con electroporación comparada con radiofrecuencia
- 5004-3 - Eventos en blanking en el aislamiento de venas pulmonares en una población contemporánea de radiofrecuencia y electroporación. ¿Son eventos tan benignos? ¿Son todos iguales?
- 6118-4 - Diferencias de sexo en la macrorreentrada auricular izquierda tras ablación de fibrilación auricular
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6110-8 - Valor pronóstico del PET-TAC en la endocarditis infecciosa
- 6106-8 - Strain auricular en pacientes adultos con D-TGA y corrección anatómica ¿se relaciona con la capacidad de esfuerzo?
- 6118-12 - Análisis de recurrencias arrítmicas en pacientes sometidos a un segundo procedimiento de ablación de fibrilación auricular con electroporación vs radiofrecuencia
- 5004-11 - Electroporación frente a radiofrecuencia en el aislamiento de venas pulmonares en pacientes con miocardiopatía dilatada y probable taquimiocardiopatía
-
Zorio Grima, Esther
- 5002-11 - Caracterización y pronóstico de la amiloidosis cardiaca hereditaria por transtirretina en España
- 6011-67 - ¿Podemos mejorar la detección precoz de arritmias en amiloidosis cardiaca por transtirretina?
- 6113-6 - Sustitución en RBM20 afectando el splicing, ¿Primera familia que demuestra la patogenicidad de este tipo de alteraciones?
- 6113-2 - Recatalogando la variante p.His90Tyr en ACTC1 para adquirir valor predictivo
