SEC 2024 - El Congreso de la Salud Cardiovascular
Introducción
Dr. José María de la Torre Hernández
Presidente del Comité Científico del Congreso. Vicepresidente de la SEC
Comités ejecutivo, organizador y científico
Comité de evaluadores
Listado completo de comunicaciones
Índice de autores
4009. Unidad de críticos cardiológicos: shock, tromboembolia pulmonar, parada cardiaca y mucho más
4009-4. Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
1Cardiología. Hospital Universitario de Getafe, Getafe (Madrid), España y 2Hospital Universitario de Getafe, Getafe (Madrid), España.
Introducción y objetivos: El papel de la inflamación y la disfunción endotelial en el infarto agudo de miocardio (IAM) es cada vez más reconocido. Estudios recientes sugieren que los pacientes con IAM con coronarias normales (MINOCA) pueden tener un perfil proinflamatorio y disfunción endotelial. Nuestro objetivo fue evaluar la relevancia diagnóstica y terapéutica de biomarcadores (BM) de inflamación y disfunción endotelial en el IAM.
Métodos: Estudio prospectivo observacional en pacientes con IAM divididos en dos grupos siguiendo definiciones de guías europeas: MICAD y MINOCA. Se determinaron los niveles de interleucina-6 (IL-6), factor de necrosis tumoral-α (TNFα), proteína C-reactiva ultrasensible (PCRus) y dimetilarginina asimétrica (ADMA) al ingreso, alta y dos meses después del IAM. El análisis de seguimiento incluyó mortalidad por cualquier causa y un compuesto de eventos adversos cardiovasculares mayores (MACE): mortalidad cardiovascular, IAM, reingresos cardiovasculares e ictus. Mediana de seguimiento: 15 meses. Se analizó la asociación de cada BM con la condición de MINOCA, así como la ocurrencia de eventos adversos en un modelo de regresión logística ajustado por edad y sexo. Se calcularon curvas ROC y se determinaron puntos de corte óptimos. Considerando la variación de los niveles de BM según el tamaño del IAM, se estandarizaron los niveles de BM dividiéndolos por el nivel máximo de troponina.
Resultados: Se analizaron 166 pacientes (media de edad 68%, 70% hombres). Las concentraciones de los BM se muestran en la tabla. Los BM con mayor capacidad para distinguir al ingreso entre MICAD y MINOCA fueron la relación ADMA/troponina, seguida por TNFα/troponina e IL-6/troponina con AUC de 0,89, 0,88 y 0,85 respectivamente. Con relación al pronóstico, la relación TNFα/troponina mostró la mayor capacidad para predecir mortalidad general (AUC 0,93) y los niveles de TNFα tanto al ingreso, al alta y durante el seguimiento se relacionaron con mayor riesgo de MACE, con OR de 7,8 (p < 0,001), 18,1 (p < 0,001) y 8 (p0,03) respectivamente.
|
Concentraciones de los biomarcadores |
|||||
|
Biomarcadores de inflamación, mediana (RIC) |
Total (N = 166) |
MICAD (N = 122) |
MINOCA N = 44 |
p |
|
|
PCR-us (mg/dl) |
Ingreso |
3,26 (1,23-9,87) |
3,47 (1,53-10,57) |
3-21 (0,83,9,36) |
0,225 |
|
Alta |
6,72 (3,01-16) |
8,46 (4,70-16,77) |
2,21 (1,35-9,67) |
0,0027 |
|
|
Seguimiento |
1,85 (0,91-4,47) |
1,83 (0,99-3,87) |
2,38 (0,69-6,58) |
0,6066 |
|
|
IL-6 (pg/ml) |
Ingreso |
5,54 (2,95-12,87) |
8,45 (4,02-15,61) |
4,21 (2,67-7,93) |
0,0136 |
|
Alta |
4,12 (2,02-7,74) |
5,11 (2,81-9,85) |
2,86 (1,22-5,07) |
0,0177 |
|
|
Seguimiento |
2,81 (1,70-5,18) |
3,39 (1,70-6,03) |
2,57 (1,69-3,90) |
0,1841 |
|
|
TNF-α (pg/ml) |
Ingreso |
1,15 (0,89-1,59) |
1,21 (0,91-1,67) |
1,09 (0,81-1,27) |
0,2404 |
|
Alta |
1,32 (0,98-1,76) |
1,32 (1,05-1,82) |
1,32 (0,90-1,55) |
0,4291 |
|
|
Seguimiento |
1,30 (0,98-1,76) |
1,39 (1,03-1,80) |
1,17 (0,93-1,30) |
0,0877 |
|
|
Biomarcador de disfunción endotelial, mediana (RIC) |
|||||
|
ADMA (ng/ml) |
Ingreso |
222,18 (181,02-342,26) |
221,59 (194,85-303,11) |
235,90 (171,21-396,33) |
0,8908 |
|
Alta |
240,29 (194,64-314,31) |
240,29 (209,08-321,55) |
241,25 (192,78-311,66) |
0,6501 |
|
|
Seguimiento |
217,99 (169,57-283,30) |
227,16 (195,57-283,70) |
193,33 (150,44-283,74) |
0,1108 |
|
|
MINOCA: infarto agudo de miocardio con arterias coronarias normales; MICAD: infarto agudo de miocardio con arterias coronarias con estenosis significativas; RIC: rango intercuartílico; IL-6: interleucina-6; TNFα: factor de necrosis tumoral-α; PCR-us: proteína C-reactiva ultrasensible; ADMA: dimetilarginina asimétrica. |
|||||
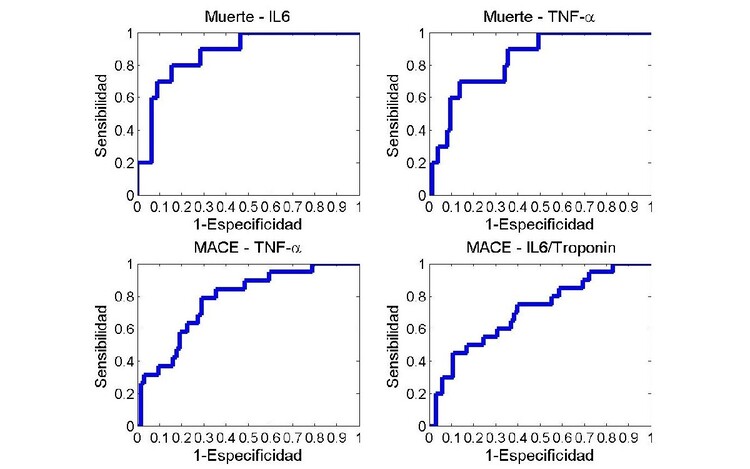
Asociaciones entre biomarcadores, mortalidad y MACE.
Conclusiones: Este estudio sugiere que el cociente ADMA/troponina podría discriminar entre MICAD y MINOCA, mientras que TNFα/troponina muestra una eficiente capacidad de predicción de la mortalidad por cualquier causa. Además, los niveles de TNFα pueden predecir MACE. Incorporar estos BMs en la práctica clínica podría ayudar a identificar tanto a pacientes con MINOCA como a aquellos con IAM de riesgo.
Comunicaciones disponibles de "4009. Unidad de críticos cardiológicos: <i>shock</i>, tromboembolia pulmonar, parada cardiaca y mucho más"
- 4009-1. Modera
- Juan Carlos García Rubira, Madrid
- 4009-2. Nueva clasificación de riesgo para pacientes con embolia aguda de pulmón en base a los estadios de shock de la escala SCAI (RISA-PE)
- Rocío Párraga1, Carlos Real1, María-Eugenia Vázquez-álvarez2, Ernesto Valero3, Maite Velázquez4, Daniel Tébar5, Neus Savatella6, Eva Rúmiz7, Valeriano Ruiz Quevedo8, Fernando Sabatel-Pérez9, Ignacio Amat-Santos10, Juan José Portero11, Ana Viana-Tejedor1, Carlos Ferrera1 y Pablo Salinas1
1Cardiología. Hospital Clínico San Carlos, Madrid, España, 2Cardiología. Hospital General Universitario Gregorio Marañón, Madrid, España, 3Cardiología. Hospital Clínico Universitario de Valencia, Valencia, España, 4Cardiología. Hospital Universitario 12 de Octubre, Madrid, España, 5Cardiología. Hospital Universitario La Paz, Madrid, España, 6Cardiología. Hospital del Mar, Barcelona, España, 7Cardiología. Hospital General Universitario, Valencia, España, 8Cardiología. Hospital Universitario de Navarra, Pamplona (Navarra), España, 9Cardiología. Hospital Universitario San Cecilio, Granada, España, 10Cardiología. Hospital Clínico Universitario de Valladolid, Valladolid, España y 11Cardiología. Complejo Hospitalario Universitario, Albacete, España.
- 4009-3. Tratamiento de la estenosis aórtica grave en shock cardiogénico en España: resultados de la TAVI frente a la cirugía y al tratamiento médico
- Carlos Ferrera Durán1, Carolina Espejo Paeres2, Náyade del Prado3, Pilar Jiménez Quevedo1, Luis Nombela Franco1, Francisco Javier Noriega Sanz1, Cristina Fernández Pérez3, Nieves Gonzalo López1, Nicolás Rosillo Ramírez4, Rodrigo Fernández Jiménez1, Iván Núñez Gil1, Javier Escaned Barbosa1, Antonio Fernández Ortiz1, Francisco Javier Elola Somoza3 y Ana Viana Tejedor1
1Servicio de Cardiología, Instituto Cardiovascular. Hospital Clínico San Carlos, Madrid, España, 2Servicio de Cardiología. Hospital Universitario Miguel Servet, Zaragoza, España, 3Fundación IMAS, Madrid, España y 4Servicio de Medicina Preventiva. Hospital Universitario 12 de Octubre, Madrid, España.
- 4009-4. Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- María Jesús Espinosa Pascual1, Nuria Gil Mancebo1, María Martín Muñoz1, Mariam El Assar de la Fuente2, José Antonio Carnicero Carreño2, Daniel Nieto Ibáñez1, Miguel de la Serna Real de Asua1, Silvia Humanes Ybañez1, Miguel Gutiérrez Muñoz1, Bárbara Izquierdo Coronel1, Renée Olsen Rodríguez1, Alfonso Fraile Sanz1, Rebeca Mata Caballero1, Paula Rodríguez Montes1 y Joaquín J. Alonso Martín1
1Cardiología. Hospital Universitario de Getafe, Getafe (Madrid), España y 2Hospital Universitario de Getafe, Getafe (Madrid), España.
- 4009-5. La oximetría cerebral como predictor de supervivencia en la parada cardiorrespiratoria extrahospitalaria
- Ruth Salaberria Udabe1, Andima Larrea Redin1, Elisabete Aramendi Ecenarro2, Rebeca Castaño Becerril1, Ander Arregui Otxotorena1, Nuria Barral Martínez1 y Aroa Hermosa Torrado1
1Emergencias, Bilbao (Vizcaya), España y 2Universidad del País Vasco, Bilbao (Vizcaya), España.
- 4009-6. Trombosis intraventricular en el síndrome de tako-tsubo: prevalencia, factores asociados y pronóstico
- Jorge Salamanca Viloria1, Lidia Vilches Miguel1, Óscar Vedia Cruz2, Aitor Uribarri González3, Emilia Blanco Ponce4, Clara Fernández Cordón5, Miguel José Corbí Pascual6, Manuel Almendro Delia7, Alberto Pérez Castellanos8, Agustín Carlos Martín García9, Albert Durán Cambra10, Víctor Manuel Becerra11, Sergio Raposeiras Roubín12, Fernando Alfonso Manterola1 e Iván Núñez Gil2
1Servicio de Cardiología. Hospital Universitario de la Princesa, Madrid, España, 2Servicio de Cardiología. Hospital Clínico San Carlos, Madrid, España, 3Servicio de Cardiología. Hospital Universitario Vall d'Hebron, Barcelona, España, 4Servicio de Cardiología. Hospital Universitari Arnau de Vilanova, Lleida, España, 5Servicio de Cardiología. Hospital Clínico Universitario de Valladolid, Valladolid, España, 6Servicio de Cardiología. Complejo Hospitalario Universitario de Albacete, Albacete, España, 7Servicio de Cardiología. Hospital Universitario Virgen Macarena, Sevilla, España, 8Servicio de Cardiología. Hospital Son Espases, Palma de Mallorca (Illes Balears), España, 9Servicio de Cardiología. Complejo Asistencial Universitario de Salamanca, Salamanca, España, 10Servicio de Cardiología. Hospital de la Santa Creu i Sant Pau, Barcelona, España, 11Servicio de Cardiología. Hospital Clínico Universitario Virgen de la Victoria, Málaga, España y 12Servicio de Cardiología. Hospital Álvaro Cunqueiro, Vigo (Pontevedra), España.
- 4009-7. Modelo de supervivencia basado en aprendizaje automático para pacientes con síndrome coronario agudo sin elevación del segmento ST (SCASEST)
- Gabriel González Barbeito1, Rodrigo Araníbar Martínez1, Vicente Piñero Maciá1, Fausto de Andrés Cardelle1, Miguel Louro Freire1, Carmen Vidau Getán1 y Guillermo Aldama López2
1Servicio de Cardiología y 2Servicio de Cardiología; Unidad de Hemodinámica. Complexo Hospitalario Universitario A Coruña, A Coruña (A Coruña), España.
Más comunicaciones de los autores
-
Alonso Martín, Joaquín J.
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 4010-2 - Factores ambientales y riesgo de infarto. ¿Cómo puede prevenir el clínico?
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6076-474 - Factores predictivos de ingreso hospitalario en pacientes con dolor torácico y curva plana de troponina
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
Carnicero Carreño, José Antonio
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
de la Serna Real de Asúa, Miguel
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6076-474 - Factores predictivos de ingreso hospitalario en pacientes con dolor torácico y curva plana de troponina
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
El Assar de la Fuente, Mariam
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
-
Espinosa Pascual, María Jesús
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
-
Fraile Sanz, Alfonso
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
Gil Mancebo, Nuria
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
-
Gutiérrez Muñoz, Miguel
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
-
Humanes Ybáñez, Silvia
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6076-474 - Factores predictivos de ingreso hospitalario en pacientes con dolor torácico y curva plana de troponina
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
Izquierdo Coronel, Bárbara
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6076-474 - Factores predictivos de ingreso hospitalario en pacientes con dolor torácico y curva plana de troponina
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
-
Martín Muñoz, María
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
Mata Caballero, Rebeca
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6076-474 - Factores predictivos de ingreso hospitalario en pacientes con dolor torácico y curva plana de troponina
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
-
Nieto Ibáñez, Daniel
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
-
Olsen Rodríguez, Renée
- 4008-3 - Impacto de variantes sinónimas en las miocardiopatías hereditarias
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 4008-6 - ¿Es útil el screening familiar en miocardiopatía hipertrófica?
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6006-19 - Evaluación pronóstica de un grupo de pacientes con dolor torácico y curva plana de troponina
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6072-450 - Strain global longitudinal en insuficiencia cardiaca con fracción de eyección preservada. ¿Es útil?
- 6076-474 - Factores predictivos de ingreso hospitalario en pacientes con dolor torácico y curva plana de troponina
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
-
Rodríguez Montes, Paula
- 4009-4 - Implicaciones diagnósticas y pronosticas de los niveles de biomarcadores de inflamación y disfunción endotelial en el infarto de miocardio con y sin arterias coronarias obstructivas
- 6063-406 - Impacto de la hiponatremia en la hospitalización por insuficiencia cardiaca
- 6104-3 - Implementación de una herramienta de inteligencia artificial en una consulta de cardiología general. Una nueva oportunidad
- 6103-11 - MINOCA vs MICAD en el paciente anciano: características y pronóstico
- 6010-46 - Diferencias entre hombres y mujeres menores de 65 años con infarto agudo de miocardio: una cohorte española
- 6048-306 - Perfil clínico y pronóstico de pacientes con infarto agudo de miocardio con arterias coronarias no obstruidas que hayan tenido un síndrome coronario agudo previo
- 6048-309 - El impacto de la enfermedad renal en pacientes con infarto agudo de miocardio con y sin lesiones obstructivas
- 6065-417 - Diferencias en cuanto al sexo en pacientes ingresados por insuficiencia cardiaca: características y pronóstico
- 6042-279 - Toma de decisiones en los pacientes con dolor torácico y curva plana de troponina
- 6048-308 - Implicaciones pronósticas de los pacientes diabéticos con MINOCA
- 5019-5 - Factores predictores de MINOCA en pacientes con infarto agudo de miocardio
- 6013-83 - Características clínicas y pronóstico del MINOCA en función de la edad
- 6045-295 - Infarto agudo de miocardio ¿ha cambiado el manejo en los últimos años?
- 6123-8 - Evolución a largo plazo y factores predictores en los pacientes con MINOCA
- 6063-404 - Impacto de la edad en la insuficiencia cardiaca. Particularidades clínicas, epidemiológicas y pronósticas en el paciente anciano
- 5019-2 - Niveles elevados de biomarcadores de inflamación y disfunción endotelial en pacientes con infarto de miocardio con arterias coronarias no obstructivas
- 6048-307 - Infarto de miocardio con arterias coronarias no obstructivas (MINOCA): características clínicas y pronóstico
- 6060-376 - Resonancia magnética cardiaca en pacientes con MINOCA en la práctica clínica habitual
- 6101-4 - Concordancia entre intervenciones cardiológicas y propuestas de inteligencia artificial para pacientes que presentan dolor torácico, basadas en interconsultas desde el servicio de urgencias a cardiología
