La declaración PRISMA (Preferred Reporting Items for Systematic reviews and Meta-Analyses), publicada en 2009, se diseñó para ayudar a los autores de revisiones sistemáticas a documentar de manera transparente el porqué de la revisión, qué hicieron los autores y qué encontraron. Durante la última década, ha habido muchos avances en la metodología y terminología de las revisiones sistemáticas, lo que ha requerido una actualización de esta guía. La declaración prisma 2020 sustituye a la declaración de 2009 e incluye una nueva guía de presentación de las publicaciones que refleja los avances en los métodos para identificar, seleccionar, evaluar y sintetizar estudios. La estructura y la presentación de los ítems ha sido modificada para facilitar su implementación. En este artículo, presentamos la lista de verificación PRISMA 2020 con 27 ítems, y una lista de verificación ampliada que detalla las recomendaciones en la publicación de cada ítem, la lista de verificación del resumen estructurado PRISMA 2020 y el diagrama de flujo revisado para revisiones sistemáticas.
Palabras clave
Las revisiones sistemáticas son útiles en muchos aspectos críticos, ya que pueden proporcionar una síntesis del estado del conocimiento en un área determinada, a partir de la cual se pueden identificar futuras prioridades de investigación, abordar preguntas que de otro modo no podrían ser respondidas por estudios individuales, identificar problemas en la investigación primaria que deben ser corregidos en futuros estudios y generar o evaluar teorías sobre cómo o por qué ocurren fenómenos de interés.
Por lo tanto, las revisiones sistemáticas generan diversos tipos de conocimientos para diferentes usuarios de las revisiones (por ejemplo, pacientes, proveedores de atención médica, investigadores y responsables de la formulación de políticas de salud)1,2.
Para garantizar que una revisión sistemática sea valiosa para los usuarios, los autores deben elaborar una publicación transparente, completa y precisa en la que se describa por qué se ha realizado la revisión, qué se ha hecho (por ejemplo, cómo se han identificado y seleccionado los estudios) y qué se ha encontrado (por ejemplo, características de los estudios incluidos y los resultados de los metanálisis).
La guía actualizada para la publicación de revisiones sistemáticas PRISMA 2020 permite a los autores alcanzar este objetivo con más facilidad3.
La declaración PRISMA publicada en 2009 (en lo sucesivo denominada PRISMA 2009)4–10 es una guía de presentación de informes diseñada para abordar los problemas en la publicación de revisiones sistemáticas11.
La declaración PRISMA 2009 comprendía una lista de 27 ítems recomendados para la publicación de revisiones sistemáticas y un documento de «explicación y elaboración»12–15 proporcionaba orientación adicional para la publicación de cada ítem, así como ejemplos de publicaciones.
Las recomendaciones han sido ampliamente aprobadas y adoptadas, como lo demuestran su publicación en múltiples revistas, las citaciones en más de 60.000 informes (Scopus, agosto de 2020), el respaldo de casi 200 revistas y organizaciones que desarrollan revisiones sistemáticas y su adopción en diversas disciplinas. La evidencia proveniente de estudios observacionales sugiere que el uso de la declaración PRISMA 2009 está asociada a publicaciones más completas de revisiones sistemáticas16–19 aunque se podría hacer más para mejorar la adhesión a la guía20.
Se han producido muchas innovaciones en la realización de revisiones sistemáticas desde la publicación de la declaración PRISMA 2009. Por ejemplo, los avances tecnológicos han permitido el uso del procesamiento del lenguaje natural y el aprendizaje automático para identificar evidencia relevante21–23, se han propuesto métodos para sintetizar y presentar los hallazgos cuando no es posible o apropiado realizar un metanálisis24–26 y se han desarrollado nuevos métodos para evaluar el riesgo de sesgo en los resultados de los estudios incluidos27,28.
Se ha acumulado evidencia sobre las fuentes de sesgo en las revisiones sistemáticas, dando lugar al desarrollo de nuevas herramientas para evaluar la realización de revisiones sistemáticas29,30. La terminología utilizada para describir determinados procesos de las revisiones también ha evolucionado, ya que se ha pasado de evaluar la «calidad» a evaluar la «certidumbre» del cuerpo de la evidencia31. Además, el panorama editorial se ha transformado y actualmente existen múltiples posibilidades para registrar y difundir protocolos de revisiones sistemáticas32,33, difundir las publicaciones de revisiones sistemáticas y compartir datos y materiales, tales como servidores de preimpresión y repositorios de acceso público.
Para incorporar estos avances en la publicación de las revisiones sistemáticas, es necesario actualizar la declaración PRISMA 2009.
DESARROLLO DE PRISMA 2020Se siguieron varios pasos para desarrollar la declaración PRISMA 2020 (se dispone de una descripción completa de los métodos utilizados en otras citaciones34). Al examinar los resultados de los estudios que investigaban la transparencia en la publicación de las revisiones16,20,35,36, los autores de la declaración original identificaron aquellos ítems de la declaración PRISMA 2009 que, a menudo, se comunicaban de manera incompleta. Identificaron posibles modificaciones en la declaración PRISMA 2009 tras revisar 60 documentos que proporcionan instrucciones para la publicación de revisiones sistemáticas (incluyendo guías de práctica clínica, manuales, herramientas y estudios de metainvestigación)37. Esta revisión de la literatura se utilizó para documentar el contenido de una encuesta con las posibles modificaciones de los 27 ítems de PRISMA 2009 y los posibles ítems adicionales. A los encuestados se les preguntó, para cada uno de los ítems de PRISMA 2009, si creían que se debían mantener sin modificaciones, modificarlos o eliminarlos, y si consideraban que se debía añadir algún ítem adicional. Se invitó a metodólogos expertos en revisiones sistemáticas y a editores de revistas para que completaran la encuesta en línea (respondieron 110 de los 220 invitados). En una reunión presencial de dos días de duración que se llevó a cabo en septiembre de 2018 en Edimburgo (Escocia), y en la que participaron 21 miembros, se discutieron el contenido y la redacción propuestos para la declaración PRISMA 2020, de acuerdo con la información obtenida de la revisión y los resultados de la encuesta. A lo largo de 2019 y 2020, a través de procesos de retroalimentación, los coautores desarrollaron un borrador inicial y cinco revisiones de la lista de verificación y del documento de explicación y elaboración. En abril de 2020, se invitó a 22 autores de revisiones sistemáticas que habían expresado su interés en proporcionar comentarios sobre la lista de verificación PRISMA 2020 para que compartieran sus puntos de vista (a través de una encuesta en línea) sobre el diseño y la terminología utilizados en una versión preliminar de la lista de verificación.
Se recibió retroalimentación de 15 individuos, y los comentarios fueron considerados por el primer autor de la versión original en inglés. Toda revisión que se consideró necesaria se incorporó antes de que la versión final fuera aprobada y respaldada por todos los coautores.
DECLARACIÓN PRISMA 2020Alcance de la guíaLa declaración PRISMA 2020ha sido diseñada principalmente para revisiones sistemáticas de estudios que evalúan los efectos de las intervenciones sanitarias, independientemente del diseño de los estudios incluidos. Sin embargo, los ítems de la lista de verificación son aplicables a las publicaciones de revisiones sistemáticas que evalúan otras intervenciones no relacionadas con la salud (por ejemplo, intervenciones sociales o educativas), y muchos ítems son también aplicables a revisiones sistemáticas con objetivos distintos a la evaluación de intervenciones (por ejemplo, evaluación de etiología, prevalencia o pronóstico). La declaración PRISMA 2020 está destinada a ser utilizada en revisiones sistemáticas que incluyen síntesis (por ejemplo, metanálisis de comparaciones por pares u otros métodos de síntesis estadística) o que no incluyen síntesis (por ejemplo, porque solo se identifica un estudio elegible). Los ítems de la declaración PRISMA 2020 son relevantes para las revisiones sistemáticas de métodos mixtos (que incluyen estudios cuantitativos y cualitativos), pero también se deben consultar las guías de presentación y síntesis de datos cualitativos38,39.
La declaración PRISMA 2020 se puede utilizar para revisiones sistemáticas originales, revisiones sistemáticas actualizadas o continuamente actualizadas («vivas»). Sin embargo, para las revisiones sistemáticas actualizadas y «vivas», puede ser necesario tener en cuenta algunas consideraciones adicionales. En el caso de contenido relevante procedente de otras guías de publicación, hacemos referencia a estas guías dentro de los ítems del documento de explicación y elaboración40 (por ejemplo, PRISMA-Search41 los ítems 6 y 7, guía de presentación de informes de síntesis sin metanálisis (Synthesis Without Meta-analysis – SWiM)26 en el ítem 13d). El cuadro 1 incluye un glosario de términos utilizados en toda la declaración PRISMA 2020.
Glosario
| Revisión sistemática: revisión que utiliza de manera explícita métodos sistemáticos para recopilar y sintetizar los hallazgos de los estudios individuales que abordan una pregunta claramente formulada42.Síntesis estadística: la combinación de resultados cuantitativos de dos o más estudios individuales. Esto abarca el metanálisis de las estimaciones del efecto (descritos abajo) y otros métodos, tales como la combinación de valores de P, cálculos del rango y distribución de los efectos observados y recuento de votos basados en la dirección del efecto (consultar McKenzie y Brennan24 para ver la descripción de cada método).Metanálisis de las estimaciones del efecto: técnica estadística utilizada para sintetizar los resultados cuando se dispone de las estimaciones de los efectos de los estudios y sus variaciones, lo que permite obtener un resumen cuantitativo de los resultados24.Desenlace: evento o medida recogida de los participantes de un estudio (por ejemplo, calidad de vida, mortalidad, etc.).Resultados: combinación de una estimación puntual (por ejemplo, diferencia de medias, razón de riesgos o proporción) y una medida de su precisión (por ejemplo, intervalo de confianza o intervalo de credibilidad) para un desenlace en particular.Publicación: documento (en papel o electrónico) que proporciona información sobre un estudio individual en particular. Puede ser un artículo de revista, una preimpresión, un resumen de congreso, una entrada en un registro de estudios, un informe de un estudio clínico, una tesis, un manuscrito no publicado, un informe gubernamental o cualquier otro documento que proporcione información relevante.Registro o cita: título o resumen (o ambos) de una publicación indexada en una base de datos o en un sitio web (por ejemplo, un título o resumen de un artículo indexado en MEDLINE). Los registros que se refieren a la misma publicación (por ejemplo, el mismo artículo de revista) son publicaciones «duplicadas», sin embargo, los registros que se refieren a publicaciones meramente similares (por ejemplo, un resumen similar presentado en dos conferencias diferentes) deberían considerarse como publicaciones únicas.Estudio: investigación (por ejemplo, un ensayo clínico) que incluye un grupo definido de participantes y una o más intervenciones y desenlaces. Un «estudio» puede tener múltiples publicaciones. Por ejemplo, las publicaciones podrían incluir el protocolo, el plan de análisis estadístico, las características basales, los resultados para el desenlace primario, los resultados de los daños o eventos adversos, los resultados para los desenlaces secundarios y los resultados de análisis adicionales de los mediadores y moderadores del efecto de un tratamiento. |
El objetivo de la declaración PRISMA 2020 no es orientar la realización de revisiones sistemáticas, para las que se dispone de varios recursos42–45. Sin embargo, estar familiarizado con PRISMA 2020 es útil a la hora de planificar y realizar revisiones sistemáticas para garantizar que se captura toda la información recomendada. Además, PRISMA 2020 no debe utilizarse para evaluar la realización o la calidad metodológica de las revisiones sistemáticas, porque ya existen herramientas para este propósito29,30. PRISMA 2020 tampoco está destinada a documentar la publicación de protocolos de revisión sistemática, para lo que ya hay disponible una declaración específica (Declaración PRISMA para protocolos [PRISMA-P] 201546,47). Por último, se han desarrollado extensiones de la declaración PRISMA 2009 para orientar la presentación de publicaciones de metanálisis en red48, metanálisis de datos de participantes individuales49, revisiones sistemáticas de daños50, revisiones sistemáticas de estudios de precisión de pruebas diagnósticas51, revisiones exploratorias (scoping reviews)52. Para este tipo de revisiones recomendamos a los autores que documenten su revisión de acuerdo con las recomendaciones de PRISMA 2020 junto con las orientaciones específicas de cada extensión.
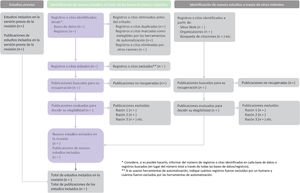
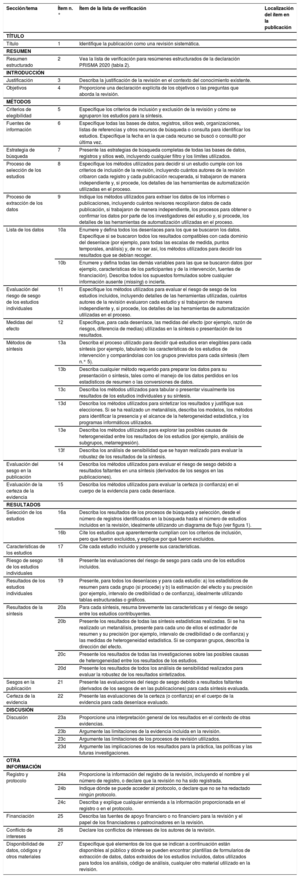
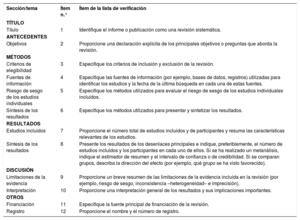
Cómo utilizar PRISMA 2020La declaración PRISMA 2020 (incluidas las listas de verificación, el documento de explicación y elaboración y el diagrama de flujo) sustituye a la declaración PRISMA 2009, que ya no debe utilizarse. El cuadro 2 resume los principales cambios de la declaración PRISMA 2009. La lista de verificación PRISMA 2020 incluye siete secciones o dominios con 27 ítems, algunos de las cuales incluyen subítems (tabla 1). En la declaración PRISMA 2020 se incluye una lista de verificación para la publicación de resúmenes estructurados de revisiones sistemáticas presentados en revistas y congresos. Esta lista de verificación para resúmenes estructurados es una actualización de la declaración de 2013 «PRISMA for Abstracts»53 que incluye contenido nuevo y modificado en la declaración PRISMA 2020 (tabla 2). Se proporciona una plantilla PRISMA para el diagrama de flujo, que se puede modificar en función de si la revisión sistemática es original o actualizada (figura 1).
Cambios importantes respecto a la declaración PRISMA 2009
| Inclusión de la publicación del resumen en la lista de verificación en PRISMA 2020 (ver ítem n.° 2 y tabla 2).Traslado del ítem «Protocolo y registro» del inicio de la sección «Métodos» de la lista de verificación a una nueva sección «Otros», con la inclusión de un subítem en el que se recomienda a los autores describir las enmiendas a la información proporcionada en el registro o en el protocolo (ver ítems n.° 24a a 24c).Modificación del ítem «Búsqueda» para recomendar a los autores que presenten las estrategias de búsqueda completas usadas en todas las bases de datos, registros y sitios web buscados, no solo para una base de datos como mínimo (ver ítem n.° 7).Modificación del ítem «Selección de los estudios» en la sección «Métodos» para recalcar la necesidad de indicar cuántos autores de la revisión cribaron cada registro y cada informe o publicación recuperada, si trabajaron de manera independiente y, si procede, los detalles de las herramientas de automatización usadas en el proceso (ver ítem n.° 8).Inclusión de un subítem al ítem «Lista de los datos» para recomendar a los autores que indiquen cómo se definieron los desenlaces, qué resultados se buscaron y los métodos para seleccionar un subconjunto de resultados de los estudios incluidos (ver ítem n.° 10a).División del ítem «Síntesis de resultados» en la sección «Métodos» en seis subítems en los que se recomienda a los autores que describan los procesos utilizados para decidir qué estudios eran elegibles para cada síntesis; los métodos requeridos para preparar los datos para la síntesis; los métodos utilizados para tabular o mostrar visualmente los resultados de los estudios individuales y las síntesis; los métodos utilizados para sintetizar los resultados; los métodos utilizados para explorar las posibles causas de heterogeneidad entre los resultados de los estudios; y el análisis de sensibilidad utilizado para evaluar la robustez de los resultados sintetizados (ver ítems n.° 13a a 13f).Inclusión de un subítem al ítem «Selección de los estudios» en la sección «Resultados» para recomendar a los autores que citen los estudios que aparentemente cumplían con los criterios de inclusión, pero que fueron excluidos, y expliquen por qué fueron excluidos (ver ítem n.° 16b).División del ítem «Síntesis de resultados» de la sección «Resultados» en cuatro subítems para recomendar a los autores que resuman las características y el riesgo de sesgo de los estudios que contribuyen a la síntesis; presenten los resultados de todas las síntesis realizadas; presenten los resultados de cualquier investigación de las posibles causas de heterogeneidad entre los resultados de los estudios; y presenten los resultados de cualquier análisis de sensibilidad (ver ítems n.° 20a a 20d).Inclusión de nuevos ítems para recomendar a los autores que indiquen o publiquen los métodos y resultados de la evaluación de la certeza (o confianza) en el cuerpo de la evidencia para cada desenlace (ver ítems n.° 15 y n.° 22).Inclusión de un nuevo ítem para recomendar a los autores que declaren cualquier conflicto de intereses (ver ítem n.° 26).Inclusión de un nuevo ítem para recomendar a los autores que indiquen si los datos, el código de análisis y otros materiales usados en la revisión están disponibles públicamente y, en caso de ser así, dónde se pueden encontrar (ver ítem n.° 27). |
Lista de verificación PRISMA 2020
| Sección/tema | Ítem n.° | Ítem de la lista de verificación | Localización del ítem en la publicación |
|---|---|---|---|
| TÍTULO | |||
| Título | 1 | Identifique la publicación como una revisión sistemática. | |
| RESUMEN | |||
| Resumen estructurado | 2 | Vea la lista de verificación para resúmenes estructurados de la declaración PRISMA 2020 (tabla 2). | |
| INTRODUCCIÓN | |||
| Justificación | 3 | Describa la justificación de la revisión en el contexto del conocimiento existente. | |
| Objetivos | 4 | Proporcione una declaración explícita de los objetivos o las preguntas que aborda la revisión. | |
| MÉTODOS | |||
| Criterios de elegibilidad | 5 | Especifique los criterios de inclusión y exclusión de la revisión y cómo se agruparon los estudios para la síntesis. | |
| Fuentes de información | 6 | Especifique todas las bases de datos, registros, sitios web, organizaciones, listas de referencias y otros recursos de búsqueda o consulta para identificar los estudios. Especifique la fecha en la que cada recurso se buscó o consultó por última vez. | |
| Estrategia de búsqueda | 7 | Presente las estrategias de búsqueda completas de todas las bases de datos, registros y sitios web, incluyendo cualquier filtro y los límites utilizados. | |
| Proceso de selección de los estudios | 8 | Especifique los métodos utilizados para decidir si un estudio cumple con los criterios de inclusión de la revisión, incluyendo cuántos autores de la revisión cribaron cada registro y cada publicación recuperada, si trabajaron de manera independiente y, si procede, los detalles de las herramientas de automatización utilizadas en el proceso. | |
| Proceso de extracción de los datos | 9 | Indique los métodos utilizados para extraer los datos de los informes o publicaciones, incluyendo cuántos revisores recopilaron datos de cada publicación, si trabajaron de manera independiente, los procesos para obtener o confirmar los datos por parte de los investigadores del estudio y, si procede, los detalles de las herramientas de automatización utilizadas en el proceso. | |
| Lista de los datos | 10a | Enumere y defina todos los desenlaces para los que se buscaron los datos. Especifique si se buscaron todos los resultados compatibles con cada dominio del desenlace (por ejemplo, para todas las escalas de medida, puntos temporales, análisis) y, de no ser así, los métodos utilizados para decidir los resultados que se debían recoger. | |
| 10b | Enumere y defina todas las demás variables para las que se buscaron datos (por ejemplo, características de los participantes y de la intervención, fuentes de financiación). Describa todos los supuestos formulados sobre cualquier información ausente (missing) o incierta. | ||
| Evaluación del riesgo de sesgo de los estudios individuales | 11 | Especifique los métodos utilizados para evaluar el riesgo de sesgo de los estudios incluidos, incluyendo detalles de las herramientas utilizadas, cuántos autores de la revisión evaluaron cada estudio y si trabajaron de manera independiente y, si procede, los detalles de las herramientas de automatización utilizadas en el proceso. | |
| Medidas del efecto | 12 | Especifique, para cada desenlace, las medidas del efecto (por ejemplo, razón de riesgos, diferencia de medias) utilizadas en la síntesis o presentación de los resultados. | |
| Métodos de síntesis | 13a | Describa el proceso utilizado para decidir qué estudios eran elegibles para cada síntesis (por ejemplo, tabulando las características de los estudios de intervención y comparándolas con los grupos previstos para cada síntesis (ítem n.° 5). | |
| 13b | Describa cualquier método requerido para preparar los datos para su presentación o síntesis, tales como el manejo de los datos perdidos en los estadísticos de resumen o las conversiones de datos. | ||
| 13c | Describa los métodos utilizados para tabular o presentar visualmente los resultados de los estudios individuales y su síntesis. | ||
| 13d | Describa los métodos utilizados para sintetizar los resultados y justifique sus elecciones. Si se ha realizado un metanálisis, describa los modelos, los métodos para identificar la presencia y el alcance de la heterogeneidad estadística, y los programas informáticos utilizados. | ||
| 13e | Describa los métodos utilizados para explorar las posibles causas de heterogeneidad entre los resultados de los estudios (por ejemplo, análisis de subgrupos, metarregresión). | ||
| 13f | Describa los análisis de sensibilidad que se hayan realizado para evaluar la robustez de los resultados de la síntesis. | ||
| Evaluación del sesgo en la publicación | 14 | Describa los métodos utilizados para evaluar el riesgo de sesgo debido a resultados faltantes en una síntesis (derivados de los sesgos en las publicaciones). | |
| Evaluación de la certeza de la evidencia | 15 | Describa los métodos utilizados para evaluar la certeza (o confianza) en el cuerpo de la evidencia para cada desenlace. | |
| RESULTADOS | |||
| Selección de los estudios | 16a | Describa los resultados de los procesos de búsqueda y selección, desde el número de registros identificados en la búsqueda hasta el número de estudios incluidos en la revisión, idealmente utilizando un diagrama de flujo (ver figura 1). | |
| 16b | Cite los estudios que aparentemente cumplían con los criterios de inclusión, pero que fueron excluidos, y explique por qué fueron excluidos. | ||
| Características de los estudios | 17 | Cite cada estudio incluido y presente sus características. | |
| Riesgo de sesgo de los estudios individuales | 18 | Presente las evaluaciones del riesgo de sesgo para cada uno de los estudios incluidos. | |
| Resultados de los estudios individuales | 19 | Presente, para todos los desenlaces y para cada estudio: a) los estadísticos de resumen para cada grupo (si procede) y b) la estimación del efecto y su precisión (por ejemplo, intervalo de credibilidad o de confianza), idealmente utilizando tablas estructuradas o gráficos. | |
| Resultados de la síntesis | 20a | Para cada síntesis, resuma brevemente las características y el riesgo de sesgo entre los estudios contribuyentes. | |
| 20b | Presente los resultados de todas las síntesis estadísticas realizadas. Si se ha realizado un metanálisis, presente para cada uno de ellos el estimador de resumen y su precisión (por ejemplo, intervalo de credibilidad o de confianza) y las medidas de heterogeneidad estadística. Si se comparan grupos, describa la dirección del efecto. | ||
| 20c | Presente los resultados de todas las investigaciones sobre las posibles causas de heterogeneidad entre los resultados de los estudios. | ||
| 20d | Presente los resultados de todos los análisis de sensibilidad realizados para evaluar la robustez de los resultados sintetizados. | ||
| Sesgos en la publicación | 21 | Presente las evaluaciones del riesgo de sesgo debido a resultados faltantes (derivados de los sesgos de en las publicaciones) para cada síntesis evaluada. | |
| Certeza de la evidencia | 22 | Presente las evaluaciones de la certeza (o confianza) en el cuerpo de la evidencia para cada desenlace evaluado. | |
| DISCUSIÓN | |||
| Discusión | 23a | Proporcione una interpretación general de los resultados en el contexto de otras evidencias. | |
| 23b | Argumente las limitaciones de la evidencia incluida en la revisión. | ||
| 23c | Argumente las limitaciones de los procesos de revisión utilizados. | ||
| 23d | Argumente las implicaciones de los resultados para la práctica, las políticas y las futuras investigaciones. | ||
| OTRA INFORMACIÓN | |||
| Registro y protocolo | 24a | Proporcione la información del registro de la revisión, incluyendo el nombre y el número de registro, o declare que la revisión no ha sido registrada. | |
| 24b | Indique dónde se puede acceder al protocolo, o declare que no se ha redactado ningún protocolo. | ||
| 24c | Describa y explique cualquier enmienda a la información proporcionada en el registro o en el protocolo. | ||
| Financiación | 25 | Describa las fuentes de apoyo financiero o no financiero para la revisión y el papel de los financiadores o patrocinadores en la revisión. | |
| Conflicto de intereses | 26 | Declare los conflictos de intereses de los autores de la revisión. | |
| Disponibilidad de datos, códigos y otros materiales | 27 | Especifique qué elementos de los que se indican a continuación están disponibles al público y dónde se pueden encontrar: plantillas de formularios de extracción de datos, datos extraídos de los estudios incluidos, datos utilizados para todos los análisis, código de análisis, cualquier otro material utilizado en la revisión. |
Lista de verificación PRISMA 2020 para resúmenes estructurados*
| Sección/tema | Ítem n.° | Ítem de la lista de verificación |
|---|---|---|
| TÍTULO | ||
| Título | 1 | Identifique el informe o publicación como una revisión sistemática. |
| ANTECEDENTES | ||
| Objetivos | 2 | Proporcione una declaración explícita de los principales objetivos o preguntas que aborda la revisión. |
| MÉTODOS | ||
| Criterios de elegibilidad | 3 | Especifique los criterios de inclusión y exclusión de la revisión. |
| Fuentes de información | 4 | Especifique las fuentes de información (por ejemplo, bases de datos, registros) utilizadas para identificar los estudios y la fecha de la última búsqueda en cada una de estas fuentes. |
| Riesgo de sesgo de los estudios individuales | 5 | Especifique los métodos utilizados para evaluar el riesgo de sesgo de los estudios individuales incluidos. |
| Síntesis de los resultados | 6 | Especifique los métodos utilizados para presentar y sintetizar los resultados. |
| RESULTADOS | ||
| Estudios incluidos | 7 | Proporcione el número total de estudios incluidos y de participantes y resuma las características relevantes de los estudios. |
| Síntesis de los resultados | 8 | Presente los resultados de los desenlaces principales e indique, preferiblemente, el número de estudios incluidos y los participantes en cada uno de ellos. Si se ha realizado un metanálisis, indique el estimador de resumen y el intervalo de confianza o de credibilidad. Si se comparan grupos, describa la dirección del efecto (por ejemplo, qué grupo se ha visto favorecido). |
| DISCUSIÓN | ||
| Limitaciones de la evidencia | 9 | Proporcione un breve resumen de las limitaciones de la evidencia incluida en la revisión (por ejemplo, riesgo de sesgo, inconsistencia –heterogeneidad– e imprecisión). |
| Interpretación | 10 | Proporcione una interpretación general de los resultados y sus implicaciones importantes. |
| OTROS | ||
| Financiación | 11 | Especifique la fuente principal de financiación de la revisión. |
| Registro | 12 | Proporcione el nombre y el número de registro. |
Esta lista de verificación conserva los mismos ítems que se incluyeron en la declaración PRISMA para resúmenes publicada en 201348, pero ha sido revisada para que la redacción sea coherente con la declaración PRISMA 2020. Además, incluye un nuevo ítem que recomienda a los autores que especifiquen los métodos utilizados para presentar y sintetizar los resultados (ítem n.° 6).
Diagrama de flujo PRISMA 2020. El nuevo diseño se ha adaptado a partir de los diagramas de flujo propuestos por Boers70, Mayo-Wilson et al.71 y Stovold et al.72. Los recuadros en gris solo se deben completar si son aplicables; de lo contrario, deben eliminarse del diagrama de flujo. Obsérvese que un «informe» puede ser un artículo de revista, una preimpresión, un resumen de conferencia, un registro de estudio, un informe de estudio clínico, una tesis/disertación, un manuscrito inédito, un informe gubernamental o cualquier otro documento que proporcione información pertinente.
Recomendamos a los autores que revisen la declaración PRISMA 2020 en las fases iniciales del proceso de escritura, porque considerar los ítems de manera prospectiva puede ayudar a asegurar que se tienen en consideración todos los ítems. Para ayudar en el seguimiento de los ítems que han sido comunicados, el sitio web de la declaración PRISMA (http://www.prisma-statement.org/) incluye plantillas de las listas de verificación que se pueden descargar y completar (también disponibles como tabla 1 y tabla 2 del material adicional). También se creó una aplicación web que permite a los usuarios completar la lista de verificación a través de una interfaz fácil de usar54 (disponible en https://prisma.shinyapps.io/checklist/ y adaptado de la aplicación de lista de verificación de transparencia55). La lista completa puede exportarse a Word o en formato PDF. Además, se pueden descargar platillas editables del diagrama de flujo desde el sitio web de la declaración PRISMA.
Se ha preparado un documento de explicación y elaboración actualizado, en el que los autores de la declaración PRISMA 2020 explican por qué se recomienda la publicación de cada ítem, y que incluye viñetas que detallan las recomendaciones para la presentación de publicaciones (que se denominan «elementos»)40. La estructura de viñetas es nueva en PRISMA 2020 y se ha adoptado para facilitar la implantación de la guía56,57. Se presenta la lista de verificación ampliada, que comprende una versión abreviada de los «elementos» presentados en el documento de explicación y elaboración, en la que se han eliminado referencias y algunos ejemplos, y que se puede encontrar como material adicional. Se recomienda consultar el documento de explicación y elaboración si se requiere mayor claridad o información.
Las revistas y las editoriales pueden imponer límites de palabras y de secciones, así como límites en cuanto al número de tablas y figuras permitidas en la publicación principal. En estos casos, si la información relevante para algunos ítems ya aparece en un protocolo de revisión públicamente accesible, referenciar el protocolo podría ser suficiente. Alternativamente, se recomienda incluir descripciones detalladas de los métodos utilizados o resultados adicionales (por ejemplo, para desenlaces menos críticos) como archivos complementarios. Idealmente, los archivos complementarios deberían alojarse en un repositorio de acceso abierto que proporcione acceso libre y permanente al material (por ejemplo, Open Science Framework, Dryad, figshare). En la publicación principal debería incluirse una referencia o un enlace a la información adicional. Por último, si bien PRISMA 2020 proporciona una plantilla para determinar dónde se puede cumplimentar la información, la localización sugerida no debe considerarse como prescriptiva; el principio de la guía es asegurar que la información sea comunicada.
DISCUSIÓNEl uso de la declaración PRISMA 2020 tiene el potencial de beneficiar a muchos grupos de interés. Las publicaciones completas de revisiones sistemáticas permiten a los lectores evaluar la idoneidad de los métodos y, por lo tanto, la fiabilidad de los hallazgos. La presentación y el resumen de las características de los estudios que contribuyen a una síntesis permiten a los responsables de la formulación de políticas de salud y a los proveedores de atención médica evaluar la aplicabilidad de los resultados en su entorno. La descripción de la certeza del cuerpo de la evidencia para un desenlace y las implicaciones de los hallazgos puede ayudar a los responsables de la formulación de políticas, gerentes y otros responsables de la toma de decisiones a formular recomendaciones apropiadas para la práctica o las políticas. La presentación completa de todos los ítems de la declaración PRISMA 2020 también facilita la replicación y actualización de las revisiones, así como la inclusión de revisiones sistemáticas en revisiones panorámicas o revisiones de revisiones sistemáticas (overviews) y guías de práctica clínica, para que los equipos puedan aprovechar el trabajo que ya está hecho y evitar esfuerzos innecesarios en investigación35,58,59.
Los autores de la presente declaración actualizaron la declaración PRISMA 2009 adaptando la guía de EQUATOR Network para el desarrollo de guías de publicación de investigación en salud60. Evaluaron la integridad de las publicaciones de revisiones sistemáticas publicadas16,20,35,36, revisaron los ítems incluidos en otros documentos de guías de presentación de publicaciones para revisiones sistemáticas37, encuestaron a metodólogos expertos en revisiones sistemáticas y editores de revistas para conocer sus puntos de vista sobre cómo revisar la declaración original PRISMA34, difundieron los resultados en una reunión presencial y prepararon este documento a través de un proceso iterativo. Sus recomendaciones se basan en las revisiones y encuestas realizadas antes de la reunión presencial, las consideraciones teóricas sobre qué ítems facilitan la reproducción y ayudan a los usuarios a evaluar el riesgo de sesgo y la aplicabilidad de las revisiones sistemáticas, así como la experiencia de los coautores en la autoría y el uso de revisiones sistemáticas.
Se han propuesto varias estrategias para aumentar el uso de las guías de presentación de publicaciones y mejorar su presentación. Estas estrategias incluyen docentes que introduzcan la guía de presentación de publicaciones en los planes de estudios de posgrado para promover buenos hábitos de presentación de publicaciones en los inicios de la carrera científica61, revisores y editores de revistas que evalúen el cumplimiento de las guías para la presentación de publicaciones17, revisores pares que evalúen la adherencia a las guías de publicación57,62, revistas que exijan a los autores que indiquen en qué parte de su manuscrito se ha descrito cada ítem63 y autores que utilicen instrumentos de escritura en línea que les permitan completar la información en la fase de redacción56.
Intervenciones multimodales, en las que se combinan varias de estas estrategias, pueden ser más efectivas (por ejemplo, la aplicación de las listas de verificación junto con los controles editoriales)64. Sin embargo, de las 31 intervenciones propuestas para incrementar la adhesión a las guías de presentación de informes, solo se han evaluado los efectos de 11, principalmente en estudios observacionales con alto riesgo de sesgo debido a confusión (confounding)65. Por lo tanto, no está claro qué estrategias deben utilizarse. Futuras investigaciones podrían explorar las barreras y los facilitadores del uso de PRISMA 2020 por parte de los autores, los editores y los revisores, mediante el diseño de intervenciones que aborden las barreras identificadas y evalúen esas intervenciones mediante ensayos clínicos aleatorios. Para aportar información para posibles revisiones de la guía, también sería valioso llevar a cabo estudios de reflexión en voz alta (think-aloud)66 con el propósito de entender cómo los autores de revisiones sistemáticas interpretan los ítems, y estudios de fiabilidad para identificar los ítems en los que hay una interpretación variada de los mismos.
Los autores de la declaración animan a los lectores a presentar evidencia que informe sobre cualquiera de las recomendaciones de PRISMA 2020 (a través del sitio web de la declaración PRISMA: http://www.prisma-statement.org/). Para mejorar la accesibilidad a la declaración PRISMA 2020, se están llevando a cabo varias traducciones de la guía (véase las traducciones disponibles en el sitio web de la declaración PRISMA). Así mismo, también animan a los revisores y editores de revistas a dar a conocer la declaración PRISMA 2020 (por ejemplo, citándola en las «Instrucciones para los autores» de su revista), respaldando su uso y aconsejando a los editores y revisores por pares que evalúen las revisiones sistemáticas presentadas en base a la lista de verificación de la declaración PRISMA 2020, y haciendo cambios en las políticas de la revista para adaptarlas a las nuevas recomendaciones de publicación. Recomiendan que las extensiones PRISMA existentes46,48–52,67,68 se actualicen para reflejar la declaración PRISMA 2020 y aconsejan a los desarrolladores de nuevas extensiones PRISMA que utilicen PRISMA 2020 como documento de base.
CONCLUSIÓNLos autores de la declaración anticipan que la declaración PRISMA 2020 beneficiará a los autores, editores y revisores por pares de revisiones sistemáticas y a los diferentes usuarios de revisiones, incluidos los desarrolladores de guías de práctica clínica, los responsables de la formulación de políticas de salud y los proveedores de atención médica, los pacientes y otros grupos de interés.
En última instancia, esperan que la adopción de la guía conduzca a la presentación de publicaciones más transparentes, completas y precisas de las revisiones sistemáticas, que faciliten la toma de decisiones basadas en la evidencia.
FINANCIACIÓNLos autores de la presente traducción agradecen la financiación proporcionada por el fondo de publicaciones de la Vicerrectoría de Investigación y Creación de la Universidad de los Andes, Bogotá, Colombia. Así mismo, los autores agradecen a la financiación proporcionada por el Departamento de Enfermería Fundamental y Médico-Quirúrgica de la Facultad de Medicina y Ciencias de la Salud de la Universitat de Barcelona (UB), Barcelona, España.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores han aprobado la versión final del artículo. La traducción al español de PRISMA 2020 se ha desarrollado acorde a la política de traducciones oficiales del grupo PRISMA69. Esta es una traducción no oficial de un artículo que se ha publicado en el British Medical Journal40. Ni el British Medical Journal ni sus licenciantes han respaldado esta traducción. A partir de la versión original del manuscrito y las listas de comprobación, uno de los autores (J.J. Yepes-Nuñez) preparó una primera versión del manuscrito y un segundo autor (S. Alonso-Fernández) tradujo las listas de verificación. Las primeras versiones en español fueron revisadas y aprobadas por dos autores (J.J. Yepes-Nuñez y S. Alonso-Fernández), lo cual dio como resultado una segunda versión que fue revisada por una traductora (Laura Sánchez Bel) especializada en Ciencias de la Salud que adaptó el texto a un castellano neutro. La versión final de este documento fue retrotraducida y revisada y consensuada por el autor principal (M. Page) del artículo original en inglés. Un tercer autor (G. Urrútia) revisó la versión final de este documento y resolvió discrepancias entre los dos autores Yepes-Nuñez y S. Alonso-Fernández. El British Medical Journal ha autorizado la publicación de este artículo. La versión original se puede consultar en el siguiente enlace: https://doi.org/10.1136/bmj.n71.
La información relativa a la contribución de los autores de la publicación original puede consultarse en la versión original en inglés https://doi.org/10.1136/bmj.n71.
CONFLICTO DE INTERESESLos autores de esta traducción han completado el formulario de divulgación uniforme del International Committee of Medical Journal Editors y declaran no tener conflictos de intereses asociados a esta traducción.
La información relacionada con los conflictos de intereses de los autores de la publicación original puede consultarse en la versión original en inglés https://doi.org/10.1136/bmj.n71.
Juan José Yepes-Nuñeza,b, Gerard Urrútiac,d, Marta Romero-Garcíae,f y Sergio Alonso-Fernándeze,f
aFacultad de Medicina, Universidad de los Andes, Bogotá, Colombia
bHospital Universitario Fundación Santa Fe de Bogotá, Bogotá, Colombia
cCentro Cochrane Iberoamericano-Institut d’Investigació Biomèdica Sant Pau (IIB Sant Pau), Barcelona, España
dCentro de Investigación Biomédica en Red de Epidemiología y Salud Pública (CIBERESP), España
eDepartamento de Enfermería Fundamental y Médico-Quirúrgica, Facultad de Medicina y Ciencias de la Salud, Escuela de Enfermería, Universitat de Barcelona (UB), L’Hospitalet de Llobregat, Barcelona, España
fGrupo de Investigación Enfermera (GRIN), Instituto de Investigación Biomédica de Bellvitge (IDIBELL), L’Hospitalet de Llobregat, Barcelona, España
* Autor para correspondencia de la presente traducción del artículo: Carrera 1 No 18 A – 10, Bloque Q Piso 8, Código, postal 111711, Bogotá , Colombia.
Correo electrónico: jj.yepesn@uniandes.edu.co (J.J. Yepes-Nuñez).
Anexo 1 se detallan los nombres y filiaciones de los autores de la presente traducción de este artículo.
Nota: En este artículo se presenta la traducción al español de la declaración PRISMA 2020 para revisiones sistemáticas. La versión original del artículo en inglés puede consultarse en: Page MJ, McKenzie JE, Bossuyt PM, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:n71. https://doi.org/10.1136/bmj.n71. El British Medical Journal ha autorizado el uso del material original de la publicación en inglés para la traducción realizada en el presente artículo. En el Anexo 1 se detallan los nombres y filiaciones de los autores de la presente traducción de este artículo.