La ablación con radiofrecuencia es un tratamiento de primera línea para una gran cantidad de taquiarritmias supraventriculares y algunas ventriculares, por su alta tasa de éxitos y baja probabilidad de complicaciones. Aunque la mayoría de éstas se relacionan con la técnica de cateterismo, algunas se deben al propio efecto de la radiofrecuencia. Presentamos el caso de un paciente con arritmia ventricular repetitiva no sostenida que tras la ablación eficaz con radiofrecuencia desarrolló una taquicardia ventricular monomórfica sostenida e incesante que requirió un nuevo procedimiento de ablación.
Palabras clave
Proarritmia
Ablación con catéter
Radiofrecuencia
Taquicardia ventricular
INTRODUCCIÓN
El efecto de la radiofrecuencia (RF) sobre el miocardio auricular o ventricular ofrece como principales ventajas, frente a la aplicación de descargas de corriente directa (DC), un mejor control del tamaño de la lesión y una alta frecuencia de las ondas que evita la despolarización de los miocitos durante la aplicación 1. Por estas razones, la incidencia de complicaciones es significativamente baja 2,3. Aunque la mayoría de éstas se relacionan con la técnica de cateterismo, algunas se deben al propio efecto de la radiofrecuencia. Presentamos un caso de probable proarritmia inducida por la ablación con catéter mediante RF del lugar de origen de una taquicardia ventricular monomórfica repetitiva.
CASO CLÍNICO
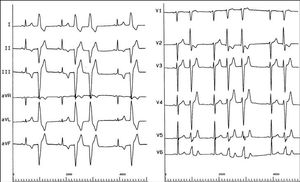
Varón de 17 años, deportista, sin antecedentes familiares de muerte súbita, que comenzó en marzo de 1997 a presentar episodios de mareo y palpitaciones ligeras relacionadas con el esfuerzo y situaciones de estrés emocional. La exploración física fue normal. En el ECG se apreciaron frecuentes extrasístoles ventriculares (EV) monomórficas, a menudo en forma de dobletes, con imagen de bloqueo de rama izquierda (BRI) y eje superior izquierdo (SI) (fig. 1). En el ecocardiograma se observó un ventrículo izquierdo (VI) dilatado (diámetro telediastólico de 62 mm) con función sistólica conservada. Durante la prueba de esfuerzo, que fue negativa para isquemia, alcanzó la V etapa del protocolo de Bruce y se registró la supresión de la extrasistolia ventricular durante el ejercicio, con reaparición de la misma en la fase de recuperación. Tras el estudio cardiológico se optó por llevar a cabo el seguimiento clínico del paciente sin tratamiento con fármacos antiarrítmicos.
Fig. 1. ECG de 12 derivaciones en ritmo sinusal con frecuentes extrasístoles ventriculares (EV) aislados o en dobletes, monomórficos, con morfología de bloqueo de rama izquierda y eje superior izquierdo.
Un año más tarde acudió a revisión refiriendo astenia, fatigabilidad fácil de aparición progresiva, palpitaciones frecuentes con mareo asociado y síncope. En el ECG se observaron extrasístoles ventriculares (EV) monomórficas frecuentes, tanto aisladas como en dobletes y tripletes. La radiografía de tórax puso de manifiesto una silueta cardíaca en el límite superior de la normalidad y el ecocardiograma un VI más dilatado (DTDVI = 76 mm) con función sistólica en límites bajos de la normalidad (FEVI = 53%). En el Holter se registraron EV muy frecuentes (55% del total de complejos registrados) y rachas de taquicardia ventricular monomórfica no sostenida (TVMNS). En la ergometría se apreció un comportamiento de las EV similar al descrito con anterioridad. Se instauró tratamiento con carvedilol y posteriormente con quinidina, que no fueron eficaces para suprimir los EV.
Dada la sintomatología del paciente, las dimensiones del VI y la poca eficacia de los fármacos antiarrítmicos empleados, se decidió realizar un estudio electrofisiológico y un intento de ablación del sustrato arritmogénico. Éste se realizó en condiciones basales y tras haber retirado los fármacos antiarrítmicos por un período de tiempo equivalente a cinco vidas medias. Se introdujeron tres catéteres por la vena femoral derecha, colocándose bajo control fluoroscópico en la orejuela de la aurícula derecha, ápex de ventrículo derecho y región del haz de His. En el laboratorio de electrofisiología, la arritmia desapareció tras la sedación. Se realizó el protocolo de estimulación ventricular de Josephson en condiciones basales sin conseguir inducir taquicardias. Seguidamente se administró isoproterenol a dosis bajas, con lo que reaparecieron las EV, que nuevamente desaparecieron al incrementar la dosis. Posteriormente se administró propranolol a una dosis de 0,2 mg/kg de peso, reapareciendo la extrasistolia. Con ninguna de estas maniobras se logró la inducción de taquicardia ventricular.
Finalmente, se introdujo un catéter de ablación de 7 French y electrodo distal de 4 mm (Marinr MC., Medtronic) y se procedió a la cartografía de activación de las extrasístoles, empleando registros bipolares y unipolares no filtrados, y a la topoestimulación. A nivel posteroseptal y basal del VD se encontró un lugar donde se registraba una actividad presistólica de -10 ms y una concordancia en las doce derivaciones del ECG de superficie durante la topoestimulación. En dicha posición se realizaron tres aplicaciones de RF durante las cuales se produjo un incremento en la frecuencia de aparición de las EV, e incluso rachas de TVMNS de igual morfología a las EV. Después de la tercera aplicación se consiguió la supresión de la extrasistolia ventricular tanto en condiciones basales como bajo la infusión de isoproterenol.
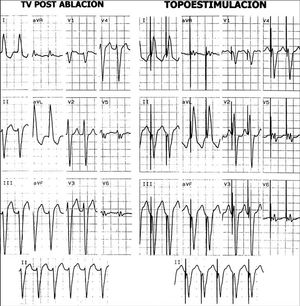
El paciente fue trasladado a la planta de hospitalización bajo monitorización telemétrica. Al cabo de 5 horas apareció, de forma espontánea, una taquicardia ventricular monomórfica sostenida (TVMS) e incesante, con una morfología parecida a la de los EV (fig. 2) con buena tolerancia clínica y hemodinámica. Se realizaron múltiples intentos de reversión farmacológica (procainamida, ATP, verapamil y amiodarona) que no fueron eficaces, por lo que se realizó un nuevo estudio electrofisiológico al día siguiente.
Fig. 2. Izquierda: ECG de 12 derivaciones durante la taquicardia monomórfica sostenida incesante que desarrolló el paciente varias horas después del primer procedimiento de ablación. Obsérvese la morfología, parecida a la de los extrasístoles ventriculares (EV). Derecha: topoestimulación en el lugar de aplicación de radiofrecuencia durante el segundo procedimiento de ablación. Existe una concordancia casi total en la morfología del QRS en las 12 derivaciones del ECG.
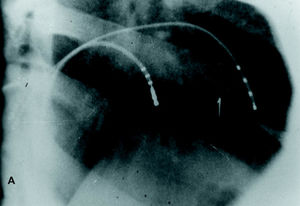
En este segundo procedimiento, al colocar el catéter en el lugar de la última aplicación de RF del primer estudio (fig. 3), inmediatamente, y por probable efecto mecánico, la taquicardia revirtió súbitamente a ritmo sinusal estable, con trastornos secundarios de la repolarización compatibles con el fenómeno de memoria cardíaca. En dicho punto se realizó topoestimulación desde el par distal del catéter de ablación, obteniéndose una morfología concordante óptima (fig. 2). Se realizó una aplicación de RF en esta localización, durante la cual, una vez más, se produjeron múltiples extrasístoles seguidas de ritmo sinusal estable con los trastornos de repolarización anteriormente descritos. Tras este segundo procedimiento no se produjeron arritmias durante la monitorización telemétrica en las 48 h siguientes a la ablación. Durante un seguimiento de 12 meses, el paciente no ha presentado síntomas. El Holter de control demostró ausencia de arritmias ventriculares y el ecocardiograma una normalización de la función y de las dimensiones del VI.
Fig. 3. Posición radiológica del catéter de ablación en el lugar de radiofrecuencia eficaz durante el segundo procedimiento. A: proyección oblicua anterior derecha 30°. B: proyección oblicua anterior izquierda 45°. C: esquema representativo del lugar de aplicación en ambas proyecciones.
DISCUSIÓN
Desde los inicios de la ablación con RF, en 1989, como terapia definitiva o paliativa de las arritmias cardíacas, hasta nuestros días, se ha demostrado que es un procedimiento relativamente seguro, con tasas de complicaciones mayores y menores bajas (< 0,05 y 1,5%, respectivamente) 2. La mayor parte de las complicaciones se atribuyen al procedimiento de cateterismo de los vasos periféricos, entre las que se cuentan neumotórax, trombosis arterial, trombosis venosa con o sin embolismo pulmonar, hematomas, seudoaneurisma femoral e infecciones, entre otras 3. Una pequeña proporción del total de complicaciones puede atribuirse a los efectos propios de la RF, por ejemplo, accidentes coronarios (0,7%), taponamientos cardíacos (0,7%) y bloqueo AV temporal o definitivo (0,7%) 3. Mucho menos frecuentes son las complicaciones proarrítmicas, de las que sólo existen casos aislados descritos en la bibliografía 4,5. Por otra parte, cada tipo de procedimiento de ablación tiene su propio riesgo de complicaciones. En el estudio MERFS 3, del total de procedimientos complicados se observó que la modificación de la unión AV en taquicardias por reentrada intranodal obtuvo la mayor incidencia de complicaciones (8%), seguida de la ablación de taquicardias ventriculares (7,5%), ablación de flúter auricular (5,0%), de vía accesoria (4,5%) y del nodo AV (3,2%). Aunque los procedimientos de ablación de taquicardia ventricular ocupan el segundo lugar en complicaciones, la proporción de episodios arrítmicos en esos casos fue muy baja en comparación con la incidencia de embolismos periféricos.
Se ha postulado que la baja incidencia de alteraciones arrítmicas de la RF se debe precisamente a su principal fundamento físico: emisión de microondas en el rango de 10 kHz a 900 MHz 6, que en general no despolarizan el tejido miocárdico excitable 7, y a la relativamente baja intensidad de energía aplicada durante un período corto de tiempo, que permite al operador controlar el tamaño de la lesión.
Sin embargo, no hay que olvidar las modificaciones en las propiedades electrofisiológicas que la hipertermia generada por la RF produce en el tejido miocárdico y que incluyen despolarización de la membrana, pérdida de la excitabilidad y automatismo anormal, que pueden ser considerados como mecanismos inductores de taquiarritmias durante la ablación 8. El caso presentado no se adapta a los mecanismos conocidos de proarritmia de la RF, pues el episodio ocurrió varias horas después de la aplicación de la misma. Aunque el bloqueo mecánico producido durante la colocación del catéter de ablación en el VD impidió estudiar el mecanismo electrofisiológico de esta taquicardia, cabe suponer que cambios en el miocardio no bien conocidos proporcionaron el sustrato adecuado para la aparición y mantenimiento de una arritmia ventricular sostenida. Por consiguiente, aunque la ablación con RF de sustratos arritmogénicos es un procedimiento eficaz y seguro en una gran variedad de taquiarritmias, debe contemplarse el riesgo de proarritmia cuando se indica este procedimiento y hace conveniente la monitorización electrocardiográfica tras la ablación de taquicardias ventriculares.
El efecto de la radiofrecuencia (RF) sobre el miocardio auricular o ventricular ofrece como principales ventajas, frente a la aplicación de descargas de corriente directa (DC), un mejor control del tamaño de la lesión y una alta frecuencia de las ondas que evita la despolarización de los miocitos durante la aplicación 1. Por estas razones, la incidencia de complicaciones es significativamente baja 2,3. Aunque la mayoría de éstas se relacionan con la técnica de cateterismo, algunas se deben al propio efecto de la radiofrecuencia. Presentamos un caso de probable proarritmia inducida por la ablación con catéter mediante RF del lugar de origen de una taquicardia ventricular monomórfica repetitiva.
CASO CLÍNICO
Varón de 17 años, deportista, sin antecedentes familiares de muerte súbita, que comenzó en marzo de 1997 a presentar episodios de mareo y palpitaciones ligeras relacionadas con el esfuerzo y situaciones de estrés emocional. La exploración física fue normal. En el ECG se apreciaron frecuentes extrasístoles ventriculares (EV) monomórficas, a menudo en forma de dobletes, con imagen de bloqueo de rama izquierda (BRI) y eje superior izquierdo (SI) (fig. 1). En el ecocardiograma se observó un ventrículo izquierdo (VI) dilatado (diámetro telediastólico de 62 mm) con función sistólica conservada. Durante la prueba de esfuerzo, que fue negativa para isquemia, alcanzó la V etapa del protocolo de Bruce y se registró la supresión de la extrasistolia ventricular durante el ejercicio, con reaparición de la misma en la fase de recuperación. Tras el estudio cardiológico se optó por llevar a cabo el seguimiento clínico del paciente sin tratamiento con fármacos antiarrítmicos.
Fig. 1. ECG de 12 derivaciones en ritmo sinusal con frecuentes extrasístoles ventriculares (EV) aislados o en dobletes, monomórficos, con morfología de bloqueo de rama izquierda y eje superior izquierdo.
Un año más tarde acudió a revisión refiriendo astenia, fatigabilidad fácil de aparición progresiva, palpitaciones frecuentes con mareo asociado y síncope. En el ECG se observaron extrasístoles ventriculares (EV) monomórficas frecuentes, tanto aisladas como en dobletes y tripletes. La radiografía de tórax puso de manifiesto una silueta cardíaca en el límite superior de la normalidad y el ecocardiograma un VI más dilatado (DTDVI = 76 mm) con función sistólica en límites bajos de la normalidad (FEVI = 53%). En el Holter se registraron EV muy frecuentes (55% del total de complejos registrados) y rachas de taquicardia ventricular monomórfica no sostenida (TVMNS). En la ergometría se apreció un comportamiento de las EV similar al descrito con anterioridad. Se instauró tratamiento con carvedilol y posteriormente con quinidina, que no fueron eficaces para suprimir los EV.
Dada la sintomatología del paciente, las dimensiones del VI y la poca eficacia de los fármacos antiarrítmicos empleados, se decidió realizar un estudio electrofisiológico y un intento de ablación del sustrato arritmogénico. Éste se realizó en condiciones basales y tras haber retirado los fármacos antiarrítmicos por un período de tiempo equivalente a cinco vidas medias. Se introdujeron tres catéteres por la vena femoral derecha, colocándose bajo control fluoroscópico en la orejuela de la aurícula derecha, ápex de ventrículo derecho y región del haz de His. En el laboratorio de electrofisiología, la arritmia desapareció tras la sedación. Se realizó el protocolo de estimulación ventricular de Josephson en condiciones basales sin conseguir inducir taquicardias. Seguidamente se administró isoproterenol a dosis bajas, con lo que reaparecieron las EV, que nuevamente desaparecieron al incrementar la dosis. Posteriormente se administró propranolol a una dosis de 0,2 mg/kg de peso, reapareciendo la extrasistolia. Con ninguna de estas maniobras se logró la inducción de taquicardia ventricular.
Finalmente, se introdujo un catéter de ablación de 7 French y electrodo distal de 4 mm (Marinr MC., Medtronic) y se procedió a la cartografía de activación de las extrasístoles, empleando registros bipolares y unipolares no filtrados, y a la topoestimulación. A nivel posteroseptal y basal del VD se encontró un lugar donde se registraba una actividad presistólica de -10 ms y una concordancia en las doce derivaciones del ECG de superficie durante la topoestimulación. En dicha posición se realizaron tres aplicaciones de RF durante las cuales se produjo un incremento en la frecuencia de aparición de las EV, e incluso rachas de TVMNS de igual morfología a las EV. Después de la tercera aplicación se consiguió la supresión de la extrasistolia ventricular tanto en condiciones basales como bajo la infusión de isoproterenol.
El paciente fue trasladado a la planta de hospitalización bajo monitorización telemétrica. Al cabo de 5 horas apareció, de forma espontánea, una taquicardia ventricular monomórfica sostenida (TVMS) e incesante, con una morfología parecida a la de los EV (fig. 2) con buena tolerancia clínica y hemodinámica. Se realizaron múltiples intentos de reversión farmacológica (procainamida, ATP, verapamil y amiodarona) que no fueron eficaces, por lo que se realizó un nuevo estudio electrofisiológico al día siguiente.
Fig. 2. Izquierda: ECG de 12 derivaciones durante la taquicardia monomórfica sostenida incesante que desarrolló el paciente varias horas después del primer procedimiento de ablación. Obsérvese la morfología, parecida a la de los extrasístoles ventriculares (EV). Derecha: topoestimulación en el lugar de aplicación de radiofrecuencia durante el segundo procedimiento de ablación. Existe una concordancia casi total en la morfología del QRS en las 12 derivaciones del ECG.
En este segundo procedimiento, al colocar el catéter en el lugar de la última aplicación de RF del primer estudio (fig. 3), inmediatamente, y por probable efecto mecánico, la taquicardia revirtió súbitamente a ritmo sinusal estable, con trastornos secundarios de la repolarización compatibles con el fenómeno de memoria cardíaca. En dicho punto se realizó topoestimulación desde el par distal del catéter de ablación, obteniéndose una morfología concordante óptima (fig. 2). Se realizó una aplicación de RF en esta localización, durante la cual, una vez más, se produjeron múltiples extrasístoles seguidas de ritmo sinusal estable con los trastornos de repolarización anteriormente descritos. Tras este segundo procedimiento no se produjeron arritmias durante la monitorización telemétrica en las 48 h siguientes a la ablación. Durante un seguimiento de 12 meses, el paciente no ha presentado síntomas. El Holter de control demostró ausencia de arritmias ventriculares y el ecocardiograma una normalización de la función y de las dimensiones del VI.
Fig. 3. Posición radiológica del catéter de ablación en el lugar de radiofrecuencia eficaz durante el segundo procedimiento. A: proyección oblicua anterior derecha 30°. B: proyección oblicua anterior izquierda 45°. C: esquema representativo del lugar de aplicación en ambas proyecciones.
DISCUSIÓN
Desde los inicios de la ablación con RF, en 1989, como terapia definitiva o paliativa de las arritmias cardíacas, hasta nuestros días, se ha demostrado que es un procedimiento relativamente seguro, con tasas de complicaciones mayores y menores bajas (< 0,05 y 1,5%, respectivamente) 2. La mayor parte de las complicaciones se atribuyen al procedimiento de cateterismo de los vasos periféricos, entre las que se cuentan neumotórax, trombosis arterial, trombosis venosa con o sin embolismo pulmonar, hematomas, seudoaneurisma femoral e infecciones, entre otras 3. Una pequeña proporción del total de complicaciones puede atribuirse a los efectos propios de la RF, por ejemplo, accidentes coronarios (0,7%), taponamientos cardíacos (0,7%) y bloqueo AV temporal o definitivo (0,7%) 3. Mucho menos frecuentes son las complicaciones proarrítmicas, de las que sólo existen casos aislados descritos en la bibliografía 4,5. Por otra parte, cada tipo de procedimiento de ablación tiene su propio riesgo de complicaciones. En el estudio MERFS 3, del total de procedimientos complicados se observó que la modificación de la unión AV en taquicardias por reentrada intranodal obtuvo la mayor incidencia de complicaciones (8%), seguida de la ablación de taquicardias ventriculares (7,5%), ablación de flúter auricular (5,0%), de vía accesoria (4,5%) y del nodo AV (3,2%). Aunque los procedimientos de ablación de taquicardia ventricular ocupan el segundo lugar en complicaciones, la proporción de episodios arrítmicos en esos casos fue muy baja en comparación con la incidencia de embolismos periféricos.
Se ha postulado que la baja incidencia de alteraciones arrítmicas de la RF se debe precisamente a su principal fundamento físico: emisión de microondas en el rango de 10 kHz a 900 MHz 6, que en general no despolarizan el tejido miocárdico excitable 7, y a la relativamente baja intensidad de energía aplicada durante un período corto de tiempo, que permite al operador controlar el tamaño de la lesión.
Sin embargo, no hay que olvidar las modificaciones en las propiedades electrofisiológicas que la hipertermia generada por la RF produce en el tejido miocárdico y que incluyen despolarización de la membrana, pérdida de la excitabilidad y automatismo anormal, que pueden ser considerados como mecanismos inductores de taquiarritmias durante la ablación 8. El caso presentado no se adapta a los mecanismos conocidos de proarritmia de la RF, pues el episodio ocurrió varias horas después de la aplicación de la misma. Aunque el bloqueo mecánico producido durante la colocación del catéter de ablación en el VD impidió estudiar el mecanismo electrofisiológico de esta taquicardia, cabe suponer que cambios en el miocardio no bien conocidos proporcionaron el sustrato adecuado para la aparición y mantenimiento de una arritmia ventricular sostenida. Por consiguiente, aunque la ablación con RF de sustratos arritmogénicos es un procedimiento eficaz y seguro en una gran variedad de taquiarritmias, debe contemplarse el riesgo de proarritmia cuando se indica este procedimiento y hace conveniente la monitorización electrocardiográfica tras la ablación de taquicardias ventriculares.
Bibliografía
[1]
Comparison of catheter ablation using radiofrequency versus direct current energy: biophysical, electrophysiologic and pathologic observations. J Am Coll Cardiol 1991; 18: 1091-1097.
[2]
Complications des ablations par radiofrequence. Arch Mal Coeur 1996; 89: 1599-1605.
[3]
The Multicentre European Radiofrequency Survey (MERFS): complications of radiofrequency catheter ablation of arrhythmias. The Multicentre European Radiofrequency Survey (MERFS) investigators of the Working Group on Arrhythmias of the European Society of Cardiology. Eur Heart J 1993; 14: 1644-1653.
[4]
Ventricular fibrillation after successful radiofrequency catheter ablation of idiopathic right ventricular tachycardia. Am Heart J 1994; 128: 1044-1045.
[5]
Ventricular fibrillation after radiofrequency ablation of the atrioventricular node. Arch Mal Coeur Vaiss 1997; 90: 411-414.
[6]
Physics and engineering of transcatheter cardiac tissue ablation. J Am Coll Cardiol 1993; 22: 921-932.
[7]
Radiofrequency ablation. En: Zipes DP, Jalife J, editores. Cardiac electrophysiology. Filadelfia: WB Saunders, 1990; 997.
[8]
Cellular electrophysiological effects of hyperthermia on isolated guinea pig papillary muscle. Circulation 1993; 88: 1826-1831.