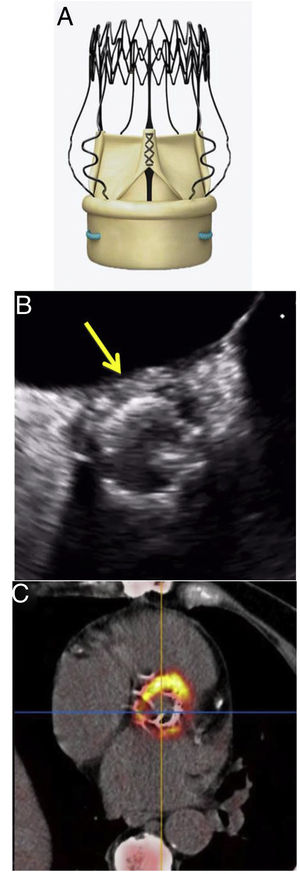
La aparición de la prótesis biológica aórtica sin sutura Perceval S (LivaNova, Italia) ha supuesto un avance en el desarrollo de los sustitutos valvulares, sobre todo para pacientes con perfil de riesgo moderado-alto1.
Esta nueva prótesis está formada por 3 hojas de pericardio bovino, montadas sobre un stent externo flexible y colapsable de nitinol (figura 1). Favorece el abordaje mínimamente invasivo y la disminución de los tiempos quirúrgicos, así como una reducción en la morbimortalidad posoperatoria. Su diseño mejora el perfil hemodinámico con menores gradientes transvalvulares en el seguimiento y menos casos de desproporción entre prótesis y paciente, lo que la convierte en la sustituta idónea para pacientes con anillo aórtico pequeño o situaciones complicadas, como la endocarditis infecciosa2. Todas estas ventajas han dado lugar a una rápida popularización de su empleo en múltiples servicios de cirugía cardiaca europeos.
La endocarditis infecciosa es una enfermedad con una alta morbimortalidad, cuya forma más grave es la endocarditis valvular protésica (EVP). La EVP se presenta en aproximadamente el 1-6% de los pacientes portadores de prótesis cardiacas, y constituye el 10-30% de todos los casos de endocarditis infecciosa. Su tratamiento quirúrgico, necesario en la mayoría de los pacientes, es a menudo un reto, con una morbimortalidad perioperatorias significativas3.
En los últimos 10 años la prótesis Perceval S se ha situado como el sustituto biológico de elección en nuestro servicio, y se emplea en pacientes mayores de 70 años y con perfil de riesgo moderado-alto, con un seguimiento medio cercano a los 7 años y una baja tasa de complicaciones. Se realizó un estudio observacional retrospectivo, con el consentimiento ético del hospital y de los pacientes, para analizar la prevalencia y las características de presentación de la EVP en este tipo de prótesis, sobre todo en lo que se refiere al diagnóstico por imagen. Desde 2015 se han implantado 670 prótesis Perceval S y se han diagnosticado 14 EVP (2,1%) en ellas. Esta cifra supone el 6,4% de todas las EVP tratadas en nuestro centro en el mismo periodo (n=220).
En la tabla 1 se describen las características clínicas, el perfil microbiológico, los hallazgos en las pruebas de imagen y la evolución de los 14 pacientes con EVP. Cabe destacar que 11 casos fueron EVP precoces, con un lapso> 3 meses tras la cirugía, y el germen más frecuente fue Staphylococcus epidermidis (n=7).
Características preoperatorias, clínicas y microbiológicas
EPOC: enfermedad pulmonar obstructiva crónica; ETE: ecocardigrama transesofágico; IQ: intervención quirúrgica; IRC: insuficiencia renal crónica; NA: no aplicable (paciente desestimado para cirugía); NC: no concluyente; PET/TC: tomografía por emisión de positrones/tomografía computarizada; SCN: Staphylococcus plasmocoagulasa negativo; SGV: Streptoccocus grupo viridans; SVA: sustitución de válvula aórtica.
Se realizó una ecocardiografía transesofágica a todos los pacientes. En esta prueba solamente 1 paciente presentó fuga periprotésica, en 2 casos se identificaron vegetaciones y en 7 se observó engrosamiento perianular, pero que no fue diagnóstico de absceso (< 10mm). Por elevada sospecha clínica, se realizó tomografía por emisión de positrones/tomografía computarizada con 18F-fluorodesoxiglucosa (18F-FDG PET/TC) a 10 pacientes: en el paciente 2, sin hallazgos en la ecocardiografía transesofágica y la PET, el diagnóstico se confirmó por necropsia; en el paciente 4, la 18F-FDG PET/TC fue la prueba inicial porque presentaba varices esofágicas, y en el paciente 5 sirvió para completar el estudio de cara a la planificación quirúrgica. Los pacientes presentaron una captación metabólica de diversa intensidad, con descripción anatómica de absceso perianular en todos ellos (figura 1).
Los 14 pacientes tenían indicación quirúrgica, pero se desestimó la cirugía en 3 casos por el riesgo excesivo. En 8 de los 11 pacientes intervenidos, se implantó una nueva protésis Perceval S tras parcheado del anillo aórtico con pericardio bovino. En todos los casos sometidos a cirugía, los hallazgos intraoperatorios se correlacionaron con los descritos en la 18F-FDG PET/TC. Además, la información anatómica generada por esta técnica permitió planificar la estrategia quirúrgica más adecuada.
La mortalidad hospitalaria fue del 14% (n=2), y la mortalidad durante el seguimiento (media, 23 meses) fue de 5 pacientes (41%), de los que 2 casos eran de los desestimados para la cirugía.
El diseño especial de la prótesis Perceval S, mediante el que la válvula queda anclada al anillo aórtico exclusivamente por la fuerza radial del stent de nitinol, hace que la presentación ecocardiográfica de la endocarditis pueda ser diferente que con los demás sustitutos valvulares. La ausencia de fuga periprótesica podría demorar el diagnóstico mediante ecocardiografía transesofágica, sobre todo si las imágenes de afección perianular no son diagnósticas de absceso.
Aunque la ecocardiografía transesofágica es la herramienta fundamental en el diagnóstico de EVP, se ha descrito hasta un 10% de falsos negativos en fases precoces de la enfermedad4. Resulta útil en este tipo de prótesis recurrir a otras técnicas de imagen, como la 18F-FDG PET/TC, un instrumento diagnóstico de gran utilidad en la sospecha de EVP, incluso en fases precoces5,6. La sensibilidad de la TC cardiosincronizada para detectar abscesos perianulares es muy elevada (> 95%) y aumenta con la información metabólica de la PET6.
En nuestra experiencia, la EVP sobre Perceval S tiene una presentación diferente que con las demás prótesis biológicas en cuanto al diagnóstico ecocardiográfico. El uso de otras técnicas, como el estudio con 18F-FDG PET/TC, permitiría un diagnóstico precoz y una mejor valoración de la afección anatómica perianular. Esta actitud permitiría anticiparse en la decisión terapéutica y minimizar el riesgo de complicaciones locales graves que impliquen mayor complejidad quirúrgica después.
FINANCIACIÓNNo existe financiación.
CONFLICTO DE INTERESESNinguno.