El 11 de noviembre de 2020, el coronavirus del síndrome respiratorio agudo grave de tipo 2 (SARS-CoV-2) había infectado a 9.187.237 personas en todo el mundo, con una mortalidad estimada del 2,7%1. Los informes iniciales insinuaban que la regulación incorrecta del sistema inmunitario podía desempeñar un papel clave en su letalidad2. Los pacientes con antecedentes de enfermedad cardiovascular (ECV) o factores de riesgo corren un riesgo especialmente mayor3.
La toma de estatinas es habitual entre los pacientes con alto riesgo y se ha demostrado que disminuyen la incidencia de morbimortalidad cardiovascular. Cabe indicar que previamente se había señalado que las estatinas pueden conferir una cualidad protectora en las infecciones víricas. En teoría, las estatinas disminuirían la incidencia de lesión grave en la enfermedad coronavírica de 2019 (COVID-19) por: a) la disminución de los mediadores posteriores del L-mevalonato; b) la inhibición de la prenilación proteínica, y c) el aumento de la concentración de la enzima de conversión de la angiotensina II4. No obstante, el mayor consumo de estatinas de los pacientes con mayor carga de ECV podría contrarrestar un posible efecto protector frente a quienes no toman estatinas. El objetivo de este estudio es describir las características y evaluar el impacto del tratamiento crónico con estatinas en el pronóstico de los pacientes ingresados en el hospital por COVID-19.
Se realizó un estudio observacional retrospectivo en 2 centros hospitalarios españoles especializados con todos los pacientes ingresados entre el 1 de marzo y el 30 de abril de 2020 con un diagnóstico definitivo de infección por SARS-CoV-2 confirmado mediante la reacción en cadena de la polimerasa con transcriptasa inversa positiva. Se registró el tratamiento prescrito antes y durante el ingreso según los protocolos de dichos centros y a juicio del equipo médico. También se registraron los resultados clínicos. Las variables categóricas se registran como valores y porcentajes absolutos. Las variables continuas se expresan como media ± desviación estándar; las variables que no siguen una distribución normal se registran como mediana [intervalo intercuartílico]. El efecto de las estatinas en el resultado principal (mortalidad hospitalaria) en la población general en estudio se evaluó con un modelo de regresión logística multivariante después de ajustar para los principales factores de confusión. Todos los análisis se realizaron con el software estadístico IBM SPSS Statistics, versión 25.0. (IBM Corp, Estados Unidos). Se consideró que las diferencias eran estadísticamente significativas cuando p <0,05. El estudio fue aprobado por el comité de ética local y no se exigió el consentimiento informado, dada su naturaleza retrospectiva y observacional.
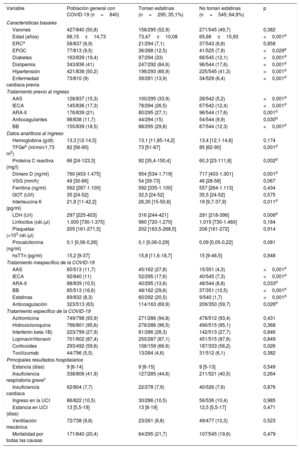
De los 840 pacientes ingresados por COVID-19, 295 (35,1%) seguían un tratamiento con estatinas antes de ingresar al hospital y 545 (64,9%) no. Los pacientes tratados con estatinas eran mayores (73,5±10,1 frente a 65,7±15,9 años; p <0,001) y presentaban un mayor predominio de varias enfermedades concomitantes, como hipertensión (el 66,9 frente al 41,3%; p <0,001), diabetes mellitus (el 33 frente al 12,1%; p <0,001) y enfermedad cardiaca previa (el 13,9 frente al 6,4%; p <0,001). Asimismo, aquellos en tratamiento con estatinas recibían con mayor frecuencia fármacos antihipertensivos, bloqueadores beta y ácido acetilsalicílico. El tiempo transcurrido desde el inicio de los síntomas hasta el ingreso no difirió entre grupos. Quienes tomaban estatinas presentaban un perfil inflamatorio más destacado en el momento del ingreso, con mayor concentración de proteína C reactiva (92 frente a 60,3mg/dl; p=0,002), interleucina 6 (26,3 frente a 19 pg/ml; p=0,011) y dímero D (954 frente a 717; p=0,001). En general, los pacientes de la cohorte tratada con estatinas recibían con mayor frecuencia un tratamiento con corticoides intravenosos (el 66,7 frente al 56,2%; p <0,026) y anticoagulantes (el 69,9 frente al 59,7%; p=0,033), pero otros fármacos provisionales para el tratamiento de la COVID-19 se utilizaban en proporciones similares. Los principales resultados hospitalarios fueron comparables: insuficiencia respiratoria aguda (9,8%), ingreso a cuidados intensivos (10,5%) y mortalidad por cualquier causa (20,4%). Las principales características basales según el tratamiento hipolipemiante al inicio se resumen en la tabla 1.
Características basales y resultados de los infectados por SARS-CoV-2 que toman estatinas frente a los que no las toman
| Variable | Población general con COVID-19 (n=840) | Toman estatinas (n=295; 35,1%) | No toman estatinas (n=545; 64,9%) | p |
|---|---|---|---|---|
| Características basales | ||||
| Varones | 427/840 (50,8) | 156/295 (52,9) | 271/545 (49,7) | 0,382 |
| Edad (años) | 68,15±14,73 | 73,47±10,08 | 65,66±15,93 | <0,001d |
| ERCa | 58/837 (6,9) | 21/294 (7,1) | 37/543 (6,8) | 0,858 |
| EPOC | 77/813 (9,5) | 36/288 (12,5) | 41/525 (7,8) | <0,029d |
| Diabetes | 163/839 (19,4) | 97/294 (33) | 66/545 (12,1) | <0,001d |
| Dislipemia | 343/836 (41) | 247/292 (84,6) | 96/544 (17,6) | <0,001d |
| Hipertensión | 421/838 (50,2) | 196/293 (66,9) | 225/545 (41,3) | <0,001d |
| Enfermedad cardiaca previa | 73/810 (9) | 39/281 (13,9) | 34/529 (6,4) | <0,001d |
| Tratamiento previo al ingreso | ||||
| AAS | 128/837 (15,3) | 100/295 (33,9) | 28/542 (5,2) | <0,001d |
| IECA | 145/836 (17,3) | 78/294 (26,5) | 67/542 (12,4) | <0,001d |
| ARA-II | 176/839 (21) | 80/295 (27,1) | 96/544 (17,6) | 0,001d |
| Anticoagulantes | 98/838 (11,7) | 44/294 (15) | 54/544 (9,9) | 0,030d |
| BB | 155/839 (18,5) | 88/295 (29,8) | 67/544 (12,3) | <0,001d |
| Datos analíticos al ingreso | ||||
| Hemoglobina (g/dl) | 13,3 [12-14,5] | 13,1 [11,85-14,2] | 13,4 [12,1-14,6] | 0,174 |
| TFGeb (ml/min/1,73 m2) | 82 [56-90] | 73 [51-87] | 85 [62-90] | 0,001d |
| Proteína C reactiva (mg/l) | 66 [24-123,3] | 92 [35,4-150,4] | 60,3 [23-111,8] | 0,002d |
| Dímero D (ng/ml) | 760 [453-1.475] | 954 [534-1.719] | 717 [403-1.301] | 0,001d |
| VSG (mm/h) | 49 [30-66] | 54 [39-73] | 46 [28-58] | 0,067 |
| Ferritina (ng/ml) | 562 [287-1.100] | 592 [335-1.100] | 557 [264-1.113] | 0,434 |
| GOT (UI/l) | 35 [24-52] | 32,5 [24-52] | 35,5 [24-52] | 0,575 |
| Interleucina 6 (pg/ml) | 21,8 [11-42,2] | 26,35 [15-50,6] | 19 [9,7-37,9] | 0,011d |
| LDH (U/l) | 297 [225-403] | 316 [244-421] | 291 [218-396] | 0,006d |
| Linfocitos (cél./μl) | 1.000 [730-1.375] | 960 [720-1.270] | 1.015 [730-1.460] | 0,184 |
| Plaquetas (×103 cél./μl) | 205 [161-271,5] | 202 [163,5-268,5] | 206 [161-272] | 0,914 |
| Procalcitonina (ng/ml) | 0,1 [0,06-0,26] | 0,1 [0,06-0,29] | 0,09 [0,05-0,22] | 0,081 |
| hsTTn (pg/ml) | 15,2 [9-37] | 15,8 [11,6-18,7] | 15 [9-46,5] | 0,948 |
| Tratamiento inespecífico de la COVID-19 | ||||
| AAS | 60/513 (11,7) | 45/162 (27,8) | 15/351 (4,3) | <0,001d |
| IECA | 92/840 (11) | 52/295 (17,6) | 40/545 (7,3) | <0,001d |
| ARA-II | 88/839 (10,5) | 40/295 (13,6) | 48/544 (8,8) | 0,033d |
| BB | 85/513 (16,6) | 48/162 (29,6) | 37/351 (10,5) | <0,001d |
| Estatinas | 69/832 (8,3) | 60/292 (20,5) | 9/540 (1,7) | <0,001d |
| Anticoagulación | 323/513 (63) | 114/163 (69,9) | 209/350 (59,7) | 0,026d |
| Tratamiento específico de la COVID-19 | ||||
| Azitromicina | 749/798 (93,9) | 271/286 (94,8) | 478/512 (93,4) | 0,431 |
| Hidroxicloroquina | 766/801 (95,6) | 276/286 (96,5) | 490/515 (95,1) | 0,368 |
| Interferón beta-1B) | 223/799 (27,9) | 81/286 (28,3) | 142/513 (27,7) | 0,846 |
| Lopinavir/ritonavir | 701/802 (87,4) | 250/287 (87,1) | 451/515 (87,6) | 0,849 |
| Corticoides | 293/492 (59,6) | 106/159 (66.6) | 187/333 (56,2) | 0,026 |
| Tocilizumab | 44/796 (5,5) | 13/284 (4,6) | 31/512 (6,1) | 0,382 |
| Principales resultados hospitalarios | ||||
| Estancia (días) | 9 [6-14] | 9 [6-15] | 9 [5-13] | 0,549 |
| Insuficiencia respiratoria gravec | 338/806 (41,9) | 127/285 (44,6) | 211/521 (40,5) | 0,264 |
| Insuficiencia cardiaca | 62/804 (7,7) | 22/278 (7,9) | 40/526 (7,6) | 0,876 |
| Ingreso en la UCI | 86/822 (10,5) | 30/286 (10,5) | 56/536 (10,4) | 0,985 |
| Estancia en UCI (días) | 13 [5,5-19] | 13 [8-19] | 12,5 [5,5-17] | 0,471 |
| Ventilación mecánica | 72/738 (9,8) | 23/261 (8,8) | 49/477 (10,3) | 0,523 |
| Mortalidad por todas las causas | 171/840 (20,4) | 64/295 (21,7) | 107/545 (19,6) | 0,479 |
AAS: ácido acetilsalicílico; ARA-II: antagonistas del receptor de la angiotensina II; BB: bloqueadores beta; EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica; hsTTn: troponina T de alta sensibilidad; IECA: inhibidores de la enzima de conversión de la angiotensina; TFGe: tasa de filtrado glomerular estimada; UCI: unidad de cuidados intensivos; VSG: velocidad de sedimentación globular.
Los valores expresan n/N (%), media ± desviación estándar o mediana [intervalo intercuartílico].
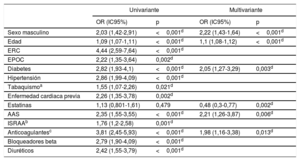
Se utilizó un modelo de regresión logística para estudiar la relación entre el tratamiento crónico con estatinas y el desenlace clínico en los pacientes ingresados por COVID-19. En el modelo definitivo se incluyeron las variables edad, sexo, hipertensión, dislipemia, diabetes, enfermedad pulmonar obstructiva crónica, enfermedad renal crónica, antecedentes de tabaquismo, enfermedad cardiaca previa y tratamientos complementarios crónicos (inhibidores del sistema renina-angiotensina-aldosterona, bloqueadores beta, ácido acetilsalicílico y anticoagulantes). En este modelo (tabla 2), el tratamiento crónico con estatinas (odds ratio ajustada = 0,48; intervalo de confianza del 95%, 0,3-0,77; p=0,002) se relacionó con menor mortalidad hospitalaria frente a quienes no tomaban estatinas. Además, los pacientes de mayor edad, los varones y los diabéticos corrían mayor riesgo de fallecer por COVID-19.
Predictores de la mortalidad a 30 días en la población de estudio
| Univariante | Multivariante | |||
|---|---|---|---|---|
| OR (IC95%) | p | OR (IC95%) | p | |
| Sexo masculino | 2,03 (1,42-2,91) | <0,001d | 2,22 (1,43-1,64) | <0,001d |
| Edad | 1,09 (1,07-1,11) | <0,001d | 1,1 (1,08-1,12) | <0,001d |
| ERC | 4,44 (2,59-7,64) | <0,001d | ||
| EPOC | 2,22 (1,35-3,64) | 0,002d | ||
| Diabetes | 2,82 (1,93-4,1) | <0,001d | 2,05 (1,27-3,29) | 0,003d |
| Hipertensión | 2,86 (1,99-4,09) | <0,001d | ||
| Tabaquismoa | 1,55 (1,07-2,26) | 0,021d | ||
| Enfermedad cardiaca previa | 2,26 (1,35-3,78) | 0,002d | ||
| Estatinas | 1,13 (0,801-1,61) | 0,479 | 0,48 (0,3-0,77) | 0,002d |
| AAS | 2,35 (1,55-3,55) | <0,001d | 2,21 (1,26-3,87) | 0,006d |
| ISRAAb | 1,76 (1,2-2,58) | 0,001d | ||
| Anticoagulantesc | 3,81 (2,45-5,93) | <0,001d | 1,98 (1,16-3,38) | 0,013d |
| Bloqueadores beta | 2,79 (1,90-4,09) | <0,001d | ||
| Diuréticos | 2,42 (1,55-3,79) | <0,001d | ||
EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica; IC95%: intervalo de confianza del 95%; ISRAA: inhibidores del sistema renina-angiotensina-aldosterona; OR: odds ratio.
Las estatinas, con sus propiedades pleotrópicas, pueden reducir la gravedad de la lesión pulmonar aguda y la mortalidad. Las observaciones realizadas coinciden con las de un estudio retrospectivo reciente que evaluó el impacto del tratamiento crónico con estatinas previo al ingreso por COVID-19, en el que la toma de estatinas previa a la hospitalización se relacionó con una reducción del 71% en la gravedad de la COVID-195. Asimismo, Zhang et al.6 observaron que el tratamiento hospitalario con estatinas también se relacionaba con mejores resultados en los pacientes con COVID-19.
Este estudio tiene varias limitaciones. Dado su diseño, no puede inferirse la causalidad de las estatinas en la mortalidad y debe considerarse para la generación de hipótesis. Puede que estos resultados sean limitados, dado que se evalúa a pacientes no ingresados en el hospital o bajo el efecto de algunos factores de confusión hospitalarios sin determinar (p. ej., mantenimiento con estatinas e impacto de los tratamientos concomitantes). No obstante, estos resultados indican que quienes toman estatinas y padecen COVID-19 corren un riesgo inicial mayor impulsado principalmente por la edad más avanzada y una mayor carga de ECV concomitantes, lo que en teoría podría ocultar un posible efecto protector de las estatinas en este particular subgrupo de pacientes. Actualmente no hay ningún ensayo clínico aleatorizado que demuestre que el tratamiento hospitalario con estatinas beneficie a los pacientes con COVID-19, pero es conveniente alertar a la comunidad internacional sobre esta posibilidad hasta que existan pruebas concluyentes (STATCO19, NCT04380402).
FINANCIACIÓNEste estudio fue financiado en parte por la Gerencia Regional de Salud de Castilla y León (GRS COVID 111/A/20) y por la Sociedad Española de Cardiología (SEC/FEC-INVCLI 20/030).
CONFLICTO DE INTERESESNo hay conflicto de intereses alguno.