Los pacientes mayores de 75 años con infarto agudo de miocardio con elevación del segmento ST sometidos a angioplastia primaria en situación de shock cardiogénico sufren una gran mortalidad. La identificación previa al procedimento de variables predictoras de la posterior mortalidad sería muy útil para guiar la toma de decisiones.
MétodosAnálisis del registro multicéntrico de angioplastia primaria en pacientes mayores de 75 años (ESTROFA MI+75), que incluye a 3.576 pacientes. Se analizaron las características y la evolución clínica del subgrupo con shock cardiogénico para identificar predictores de supervivencia a 1 año tras la angioplastia y elaborar un índice pronóstico. Se validó el índice en una cohorte independiente.
ResultadosSe incluyó a 332 pacientes. Los predictores basales independientes fueron: la localización anterior (HR=2,8; IC95%, 1,4-6,0; p=0,005), una fracción de eyección<40% (HR=2,3; IC95%, 1,14-4,50; p=0,018) y un tiempo entre el inicio de los síntomas y la angioplastia >6 h (HR=3,2; IC95%, 1,6-7,5; p=0,001). Se diseñó un índice basado en estas variables (índice «6-ANT-40»). La supervivencia a 1 año fue del 54,5% de aquellos con índice 0, el 32,3% con índice 1, el 27,4% con índice 2 y el 17% con índice 3 (p=0,004, estadístico C=0,70). En una cohorte independiente de 124 pacientes, las supervivencias a 1 año fueron del 64,5, el 40,0, el 28,9 y el 22,2% respectivamente (p=0,008; estadístico C=0,68).
ConclusionesUn índice basado en simples variables clínicas previas al procedimiento (localización anterior, fracción de eyección<40%, demora >6 h) permite estimar la supervivencia tras una angioplastia primaria de los pacientes mayores con shock cardiogénico, y así ayudar en la toma de decisiones.
Palabras clave
Dado el envejecimiento de la población en los países occidentales, se está produciendo un aumento progresivo de la proporción de pacientes ingresados en los hospitales con diagnóstico de infarto agudo de miocardio con elevación del segmento ST (IAMCEST)1. La angioplastia primaria es el tratamiento de elección para la reperfusión cuando puede realizarse en el momento oportuno. Aunque la edad avanzada se asocia con peor pronóstico tras el IAMCEST, la angioplastia primaria continúa siendo la estrategia de reperfusión preferida para estos pacientes2,3.
El shock cardiogénico (SC) es la complicación más importante en los pacientes con IAMCEST. La incidencia del SC es de alrededor de un 6% y se ha descrito una mortalidad a corto plazo de un 45-50%4,5. En la población anciana (mayor de 75 años), la incidencia es de alrededor de un 10% en registros amplios publicados recientemente6,7. Esta afección aumenta drásticamente la mortalidad a corto plazo de estos pacientes8-11. El beneficio en supervivencia que aporta la revascularización de los mayores de 75 años en SC se ha puesto en duda tras la publicación de un análisis preespecificado de subgrupos del ensayo SHOCK12. En estudios posteriores, incluido el SHOCK, se ha observado un efecto beneficioso de la intervención coronaria percutánea (ICP) en esos pacientes, pero su magnitud es todavía objeto de controversia10,13-16.
La información sobre los predictores de la mortalidad de los pacientes ancianos con un SC como complicación de un IAMCEST y tratados con angioplastia primaria es escasa. Se han identificado como predictores el fracaso terapéutico de la ICP, el flujo Thrombolysis in Myocardial Infarction (TIMI) final de grado 0-2 y la enfermedad multivaso11,16, que son factores que no se conocen antes de la ICP. Estos análisis se llevaron a cabo en series de pacientes pequeñas y, por consiguiente, no permitieron identificar predictores basales (pre-ICP) del resultado clínico. Dada la gran mortalidad que se observa en los pacientes ancianos en SC tratados con ICP, la identificación de predictores previos a la intervención podría ser de especial utilidad para orientar la toma de decisiones clínicas.
El objetivo de este estudio es describir las características basales, el tratamiento, los resultados y los factores predictores pronósticos de los pacientes ancianos ingresados en SC como complicación de un IAMCEST y tratados con ICP primaria según los estándares actuales.
MÉTODOSEste análisis se llevó a cabo en un registro de ámbito nacional centrado en los pacientes ancianos con IAMCEST a los que se practicó una angioplastia primaria en 31 centros de toda España7. Este registro cuenta con el apoyo del Grupo de Trabajo de Cardiología Intervencionista de la Sociedad Española de Cardiología y forma parte del grupo de estudio ESTROFA (Estudio Español Sobre Trombosis de Stents Farmacoactivos).
PoblaciónCada centro participante incluyó de manera retrospectiva una serie estrictamente consecutiva de pacientes de edad> 75 años con IAMCEST a los que se practicó una ICP primaria en las primeras 24 h tras el inicio del dolor. No se aplicaron criterios de exclusión clínicos ni angiográficos. El tamaño muestral de la serie de cada centro dependió del número de ingresos de pacientes con IAMCEST en ese centro. Tan solo se incluyó a los pacientes con al menos 1 año de seguimiento tras la fecha de inicio de la inclusión. El periodo de inclusión se inició en 2006 (en el caso más temprano) y finalizó en 2013, si bien se incluyó a la mayoría de los pacientes entre 2010 y 2013. Para los fines del presente análisis, se identificó el subgrupo de pacientes con SC en el momento de la intervención.
Se seleccionó una cohorte de validación para el índice pronóstico, reclutada en un periodo posterior (2014-2016). Formaron esta cohorte los pacientes ancianos consecutivos tratados con una ICP primaria en situación de SC.
Las intervenciones se realizaron según las preferencias de cada operador y de cada centro. Se recogió la información clínica, angiográfica, de la intervención y de seguimiento en una base de datos diseñada específicamente para el estudio. El investigador principal tuvo pleno acceso a todos los datos del estudio y asume la responsabilidad de su integridad y del análisis de los datos. Se garantizó el estricto anonimato de los datos.
El SC se definió como una presión arterial sistólica <90mmHg durante más de 30min o por la necesidad de fármacos inotrópicos para mantener una presión arterial sistólica> 90mmHg y no debida a una reacción vagal, signos de bajo gasto cardiaco, hipoperfusión de órganos finales (p. ej., taquicardia en reposo, oliguria, extremidades frías o alteración del estado mental) o presiones de llenado elevadas (p. ej., congestión pulmonar a la exploración en la radiografía de tórax).
La fracción de eyección del ventrículo izquierdo (FEVI) fue la de la primera determinación y correspondió siempre al periodo periintervención, la mayoría de las veces antes de la ICP y en ocasiones durante esta o en los primeros 60min tras ella.
El objetivo principal de este estudio es la mortalidad por cualquier causa. Los investigadores determinaron la supervivencia de los pacientes mediante las historias clínicas, los informes y las bases de datos, y a través del contacto directo con los pacientes o sus familiares.
Análisis estadísticoLas variables continuas se presentan en forma de media±desviación estándar. Las variables discretas se expresan en porcentajes. Las variables continuas se compararon con la prueba de la t de Student si seguían una distribución normal o con la prueba de Wilcoxon en caso contrario (el tipo de distribución se determinó con la prueba de Kolmogorov-Smirnov). Las variables discretas se compararon con la prueba de la χ2 o con la prueba exacta de Fischer, según procediera. Se obtuvieron las curvas de Kaplan-Meier de la supervivencia sin eventos, para cada grupo o subgrupo preespecificado, y se compararon mediante log-rank test. Se llevó a cabo un análisis de regresión logística para establecer los factores asociados de manera independiente con el SC. Mediante regresión de riesgos proporcionales de Cox, se determinaron las hazard ratio (HR) de mortalidad a 1 año en los subgrupos analizados y se identificaron los factores independientes predictivos de la mortalidad. Los centros se incluyeron en el análisis y se clasificaron en grupos según sus tasas de mortalidad a 1 año. Se eligió un valor de corte predefinido de tiempo hasta el tratamiento> 6 h y un valor <40% para establecer la reducción grave de la FEVI. Se obtuvo el estadístico C a partir de las curvas de características operativas del receptor para las combinaciones de las variables predictivas y para el índice predictivo derivado de ellas. Se realizó una validación independiente en una población distinta de la utilizada para el desarrollo del modelo. El modelo incluyó todas las variables que mostraban una asociación con la incidencia de mortalidad a 1 año en el análisis univariante (p <0,2). Se consideró estadísticamente significativo un valor de p <0,05. Todos los análisis estadísticos se llevaron a cabo con el programa SPSS versión 19 para Windows.
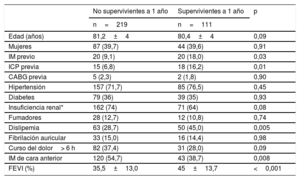
RESULTADOSSe incluyó en el estudio a un total de 3.576 pacientes de 31 centros, y 332 de ellos estaban en SC en el momento de la ICP. Las características clínicas de los pacientes con y sin SC se muestran en la tabla 1. En los primeros había una mayor frecuencia de diabetes, eran más probables la insuficiencia renal y una FEVI más baja, y se observó una tendencia a mayor frecuencia de infartos de la cara anterior y tiempos hasta la ICP más largos.
Características clínicas
| Shock cardiogénico | Sin shock cardiogénico | p | |
|---|---|---|---|
| n=332 | n=3.244 | ||
| Edad (años) | 81±4,2 | 81,2±4,4 | 0,42 |
| Mujeres | 131 (39,5) | 1.277 (39,4) | 0,98 |
| IM previo | 40 (12) | 376 (11,6) | 0,89 |
| ICP previa | 34 (10,2) | 306 (9,4) | 0,70 |
| CABG previa | 7 (2,1) | 43 (1,3) | 0,34 |
| Hipertensión | 244 (73,5) | 2.301 (70,9) | 0,35 |
| Diabetes | 119 (35,8) | 985 (30,4) | 0,049 |
| Insuficiencia renal* | 233 (70,2) | 1.502 (46,3) | <0,0001 |
| Fumadores | 40 (12) | 499 (15,4) | 0,11 |
| Dislipemia | 113 (34,0) | 1.401 (43,2) | 0,0015 |
| Fibrilación auricular | 49 (14,7) | 460 (14,2) | 0,86 |
| Curso del dolor> 6 h | 113 (34,0) | 955 (29,4) | 0,09 |
| Curso del dolor> 12 h | 50 (15) | 294 (9) | 0,0006 |
| IM de cara anterior | 163 (49,1) | 1.423 (43,9) | 0,08 |
| FEVI (%) | 39±14 | 48,6±12 | <0,0001 |
CABG: cirugía de revascularización coronaria; FEVI: fracción de eyección del ventrículo izquierdo; ICP: intervención coronaria percutánea; IM: infarto de miocardio.
Los valores expresan n (%) o media±desviación estándar.
Definida como una tasa de filtrado glomerular <60ml/min y basada en la primera muestra de sangre obtenida tras el ingreso. Dado que no se conocía la función renal inmediatamente previa al episodio, no quedó claro si se debía a una insuficiencia renal aguda o a una insuficiencia renal crónica preexistente. Lo más probable es que fuera una combinación de las dos, y que ambas estuvieran relacionadas con un resultado clínico adverso.
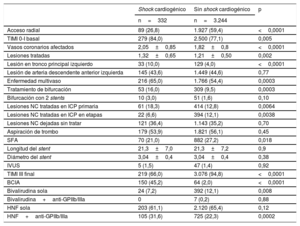
Las características angiográficas y de la intervención de los 2 grupos se presentan en la tabla 2. Hubo diferencias significativas en muchas variables. En términos generales, los pacientes con SC tenían una enfermedad coronaria más grave. En esos pacientes se usaron menos la vía de acceso radial, la bivalirudina y los stents farmacoactivos, y más los inhibidores de la glucoproteína IIb/IIIa y el balón de contrapulsación intraaórtico. Los factores en asociación independiente con el SC fueron la FEVI (odds ratio [OR]=0,93; intervalo de confianza del 95% [IC95%], 0,92-0,94; p <0,0001) y la insuficiencia renal (OR=2,38; IC95%, 1,75-3,24; p <0,0001).
Características angiográficas y de la intervención
| Shock cardiogénico | Sin shock cardiogénico | p | |
|---|---|---|---|
| n=332 | n=3.244 | ||
| Acceso radial | 89 (26,8) | 1.927 (59,4) | <0,0001 |
| TIMI 0-I basal | 279 (84,0) | 2.500 (77,1) | 0,005 |
| Vasos coronarios afectados | 2,05±0,85 | 1,82±0,8 | <0,0001 |
| Lesiones tratadas | 1,32±0,65 | 1,21±0,50 | 0,002 |
| Lesión en tronco principal izquierdo | 33 (10,0) | 129 (4,0) | <0,0001 |
| Lesión de arteria descendente anterior izquierda | 145 (43,6) | 1.449 (44,6) | 0,77 |
| Enfermedad multivaso | 216 (65,0) | 1.766 (54,4) | 0,0003 |
| Tratamiento de bifurcación | 53 (16,0) | 309 (9,5) | 0,0003 |
| Bifurcación con 2 stents | 10 (3,0) | 51 (1,6) | 0,10 |
| Lesiones NC tratadas en ICP primaria | 61 (18,3) | 414 (12,8) | 0,0064 |
| Lesiones NC tratadas en ICP en etapas | 22 (6,6) | 394 (12,1) | 0,0038 |
| Lesiones NC dejadas sin tratar | 121 (36,4) | 1.143 (35,2) | 0,70 |
| Aspiración de trombo | 179 (53,9) | 1.821 (56,1) | 0,45 |
| SFA | 70 (21,0) | 882 (27,2) | 0,018 |
| Longitud del stent | 21,3±7,0 | 21,3±7,2 | 0,9 |
| Diámetro del stent | 3,04±0,4 | 3,04±0,4 | 0,38 |
| IVUS | 5 (1,5) | 47 (1,4) | 0,92 |
| TIMI III final | 219 (66,0) | 3.076 (94,8) | <0,0001 |
| BCIA | 150 (45,2) | 64 (2,0) | <0,0001 |
| Bivalirudina sola | 24 (7,2) | 392 (12,1) | 0,008 |
| Bivalirudina+anti-GPIIb/IIIa | 0 | 7 (0,2) | 0,88 |
| HNF sola | 203 (61,1) | 2.120 (65,4) | 0,12 |
| HNF+anti-GPIIb/IIIa | 105 (31,6) | 725 (22,3) | 0,0002 |
Anti-GPIIb/IIIa: antagonistas de la glucoproteína IIb/IIIa; BCIA: balón de contrapulsación intraaórtico; HNF: heparina no fraccionada; ICP: intervención coronaria percutánea; IVUS: ecografía intravascular; NC: no culpable; SFA: stent farmacoactivo; TIMI: Thrombolysis in Myocardial Infarction.
Los valores expresan n (%) o media±desviación estándar.
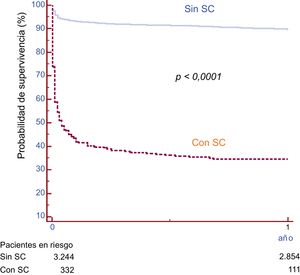
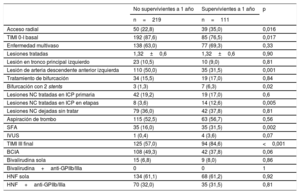
La supervivencia libre de muerte de los pacientes con y sin SC se muestra en la figura 1. Tal como se preveía, se observó una diferencia notable, con una supervivencia muy inferior entre los pacientes con SC (el 34,1 frente al 89,5% a los 12 meses; p <0,0001). De los 332 pacientes con SC, 180 (54,2%) fallecieron durante la hospitalización y 39 (11,7%), después del alta. Tan solo se perdió el seguimiento de 2 pacientes (0,6%). Las características clínicas de los pacientes según su supervivencia a 1 año se describen en la tabla 3. Los pacientes que sobrevivieron tenían más antecedentes de cardiopatía isquémica, menos infartos de cara anterior, una FEVI superior y más dislipemia, pero mostraron una tendencia a tener menos edad, insuficiencia renal y tiempo hasta el tratamiento. El análisis de las variables angiográficas y de la intervención mostró que el uso de la vía de acceso radial, stents farmacoactivos y una ICP en etapas, así como el tratamiento de la arteria descendente anterior, fueron más frecuentes en los pacientes que sobrevivieron. En ellos fue menos frecuente un flujo TIMI basal 0-I y se alcanzó con más frecuencia un flujo final TIMI III (tabla 4).
Características clínicas según la supervivencia a 1 año
| No supervivientes a 1 año | Supervivientes a 1 año | p | |
|---|---|---|---|
| n=219 | n=111 | ||
| Edad (años) | 81,2±4 | 80,4±4 | 0,09 |
| Mujeres | 87 (39,7) | 44 (39,6) | 0,91 |
| IM previo | 20 (9,1) | 20 (18,0) | 0,03 |
| ICP previa | 15 (6,8) | 18 (16,2) | 0,01 |
| CABG previa | 5 (2,3) | 2 (1,8) | 0,90 |
| Hipertensión | 157 (71,7) | 85 (76,5) | 0,45 |
| Diabetes | 79 (36) | 39 (35) | 0,93 |
| Insuficiencia renal* | 162 (74) | 71 (64) | 0,08 |
| Fumadores | 28 (12,7) | 12 (10,8) | 0,74 |
| Dislipemia | 63 (28,7) | 50 (45,0) | 0,005 |
| Fibrilación auricular | 33 (15,0) | 16 (14,4) | 0,98 |
| Curso del dolor> 6 h | 82 (37,4) | 31 (28,0) | 0,09 |
| IM de cara anterior | 120 (54,7) | 43 (38,7) | 0,008 |
| FEVI (%) | 35,5±13,0 | 45±13,7 | <0,001 |
CABG: cirugía de revascularización coronaria; FEVI: fracción de eyección del ventrículo izquierdo; ICP: intervención coronaria percutánea; IM: infarto de miocardio.
Los valores expresan n (%) o media±desviación estándar. No se incluyó a 2 pacientes perdidos para el seguimiento.
Características angiográficas y de la intervención según la supervivencia a 1 año
| No supervivientes a 1 año | Supervivientes a 1 año | p | |
|---|---|---|---|
| n=219 | n=111 | ||
| Acceso radial | 50 (22,8) | 39 (35,0) | 0,016 |
| TIMI 0-I basal | 192 (87,6) | 85 (76,5) | 0,017 |
| Enfermedad multivaso | 138 (63,0) | 77 (69,3) | 0,33 |
| Lesiones tratadas | 1,32±0,6 | 1,32±0,6 | 0,90 |
| Lesión en tronco principal izquierdo | 23 (10,5) | 10 (9,0) | 0,81 |
| Lesión de arteria descendente anterior izquierda | 110 (50,0) | 35 (31,5) | 0,001 |
| Tratamiento de bifurcación | 34 (15,5) | 19 (17,0) | 0,84 |
| Bifurcación con 2 stents | 3 (1,3) | 7 (6,3) | 0,02 |
| Lesiones NC tratadas en ICP primaria | 42 (19,2) | 19 (17,0) | 0,6 |
| Lesiones NC tratadas en ICP en etapas | 8 (3,6) | 14 (12,6) | 0,005 |
| Lesiones NC dejadas sin tratar | 79 (36,0) | 42 (37,8) | 0,81 |
| Aspiración de trombo | 115 (52,5) | 63 (56,7) | 0,56 |
| SFA | 35 (16,0) | 35 (31,5) | 0,002 |
| IVUS | 1 (0,4) | 4 (3,6) | 0,07 |
| TIMI III final | 125 (57,0) | 94 (84,6) | <0,001 |
| BCIA | 108 (49,3) | 42 (37,8) | 0,06 |
| Bivalirudina sola | 15 (6,8) | 9 (8,0) | 0,86 |
| Bivalirudina+anti-GPIIb/IIIa | 0 | 0 | 1 |
| HNF sola | 134 (61,1) | 68 (61,2) | 0,92 |
| HNF+anti-GPIIb/IIIa | 70 (32,0) | 35 (31,5) | 0,81 |
Anti-GPIIb/IIIa: antagonistas de la glucoproteína IIb/IIIa; BCIA: balón de contrapulsación intraaórtico; HNF: heparina no fraccionada; ICP: intervención coronaria percutánea; IVUS: ecografía intravascular; NC: no culpable; SFA: stent farmacoactivo; TIMI: Thrombolysis in Myocardial Infarction.
Los valores expresan n (%) o media±desviación estándar.
No se incluyó a 2 pacientes perdidos para el seguimiento.
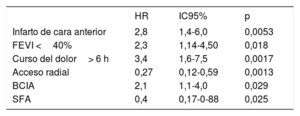
En la tabla 5 se presentan los factores independientes predictivos de la mortalidad a 1 año. Las variables basales y previas a la intervención que se identificaron como predictivas fueron el infarto de cara anterior, la FEVI <40% y el tiempo desde el inicio del dolor hasta la ICP> 6 h. Los factores de la intervención con una asociación independiente con el pronóstico fueron el uso de la vía de acceso radial, el balón de contrapulsación intraaórtico y los stents farmacoactivos. La asignación del centro no tuvo valor predictivo.
Predictores independientes de la mortalidad a 1 año
| HR | IC95% | p | |
|---|---|---|---|
| Infarto de cara anterior | 2,8 | 1,4-6,0 | 0,0053 |
| FEVI <40% | 2,3 | 1,14-4,50 | 0,018 |
| Curso del dolor> 6 h | 3,4 | 1,6-7,5 | 0,0017 |
| Acceso radial | 0,27 | 0,12-0,59 | 0,0013 |
| BCIA | 2,1 | 1,1-4,0 | 0,029 |
| SFA | 0,4 | 0,17-0-88 | 0,025 |
BCIA: balón de contrapulsación intraaórtico; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; SFA: stent farmacoactivo.
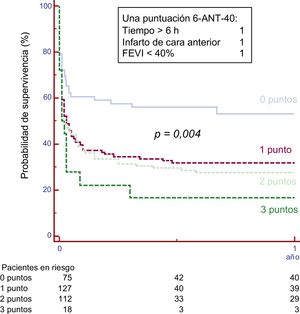
A partir de estos resultados, se creó un índice predictivo previo a la intervención que incluye los 3 factores pronósticos: infarto en cara anterior, FEVI <40% y tiempo hasta el tratamiento> 6 h. En la figura 2 se presenta la supervivencia de los pacientes según la escala «6-ANT-40». Los resultados fueron significativamente diferentes entre los subgrupos. La supervivencia a 1 año fue del 54,5% de los pacientes con 0 en la escala, el 32,3% de los pacientes con 1 en la escala, el 27,4% con 2 en la escala y el 17% con 3 en la escala (p=0,004; estadístico C=0,70).
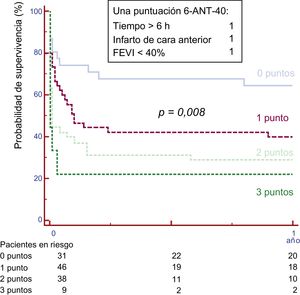
Formaron la cohorte de validación 124 pacientes. Las características basales se enumeran en la tabla 1 y la . La supervivencia total a 1 año en esta cohorte fue del 40%, con pérdida para el seguimiento del 0,8% de los pacientes. En la figura 3 se muestran las curvas de supervivencia según los valores del índice en la cohorte de validación. La supervivencia a 1 año mostró diferencias significativas entre los grupos definidos según la escala (el 64,5% de los pacientes con 0 en la escala, el 40,0% con 1, el 28,9% con 2 y el 22,2% con 3 (p=0,008; estadístico C=0,68).
Supervivencia libre de muerte según la escala 6-ANT-40 en la cohorte de validación. La supervivencia a 1 año fue del 64,5% de los pacientes con 0 puntos, el 40,0% con 1 punto, el 28,9% con 2 puntos y el 22,2% con 3 puntos (p=0,008). FEVI: fracción de eyección del ventrículo izquierdo.
Los principales resultados de este estudio pueden resumirse como sigue: a) la incidencia de SC en los pacientes de más de 75 años tratados con ICP primaria fue del 9,3%; b) la FEVI y la insuficiencia renal fueron factores independientes predictivos de SC; c) el SC se asoció con una mortalidad muy alta y concentrada en el periodo de hospitalización, y d) un índice predictivo previo a la intervención, basado en 3 variables clínicas sencillas (localización en cara anterior, FEVI <40% y tiempo hasta el tratamiento> 6 h) puede usarse para estimar la supervivencia tras la ICP y orientar la toma de decisiones.
En este registro, la mortalidad fue alta, en especial durante el ingreso hospitalario, en el que fallecieron más de la mitad de los pacientes. Estos resultados están dentro del intervalo de valores de las tasas de letalidad descritas anteriormente en otros registros6,8-11. Tiene interés señalar que la mortalidad a 1 año de los pacientes dados de alta fue de alrededor del 10%, que es una cifra no demasiado alta. Entre los factores independientes predictivos de la mortalidad identificados, se hallaron 3 variables basales previas a la intervención y 3 factores que se determinan durante la intervención. Por lo que respecta a estos, hay una alta probabilidad de sesgo. Se podría haber tratado con más frecuencia con balón de contrapulsación intraaórtico a los pacientes con mayor riesgo (con un SC más profundo), mientras que para los pacientes con menor riesgo (con un SC menos profundo) podría haberse utilizado en mayor medida el acceso radial y el implante de stents farmacoactivos. El uso de balón de contrapulsación intraaórtico no mostró un efecto beneficioso en el subgrupo de pacientes ancianos en el ensayo IABP-SHOCK II17. Los stents farmacoactivos no se han asociado con una mejora de la supervivencia de los pacientes con SC18. Por lo que respecta a la vía de acceso radial, la reducción de la mortalidad observada en los ensayos realizados en pacientes con IAMCEST podría indicar cierto papel protector de esta vía de acceso vascular en los pacientes con SC19,20.
Por lo que respecta a las estrategias de revascularización para la enfermedad multivaso, hubo más intervenciones por etapas en el grupo de supervivientes. No obstante, esta diferencia se debió a un sesgo de selección no desdeñable, puesto que tan solo los pacientes que sobrevivieron a los primeros 3 o 4 días críticos del IM podían ser tratados con una intervención en etapas para completar la revascularización.
La combinación de los 3 factores predictivos clínicos (infarto de cara anterior, FEVI <40% y tiempo hasta el tratamiento> 6 h) en una escala que asigna 1 punto a cada factor presente permite establecer una estratificación de los pacientes según su pronóstico. Este índice se ha validado en una cohorte independiente. La puntuación basada en variables clínicas previas a la intervención podría ser útil para orientar la toma de decisiones en estas situaciones de gran complejidad.
Tan solo en unos pocos estudios se han propuesto índices de riesgo para los pacientes en SC sometidos a una ICP primaria contemporánea en el IAMCEST, y ninguna de ellas se diseñó para los pacientes ancianos. El índice propuesto por García-Álvarez et al.21 se basó en 74 pacientes, lo cual es una muestra pequeña para este fin. Más recientemente se han publicado 2 escalas para predecir la mortalidad tras la ICP primaria en la población general con SC22,23. La primera se elaboró a partir de 388 pacientes tratados entre 1995 y 2013, e incluyó 3 variables (edad> 75 años, parada cardiaca en la situación inicial y fracaso de la ICP primaria), y mostró un estadístico C=0,66 para la mortalidad de causa cardiaca a 2 años22. La segunda se elaboró a partir de los datos del ensayo IABP-SHOCK y se validó luego en registros independientes23. Esta escala de predicción de la mortalidad a 30 días incluye 6 variables: edad> 73 años, antecedentes de ictus, glucosa> 191mg/dl, creatinina> 1,5mg/dl, lactato> 5 mmol/l y flujo TIMI <3 después de la ICP. Se obtuvieron estadísticos C de 0,79 y 0,73 en las cohortes de derivación y de validación respectivamente. No obstante, estas escalas se obtuvieron en la población general, por lo que su valor en la población anciana es limitado. Ambos índices incluyen los resultados de la ICP primaria y, por consiguiente, no pueden usarse para estimar adecuadamente los resultados y orientar la toma de decisiones antes de dicha ICP primaria. La primera escala se obtuvo a partir de una cohorte de pacientes tratados entre 1995 y 2013, y por consiguiente incluyó en parte técnicas de ICP no contemporáneas. Además, no se validó en otra cohorte. Por otra parte, el antecedente de reanimación de una parada cardiaca fuera del hospital es mucho menos frecuente en los mayores de 75 años y, por consiguiente, es mucho menos útil22. La segunda escala requiere 3 determinaciones analíticas al ingreso23. Los valores de corte de la concentración sérica, en especial de la creatinina, pueden no ser adecuados para la discriminación pronóstica en los ancianos, y en general estos valores de corte son muy sensibles a las diferencias de la población, el momento de obtención de las muestras y los métodos de laboratorio. Todos estos factores dificultan la aplicación amplia de esta escala en la práctica clínica.
En cambio, nuestro índice pronóstico se ha elaborado y validado específicamente en una población anciana tratada con una ICP primaria contemporánea y se basa en 3 variables clínicas previas a la intervención y muy sencillas. Teniendo en cuenta estas características, la escala 6-ANT-40 podría utilizarse en el proceso de toma de decisiones antes de la ICP primaria, que es de especial importancia en el contexto de los pacientes en SC muy ancianos.
Creemos firmemente que no se debe negar a los pacientes ancianos con IAMCEST y SC los posibles efectos favorables de la ICP primaria, pero se debe reconocer que los beneficios que obtienen de esta intervención son escasos. Además, en algunos pacientes, la ICP y nuevas intervenciones posteriores podrían conducir a un abordaje terapéutico agresivo que daría lugar a cierta distanasia. Nuestro estudio proporciona un índice predictivo basado en variables clínicas sencillas que pueden ser útiles para orientar la toma de decisiones en este escenario complejo.
LimitacionesEste es un registro retrospectivo y, aunque se fomentó fuertemente la inclusión consecutiva, no puede garantizarse por completo. No se incluyó en este registro a los pacientes ancianos en SC como complicación de un IAMCEST para los que no se consideró la ICP (en su mayor parte por considerarse que tenían un pronóstico muy malo a corto plazo). No obstante, los resultados son aplicables a la población cada vez más amplia de pacientes ancianos con SC a los que en general se indica la ICP. La aplicación de los criterios diagnósticos del SC fue uniforme, pero la asignación final fue una decisión del investigador, y podría haber cierta heterogeneidad. La identificación de un valor pronóstico para los factores propios de la intervención parece verse afectada en cierta medida por un sesgo de selección. Por consiguiente, estas asociaciones deben interpretarse con precaución y solo como generadoras de hipótesis.
CONCLUSIONESLa incidencia de SC en los pacientes de más de 75 años tratados con ICP primaria fue del 9,3%. El SC se asoció con una mortalidad muy alta y concentrada en el periodo de hospitalización. Un índice previo a la intervención, basado en 3 variables clínicas sencillas (localización en la cara anterior, FEVI <40% y tiempo hasta el tratamiento> 6 h) puede usarse para estimar la supervivencia tras la ICP y orientar la toma de decisiones antes y después de la intervención.
- –
Dado el envejecimiento de la población en los países occidentales, se está produciendo un aumento de la proporción de pacientes mayores ingresados con diagnóstico de IAMCEST.
- –
El SC es más frecuente en esta población y aumenta drásticamente su mortalidad a corto plazo, incluso tras el tratamiento con angioplastia primaria.
- –
La información sobre los perfiles clínicos, los resultados y los predictores de la mortalidad a corto y a largo plazo de los pacientes ancianos con SC como complicación de un IAMCEST tras la angioplastia primaria es escasa.
- –
El estudio incluye una serie amplia de pacientes de más de 75 años con SC como complicación de un IAMCEST y tratados mediante angioplastia primaria, lo cual permitió la caracterización e identificación de los predictores del SC, los resultados clínicos y las variables pronósticas.
- –
Se ha elaborado y validado un índice pronóstico basado en las variables clínicas basales para esta población específica. Este índice predice bastante bien los resultados clínicos tras una eventual angioplastia primaria y, por consiguiente, podría aplicarse en el proceso de toma de decisiones antes de la intervención.