El tratamiento habitual de un paciente con cardiopatía congénita (CC) que contrae hipertensión pulmonar (HTP) grave es el tratamiento médico con vasodilatadores pulmonares y la corrección de la cardiopatía si es posible. Cuando no es posible este tratamiento por HTP grave con resistencias pulmonares fijas y refractariedad al tratamiento médico, pueden considerarse el trasplante cardiopulmonar y el trasplante pulmonar (TP) combinado con la corrección de la CC. Desde la primera descripción exitosa de corrección de una CC junto con TP en 19901, se han comunicado algunos casos2–4. En nuestro medio se han publicado algunos casos de adultos con cardiopatías simples5. No se conoce de ningún caso pediátrico de estas características publicado en nuestro país.
Se describe a un varón de 15 años con HTP grave y una CC consistente en anomalías de los drenajes venosos pulmonar y sistémico con una comunicación interauricular (CIA) grande. El paciente presentaba disnea en reposo o ante mínimos esfuerzos, con dolor precordial de características anginosas a pesar del tratamiento con sildenafilo y bosentán vía oral y treprostinil subcutáneo.
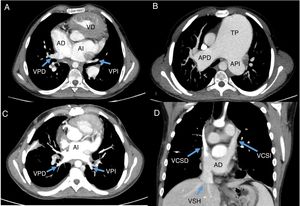
En la tomografía computarizada se observó interrupción de la vena cava inferior con continuación con la vena ácigos hasta la vena cava superior izquierda que drenaba al seno coronario (ausencia del tronco venoso innominado). El drenaje venoso pulmonar derecho llegaba a través de 2 venas pulmonares a la aurícula derecha (figura 1A). También se visualizó un aneurisma gigante (más de 8 cm) de la arteria pulmonar que desplazaba y comprimía estructuras vecinas (figura 1B). Finalmente, había una gran CIA tipo ostium secundum con cortocircuito derecha-izquierda.
Tomografía computarizada prequirúrgica y resultado tras el trasplante. A: anomalía del drenaje venoso pulmonar. B: aneurisma pulmonar. C: drenaje venoso pulmonar. D: drenaje venoso sistémico. AD: aurícula derecha; APD: arteria pulmonar derecha; API: arteria pulmonar izquierda; AI: aurícula izquierda; TP: tronco pulmonar; VCSD: vena cava superior derecha; VCSI: vena cava superior izquierda; VD: ventrículo derecho; VPD: vena pulmonar derecha; VPI: vena pulmonar izquierda; VSH: venas suprahepáticas.
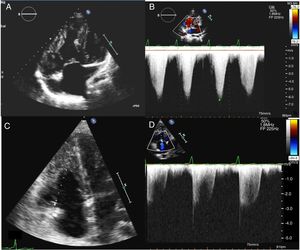
El ecocardiograma mostró una hipertrofia grave del ventrículo derecho (figura 2A), insuficiencia tricuspídea grave con presión pulmonar suprasistémica (figura 2B) y un gran aneurisma de la arteria pulmonar.
En el cateterismo preoperatorio se confirmaron los hallazgos previos: HTP suprasistémica (presión arterial pulmonar media >90mmHg y resistencias vasculares pulmonares 32 UW). Además, se objetivó la compresión del tronco coronario izquierdo por el aneurisma pulmonar.
Se decidió realizar TP bilateral con corrección de la CC en el mismo procedimiento. La cirugía se llevó a cabo con asistencia mediante circulación extracorpórea. Se canularon las 3 venas cavas y la aorta ascendente. Tras realizar la anastomosis bronquial en el lado derecho, se pinzó la aorta y se administró cardioplegía hasta conseguir la parada cardiaca. A continuación, se abrió la aurícula derecha y, a través de la CIA, se identificó la aurícula izquierda y se anastomosó el casquete de las venas pulmonares derechas del donante al cuerpo de la aurícula izquierda del receptor (figura 1C). Finalmente se cerraron la CIA y la atriotomía derecha y se implantó el pulmón izquierdo. Los tiempos de isquemia y circulación extracorpórea fueron de 45 y 185min respectivamente. En las primeras horas del posoperatorio, apareció deterioro de la oxigenación, con saturaciones de O2 bajas —que requirieron broncoscopias de limpieza— y también una hemorragia posquirúrgica significativa. Se requirió intubación prolongada por delirio posoperatorio y crisis comiciales en relación con concentraciones supraterapéuticas de tacrolimus, y se precisó una traqueotomía. La evolución posterior transcurrió sin incidencias y 5 días después se pudo retirar la asistencia ventilatoria y posteriormente la cánula. Se dio al paciente el alta a domicilio a los 30 días de la cirugía. Tras 1 año de seguimiento, el paciente estaba asintomático y con saturaciones en pulsioximetría del 96-97%. En la ecocardiografía se observaron mejoría de la HTP e insuficiencia tricuspídea leve (figura 2D), buena función biventricular y ausencia de defectos residuales significativos. La espirometría mostró una capacidad vital forzada de 3,73 (71%), un volumen espiratorio forzado de 1,96 (62%) y un índice de 71.
En la literatura, los artículos sobre cirugía combinada de TP y corrección de la CC son excepcionales, se reducen a pequeñas series o casos clínicos1-4. En la serie más larga hasta la fecha6 se describe a 51 pacientes con CC e HTP grave sometidos a trasplante cardiopulmonar (n=16) o TP con corrección de la CC (n=35). Las complicaciones posoperatorias graves y la mortalidad hospitalaria de este último grupo fueron significativas. Resulta interesante que, en el grupo de TP más corrección de la CC, la media de edad en el momento de la cirugía era 1,7 años y la presión arterial media y la resistencia vascular pulmonar, 66 y 21mmHg respectivamente. Estas cifras contrastan con la edad y el grado de HTP de nuestro paciente, lo que podría indicar que estos pacientes en nuestro medio se mantienen con tratamiento médico.
En conclusión, el TP combinado con corrección de CC representa una opción en nuestro medio para pacientes con CC e HTP grave. Se debe considerar este tratamiento para los pacientes con CC sintomáticos y HTP grave refractaria a tratamiento médico, independientemente de la edad.