El stent es un tratamiento eficaz en la coartación y la recoartación. Sin embargo, en jóvenes y adultos pueden ocurrir rotura de pared y disección de aorta y, en el seguimiento, aneurismas. Con el fin de reducir estas complicaciones, implantamos el stent recubierto mayoritariamente de manera electiva.
MétodosDesde 2005 realizamos el procedimiento en 17 pacientes (2 adolescentes y 15 adultos) acceso femoral, 16 de manera electiva y en 1 como rescate. Seguimos técnica de Mullins con implantación de stent recubierto de NuMED®.
ResultadosBuena aposición del stent en 17 casos, con acampanamiento distal en 8. Reducción del gradiente de 40±16 a 2±2mmHg (p<0,001) y aumento del diámetro de luz de 4±2 a 19±3mm (p<0,001). Se comentan dos casos excepcionales: uno con rotura que se trató de rescate con stent en el stent, y otro con obstrucción total y aneurisma intercostal que presentó una evolución fatal, pues murió a las 48 h del procedimiento (se muestra la necropsia). El seguimiento clínico fue de 4 años, con estudio con ecocardiograma Doppler, y en 13 de los pacientes con otra técnica de imagen, todos ellos con buena evolución.
ConclusionesEl stent recubierto es un tratamiento eficaz en la coartación y la recoartación del joven y el adulto, de elección en los casos con anatomía compleja, y es necesario como dispositivo de rescate en los casos de stent no recubierto.
Palabras clave
El tratamiento con stent en la coartación nativa y la recoartación es una alternativa a la cirugía clásica en el niño mayor, el adolescente y el adulto1–9. Sin embargo, en coartaciones complejas, muy graves, tortuosas o excéntricas y en pacientes jóvenes y adultos, que con frecuencia presentan degeneración quística de la media y desestructuración de la pared aórtica, pueden producirse complicaciones como aneurisma, seudoaneurisma, disección y la temida rotura de aorta, que puede ser fatal con muerte inmediata del paciente, tanto tras la angioplastia convencional como en la implantación de stent8–16.
Con el fin de reducir estas complicaciones y después de haber vivido un caso de rotura aórtica, que se expone, para pacientes con coartación y recoartación a partir de la juventud, decidimos implantar de manera electiva el stent recubierto (SR) de politetrafluoroetileno expandido (ePTFE) de la casa comercial NuMED® (Hopkinton, Nueva York, Estados Unidos), que va montado sobre balón y protege la pared vascular en su expansión6,15–19.
MÉTODOSDesde noviembre de 2005 a enero de 2012, resolvimos 17 casos (2 adolescentes y 15 adultos) de coartación y recoartación mediante implante de un SR de ePTFE.
Este SR de NuMED® está fabricado en aleación del 90% de platino y el 10% de iridio tratado con calor, que se distribuye en filas soldadas por láser, con un patrón en zigzag, y con protección de oro en los puntos de soldadura6,15,18. El número de zigzag de cada fila puede variar y ello afecta a la fuerza radial, su diámetro de expansión y su acortamiento porcentual; mientras tanto, el número de filas determina la longitud previa a la expansión.
El SR de 8 zigzag para la coartación va cubierto de un tejido de PTFE que se expande con el stent y protege el tejido vascular. La longitud del stent va de 16 a 45mm, se expande hasta 24mm y puede alcanzar hasta 28mm. Para estos diámetros máximos, el acortamiento va del 33 al 40% de su longitud total.
Con anestesia general y anticoagulación con heparina sódica, los primeros 2 casos se realizaron por disección quirúrgica de la arteria femoral y los demás, con implantación previa del ProStar XL 10 Fr (Abbot Vascular Devices; Redwood City, California, Estados Unidos). Para el control angiográfico, utilizamos acceso por la arteria radial hasta el arco. Se midió el diámetro de la aorta previo, posterior y en el punto de coartación, así como la longitud del segmento.
Para la expansión del stent, empleamos balones Z-Med (NuMED®) o BIB Balloon (NuMED®) de diámetro similar a la aorta previa a la coartación o en la porción terminal del arco para luego, si fuera preciso, redilatar y acampanar el stent mediante un segundo balón de mayor diámetro (tabla 1). Según los diámetros de balón necesarios, accedimos con vainas de Mullins de 12-16 Fr y expandimos los stents mediante la técnica de Mullins, es decir, retirando la vaina y exponiendo el stent en la porción media de la coartación.
En casos de obstrucción completa, realizamos perforación desde la porción superior con guías de desobstrucción coronaria tipo Hi-Torque Cross-It 200 o Asahi Confianza (Abbot), para luego capturar con un lazo de Amplatz GooseNeck™ (ev3 Inc.; Plymouth, Minnesota, Estados Unidos) en la porción distal y establecer un raíl arterial radial-femoral como ya se ha descrito5,20.
El montaje del stent en el balón se debe realizar con irrigación continua de suero fisiológico, realizando movimientos rotatorios sobre el balón bien plegado. Este conjunto se introduce en el cargador, también con irrigación y rotación, y una vez dentro del cargador, este se introduce en la vaina de Mullins liberando la válvula.
Una vez realizado el procedimiento, los pacientes fueron controlados en la unidad coronaria, donde se inició la antiagregación plaquetaria durante 6 meses. Se administró, además, cefuroxima en tres dosis intravenosas de 1,5g como profilaxis antibiótica.
Las variables cualitativas se han descrito mediante distribuciones de frecuencia y porcentaje y las variables cuantitativas, mediante media±desviación típica. La comparación de dos variables continuas de antes y después se ha realizado mediante la prueba no paramétrica de Wilcoxon, puesto que el tamaño de la muestra era pequeño. Para estudiar la correlación entre diámetro de balón y diámetro de la aorta previo a la coartación, se ha utilizado la correlación de Spearman. Se consideró significativo p<0,05. Se utilizó el software estadístico SPSS v. 19.0.
RESULTADOSComo ya hemos referido, en 7 años realizamos 17 procedimientos mediante SR en 13 varones y 4 mujeres, con una media de edad de 35±15 (14-65) años. En 7 casos tenían asociada válvula aórtica bicúspide y en 1 caso, comunicación interventricular muscular pequeña (caso 9, tabla 1); 5 casos tenían pendiente cirugía cardiaca en un segundo tiempo: 2 por insuficiencia aórtica, 2 por estenosis y 1 por ectasia de la aorta ascendente; 9 pacientes se encontraban en tratamiento por hipertensión arterial y 15 estaban en clase funcional I de la New York Heart Association (NYHA), 1 estaba en NYHA II y 1 en NYHA III (tabla 1).
En 11 casos la coartación era nativa y en 6, recoartación, que era secundaria a cirugía terminoterminal en 5 y a cirugía con parche de ampliación en 1. En 16 casos el SR se implantó de manera electiva y en 1 caso, en situación extrema por rotura de la aorta tras la expansión de un stent convencional11 (caso 2, tablas 1 y 2). La longitud del SR fue de 40±4mm montado sobre balones con diámetro de 19±3 mm, con buena correlación con el diámetro de aorta previo a la coartación de 18±4mm. En 8 casos se redilató la porción distal con un balón de mayor diámetro (25±3mm). La implantación fue directa, salvo en los casos con obstrucción completa o estenosis muy intensa, en los cuales, además de la técnica especial referida, realizamos dilatación previa con balones de 8–10mm de diámetro (casos 1 y 16; tablas 1 y 2).
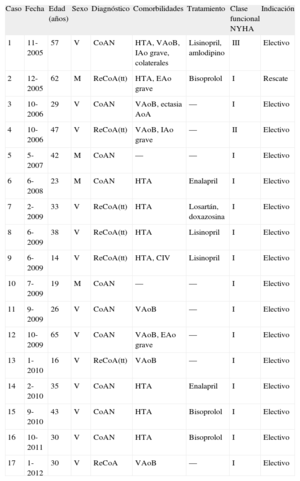
Características clínicas de los pacientes (media de edad, 35,0±15,2 años)
| Caso | Fecha | Edad (años) | Sexo | Diagnóstico | Comorbilidades | Tratamiento | Clase funcional NYHA | Indicación |
| 1 | 11-2005 | 57 | V | CoAN | HTA, VAoB, IAo grave, colaterales | Lisinopril, amlodipino | III | Electivo |
| 2 | 12-2005 | 62 | M | ReCoA(tt) | HTA, EAo grave | Bisoprolol | I | Rescate |
| 3 | 10-2006 | 29 | V | CoAN | VAoB, ectasia AoA | — | I | Electivo |
| 4 | 10-2006 | 47 | V | ReCoA(tt) | VAoB, IAo grave | — | II | Electivo |
| 5 | 5-2007 | 42 | M | CoAN | — | — | I | Electivo |
| 6 | 6-2008 | 23 | M | CoAN | HTA | Enalapril | I | Electivo |
| 7 | 2-2009 | 33 | V | ReCoA(tt) | HTA | Losartán, doxazosina | I | Electivo |
| 8 | 6-2009 | 38 | V | ReCoA(tt) | HTA | Lisinopril | I | Electivo |
| 9 | 6-2009 | 14 | V | ReCoA(tt) | HTA, CIV | Lisinopril | I | Electivo |
| 10 | 7-2009 | 19 | M | CoAN | — | — | I | Electivo |
| 11 | 9-2009 | 26 | V | CoAN | VAoB | — | I | Electivo |
| 12 | 10-2009 | 65 | V | CoAN | VAoB, EAo grave | — | I | Electivo |
| 13 | 1-2010 | 16 | V | ReCoA(tt) | VAoB | — | I | Electivo |
| 14 | 2-2010 | 35 | V | CoAN | HTA | Enalapril | I | Electivo |
| 15 | 9-2010 | 43 | V | CoAN | HTA | Bisoprolol | I | Electivo |
| 16 | 10-2011 | 30 | V | CoAN | HTA | Bisoprolol | I | Electivo |
| 17 | 1-2012 | 30 | V | ReCoA | VAoB | — | I | Electivo |
AoA: aorta ascendente; CIV: comunicación interventricular; CoAN: coartación de aorta nativa; EAo: estenosis aórtica; HTA: hipertensión arterial; IAo: insuficiencia aórtica; M: mujer; NYHA: New York Heart Association; ReCoA(tt): recoartación de aorta con anastomosis terminoterminal previa; V: varón; VAoB: válvula aórtica bicúspide.
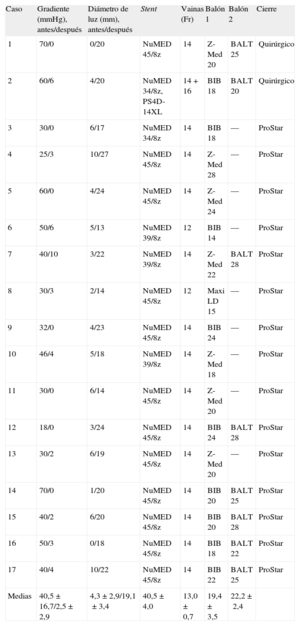
Características del procedimiento
| Caso | Gradiente (mmHg), antes/después | Diámetro de luz (mm), antes/después | Stent | Vainas (Fr) | Balón 1 | Balón 2 | Cierre |
| 1 | 70/0 | 0/20 | NuMED 45/8z | 14 | Z-Med 20 | BALT 25 | Quirúrgico |
| 2 | 60/6 | 4/20 | NuMED 34/8z, PS4D-14XL | 14+16 | BIB 18 | BALT 20 | Quirúrgico |
| 3 | 30/0 | 6/17 | NuMED 34/8z | 14 | BIB 18 | — | ProStar |
| 4 | 25/3 | 10/27 | NuMED 45/8z | 14 | Z-Med 28 | — | ProStar |
| 5 | 60/0 | 4/24 | NuMED 45/8z | 14 | Z-Med 24 | — | ProStar |
| 6 | 50/6 | 5/13 | NuMED 39/8z | 12 | BIB 14 | — | ProStar |
| 7 | 40/10 | 3/22 | NuMED 39/8z | 14 | Z-Med 22 | BALT 28 | ProStar |
| 8 | 30/3 | 2/14 | NuMED 45/8z | 12 | Maxi LD 15 | — | ProStar |
| 9 | 32/0 | 4/23 | NuMED 45/8z | 14 | BIB 24 | — | ProStar |
| 10 | 46/4 | 5/18 | NuMED 39/8z | 14 | Z-Med 18 | — | ProStar |
| 11 | 30/0 | 6/14 | NuMED 45/8z | 14 | Z-Med 20 | — | ProStar |
| 12 | 18/0 | 3/24 | NuMED 45/8z | 14 | BIB 24 | BALT 28 | ProStar |
| 13 | 30/2 | 6/19 | NuMED 45/8z | 14 | Z-Med 20 | — | ProStar |
| 14 | 70/0 | 1/20 | NuMED 45/8z | 14 | BIB 20 | BALT 25 | ProStar |
| 15 | 40/2 | 6/20 | NuMED 45/8z | 14 | BIB 20 | BALT 28 | ProStar |
| 16 | 50/3 | 0/18 | NuMED 45/8z | 14 | BIB 18 | BALT 22 | ProStar |
| 17 | 40/4 | 10/22 | NuMED 45/8z | 14 | BIB 22 | BALT 25 | ProStar |
| Medias | 40,5±16,7/2,5±2,9 | 4,3±2,9/19,1±3,4 | 40,5±4,0 | 13,0±0,7 | 19,4±3,5 | 22,2±2,4 |
Tras el procedimiento observamos una reducción del gradiente de 40±16 a 2±2 mmHg (p<0,001) y un aumento del diámetro de la luz de 4±2 a 19±3 mm (p<0,001). Finalmente, se realizó aortografía y después el cierre quirúrgico o con el ProStar XL de la arteriotomía femoral. No hubo complicaciones locales, salvo en el caso 12, que presentó un hematoma que se resolvió espontáneamente. No fue preciso intervencionismo con stent a nivel femoroiliaco en ningún caso.
De la serie, debemos destacar dos casos excepcionales:
- •
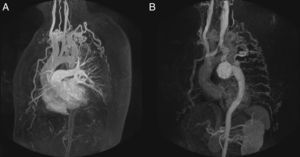
El caso 1 era un varón de 57 años con insuficiencia aórtica grave y disnea en NYHA III, y se decidió intervencionismo percutáneo previo a la cirugía. Tenía una gran suplencia colateral con obstrucción completa de la aorta y un aneurisma intercostal gigante posterior a la coartación (fig. 1). Se desobstruyó la aorta con la técnica referida y se implantó un SR con el fin de excluir el aneurisma. El resultado final fue muy bueno, con desaparición del gradiente y gran aumento de la luz. Realizamos también una redilatación para obtener una buena aposición distal, y en la inyección final se visualizaba muy tenuemente el aneurisma (fig. 2). La evolución fue trágica. Dos días después el paciente sufrió una hematemesis masiva y murió. La necropsia mostró la coartación bien resuelta y el stent sin su recubrimiento, dejando el aneurisma comunicado con una aorta descendente. Consideramos que el gran aumento de presión tras la coartación, de 70 a 150mmHg de presión arterial sistólica, resultó en un flujo retrógrado de alta presión en el aneurisma que llegó a fisurar en las horas siguientes la impronta del aneurisma en el esófago, con una hemorragia digestiva fatal (fig. 3).
Figura 2.Coartación con obstrucción completa y aneurisma gigante intercostal (caso 1). A: aortografía en el arco, que muestra la obstrucción completa de la aorta con el lazo posicionado. B: en fases tardías de la aortografía y en proyección oblicua anterior izquierda de 40°, se visualiza una gran colateral (flechas) que da flujo a la aorta descendente y se contrasta un gran aneurisma intercostal (cabezas de flecha). C: perforación con guía Crossit 300 y entrada en el lazo de GooseNeck™. D: captura de la guía por el lazo y extracción estableciendo raíl radiofemoral. E: dilatación con balón coronario Maverick de 2×20 mm. F: inversión del circuito y posicionamiento de la guía 0,035 y dilatación con balón de Balt de 8×20mm. G: posicionamiento del stent recubierto. H: expansión. I: resultado con buena aposición del stent a la pared.
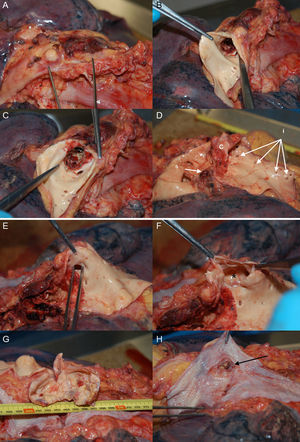
(0.66MB).Figura 3.Necropsia del caso 1. A: vista de la aorta en su porción ístmica. B y C: apertura de la aorta y visualización del stent desnudo, sin la cubierta de politetrafluoroetileno. D: extraído el stent, se visualiza el punto de coartación obstructivo (c), el orificio de la subclavia izquierda (s) y los orificios de las arterias intercostales (i), la de mayor tamaño en relación con el aneurisma. E: la pinza muestra el orificio intercostal. F: apertura del orificio que muestra el aneurisma (*). G: apertura del aneurisma, que mide 7 cm. H: esófago con zona de inflamación crónica por la impronta del aneurisma; la flecha señala una solución de continuidad que comunica con el aneurisma, comprobado durante la necropsia.
(0.47MB). - •
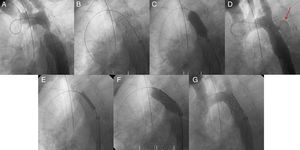
El caso 2 era una mujer con recoartación de larga evolución a la que se implantó un stent convencional de Palmaz; presentó subexpansión medial, y se redilató con un balón de Mullins de alta presión. Se produjo una rotura de aorta con hemorragia torácica masiva. Debido a ello, sufrió hipotensión, bradicardia extrema y parada cardiaca; rápidamente se implantó un SR en el stent y se pudo recuperar a la paciente (fig. 4). Después se realizó evacuación del hemotórax con un tubo de drenaje, y la evolución fue favorable.
Figura 4.Rotura de aorta, caso 2. A: aortografía que muestra la gran recoartación. B: subexpansión del stent de Palmaz. C: posdilatación a 9 atm con el balón de Mullins. D: rotura de la aorta y fuga de contraste al tórax (flecha). E: stent recubierto en el stent previo a la expansión. F: expansión del stent recubierto en el stent. G: sellado completo de la rotura aórtica.
(0.33MB).
El seguimiento de 4±2,5 años fue por clínica y estudio con ecocardiograma Doppler. Se objetivó en todos los casos la persistencia del buen resultado inicial, sin datos de reobstrucción alguna. Los pacientes 2, 3, 4 y 12 fueron operados entre los 4 y los 8 meses de nuestro procedimiento. Se implantaron dos válvulas mecánicas, una biológica y una sustitución de aorta ascendente por un tubo de dacrón. Todos ellos evolucionaron favorablemente. El paciente con comunicación interventricular muscular pequeña no precisó cierre del defecto.
A 13 de estos pacientes se les realizó estudio de imagen, sin observarse aneurismas, disecciones y/o procesos obstructivos. En 5 pacientes fue posible reducir la medicación para la hipertensión y en 2 no se pudo suspenderla.
DISCUSIÓNNuestra serie de 17 casos (incluido el stent en el stent referido en el caso 2), con implantación consecutiva de SR de ePTFE en la coartación y recoartación de 2 adolescentes y 15 adultos, es una serie realizada en 7 años comparable con otras publicadas16-19. Los resultados inmediatos son muy buenos y similares a los obtenidos con el stent convencional5.
El interés de la serie se centra en la elección de SR para todos los casos consecutivos a partir de la juventud, sobre todo en el intento de reducir complicaciones graves. Se debe subrayar que la pared de la aorta adyacente a la coartación presenta desestructuración por necrosis quística de la media y que con la edad se depositan polisacáridos y se fracturan las fibras elásticas de la media, con fibrosis y proliferación de colágeno que debilitan su estructura12,14.
Aunque la incidencia de aneurismas es mayor en los casos de coartación hipoplásica del niño21, esta complicación ocurre también tras el stent convencional en el adulto, con cifras próximas al 5%4,8,18,22,23. La posibilidad de rotura de estos aneurismas en el seguimiento no es despreciable y su intervención supone una cirugía de riesgo elevado24,25.
Otra complicación grave en el intervencionismo sobre la aorta es la rotura, que es infrecuente, aunque se cree que también se declara poco4,11,13,16. La situación, como en nuestro caso11, es dramática, y se produce el fallecimiento en la sala en la mitad de los casos referidos. En el nuestro, al ser una recoartación de larga evolución, preparamos el SR y todo el material necesario para poder implantarlo en el stent de manera rápida y salvadora. En este caso lo utilizamos como dispositivo de rescate, y en el resto de la serie la indicación fue electiva y de primera intención.
El mecanismo del tratamiento con stent en la aorta implica un daño controlado de la pared enferma, con remodelado agudo del vaso. Se trata de un andamiaje con lesión de pared seguida de cicatrización, que en la mayoría de los pacientes es favorable, sin producirse aneurismas, disecciones y/o reestenosis. Sin embargo, en la coartación desfavorable y compleja, la posibilidad de daño incontrolado es mayor y se producen complicaciones agudas y tardías.
Por ello, la incidencia de rotura, disección y aneurismas de aorta en la implantación del stent convencional es mayor, sin duda, en:
- •
Los adultos con aorta poco distensible antes y después de la coartación, donde hay facilidad tanto para la rotura como para la disección14.
- •
Los casos con obstrucción completa (mal llamada atresia) donde se produce una enorme ganancia de luz y puede condicionar un daño de pared significativo10,17.
- •
Los casos con coartación distorsionada/angulada por la desigualdad de fuerzas en la expansión del stent10.
- •
Los casos con mayor degeneración de la pared donde aparece calcificación10.
- •
La recoartación del adulto de larga evolución, como nuestro caso 2, especialmente secundarios a cirugía terminoterminal, en que se produce una cicatriz circunferencial inexpandible que hace necesario balón de alta presión y al expandirse el stent puede romper la aorta11,13,14,16.
- •
En los casos con aneurisma previo nativo, posquirúrgico o tras intervención percutánea.
El SR presenta, por lo tanto, ventajas innegables, y ofrece sobre todo mayor seguridad; sin embargo, también muestra ciertas desventajas con respecto al stent convencional:
- •
Precisa de unas arterias femorales adecuadas para unas vainas más gruesas, de 12–16 Fr, y la utilización de estas vainas supone mayor riesgo de hemorragia. Por ello es importante tener un adecuado manejo del ProStar XL. Para pacientes más jóvenes con dificultad de acceso por su tamaño, se ha señalado la posibilidad de implantar un stent de menor perfil, de 8–11 Fr, como el Advanta™ V12 Covered Stent (Atrium Medical; Hudson, New Hampshire, Estados Unidos), que viene premontado en balones con diámetro de 12, 14 y 16 mm y puede expandirse hasta 22mm26. Bruckheimer et al desarrollaron una forma ingeniosa de implantación de stent y describieron 9 casos de implantación con un balón de menor tamaño para, en un segundo paso o un segundo procedimiento, redilatar al diámetro referido, disminuyendo netamente el grosor del catéter; quizá esta técnica puede incrementar el número de deslizamientos y de embolizaciones27.
- •
Con el SR se plantea también la posibilidad de obstrucción de una rama aórtica importante, como carótida, subclavia, etc. Parece que la obstrucción de la subclavia izquierda se tolera bien, aunque ocasionalmente se ha precisado de un puente carotidosubclavio. Para evitar la isquemia en la extremidad superior derecha, Tsai et al28 describieron la perforación del stent desde la vía radial-subclavia con eficaces perforación y dilatación de la malla. Recientemente, en caso de que la subclavia esté muy próxima a la coartación, Lampropoulos et al29 describieron la técnica de doble guía y kissing.
Nos parece obligado comentar el caso 1 con el fin de que se conozca esta complicación fatal y no se repita. Demuestra la importancia del manejo técnico y la dificultad que puede existir en el paso del SR montado en el balón desde la cánula a la vaina; esta transición no será precisa en el próximo implante, que tiene características similares a la válvula pulmonar percutánea Melody® (Medtronic; Minneapolis, Minnesota, Estados Unidos)30.
Los aneurismas intercostales son una entidad bien conocida que ocurre en la coartación con una incidencia de un 3–10%31,32 y pueden ser verdaderos33 o falsos34. Se forman por la debilidad referida de la capa media arterial junto con el hiperaflujo colateral, y muchas veces se los considera erróneamente aneurismas de la pared aórtica. En sí mismos suponen un riesgo añadido a la intervención quirúrgica de la coartación35-37.
Por la literatura médica revisada, creemos que este es el primer caso de intervencionismo con SR sobre un caso con obstrucción completa y aneurisma intercostal gigante que tuvo evolución catastrófica y muerte.
LimitacionesLas limitaciones de este trabajo son, fundamentalmente, que se trata de un estudio retrospectivo observacional y sin grupo comparativo de tratamiento con stent convencional. Aunque clínicamente se han seguido todos los casos, no a todos ellos se hizo estudio de imagen en el seguimiento, por lo que no podemos definir con seguridad la incidencia de posibles aneurismas. En ningún caso el fallecimiento de nuestro caso 1 por un problema técnico desvirtúa el interés y la seguridad que puede proporcionar el SR.
CONCLUSIONESEl SR de ePTFE es eficaz en el tratamiento de la coartación y la recoartación del adulto. Lo consideramos de elección en los casos de riesgo, con obstrucción completa o muy intensa, aorta distorsionada, angulada o calcificada, recoartación de larga evolución y cuando se asocie a formaciones aneurismáticas.
El SR de ePTFE debe estar presente en la sala como dispositivo de rescate cuando se implanta un stent convencional; puede ser salvador de una complicación aguda, como la rotura y/o disección de aorta.
CONFLICTO DE INTERESESNinguno.
Al especialista de producto Alberto Martinez Albalat; al equipo de enfermería de la sección de hemodinámica (Asunción Ocariz, Javier Hernando, M. Antonia Pereiro, M. Isabel Peña, M. Victoria Izquierdo y Fernando Gómez); a las auxiliares de enfermería Josefina Garcia, Felicidad Gutierrez y M. Ángeles Bañuelos, y a la auxiliar administrativa M. Teresa Vivas.