Aproximadamente un 5-10% de los pacientes remitidos para cateterismo con un diagnóstico inicial de infarto de miocardio no tienen lesiones obstructivas en la coronariografía, una entidad conocida como MINOCA por sus siglas en inglés. El interés en este problema ha crecido en los últimos años, y se ha plasmado en un artículo de posicionamiento1 y en recomendaciones específicas en la guía europea de síndrome coronario agudo sin elevación de ST2. En un artículo publicado recientemente por García-Blas et al. en Revista Española de Cardiología3, se presenta un estudio observacional que analiza el pronóstico a largo plazo de los pacientes con MINOCA, con especial foco en la importancia de la carga de placa ateroesclerótica. Los autores estudiaron a 591 pacientes consecutivos con infarto, y el 20% de ellos no tenían lesiones obstructivas. Encontraron que el riesgo de eventos adversos cardiovasculares mayores (MACE) a 5 años fue menor en los pacientes con MINOCA que en aquellos con enfermedad obstructiva, con un riesgo relativo de 0,63. Lo que más interés añade al artículo es que los autores analizaron el pronóstico de los 121 pacientes con MINOCA en función de su carga de placa —coronarias lisas, enfermedad leve (0-30% estenosis) o enfermedad moderada (30-49%)— y encontraron un importante incremento del riesgo de MACE con cada nivel de ateromatosis. El riesgo relativo de la enfermedad leve fue de 2,45 y el de la moderada, 3,64 tomando como referencia los pacientes con coronarias lisas. Así pues, parece que la ateromatosis coronaria, incluso no significativa, es importante en el pronóstico de los pacientes con MINOCA. Cabe resaltar que estos resultados son claramente peores que los de los pacientes afectos de síndromes coronarios crónicos: la tasa de eventos en los pacientes con MINOCA y enfermedad moderada fue >50% a 5 años, lo que triplica la encontrada en la cohorte registro del ensayo FAME 24. Este hallazgo enfatiza el carácter potencialmente inestable de la enfermedad coronaria en el MINOCA y subraya la importancia de hacer un buen diagnóstico fisiopatológico en estos pacientes (figura 1).
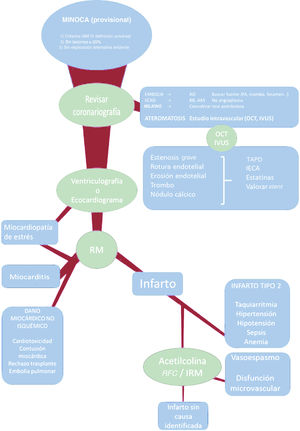
Propuesta de diagnóstico estratificado en MINOCA. AAS: ácido acetilsalicílico; AO: anticoagulación oral; BB: bloqueadores beta; IAM: infarto agudo de miocardio; IRM: índice de resistencia microvascular; IVUS: ecografía intravascular; MINOCA: infarto de miocardio sin lesiones coronarias obstructivas; OCT: tomografía de coherencia óptica; RFC: reserva de flujo coronario; RM: resonancia magnética cardiaca; SCAD: disección coronaria espontánea; TAPD: tratamiento antiagregante plaquetario doble.
La frecuencia y el pronóstico del MINOCA son variables según los estudios, debido sobre todo a la considerable confusión terminológica y la variabilidad metodológica de estos. Tanto el documento de posicionamiento europeo1 como la guía europea de SCASEST2 han tratado de armonizar la terminología y orientar sobre el proceso diagnóstico y terapéutico del MINOCA. No obstante, el amplio abanico de enfermedades que engloba este término, añadido a la multitud de estudios diagnósticos recomendados y la falta de un protocolo estandarizado, hace que las estrategias diagnósticas y terapéuticas con estos pacientes sean muy variables y no siempre basadas en la mejor evidencia. Es comprensible que muchos clínicos e intervencionistas crean que no es realista en nuestro medio (por motivos organizativos y económicos) realizar el tipo de estudio exhaustivo que parecen proponer las guías para todos los pacientes con MINOCA. A continuación se detalla una propuesta para afrontar este problema de manera práctica y realista en nuestro medio.
Operativamente, el término MINOCA debe entenderse como un diagnóstico provisional, de trabajo. Así, a un paciente se lo cataloga como MINOCA si cumple los criterios de la definición universal de infarto, no tiene lesiones significativas (50%) en la angiografía y no hay en ese momento un diagnóstico alternativo evidente (p. ej., embolia de pulmón o miocarditis)1. Debe enfatizarse que, en ese momento, lo que el paciente tiene con seguridad es un daño miocárdico, sin que se deba presuponer el infarto, que es por definición de etiología isquémica. A partir de ahí, debe arrancarse el proceso diagnóstico con el objetivo de encontrar el mecanismo etiológico específico (p. ej., miocarditis, embolia coronaria o infarto por placa inestable trombótica), que llevará a un diagnóstico definitivo y, si es posible, un tratamiento dirigido. En situación ideal, no se debería dar de alta a ningún paciente con diagnóstico de MINOCA, sino con un diagnóstico específico. En la práctica, aun tras un estudio sistemático, una minoría de pacientes quedarán sin diagnóstico etiológico, pero al menos se habrá establecido o descartado un mecanismo isquémico y se habrán descartado las causas más importantes de daño miocárdico no isquémico.
Puesto que el diagnóstico provisional de MINOCA se establece al realizar la coronariografía, el primer paso en la profundización del estudio, y a menudo el más importante, comienza mientras el paciente se encuentra aún en el laboratorio de hemodinámica. Una revisión minuciosa de las imágenes puede revelar una causa de infarto en las arterias epicárdicas, sin gasto adicional ni riesgo para el paciente. Así, la amputación distal abrupta de un pequeño vaso orienta a una embolia coronaria; una imagen de doble luz, radiolucencia o estrechamiento moderado difuso indica una disección coronaria espontánea; un trayecto intramiocárdico de la descendente anterior se asocia con frecuencia a disfunción endotelial e isquemia por vasoespasmo y, por último, la presencia de ateromatosis no significativa debe alertar sobre la posibilidad de una placa complicada, a menudo con rotura endotelial y trombo asociado.
Este último caso es muy importante, ya que, como señala el artículo de García-Blas et al.3, la presencia de placas no significativas es un marcador pronóstico, probablemente sobre todo en función de su inestabilidad y vulnerabilidad. La angiografía tiene poca precisión para determinar la inestabilidad de una placa, por lo que se recomienda estudiarlas con ecografía intravascular (IVUS) o tomografía de coherencia óptica (OCT). Esta última, por su mayor resolución espacial, permite valorar mejor la presencia de marcadores de inestabilidad o vulnerabilidad en una placa: rotura endotelial, trombo, erosión, fibroateroma de capa fina o nódulo cálcico. Además, la imagen a menudo permite reconocer que una placa que parece leve en angiografía en realidad es obstructiva5. La IVUS en pacientes con MINOCA ha demostrado que las lesiones correspondientes a una placa con rotura endotelial presentan mayor carga de placa y mayor remodelado positivo, lo que ilustra cómo estenosis leves aparentemente inocentes por angiografía pueden esconder una gran placa inestable6. Todo ello ayuda a tomar la decisión de tratar estas lesiones con angioplastia si es preciso o indicar un tratamiento farmacológico intensivo. Por desgracia, el empleo de imagen intracoronaria en el artículo de García-Blas et al.3 fue muy infrecuente, lo que refleja la realidad de la práctica en muchos centros, y ello impide profundizar en los mecanismos concretos por los que la ateromatosis no significativa empeoró el pronóstico de modo tan relevante. Cuando se ha utilizado sistemáticamente en pequeñas series, la OCT ha revelado rotura de la placa en al menos un tercio de los casos7–9. Si lo anterior no ofrece hallazgos que orienten a una etiología específica y el paciente no tiene un ecocardiograma previo, una ventriculografía izquierda realizada en la sala de hemodinámica puede apoyar el diagnóstico de miocardiopatía de estrés o mostrar un patrón de contracción regional que oriente a etiología isquémica. Una disfunción sistólica difusa del ventrículo izquierdo orientaría hacia miocardiopatía o miocarditis.
Si la valoración invasiva minuciosa no revela una causa específica del daño miocárdico, debe tenerse en cuenta que un tercio de los pacientes con diagnóstico inicial de MINOCA tienen una miocarditis10. La edad menor, el sexo masculino y las coronarias lisas en la angiografía son predictores de esta etiología10. Por ello, el siguiente paso lógico es realizar una resonancia magnética cardiaca. La resonancia permite distinguir entre infarto de miocardio, miocarditis y miocardiopatía de estrés, en función de la presencia y la distribución del realce tardío y el edema. Así, una estrategia combinada de OCT seguida de resonancia magnética cardiaca ha mostrado un alto rendimiento diagnóstico en algunos estudios pequeños, y ha permitido llegar a un diagnóstico etiológico en más del 85% de los casos en algunas series7–9.
Si tras la revisión minuciosa de las coronarias y la resonancia no se ha llegado a un diagnóstico concreto, se debe considerar un conjunto heterogéneo de causas de infarto tipo 2 (taquiarritmia, anemia, sepsis, etc.), de daño miocárdico no isquémico (cardiotoxicidad por quimioterapia, rechazo de trasplante) y de enfermedades extracardiacas (tromboembolia pulmonar, infarto cerebral, etc.). Lógicamente, en realidad esto se hace paralelamente a lo anterior, basándose en anamnesis, exploración física y pruebas básicas que se realizan a todo paciente con síndrome coronario agudo, y habrá casos en que la valoración inicial apunte directamente a alguna de estas causas.
Por último, 2 causas mencionadas en el documento de posicionamiento europeo merecen especial atención: el vasoespasmo y la disfunción microvascular. Respecto al primero, un metanálisis11 ha cifrado en un 28% la prevalencia de pruebas de provocación positivas en pacientes con MINOCA. No obstante, los estudios recogidos en este análisis son muy pequeños y heterogéneos, y encontraron prevalencias que oscilaron entre el 0 y el 95%, por lo que está claro que hace falta mejor evidencia al respecto. En cuanto a la disfunción microvascular, su prevalencia está en torno al 30% de los pacientes con angina sin lesiones12 y no hay datos específicos en pacientes con MINOCA. Por ello, es de esperar que un porcentaje considerable de los pacientes con MINOCA tengan disfunción microvascular, pero esto no necesariamente debe llevar a la conclusión de que la disfunción microvascular es el origen del infarto. De hecho, en casos de infarto aterotrombótico o embólico, la disfunción microvascular podría ser consecuencia del infarto. También es conocida la presencia de disfunción microvascular en la mayoría de las miocardiopatías. Por todo esto, el vasoespasmo y la disfunción microvascular deben considerarse causas posibles, pero probablemente (salvo en casos con alta sospecha clínica inicial de vasoespasmo) merece la pena reservar el estudio invasivo (prueba de acetilcolina13 y medición de reserva de flujo coronario y resistencias microvasculares) para pacientes seleccionados cuyo estudio sistemático previo no haya dado resultados.
El objetivo de este proceso diagnóstico es sentar las bases para un tratamiento específico. Hay pocos datos sobre la eficacia del tratamiento habitual en el MINOCA. Probablemente la mejor evidencia proviene de un subestudio del registro SWEDEHEART, publicado hace pocos años14. Este análisis, que incluyó a casi 10.000 pacientes con MINOCA, mostró una reducción de MACE significativa con las estatinas y los inhibidores de la enzima de conversión de la angiotensina, y una tendencia con los bloqueadores beta, mientras que la doble antiagregación plaquetaria no tuvo efecto beneficioso. El ensayo aleatorizado MINOCA-BAT15, con un diseño factorial, estudiará la eficacia de los bloqueadores beta y los inhibidores de la enzima de conversión de la angiotensina en pacientes con MINOCA. Este ensayo contribuirá a mejorar la evidencia científica sobre estos fármacos, pero en cualquier caso va a incluir una cohorte relativamente heterogénea, ya que en su diseño no dicta una estrategia diagnóstica sistemática, por lo que es previsible que se incluya a pacientes con miocarditis y miocardiopatía de estrés, entre otras causas.
Creemos que el tratamiento personalizado debe ser el principio básico en estos pacientes. Por poner solo un ejemplo, la doble antiagregación plaquetaria no mostró beneficio en el estudio SWEDEHEART, pero evidentemente el hallazgo de una placa rota trombótica, con o sin posterior implante de un stent, indicaría este tratamiento. Por el contrario, en un paciente con embolia coronaria por fibrilación auricular, el tratamiento indicado es la anticoagulación, y añadir doble antiagregación plaquetaria sería inútil o incluso perjudicial.
La validación científica del tratamiento personalizado podría producirse por 2 tipos de estudios. Por una parte, estudios que evalúen la eficacia de tratamientos concretos en situaciones específicas relacionadas con el MINOCA como, por ejemplo, el beneficio de las estatinas o la doble antiagregación plaquetaria en función de la carga y las características de la placa encontrada en la IVUS o la OCT. Y, por otra parte, estudios clínicos que evalúen la eficacia de una estrategia de diagnóstico y tratamiento estratificado, como hizo el ensayo CorMicA16 en el contexto de la angina sin lesiones coronarias. Dentro de esta estrategia diagnóstica para el MINOCA, el análisis de la ateromatosis coronaria y la búsqueda de características de alto riesgo mediante imagen intracoronaria deben tener en el futuro un papel central.
FINANCIACIÓNEste artículo no ha recibido financiación.
CONFLICTO DE INTERESESLos autores declaran no tener conflictos de intereses.