La litoplastia coronaria (LC) es un tratamiento novedoso que utiliza pulsos de alta energía mecánica para fragmentar los depósitos cálcicos de la arterioesclerosis coronaria. Estas ondas también se usan para fragmentar cálculos en diversas localizaciones, principalmente renales (litotricia). La aplicación intracoronaria es innovadora, por lo que hay pocos casos descritos1,2.
La LC consiste en un balón de nailon que, una vez en posición diana, se conecta a una consola externa portátil que emite a demanda ondas mecánicas pulsátiles durante microsegundos (pulsos), lo cual genera una presión intermitente en la pared del vaso de 50-60 atm (3-4 veces superior a lo que se consigue con otros dispositivos). El tamaño del balón debe estar en relación 1:1 con el de la arteria, ya que la emisión y la propagación de la energía mecánica a la pared del vaso se producen cuando el balón de LC contacta con la íntima arterial1. Las ondas se propagan por la pared del vaso y el tejido conectivo y producen microfracturas en los tejidos calcíficos, lo que permite una buena expansión de la lesión y el adecuado implante del stent2.
Se presenta a 3 pacientes con enfermedad coronaria (EC) multivaso gravemente calcificada, intervenidos por 6 lesiones tratadas con éxito mediante LC. Los 3 casos comparten características habituales en la población que hoy se deriva para intervencionismo: edad y clase funcional avanzada, alto riesgo quirúrgico, revascularización previa y alto riesgo de aterectomía rotacional (AR).
El balón de LC se empleó de forma eficaz en todas las lesiones y no hubo complicaciones intraprocedimiento, como disecciones o perforaciones.
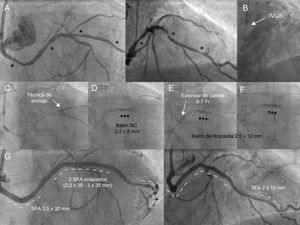
El paciente 1, de 73 años, tenía insuficiencia renal grave y portaba un bypass ileo-femoral bilateral. La EC de 3 vasos presentaba la particularidad de que la arteria circunfleja (CX) nacía del seno derecho y tenía 3 características adversas para el tratamiento percutáneo: calcificación, tortuosidad grave y enfermedad difusa distal (figura 1A, ). Se trató inicialmente la descendente anterior (DA) con balón de LC, seguido de stent farmacoactivo (SFA), y en el mismo procedimiento se trató la CX con un catéter multipropósito y 2 guías de trabajo. Tras un intento fallido de avanzar el catéter con ecocardiografía intravascular (figura 1B) y la falta de éxito con la técnica de anclaje en marginal (figura 1C), se dilató parcialmente la lesión media con balón no compliante (NC) de 2,5 mm (figura 1D) (). Esta maniobra permitió avanzar el extensor de catéter (6 en 7 Fr) y hacer llegar el balón de LC de 2,5 mm que trató y expandió la lesión tras 60 pulsos (figura 1E-F). Las lesiones proximal y media se trataron con balón de LC de 3 mm, y se implantaron 4 SFA (figura 1G y ).
A: CX calcificada y tortuosa con lesiones distal, medial y proximal (asterisco). B: el catéter de ultrasonidos no avanzó. C: la técnica de anclaje con balón en marginal no permitió avanzar el balón de LC. D: infraexpansión a nivel medio del balón NC de 2,5 mm, que permite avanzar el extensor de catéter y progresar el balón de LC (E). E: dilatación durante 40 pulsos, sin éxito. F: apertura de la lesión tras 60 pulsos. G: resultado final tras el implante de 4 SFA. CX: circunfleja; IVUS: ecocardiografía intravascular; LC: litoplastia coronaria; NC: no compliante; SFA: stent farmacoactivo.
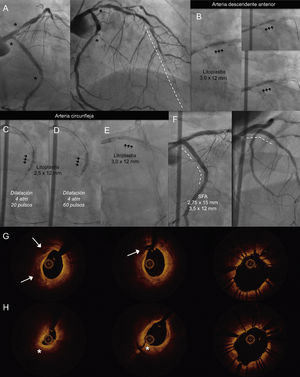
El paciente 2 es un varón de 63 años, diabético con EC de 3 vasos que en 2014 no era revascularizable quirúrgicamente por el mal lecho distal de la DA. Se trató inicialmente con AR sobre una CX dominante y se implantaron 3 SFA. En 2018, por angina refractaria, se realizó una coronariografía y se observaron lesiones calcificadas en la CX (ostial, y otra distal al stent) y en la DA, ostial (figura 2A y ). Se practicó la LC de dichas lesiones (figura 2B-E), con excelente resultado (figura 2F y ). En el estudio por tomografía de coherencia óptica, se observó en varios puntos la fractura de la placa en la íntima e incluso la media (figura 2G y H).
A: lesiones calcificadas en CX ostial y medio-distal y DA ostial (asterisco) con enfermedad difusa en el vaso distal de la DA (línea discontinua). Litoplastia coronaria con balón de 3 mm en la DA ostial (B) y en la CX medio-distal a 4 atm, 20 pulsos (C), 60 pulsos (D) y ostial (E). F: implante de 3 SFA, con buen resultado; imágenes de OCT previas a la LC; rotura de placa cálcica (flecha) y disección de placa fibrosa (asterisco). G y H: imágenes tras la LC y el implante de stent en la CX ostial (G) y medio-distal (H). CX: circunfleja; DA: descendente anterior; LC: litoplastia coronaria; OCT: tomografía de coherencia óptica; SFA: stent farmacoactivo.
La paciente 3, de 81 años, presentaba EC no tributaria de cirugía por enfermedad distal. Se trató en un primer tiempo la CD proximal con AR. En un segundo tiempo se trató el tronco común distal y la DA proximal-medial (). Se utilizó balón NC y balón de corte de 2 mm en la DA distal. La DA proximal y el tronco común distal se trataron con LC y 2 SFA solapados. El tronco común distal requirió posdilatación con balón de doble capa ().
De nuestra experiencia inicial, destacaríamos: a) seguridad y eficacia en casos no adecuados para AR; b) uso sencillo con guías de trabajo habituales y sin «curva de aprendizaje», y c) posibilidad de proteger los ramos laterales. Por contra, la LC debe mejorar el perfil de cruce, inferior a balones NC de última generación, y requiere al menos un catéter de 6 Fr. Los balones disponibles actualmente tienen una única longitud (12 mm) y diámetros desde 2,5 a 4 mm.
En conclusión, la LC permite el tratamiento de lesiones coronarias gravemente calcificadas de manera segura y eficaz y probablemente tendrá un papel fundamental en el arsenal para la modificación de la placa coronaria3.