La antiagregación desempeña un papel fundamental en el manejo del síndrome coronario agudo sin elevación del ST. Este tratamiento se enfrenta al difícil reto de disminuir la recurrencia de eventos isquémicos sin aumentar el riesgo de sangrado; con este fin, se han venido proponiendo múltiples protocolos de antiagregación y el desarrollo de nuevas terapias. En este artículo se presentan los principales antiagregantes actualmente disponibles para el tratamiento del síndrome coronario agudo sin elevación del ST y se revisa la evidencia científica más reciente.
Palabras clave
Las plaquetas desempeñan un papel fundamental en la aparición de eventos aterotrombóticos, tanto en pacientes con síndrome coronario agudo (SCA) como tras el intervencionismo coronario percutáneo (ICP)1, 2, 3, 4. La terapia antitrombótica en los últimos años ha crecido exponencialmente y han aparecido múltiples dianas y fármacos antiplaquetarios, evaluados tanto en el ámbito de los SCA con elevación del segmento ST (SCACEST) como en los SCA sin elevación (SCASEST)5. De hecho, este crecimiento y la mejora en el manejo de los pacientes con SCA están bien documentados en numerosos registros, como el recientemente publicado estudio DIOCLES, donde se evidencia un mayor uso de las nuevas terapias antiagregantes, crecimiento que podría ayudar a explicar en parte la tendencia a menor mortalidad objetivada en pacientes con SCASEST6,7.
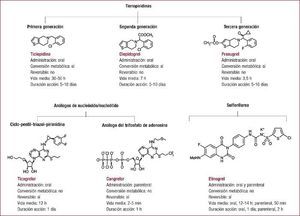
Los antiagregantes actualmente aprobados para el tratamiento del SCASEST actúan fundamentalmente mediante tres mecanismos: la inhibición de la ciclooxigenasa 1 (COX-1) con ácido acetilsalicílico (AAS), el antagonismo del receptor P2Y12 del difosfato de adenosina (ADP) (ticlopidina, clopidogrel, prasugrel, ticagrelor y cangrelor) o el bloqueo del receptor de la glucoproteína IIb/IIIa (abciximab, eptifibatida y tirofibán)8,9 (Figura). En este artículo se revisan las novedades y evidencias más recientes sobre el tratamiento antiagregante actualmente recomendado en el manejo del SCASEST (Tabla) y se discuten las posibilidades de los fármacos que todavía están en fase de experimentación clínica.
Figura. Mecanismos de acción de los principales agentes antiplaquetarios. Adaptado con permiso de Vivas et al 5 . AA: ácido araquidónico; AAS: ácido acetilsalicílico; AC: adenilatociclasa; ADP: difosfato de adenosina; AMPc: monofosfato cíclico de adenosina; ATP: trifosfato de adenosina; COX-1: ciclooxigenasa 1; FvW: factor de von Willebrand; Gp: glucoproteína; PAR: receptor activado por proteasas; TXA2: tromboxano A2; VASP: proteína estimulada por vasodilatadores.
Ensayos clínicos en que se basan las últimas recomendaciones sobre los antagonistas del receptor P2Y12 del difosfato de adenosina actualmente empleados en el SCASEST
| Población | Pauta del fármaco | Objetivo primario | Resultado | |
| Clopidogrel | ||||
| CURRENT/OASIS-7 10 | SCA | Dosis alta frente a dosis estándar | Muerte cardiovascular, infarto de miocardio o ictus a los 30 días | NS |
| GRAVITAS 11 | Angina estable o SCASEST con alta reactividad plaquetaria | Dosis alta frente a dosis estándar | Muerte cardiovascular, infarto de miocardio o trombosis del stent a los 6 meses | NS |
| Prasugrel | ||||
| TRITON TIMI-38 12 | SCA | Prasugrel frente a clopidogrel | Muerte cardiovascular, infarto de miocardio o ictus tras 6–15 meses de seguimiento | SCASEST: el 9,9% con prasugrel y el 12,1% con clopidogrel (HR = 0,82; p = 0,002) |
| ACCOAST 13 | SCASEST | Pretratamiento frente a poscoronariografía diagnóstica | Muerte cardiovascular, infarto de miocardio, ictus, revascularización urgente o tratamiento con inhibidores de la glucoproteína IIb/IIIa | NS |
| TRILOGY ACS 14 | SCASEST con manejo conservador | Prasugrel frente a clopidogrel | Muerte cardiovascular, infarto de miocardio o ictus hasta 30 meses de seguimiento | NS |
| Ticagrelor | ||||
| PLATO 15 | SCA | Ticagrelor frente a clopidogrel | Muerte cardiovascular, infarto de miocardio o ictus a los 12 meses de seguimiento | SCA: el 9,8% con ticagrelor y el 11,7% con clopidogrel (HR = 0,84; p = 0,0001) |
HR: hazard ratio; NS: diferencias estadísticamente no significativas; SCA: síndrome coronario agudo; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
El AAS fue el primer antiagregante empleado clínicamente16 y sigue siendo el primer antiagregante recomendado en el tratamiento de los pacientes con SCASEST5,6. La dosis óptima de mantenimiento (75–300 mg/día) tras un SCA sigue siendo un importante tema de debate17. En el estudio CURRENT/OASIS-710, la administración de una dosis diaria de AAS de 300 mg, comparado con 100 mg, no se asoció a una disminución en los eventos cardiovasculares. Por otra parte, los resultados del estudio PLATO18 en la subpoblación de pacientes estadounidenses indican que una dosis alta de AAS podría limitar los beneficios clínicos del tratamiento combinado con ticagrelor. Además, en cuanto a la seguridad, diversos estudios han evidenciado una relación dependiente de la dosis entre el riesgo de hemorragias gastrointestinales y la dosis de AAS empleada19. Por último, hay que mencionar que en ocasiones se ha descrito la existencia de una pobre respuesta o «resistencia» al AAS que se ha relacionado con problemas de adherencia terapéutica, interacciones farmacológicas (p. ej., con los antiinflamatorios no esteroideos [AINE]), estados inflamatorios o la presencia de polimorfismos genéticos de la COX-120,21, pero que no se ha podido relacionar de forma convincente con un mayor riesgo de eventos clínicos.
Novedades en clopidogrelEl clopidogrel es una tienopiridina de segunda generación, un profármaco que, una vez activado por el metabolismo hepático, inhibe selectiva e irreversiblemente el receptor plaquetario P2Y1222. A pesar de los indiscutibles beneficios aportados por la introducción de la doble antiagregación con AAS y clopidogrel en el manejo del SCASEST23, numerosos estudios muestran la existencia de una considerable proporción de pacientes que quedan con una inhibición plaquetaria escasa tras la doble antiagregación24. Hay múltiples factores, genéticos y clínicos, que pueden explicar la variabilidad interindividual del efecto antiagregante del clopidogrel24,25. Con idea de reducir esta variabilidad, el ensayo CURRENT/OASIS-7 valoró la eficacia de una dosis de clopidogrel alta (dosis de carga de 600 mg, seguida de 150 mg diarios la primera semana y luego 75 mg diarios) comparada con la dosis estándar (carga de 300 mg seguida de 75 mg diarios) en pacientes con SCA y estrategia de revascularización precoz. En la población general del estudio (SCASEST en el 70,8%), no se observaron diferencias en la eficacia de esta pauta; sin embargo, en el grupo de pacientes en los que se procedió a ICP (el 69% del estudio), el tratamiento con dosis más altas de clopidogrel redujo los eventos isquémicos (combinación de muerte cardiovascular, infarto de miocardio e ictus) a los 30 días (el 3,9 frente al 4,5%; hazard ratio [HR] ajustada = 0,86; p = 0,039) y también la trombosis del stent (el 0,7 frente al 1,3%; HR = 0,54; p = 0,0001). El análisis de seguridad en este subgrupo evidenció un aumento significativo de los sagrados mayores, definidos por criterios CURRENT (el 1,6 frente al 1,1%; HR = 1,41; p = 0,009), aunque sin diferencia significativa en sangrados intracraneales, sangrados mortales, sangrados relacionados con cirugía de revascularización y sangrados mayores según los criterios TIMI10. Considerando estos resultados, esta dosis alta de clopidogrel no está recomendada actualmente; además, no se ha logrado reproducir en otros estudios los resultados del ensayo CURRENT. En concreto, el estudio GRAVITAS11 encontró que, en pacientes con reactividad plaquetaria residual alta, duplicar la dosis de mantenimiento de clopidogrel no reduce el riesgo de eventos isquémicos después del ICP.
Por otro lado, el riesgo de neutropenia del clopidogrel comparado con la ticlopidina es mucho menor, aunque sigue presente26. Finalmente, es importante reseñar que, aunque han aparecido nuevos antiagregantes más potentes, el clopidogrel sigue siendo la opción terapéutica favorita en casos con alto riesgo de sangrado, como pueden ser los pacientes en tratamiento con anticoagulantes orales4. Dado su efecto irreversible en las plaquetas, en caso de cirugía se recomienda interrumpirlo 5–7 días antes27.
Novedades en prasugrelEl prasugrel es una tienopiridina de tercera generación. Presenta un inicio de acción más rápido y menos variabilidad interindividual que el clopidogrel y consigue mayor inhibición plaquetaria28. El TRITON-TIMI 3812 es el estudio que validó la eficacia clínica y la seguridad del tratamiento con prasugrel (60 mg de dosis de carga, seguida de 10 mg/día de mantenimiento) comparado con clopidogrel (300 mg de dosis de carga, seguida de 75 mg/día de mantenimiento). En este estudio se incluyó a 13.608 pacientes con SCA de riesgo intermedio-alto candidatos a revascularización percutánea, de los que el 74% tenían SCASEST. Resultó en una reducción significativa del objetivo primario (combinación de muerte cardiovascular, infarto del miocardio e ictus no mortal) a favor del prasugrel (el 9,9 y el 12,1%; HR = 0,82; p = 0,002). Lo que más incidió en las diferencias halladas en la cohorte general fueron las tasas de infartos de miocardio no mortales (el 7,3% con prasugrel y el 9,5% con clopidogrel; HR = 0,76; p = 0,001); las tasas de muertes cardiovasculares y los ictus resultaron sin diferencias significativas. Además, destacó una significativa reducción de la tasa de trombosis del stent (el 1,1 frente al 2,4%; HR = 0,48; p = 0,001), tanto tempranas como tardías e independiente de que el stent tuviera recubrimiento farmacoactivo o no29. Por otra parte, la mayor eficacia antiplaquetaria del prasugrel resultó en un riesgo aumentado de sangrados mayores (criterio TIMI) no relacionados con la cirugía de revascularización coronaria (el 2,4 y el 1,8%; HR = 1,32; p = 0,03). De todas formas, el beneficio clínico neto del prasugrel fue superior al del clopidogrel (el 12,2 frente al 13,9%; HR = 0,87; p = 0,0004), fue nulo en los subgrupos de pacientes de edad avanzada (> 75 años) y bajo peso (< 60 kg), mientras que en pacientes con antecedentes de ictus o accidente isquémico cerebral transitorio, el prasugrel mostró peores resultados que el clopidogrel30. Por otra parte, es de destacar que, en el subgrupo de pacientes con diabetes mellitus, el beneficio clínico del prasugrel no se acompañó de aumento del riesgo hemorrágico31.
Dado que en el estudio TRITON-TIMI 38 se incluyó a pacientes con SCASEST candidatos a ICP y, por lo tanto, la administración de clopidogrel o prasugrel se realizó en el laboratorio de hemodinámica una vez conocida la anatomía coronaria, se diseñó otro estudio que valorara el efecto de iniciar el tratamiento con prasugrel antes o después de la coronariografía diagnóstica. Así, el estudio ACCOAST13 aleatorizó a 4.033 pacientes con un SCASEST de alto riesgo candidatos a estrategia invasiva con coronariografía y eventualmente revascularización en las siguientes 48 h a recibir prasugrel (dosis de carga, 30 mg) o placebo. Una vez conocida la anatomía coronaria e indicada la angioplastia, se completó la carga de prasugrel con otros 30 mg en el grupo de pretratamiento con prasugrel y se administró la carga completa de 60 mg a los pacientes del grupo control. El inicio precoz del tratamiento con prasugrel no aportó beneficio al riesgo de muerte cardiovascular, infarto de miocardio, ictus, revascularización urgente o necesidad de tratamiento de rescate con inhibidores de la glucoproteína IIb/IIIa (el 10% con pretratamiento y el 9,8% en el grupo control; HR = 1,02; p = 0,81). Sin embargo, sí se objetivó un incremento en la tasa de sangrados mayores (el 2,6 frente al 1,4% según criterios TIMI; HR = 1,9; p = 0,006), aunque no en sangrados mortales o hemorragias intracraneales. Tras estos resultados, el pretratamiento con prasugrel sin conocer la anatomía coronaria queda relegado a pacientes con SCACEST que van a ser tratados con angioplastia primaria.
Otro de los puntos que quedaron sin aclarar en el estudio TRITON-TIMI 38 es el posible beneficio de administrar prasugrel a pacientes tratados de manera conservadora (no invasiva). El estudio TRILOGY-ACS14 se diseñó para evaluar el tratamiento con prasugrel comparado con clopidogrel en pacientes con un SCASEST de alto riesgo tratados de manera conservadora. En ese estudio, los pacientes aleatorizados en las primeras 72 h de evolución de un SCASEST recibieron una dosis de carga de 30 mg de prasugrel seguida de una dosis de mantenimiento de 10 o 5 mg de prasugrel en función de si el paciente era menor o mayor de 75 años, respectivamente, comparado con 300 mg de clopidogrel seguidos de 75 mg diarios. Los pacientes incluidos a partir de las 72 h de inicio del SCA debían tener tratamiento previo con clopidogrel, y no se administraba la dosis de carga (únicamente la de mantenimiento). En este estudio, se aleatorizó a 9.326 pacientes (7.243 menores de 75 años) y el prasugrel no demostró una reducción en la recurrencia de eventos isquémicos en menores de 75 años (el 13,9% en el grupo de prasugrel y el 16,0% en el de clopidogrel; HR = 0,91; p = 0,21) ni tampoco un riesgo aumentado de sangrados mayores. Estos resultados neutros se mantuvieron en la población total, independientemente de la edad. Con los resultados de este estudio, no se puede recomendar el prasugrel como antiagregante para los pacientes con SCASEST tratados de manera conservadora4. Por otro lado, se recomienda suspender el prasugrel al menos 7 días antes de proceder a una cirugía de revascularización miocárdica27.
Novedades en ticagrelorEl ticagrelor pertenece a una nueva clase de inhibidores directos e irreversibles del receptor P2Y12. Comparándolo con el clopidogrel, destaca por su rapidez de inicio de acción y la fuerte inhibición plaquetaria32. El estudio PLATO15 ha valorado los efectos del ticagrelor (180 mg de dosis de carga, seguida de 90 mg/12 h) comparado con clopidogrel (300 o 600 mg de dosis de carga, seguida de 75 mg/día) en la prevención de eventos cardiovasculares en 18.624 pacientes con SCA. Comparado con el estudio TRITON-TIMI 38, el diseño del estudio PLATO reproduce mejor la práctica clínica habitual de administrar la doble antiagregación en el momento del diagnóstico clínico, sin esperar a la coronariografía diagnóstica. Además, se podía incluir en el ensayo a los pacientes previamente tratados con clopidogrel. A los 12 meses de seguimiento en el estudio PLATO, el objetivo primario (muerte cardiovascular, infarto de miocardio o ictus no mortal) resultó significativamente menor en el grupo de ticagrelor (el 9,8 y el 11,7%; HR = 0,84; p = 0,0001), por una reducción tanto de las muertes cardiovasculares (el 4 y el 5,1%; HR = 0,79; p = 0,001) como de los infartos de miocardio (el 5,8 y el 6,9%; HR = 0,84; p = 0,005)32.
Este beneficio del ticagrelor sobre el clopidogrel se observó en los distintos subgrupos analizados, independientemente de la edad33, en los pacientes con SCASEST tratados, ya fuera con estrategia conservadora o invasiva34,35, y hasta en los derivados a cirugía de revascularización coronaria36. Aunque no se encontraron diferencias en los objetivos de seguridad primarios según los criterios TIMI y PLATO de sangrado mayor no relacionados con la cirugía de revascularización, la mayor potencia antiplaquetaria del ticagrelor se acompañó de una mayor tasa de sangrados (HR = 1,25 y HR = 1,19 respectivamente), entre los cuales destaca un pequeño número, pero mayor que con clopidogrel, de hemorragias intracraneales mortales (el 0,1 y el 0,01%; p = 0,02) sin que el antecedente de ictus isquémico fuese un factor de riesgo de este evento32.
Por otro lado, durante la primera semana de tratamiento, se observó una mayor prevalencia de pausas ventriculares en el grupo tratado con ticagrelor, sin que este dato llegara a correlacionarse con eventos clínicos significativos37. Otro efecto adverso del ticagrelor fue la disnea, que en un pequeño número de casos llegó a ser razón para suspender la medicación38. Finalmente, hay que destacar que, al igual que los demás antiagregantes, el ticagrelor está contraindicado para pacientes con antecedentes de ictus hemorrágico o con hepatopatía grave, y las guías de práctica clínica recomiendan suspenderlo al menos 5 días antes de proceder a cirugía de revascularización27 (según ficha técnica, 7 días).
Novedades en inhibidores intravenososInhibidores de la glucoproteína IIb/IIIaEl uso prolongado de inhibidores de la glucoproteína IIb/IIIa por vía oral para la prevención secundaria tras un SCA se ha relacionado con un aumento de la mortalidad39, por lo que actualmente su uso está restringido a la vía intravenosa. Los fármacos intravenosos aprobados para el uso clínico son abciximab, tirofibán y eptifibatida. Los tres son potentes fármacos antiagregantes que destacan tanto por su rápido inicio de acción como por su corto tiempo de aclaramiento. Antes de comentar la evidencia relativa a estos fármacos, vale la pena recordar que la mayoría de los estudios clínicos sobre ellos se realizaron en una era en la que el uso de la doble antiagregación y la estrategia invasiva precoz no estaban tan establecidos como en la actualidad. En ese contexto, el tirofibán comparado con placebo redujo la mortalidad a los 30 días40; sin embargo, su uso generalizado añadido a las estrategias de tratamiento actual no está validado. Por otra parte, el uso de abciximab en pacientes con SCASEST de riesgo bajo-intermedio programados para coronariografía y pretratados con clopidogrel no aportó beneficios significativos41, mientras que su administración en los SCASEST de alto riesgo con estrategia de revascularización invasiva disminuyó los eventos cardiovasculares42. En cuanto a los tiempos de administración, se ha evidenciado que la pauta de eptifibatida previa a la angiografía no aporta beneficios con respecto a la administración posterior43. Finalmente, de los tres se ha demostrado que aumentan el riesgo de sangrado44 y pueden producir trombocitopenia40,45.
Actualmente, el empleo de estos fármacos en el SCASEST queda esencialmente restringido a situaciones concretas durante la ICP, como lesiones con alta carga trombótica, reoclusiones del stent o fenómenos de no-reflow, siempre y cuando el riesgo hemorrágico no resulte elevado. Otra indicación puede ser el tratamiento puente en un paciente con stent recientemente implantado que requiera intervención quirúrgica27.
CangrelorEl cangrelor es un inhibidor del receptor del ADP P2Y12 de administración intravenosa que, por su inicio de acción inmediato y su vida media muy corta, se presenta como una opción terapéutica prometedora46. Sin embargo, los estudios CHAMPION-PCI y PLATFORM, pese a documentar una reducción significativa de los infartos periprocedimiento y de las trombosis del stent sin que aumentara el riesgo de sangrados mayores47, no consiguieron demostrar la superioridad del cangrelor frente al clopidogrel solo en los objetivos primarios del estudio48. Se ha especulado que estos resultados podrían estar limitados por la definición de infarto usada como objetivo primario en estos estudios. Se realizó entonces el estudio CHAMPION-PHOENIX que, al incluir la trombosis del stent y los infartos periprocedimiento en la composición del objetivo primario, pretendió demostrar la superioridad del cangrelor frente al clopidogrel solo a las 48 h de inicio del tratamiento (el 4,7 frente al 5,9%; HR = 0,78; p = 0,005) sin empeorar la seguridad del paciente49. No obstante, las críticas al diseño de este estudio han limitado la aceptación del fármaco en la práctica clínica habitual. En concreto, la dosis utilizada de clopidogrel fue mayor en el grupo tratado con cangrelor, hecho que puede haber influido significativamente en los eventos isquémicos periprocedimiento. Y, además, cabe destacar que los SCASEST representaron únicamente un cuarto de la población general del estudio, por lo que los resultados generales son poco extrapolables a este contexto clínico50.
Un escenario prometedor para el uso de cangrelor puede ser de nuevo el tratamiento antiplaquetario puente para pacientes con estrategia de cirugía de revascularización o que necesitan cualquier otra cirugía por la que sea preciso suspender la doble antiagregación oral51.
Novedades en inhibidores del receptor de la trombinaEl receptor activado por proteasas 1 (PAR-1) es el principal receptor plaquetario de trombina. Su activación desempeña un papel importante en la respuesta plaquetaria que aparece en situaciones patológicas, sin intervenir en la activación plaquetaria que acompaña a la hemostasia fisiológica. Por lo tanto, desde un punto de vista experimental, su inhibición podría reducir los eventos isquémicos sin aumentar el riesgo de sangrados mayores52. Actualmente se dispone de evidencia clínica con dos inhibidores orales de PAR-1: vorapaxar y atopaxar.
En el estudio TRACER se valoró la eficacia del vorapaxar (40 mg de dosis de carga y 2,5 mg/día de mantenimiento) como tratamiento añadido a la doble antiagregación estándar para pacientes con SCASEST. La reducción del objetivo primario combinado (muerte cardiovascular, infarto del miocardio, ictus, isquemia recurrente con rehospitalización o revascularización urgente) no alcanzó la significación estadística (el 18,5 frente al 19,9%; HR = 0,92; p = 0,07) y, contra lo que se pensaba, en el seguimiento se evidenció un aumento de los sangrados mayores con vorapaxar (el 7,2 frente al 5,2%; HR = 1,35; p < 0,001), incluidas las hemorragias intracraneales53. En análisis posteriores se ha comprobado que los pacientes con mayor riesgo de hemorragia intracraneal eran aquellos con antecedente de ictus54.
En un ensayo clínico de fase II, el atopaxar no evidenció un riesgo aumentado de sangrados en pacientes con enfermedad coronaria estable55; sin embargo, no disponemos de datos concluyentes sobre su eficacia y su seguridad en el tratamiento del SCASEST.
Otras terapias en estudioEl cilostazol es un inhibidor de la fosfodiesterasa 3 con efecto antiplaquetarario y vasodilatador, aprobado para el tratamiento sintomático de los pacientes con vasculopatía periférica56. Su administración a pacientes con SCASEST tratados mediante revascularización percutánea, añadido a la doble antiagregación estándar con AAS y clopidogrel, ha mostrado incrementos significativos de la inhibición plaquetaria, pero el pequeño tamaño muestral del estudio no permite sacar conclusiones sobre la eficacia clínica y la seguridad de este fármaco57,58.
El elinogrel es un inhibidor directo y reversible del receptor P2Y12, disponible para vías oral e intravenosa; actualmente se encuentra en fase de estudio en el manejo del SCACEST y el ICP59. Finalmente, existen otros fármacos todavía sin evidencias clínicas, como el egaptivon-pegol, un inhibidor de la glucoproteína plaquetaria 1b implicada en la activación mediada por el factor de von Willebrand, o el sarpogrelato, un antagonista del receptor plaquetario serotonina-2A que inhibe la agregación plaquetaria.
ConclusionesLa aparición de nuevos antiagregantes más potentes y con inicio de acción más rápido ha supuesto una mejora en el manejo de los pacientes con SCASEST. Sin embargo, a pesar de los logros clínicos conseguidos, cabe destacar que a la investigación clínica y farmacológica aún le quedan amplios márgenes de desarrollo para alcanzar el mejor perfil de eficacia y seguridad para los pacientes.
Conflicto de interesesNinguno.
Autor para correspondencia: Servicio de Cardiología, Instituto Cardiovascular, Hospital Clínico San Carlos, Prof. Martín Lagos s/n, 28040 Madrid, España. antonio.fernandezortiz@salud.madrid.org