La telemedicina permite la prestación de atención médica a distancia mediante tecnologías de la información y la comunicación, que hacen posible el envío de datos, la participación del paciente, la promoción de hábitos cardiosaludables, el diagnóstico, la detección precoz de las descompensaciones agudas, la monitorización y el seguimiento de las enfermedades cardiovasculares. Los dispositivos portátiles tienen múltiples aplicaciones clínicas, que van desde la detección de arritmias hasta el control a distancia de enfermedades crónicas o los factores de riesgo. Será necesario un enfoque multidisciplinario para integrar de manera efectiva y segura estas tecnologías a nuestra práctica clínica habitual. Los avances tecnológicos y la gestión de los datos conllevarán un incremento de las estrategias de telemonitorización, que permitirán mayores accesibilidad y equidad, así como una atención sanitaria más eficiente y precisa de los pacientes. Todavía quedan cuestiones no resueltas, como la infraestructura tecnológica más adecuada, la integración de estos datos en la historia clínica y la brecha digital que puede dificultar al paciente la adopción de la atención a distancia. En este artículo se ofrece una visión general actualizada de las herramientas digitales para un mejor abordaje de la fibrilación auricular, la insuficiencia cardiaca, los factores de riesgo y la adherencia al tratamiento.
Palabras clave
La enfermedad cardiovascular es una de las principales causas de morbilidad y mortalidad en el mundo y el exponente principal de las enfermedades crónicas. El tradicional seguimiento presencial presenta inconvenientes como las barreras geográficas, inconvenientes logísticos, costes económicos, de acceso y de tiempo y suponen una gran sobrecarga del sistema de salud. El progresivo envejecimiento de la población y la mayor prevalencia de factores de riesgo y de enfermedad cardiovascular agravan esta situación.
Además, y pese a disponerse de tratamientos efectivos basados en evidencia científica contrastada, los beneficios a largo plazo en la vida real no son los obtenidos en los ensayos clínicos, posiblemente debido a la falta de adherencia.
Desde hace unos años, estamos inmersos en una revolución digital y la reciente pandemia de COVID-19ha acelerado la utilización de la telemedicina y la eHealth, eSalud o salud digital, dado que los profesionales sanitarios nos vimos obligados a limitar las visitas presenciales. La telemedicina, como forma de prestación de servicios médicos que utiliza tecnologías de la información y la comunicación para brindar atención médica a distancia, permite a los profesionales de la salud evaluar, diagnosticar y tratar a los pacientes sin que sea necesario un encuentro presencial.
La atención sanitaria basada en telemedicina y dispositivos portátiles que integran toda la información brinda la oportunidad de rediseñar y mejorar la asistencia de los pacientes con enfermedades cardiovasculares. No obstante, dichas herramientas deben estar reguladas por las autoridades competentes, ya que son dispositivos de uso médico.
Se ofrece una visión general actualizada de las herramientas digitales para un mejor abordaje de las arritmias, la insuficiencia cardiaca y los factores de riesgo cardiovascular, así como unas recomendaciones personales de los autores basadas en la evidencia actual.
HERRAMIENTAS PARA LA DETECCIÓN Y MONITORIZACIÓN DE ARRITMIASHerramientas digitales para la detección de arritmiasLa detección temprana de arritmias permite implementar intervenciones invasivas o farmacológicas apropiadas, y en algunos casos reducir la morbimortalidad1. Para ello, el electrocardiograma (ECG) de 12 derivaciones sigue siendo el estándar en el diagnóstico de cualquier arritmia. Sin embargo, el acceso a un ECG puede estar limitado o resultar inútil para el diagnóstico de arritmias paroxísticas si se realiza entre episodios. La utilidad de otros métodos tradicionales de cribado, como el Holter ambulatorio, se ve limitada por su disponibilidad y un tiempo de monitorización relativamente corto. Los registradores de eventos implantables superan este obstáculo, pero su alto coste inicial limita su uso2. Impulsado por la pandemia de COVID-19, el desarrollo de dispositivos digitales para la detección y la monitorización de arritmias cardiacas ha experimentado un importante auge. Aunque muchos profesionales integran ya estos dispositivos en su práctica clínica, aún preocupan su precisión, su utilidad y su integración a los algoritmos de tratamiento3. La European Heart Rhythm Association ha publicado recientemente un documento para guiar la implementación de estas tecnologías3. Aunque presentan múltiples ventajas, requieren que el clínico esté familiarizado con la adquisición y la interpretación de las señales y con sus limitaciones.
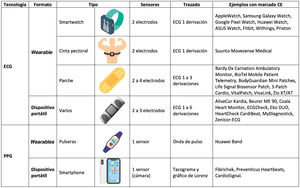
Esencialmente, estos dispositivos pueden dividirse según su tecnología en los que emplean señales electrocardiográficas y los que se sirven de señales no electrocardiográficas, entre las que destaca la fotopletismografía. A su vez, esta tecnología puede emplearse en wearables (dispositivos que el usuario lleva a modo de prenda o complemento), entre los que están relojes inteligentes, parches, textiles y otros, o en dispositivos portátiles, como los teléfonos inteligentes y dispositivos dedicados (figura 1).
La precisión diagnóstica de estos dispositivos dependerá del algoritmo utilizado, la población que lo emplee, las condiciones en que el registro se lleva a cabo y la interpretación profesional de los trazados. La recomendación de su uso debería basarse en la frecuencia de los síntomas, el tiempo de monitorización deseado, la infraestructura del centro, la competencia digital del paciente y sus preferencias personales.
Dispositivos basados en señales electrocardiográficasEstos dispositivos emplean electrodos para obtener trazados electrocardiográficos que un profesional sanitario capacitado puede analizar e interpretar directamente, lo que permite el diagnóstico directo de arritmias cardiacas.
Existen innumerables dispositivos comercializados, muchos con estudios clínicos de validación, fundamentalmente para la detección de fibrilación auricular (FA), y algunos con marcado CE. Entre los wearables, destacan por su popularidad los relojes inteligentes, que utilizan electrodos incorporados en la caja o en la corona del reloj para obtener ECG de 1 derivación que puede revisarse en la propia pantalla o almacenarse en aplicaciones móviles (figura 2A). También existen parches, dispositivos adhesivos sencillos de usar y resistentes al agua, que han demostrado una alta rentabilidad diagnóstica y cuya limitación principal es la duración de la batería, el componente adhesivo (aunque los hay reutilizables) y las bandas pectorales. Existen también infinidad de dispositivos portátiles, la mayoría proporciona trazados de 1 derivación (normalmente DI), aunque algunos permiten obtener hasta 6 derivaciones (figura 2B).
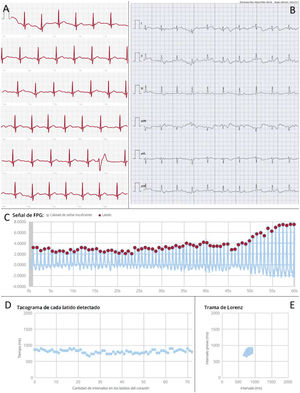
Ejemplos de registros de ritmo proporcionados por dispositivos digitales. A: registro de ECG de 1 derivación obtenido mediante reloj inteligente Apple Watch (Apple, Estados Unidos) en un paciente con ritmo sinusal y un extrasístole ventricular. B: registro de ECG de 6 derivaciones obtenido mediante dispositivo dedicado Kardia Mobile 6L, (AliveCor, Estados Unidos) en un paciente en ritmo sinusal. C: señal fotopletismográfica obtenida mediante teléfono inteligente y procesada con la aplicación FibriCheck (Corda Campus, Bélgica) que muestra la intensidad de la señal fotopletismográfica de cada latido a lo largo de 1 min en un paciente en ritmo sinusal. D: tacograma derivado de la señal fotopletismográfica previa que muestra la duración del intervalo R-R de cada latido. E: gráfico de Poincaré derivado de la señal fotopletismográfica anterior que muestra la aleatoriedad del ritmo cardiaco representando el intervalo R-R de cada latido respecto del latido previo. F: señal fotopletismográfica, tacograma y gráfico de Poincaré obtenido con la misma app en un paciente con fibrilación auricular. Nótese la irregularidad en la intensidad de la señal fotopletismográfica e intervalo R-R de cada latido y la dispersión de puntos en el gráfico de Poincaré como manifestación de la aleatoriedad del ritmo. FPG: fotopletismografía.
Entre las tecnologías no electrocardiográficas destaca la fotopletismografía, una técnica óptica que emplea una fuente de luz y un sensor capaces de detectar las variaciones en el volumen sanguíneo de una superficie cutánea a través de cambios en la intensidad de la luz reflejada, lo que permite la monitorización del ritmo cardiaco a través del pulso periférico. La información de la onda de pulso se analiza por algoritmos integrados capaces de detectar un pulso anormal y emitir un aviso al paciente ante la sospecha de FA. Sin embargo, para el diagnóstico definitivo de la arritmia, se necesita un registro electrocardiográfico posterior que confirme el hallazgo. Algunos dispositivos permiten el análisis de los datos en bruto (figura 2C), así como su representación gráfica a través de un tacograma (figura 2D), que muestra la frecuencia cardiaca para cada latido, y un gráfico de Poincaré (figura 2E), que muestra el intervalo R-R de cada latido frente al latido previo. Algunas representaciones gráficas pueden orientar hacia la existencia de arritmias concretas distintas de la FA4.
Aunque la fotopletismografía está presente en dispositivos médicos habitualmente utilizados para la medición de la frecuencia cardiaca y la saturación de oxígeno, su uso en todo tipo de wearables (pulseras, brazaletes, bandas pectorales, anillos, auriculares) y dispositivos portátiles (fundamentalmente teléfonos inteligentes, que usan el flash como fuente de luz y la cámara como sensor) proporcionan una herramienta asequible y cómoda, dada su ubicuidad, para la detección de arritmias de todo tipo.
Existen otras tecnologías no basadas en señales electrocardiográficas, como la mecanocardiografía, que emplea sensores de movimiento (como el acelerómetro o el giroscopio, presentes también en teléfonos inteligentes) para detectar la actividad mecánica cardiaca, o la fotopletismografía sin contacto (denominada también videopletismografía o fotopletismografía de imagen), basada en el análisis de señales pulsátiles corporales detectadas por vídeo, entre otras.
CRIBADO DE FIBRILACIÓN AURICULARLa European Heart Rhythm Association recomienda realizar un cribado sistemático de FA en pacientes con ictus, mayores de 75 años o mayores de 65 años con comorbilidad, y oportunístico en mayores de 65 años sin comorbilidad o menores con comorbilidad5. Para ello, se prefieren los dispositivos basados en ECG o en fotopletismografía a la toma de pulso, ya que esta última tecnología ha demostrado un valor predictivo positivo elevado para el diagnóstico de FA en grandes estudios poblacionales6,7. En menores de 65 años sanos no se recomienda el cribado, aunque los dispositivos digitales portátiles podrían ser de utilidad en pacientes con síntomas compatibles con la FA.
HERRAMIENTAS DIGITALES PARA LA MONITORIZACIÓN Y EL SEGUIMIENTO DE PACIENTES CON ARRITMIASMás allá de la detección de arritmias, las herramientas digitales descritas han demostrado utilidad en pacientes con diagnóstico de FA establecido, tanto para la monitorización de la frecuencia cardiaca (que permite el ajuste telemático de fármacos frenadores) como para la monitorización del ritmo de pacientes en los que se persigue mantener el ritmo sinusal. En esta situación, su uso podría facilitar la aplicación de una estrategia wait-and-see (tratamiento ambulatorio con cardioversión diferida) para los pacientes que acuden a urgencias con FA de reciente diagnóstico, pues permite detectar qué pacientes precisarían finalmente una cardioversión por ausencia de conversión espontánea a ritmo sinusal8 y mejorar el seguimiento de pacientes sometidos a ablación con una monitorización prolongada que incrementaría la detección de recurrencias frente a una estrategia convencional basada en ECG en consulta o monitorización con Holter de corta duración9.
Por último, las herramientas digitales basadas en plataformas y aplicaciones móviles pueden ser de utilidad en el tratamiento integral del paciente con FA, pues permiten optimizar la anticoagulación, facilitan la toma de decisiones en el tratamiento de síntomas y mejoran el control de otros factores de riesgo y comorbilidades a través de la formación y la incentivación de hábitos de vida saludable, lo que tiene un demostrado impacto en la aparición de eventos clínicos (tromboembólicos, hemorrágicos, recurrencias de FA, síntomas, hospitalizaciones e insuficiencia cardiaca)10.
Consideraciones de los autoresLos autores consideran que sería recomendable el uso de dispositivos digitales para el cribado de FA en personas con indicación de anticoagulación (mayores de 65 años o con comorbilidades) y que podrían ser útiles en pacientes con diagnóstico de FA establecido para la monitorización de la frecuencia cardiaca y el ritmo, así como para el abordaje integral con un objetivo de reducción de eventos clínicos. Por último, aunque con mucha menos evidencia, los autores consideramos que podría recomendarse el uso de dispositivos digitales, especialmente basados en ECG, para el diagnóstico de arritmias paroxísticas en pacientes con síntomas compatibles, sobre todo si son infrecuentes o de corta duración.
HERRAMIENTAS PARA EL SEGUIMIENTO DE LOS PACIENTES CON INSUFICIENCIA CARDIACALa mayor parte de los costes del abordaje de la insuficiencia cardiaca (IC) comprenden visitas de pacientes ambulatorios a urgencias y hospitalizaciones11. Hasta el 40% de los pacientes con IC tienen al menos 4 hospitalizaciones durante la duración de su enfermedad, y cada una de ellas incrementa el riesgo de mortalidad11. Uno de los factores que contribuyen a las hospitalizaciones repetidas es la baja adherencia del paciente a los tratamientos farmacológicos recomendados —sobre todo a los cambios en el estilo de vida—, que suele disminuir a lo largo del tiempo tras la hospitalización12.
Por otro lado, en muchas ocasiones el paciente no es capaz de identificar los signos y síntomas precoces del empeoramiento, por lo que solicita atención tarde y el pronóstico se ve afectado.
En los últimos años, se ha invertido un gran esfuerzo en métodos de telemedicina en IC, con innumerables ventajas (tabla 1), ya que facilitan la adherencia del paciente, predicen y evitan episodios de empeoramiento de la IC y permiten un seguimiento más estrecho sin necesidad de acudir a los centros sanitarios.
Ventajas de la telemedicina en la insuficiencia cardiaca
| • Mejora del acceso a la atención especializada, especialmente en zonas rurales o con escasez de recursos humanos o materiales |
| • Optimización del seguimiento clínico y el ajuste terapéutico mediante el uso de dispositivos que permiten monitorizar parámetros como el peso, la presión arterial, la frecuencia cardiaca o el oxígeno en sangre, así como recoger información sobre los síntomas y la adherencia al tratamiento |
| • Prevención y detección precoz de las descompensaciones agudas |
| • Formación sanitaria y empoderamiento del paciente mediante programas que fomentan el autocuidado, el conocimiento de la enfermedad y el manejo de los factores de riesgo |
| • Reducción de los costes sanitarios asociados a la insuficiencia cardiaca, al disminuir las visitas presenciales innecesarias, las consultas a urgencias, los ingresos hospitalarios y la mortalidad |
Una parte de esta telemedicina es la telemonitorización (TM), que permite a los pacientes el envío a distancia de sus datos de salud, principalmente datos sobre los síntomas, peso, frecuencia cardiaca y presión arterial almacenados en dispositivos electrónicos que se utilizan para ajustar su tratamiento (directamente o a través de un profesional sanitario) o pedir consejo médico. La TM domiciliaria puede ayudar a mantener o mejorar la calidad de la atención, facilitar el rápido acceso a la atención médica cuando sea necesario, reducir los gastos de desplazamiento de los pacientes y minimizar la frecuencia de las consultas13. La interrupción forzosa de consultas presenciales en numerosos países debido a la pandemia de COVID-19ha destacado las ventajas potenciales de la TM domiciliaria14.
Los estudios sobre TM domiciliaria en IC para predecir descompensaciones presentan resultados muy variados, ya que una de las limitaciones es que la adherencia a las mediciones no suele ser completa y los algoritmos para su detección no son del todo precisos. Sin embargo, los sistemas dirigidos a optimizar el tratamiento y mejorar la adherencia tienen la ventaja de que solo necesitan estar dotados de personal durante la jornada laboral estándar; sin embargo, los que ofrecen una ayuda requieren más recursos.
No está clara la eficacia comparativa ni la relación coste-eficacia de cada una de estas estrategias. No obstante, parece que los sistemas centrados en la optimización continua de la atención (enfoque de mantenimiento de la salud) son más efectivos que los sistemas que intentan anticiparse y tratar episodios de descompensación, ya que esta última estrategia puede presentar falsos positivos y, por lo tanto, generar un consumo de recursos con alarmas innecesarias que podrían desmotivar al personal sanitario15. Quizá con el desarrollo de algoritmos de inteligencia artificial que incluyan datos a gran escala de muchos ámbitos de la vida del paciente (big data) se podrían refinar dichas alertas haciéndolas más precisas. Además, no se puede olvidar que los sistemas de TM se pueden utilizar como métodos eficientes para formar y motivar al paciente, pero unos de los problemas aun sin resolver en nuestro sistema sanitario es que dichos sistemas se deben adaptar e integrar con los servicios de salud existentes16.
Una revisión Cochrane de 2017, en la que se identificaron 39 estudios importantes sobre TM domiciliaria en IC basados en la evaluación de síntomas, peso, frecuencia, ritmo cardiaco y presión arterial, mostró que la TM se asoció con una reducción del 20% de la mortalidad por cualquier causa y del 37% de la hospitalización por IC17. Desde entonces, se han publicado varios estudios que no obtuvieron resultados significativos y uno con resultados positivos15,18–20. Es posible que la heterogeneidad de los estudios (unicéntricos frente a muticéntricos) y que no se haya identificado una estrategia de TM estándar para todas las unidades clínicas ni para todos los grupos de pacientes pudieran penalizar los resultados.
El estudio alemán TIM-HF220, con 1.571 pacientes con IC crónica e ingreso hospitalario previo, asignados al azar a recibir atención habitual más TM diaria o solo atención habitual durante 12 meses, mostró que el grupo con TM tuvo un 21% de menos días hospitalizados por causas cardiovasculares (17 frente a 22 días cada 100 pacientes-año) y un 36% de menos de muertes por cualquier causa (4 frente a 7 muertes/100 pacientes-año) que el grupo sin TM (ambos, p <0,001). En el estudio español iCOR21 aleatorizó a 178 pacientes con IC a un seguimiento presencial o a asistencia con telemedicina que incluía comunicación de signos y síntomas diarios con TM y un seguimiento estructurado mediante videoconferencia o audioconferencia. El objetivo principal del estudio fueron los episodios de IC no mortales (descompensaciones que precisaron tratamiento parenteral), que tras 6 meses de seguimiento se redujeron un 65% (0,35; intervalo de confianza del 95% [IC95%], 0,20-0,59; p <0,001); los reingresos por IC, un 61% (0,39; IC95%, 0,19-0,77; p=0,007), y los reingresos cardiovasculares, el 57% (0,43; IC5%, 0,23-0,80; p=0,008) en el grupo de telemedicina; la mortalidad fue similar en ambos grupos y además hubo una reducción neta media significativa de los costes hospitalarios directos de 3.546 euros por paciente. Este estudio de prueba de concepto se ha ratificado en los resultados del estudio multicéntrico HERMeS22, con 506 pacientes con ingreso reciente, cuyos resultados preliminares se han presentado en el Congreso Europeo de Insuficiencia Cardiaca en mayo 2023 y muestran una reducción del 59% del objetivo combinado de muerte cardiovascular o empeoramiento por IC con un número de pacientes que es necesario tratar de 423.
Dispositivos específicos para medición y telemonitorizaciónA pesar de que existen en el mercado dispositivos no invasivos portátiles para la monitorización del ritmo cardiaco y la congestión pulmonar (bioimpedancia), no está del todo claro si proporcionan beneficios adicionales a la TM convencional24. En cuanto a los dispositivos de TM invasivos, sabemos que los dispositivos implantables (terapia de resincronización cardiaca, desfibrilador automático implantable) más actuales proporcionan, mediante conexión inalámbrica a distancia, información sobre el propio dispositivo (generador y funcionamiento de los electrodos), arritmias o datos fisiológicos del paciente (frecuencia cardiaca, actividad, ruidos cardiacos, bioimpedancia) e incluso algoritmos de detección de congestión (Optivol Medtronic, Estados Unidos; HeartLogic, Boston Scientific, Estados Unidos, etc.). Sin embargo, en los distintos estudios se obtiene que dicha TM es más útil para detectar el mal funcionamiento del dispositivo y arritmias como la FA, sin que la detección de la congestión por los dispositivos se asocie con una evidencia sólida con una reducción de los ingresos por IC o la mortalidad25–27. Podrían ser de utilidad otros dispositivos de TM implantables como las grabadoras en bucle subcutáneas que, aparte de monitorizar la frecuencia y el ritmo cardiacos, detectan la actividad y la bioimpedancia.
Otros dispositivos con implantación en la arteria pulmonar (CardioMEMS, Abbott, Estados Unidos) se han desarrollado para monitorizar su presión (el aumento de la presión diastólica de la arteria pulmonar es uno de los signos más precoces de congestión), y permiten ajustar el tratamiento precozmente. Sin embargo, los resultados son dispares; algunos muestran una reducción del riesgo de hospitalizaciones por IC28 y mejora de la calidad de vida29; en otros, como el ensayo clínico aleatorizado GUIDE-HF30 con más de 1.000 pacientes incluidos, no hubo diferencias en el objetivo primario de mortalidad por cualquier causa, hospitalización o visitas a urgencias entre los pacientes ambulatorios estables con IC crónica cuando se compara el tratamiento basado en las presiones de medidas por CardioMEMS con la atención habitual. No obstante, los autores consideran que la pandemia de COVID-19 puede haber contribuido a este resultado, ya que sí hubo beneficio en la cohorte inscrita antes de la pandemia31.
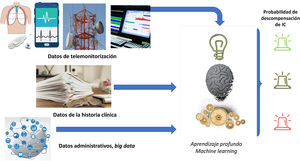
Inteligencia artificialAdelantarse a las descompensaciones quizá sea el objetivo más ambicioso de la eSalud en IC. Para ello, la inteligencia artificial con algoritmos de predicción basada en big data es un complemento ideal que podría otorgar a la TM un beneficio adicional. En una revisión reciente32, se describen las estrategias y el rendimiento de los algoritmos basados en inteligencia artificial para la predicción del ingreso hospitalario de pacientes con IC. De los artículos analizados, 16 predijeron el (re)ingreso hospitalario a los 30 días, y de 6 meses a 3 años, con áreas bajo la curva entre 0,61 y 0,79. Los estudios que incluían parámetros de TM fueron los más precisos. Así, el estudio que evaluó prospectivamente el funcionamiento de un parche sensorial desechable, en el domicilio tras la hospitalización, dio como resultado un área bajo la curva de 0,89 para la predicción de ingreso33. Este estudio incluía un parche de 7 días de duración que recogía la forma de onda continua del ECG, la acelerometría continua de 3 ejes, la impedancia y la temperatura de la piel y la información sobre la actividad y la postura. Los datos obtenidos se integraron con los datos administrativos y de historia clínica del paciente y se analizaron mediante modelos de machine learning y aprendizaje profundo (figura 3).
Figura central. Esquema de funcionamiento de la integración de los distintos datos obtenidos de diferentes fuentes y su análisis mediante modelos de machine learning y aprendizaje profundo. Elaborado con datos de Stehlik et al.33. IC: insuficiencia cardiaca.
Otras opciones de telemedicina en IC también relacionadas con la inteligencia artificial tienen que ver con el análisis del habla en la detección de la sobrecarga de líquido pulmonar. Se ha desarrollado una aplicación para dispositivos móviles que, mediante el análisis del sonido de la voz, permite identificar con éxito las condiciones clínicas que afectan a la mecánica de vibración de las cuerdas vocales. Solo con la grabación diaria de 6 frases, la aplicación HearO (Cordio, Israel) permitió detectar en más del 90% alteraciones de la voz que reflejaban aumento de congestión34. Se trata de una aplicación de procesamiento y análisis del habla que detecta las características del habla al ingreso (húmedo) diferenciándolas de las del alta (seco) del hospital. Recientemente, en un análisis de datos preliminares de 253 pacientes ambulatorios con IC, la aplicación detectó el 80% de las descompensaciones con una precocidad media de 22,5 días frente a la estrategia convencional y con muy pocos falsos positivos (2,8 alertas falsas por año).
Consideraciones de los autoresBasándonos en los datos de que disponemos, ya explicados, la guía de práctica clínica de la Sociedad Europea de Cardiología35 considera que se podría utilizar la TM tanto no invasiva como invasiva (pulmonar) con una recomendación baja (IIb) y un nivel de evidencia B (tabla 2). A nuestro parecer, los estudios realizados, la falta de estandarización de los métodos, la pobre adaptación al contexto local, la dificultad para integrarla en los sistemas informáticos existentes (seguridad y confidencialidad de los datos), la falta de financiación adecuada y de incentivos para su uso en la práctica real no refleja adecuadamente lo que la telemedicina y la TM podrían aportar. Para los autores, la telemedicina y, por lo tanto, la TM en IC deberían servir para: a) asistir en la detección precoz de las descompensaciones; b) motivar al paciente y mejorar su adherencia a los tratamientos, y c) facilitar la formación del paciente sobre su enfermedad. Aun así, y en caso de que la TM no lograra mejorar los beneficios en salud frente a la presencialidad de los pacientes en las consultas y fuera al menos igual, el balance general de incluirla es muy positivo (comodidad para el paciente, ahorro de tiempo y de recursos, etc.). Sin embargo, con los últimos resultados del estudio multicéntrico HERMeS22, cuyo número de pacientes que es necesario tratar para evitar un evento fue tan bajo, en opinión de los autores debería tener un peso muy importante para que en las próximas guías esta recomendación fuera más fuerte.
Recomendaciones sobre la telemonitorización en la insuficiencia cardiaca
| Recomendaciones | Clase | Nivel |
|---|---|---|
| Se puede considerar la TM no invasiva para los pacientes con IC a efectos de reducir el riesgo de hospitalizaciones recurrentes por IC y causas cardiovasculares y la mortalidad cardiovascular | IIb | B |
| Se puede considerar la monitorización de la presión arterial pulmonar mediante un sistema hemodinámico inalámbrico para los pacientes con IC a efectos de mejorar los resultados clínicos | IIb | B |
Recomendaciones para la telemonitorización en insuficiencia cardiaca según la guía europea sobre insuficiencia cardiaca IC, según McDonagh et al.35. IC: insuficiencia cardiaca; TM: telemonitorización.
La telemedicina puede ayudar a la modificación de los factores de riesgo, la adherencia terapéutica y el control de los síntomas. En el proceso de modificación de los factores de riesgo se incluyen el control y la mejora de la presión arterial y las concentraciones de lípidos, el fomento del ejercicio y los cambios en la dieta, y el asesoramiento para dejar de fumar36. Existen múltiples herramientas sencillas, como llamadas telefónicas, mensajes de texto cortos o portales en línea o web, mediante las que se puede realizar un seguimiento del progreso de los signos vitales y las pruebas de laboratorio, proporcionar ajustes de dosis y fomentar la actividad física, la dieta adecuada y el cumplimiento del tratamiento. Los datos de pequeños ensayos controlados y aleatorizados y metanálisis demuestran una mejora significativa en los factores de riesgo con la telemedicina, aunque la durabilidad de las intervenciones no está bien definida36–38. El abordaje global de los factores de riesgo cardiovascular se ha valorado de forma integral en programas de rehabilitación cardiaca, y las guías recomiendan la telemedicina como una opción válida en el seguimiento para incrementar la adherencia a largo plazo (nivel de recomendación IIb, nivel de evidencia B)39, pero el análisis del papel de la telemedicina en rehabilitación cardiaca va más allá del objetivo de este documento.
Herramientas digitales para la hipertensiónDispositivos digitales para la medición de presión arterialLa investigación en torno a la monitorización de la presión arterial sigue principalmente 2 enfoques; el primero es conseguir que los sistemas de medición ya existentes, basados en manguitos, sean más fáciles de usar o ajustables a la vida cotidiana; otro es utilizar señales biomédicas fácilmente accesibles para encontrar una técnica que la mida con una precisión razonable. Dado que el nivel de precisión del primer enfoque ya es adecuado, hacerlo más pequeño, más eficiente y robusto es el objetivo principal de los dispositivos más nuevos. En el segundo enfoque, la precisión es la mayor preocupación y la versatilidad en términos de edad y otros factores son los aspectos más complejos de resolver40.
Al igual que en el campo del ritmo cardiaco, en la presión arterial también se persigue la monitorización continua no invasiva, con dispositivos no basados en pletismografía y onda de pulso41.
Pero por ahora estos dispositivos sin manguito necesitan todavía mejores resultados para recomendar su uso en práctica clínica, ya que hasta la fecha han generado dudas importantes en cuanto a su reproducibilidad y precisan aún una validación42, por lo que hasta el momento las sociedades científicas no los recomiendan43 y recientemente se han propuesto métodos para su validación44.
Dispositivos para mejorar el control de la presión arterialExisten dispositivos que pueden ayudar en el control y la transmisión de la presión arterial basados en aplicaciones móviles que combinan telemedicina y educación sanitaria. Hay muchos ejemplos recientes: en una revisión sistemática se demuestra que la atención basada en la TM domiciliaria de la presión arterial con transmisión automática de datos puede ser más eficaz que el tratamiento clásico de la hipertensión45. En particular, los estudios que utilizan aplicaciones para teléfonos inteligentes han mostrado efectos beneficiosos en este metanálisis45, y otro ejemplo reciente del papel de la aplicación en este contexto es el estudio HERB DH146.
Estas estrategias de TM se han combinado con éxito en programas de prevención junto con el control de otros factores de riesgo (como los lípidos) y han mostrado reducción de las visitas a los centros sanitarios47.
Herramientas digitales para las dislipemiasMúltiples estudios muestran que el control del colesterol unido a lipoproteínas de baja densidad en pacientes en prevención secundaria son insuficientes48. Las soluciones basadas en telemedicina pueden ser una oportunidad para mejorarlo; un buen ejemplo que ha demostrado buenos resultados es la consulta virtual de lípidos49 basada en un estricto seguimiento virtual (historia electrónica y llamadas telefónicas) tras el alta hospitalaria con análisis consecutivos y ajuste del tratamiento hipolipemiante, que ha demostrado un alto grado de control del colesterol unido a lipoproteínas de baja densidad tras un síndrome coronario agudo.
Estas estrategias de TM de los lípidos se han combinado en programas de prevención junto con el tratamiento de otros factores de riesgo como la hipertensión, con éxito demostrado47.
Herramientas digitales para la diabetesDispositivos digitales para la medición de la glucemiaExisten dispositivos invasivos o directos de medición continua de la glucemia claramente contrastados que se emplean en la diabetes mellitus 1 y 250.
Hay en desarrollo métodos no invasivos para evaluar la glucemia51 que probablemente acaben llegando al consumidor al igual que ha ocurrido con los dispositivos para la detección de arritmias52, por lo que se debe estar atentos para valorar su empleo en el futuro y valorar en qué casos deben indicarse estas tecnologías.
Herramientas digitales para el tratamiento de la diabetesSe ha demostrado que las herramientas digitales tipo aplicación mejoran el control de la diabetes en diferentes aspectos53, sobre todo actuando sobre el estilo de vida54. Este beneficio parece ser más evidente en los pacientes más jóvenes y en aquellos sistemas que proporcionen retroalimentación o feedback con el personal sanitario.
Herramientas digitales para el abordaje del tabaquismoAbordar el tabaquismo en las enfermedades cardiovasculares es vital55, ya que en las enfermedades respiratorias se ha demostrado que la telemedicina puede ser de gran utilidad56. Hay evidencia de que las estrategias basadas en la telemedicina que emplean mensajería han mostrado beneficio en el abandono del tabaquismo57.
Herramientas digitales para fomentar la adherenciaLa adherencia al tratamiento es de gran importancia en el tratamiento de las enfermedades cardiovasculares58. Para ello, se han empleado estrategias como las combinaciones de fármacos59, pero puede haber también un papel para las estrategias basadas en telemedicina.
Existen múltiples publicaciones de distintas estrategias que han intentado mejorar la adherencia empleando desde mensajería (sin éxito)60 o, con cierto éxito, aproximaciones que integran múltiples herramientas61.
Consideraciones de los autoresEn este momento no recomendamos los dispositivos sin manguito para la monitorización de la presión arterial y sí la TM con el envío automático de los registros de la presión arterial para mejorar su control, especialmente con sistemas basados en aplicaciones e integrados en la historia clínica. Para mejorar el control de lípidos, recomendamos implementar estrategias y algoritmos en las historias clínicas que induzcan «alertas» en forma de llamadas telefónicas o recordatorios por mensajería. No recomendamos el uso de dispositivos no invasivos para la monitorización de la glucemia. Cuando se requiera dicha monitorización con precisión, se debe recurrir a dispositivos invasivos. Para mejorar el control de la diabetes, el abandono del tabaco y la adherencia al tratamiento, recomendamos el empleo de sistemas basados en aplicaciones validados con estudios clínicos. No recomendamos el uso de estrategias basadas exclusivamente en mensajería para mejorar la adherencia.
DESAFÍOS FUTUROSLos desafíos futuros de la telemedicina en el campo de las enfermedades cardiovasculares que debemos plantearnos son:
- •
Garantizar que todos los pacientes tengan acceso a la tecnología necesaria, así como el conocimiento de su uso.
- •
Establecer medidas de privacidad y seguridad de datos para proteger dicha información.
- •
Abordaje multidisciplinario (enfermería, atención primaria, etc.) con integración fácil e interoperabilidad con la historia clínica.
- •
Generación de más evidencia que evalúe la calidad de la atención, los resultados clínicos y la satisfacción del paciente.
- •
Capacitación adecuada en el uso de la telemedicina y comprender sus beneficios y limitaciones de los pacientes y profesionales.
- •
Integración con la inteligencia artificial y big data que facilitará una atención médica más personalizada, detección temprana, asistencia en la toma de decisiones clínicas y seguimiento de los pacientes a distancia.
Ninguna.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores han contribuido sustancialmente a la concepción y el diseño, la adquisición de información y a la redacción del artículo y la revisión crítica de su contenido intelectual, han dado la aprobación a la versión final y acceden a asumir responsabilidades sobre todos los aspectos del artículo y a investigar y resolver cualquier cuestión relacionada con la exactitud y veracidad de cualquier parte del trabajo.
CONFLICTO DE INTERESESNinguno.