Full English text available from: www.revespcardiol.org/en
La idea de incluir varios fármacos en una combinación a dosis fijas para prevención cardiovascular nació a principios de este siglo. Aunque inicialmente recibió escasa atención, la publicación del trascendental trabajo de Wald y Law en 2003, en el que aparecía el término polypill («policomprimido», en su traducción al castellano), atrajo el interés de investigadores y medios de comunicación, al tiempo que se iniciaba una importante controversia, que todavía hoy continúa1. Para algunos profesionales de la salud, la idea de un policomprimido para prevención cardiovascular no es más que una idea interesante, pero de escasas utilidad y aplicabilidad, una quimera, que la Real Academia Española de la Lengua describe como «aquello que se propone a la imaginación como posible o verdadero, no siéndolo». Para otros, sin embargo, es una estrategia que puede salvar miles de vidas si se aplica en el contexto y con la indicación adecuados.
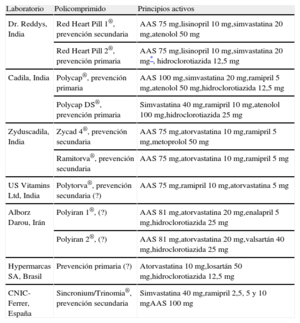
Independientemente de la controversia, el policomprimido es hoy una realidad; de hecho, se han desarrollado diferentes policomprimidos (tabla 1). Uno de ellos, el desarrollado en colaboración por el Centro Nacional de Investigaciones Cardiovasculares (CNIC) y Ferrer, que contiene ácido acetilsalicílico, simvastatina y ramipril, ya forma parte del arsenal terapéutico de varios países americanos: México, Guatemala, Nicaragua, República Dominicana, Honduras, El Salvador y Argentina. Se ha aprobado el registro en España y Suecia, entre otros países europeos, de un segundo policomprimido, en el que se ha sustituido la simvastatina por atorvastatina, y estará disponible para su prescripción durante el presente año.
Diferentes policomprimidos actualmente desarrollados
| Laboratorio | Policomprimido | Principios activos |
| Dr. Reddys, India | Red Heart Pill 1®, prevención secundaria | AAS 75mg,lisinopril 10mg,simvastatina 20mg,atenolol 50 mg |
| Red Heart Pill 2®, prevención primaria | AAS 75mg,lisinopril 10mg,simvastatina 20mg*, hidroclorotiazida 12,5mg | |
| Cadila, India | Polycap®, prevención primaria | AAS 100mg,simvastatina 20mg,ramipril 5mg,atenolol 50mg,hidroclorotiazida 12,5 mg |
| Polycap DS®, prevención primaria | Simvastatina 40mg,ramipril 10mg,atenolol 100mg,hidroclorotiazida 25 mg | |
| Zyduscadila, India | Zycad 4®, prevención secundaria | AAS 75mg,atorvastatina 10mg,ramipril 5mg,metoprolol 50 mg |
| Ramitorva®, prevención secundaria | AAS 75mg,atorvastatina 10mg,ramipril 5 mg | |
| US Vitamins Ltd, India | Polytorva®, prevención secundaria (?) | AAS 75mg,ramipril 10mg,atorvastatina 5 mg |
| Alborz Darou, Irán | Polyiran 1®, (?) | AAS 81mg,atorvastatina 20mg,enalapril 5mg,hidroclorotiazida 25 mg |
| Polyiran 2®, (?) | AAS 81mg,atorvastatina 20mg,valsartán 40mg,hidroclorotiazida 25 mg | |
| Hypermarcas SA, Brasil | Prevención primaria (?) | Atorvastatina 10mg,losartán 50mg,hidroclorotiazida 12,5 mg |
| CNIC-Ferrer, España | Sincronium/Trinomia®, prevención secundaria | Simvastatina 40mg,ramipril 2,5, 5 y 10 mgAAS 100 mg |
AAS: ácido acetilsalicílico; (?): Indicación no especificada.
¿Por qué persiste, pues, la polémica en torno al concepto de policomprimido? Varios factores pueden explicar las reticencias respecto a esta estrategia de prevención cardiovascular (tabla 2), pero sin duda han sido determinantes las diferentes interpretaciones que han ido apareciendo en la literatura desde el trabajo de Wald y Law sobre el papel del policomprimido y sus posibles indicaciones.
Argumentos a favor y en contra del concepto de policomprimido
| A favor |
| Mejor adherencia de los pacientes al tratamiento |
| Reducción de la complejidad del tratamiento para pacientes con múltiples medicaciones |
| Mayor facilidad en la prescripción |
| Mayor disponibilidad del medicamento en países en desarrollo |
| Menor coste |
| Menor coste de la medicación en comparación con los genéricos en determinados países, especialmente países en desarrollo |
| Menor coste por la reducción de eventos cardiovasculares al mejorar la adherencia y la prevención |
| En contra |
| En la «estrategia de vacunación» |
| Riesgos de la administración sistemática a toda la población sin evaluación previa: |
| • Medicalización de la población «sana» |
| • Efectos psicológicos adversos |
| • Efecto negativo en los estilos de vida saludables |
| • Temor a las reacciones adversas |
| En la prevención primaria |
| Ausencia de estudios que prueben su eficacia y la aceptación de pacientes y profesionales: |
| • Expectativas demasiado optimistas |
| • Coste-efectividad |
| Dificultad en la selección de fármacos y dosis |
| Dificultad para identificar a los pacientes adecuados (indicación) y el nivel de riesgo requerido para iniciar la terapia |
| Efecto negativo en los estilos de vida saludables |
| En prevención secundaria |
| Dificultad en individualizar las dosis y alcanzar las recomendadas por las guías |
La propuesta inicial de Wald y Law consistía en administrar un policomprimido con 6 principios activos a todos los individuos mayores de 55 años, independientemente de sus factores de riesgo y sin necesidad de conocer sus concentraciones de colesterol o las cifras de presión arterial1. La propuesta —definida por los autores como una «estrategia de vacunación»— ha encontrado fuerte oposición entre los profesionales, porque las consecuencias de medicalizar a toda la población son desconocidas, especialmente las reacciones adversas y su coste, los efectos psicológicos en una población sana o la posibilidad de que favorezca el abandono de los hábitos de vida saludables2. Sin estudios clínicos apropiados que demuestren su eficacia, es difícil que esta indicación gane en un futuro próximo la aceptación de profesionales y autoridades sanitarias.
Partiendo de la idea inicial de Wald y Law, varios autores propusieron utilizar el policomprimido más selectivamente en individuos sin enfermedad cardiovascular pero en riesgo elevado de padecerla (prevención primaria)3. Aunque varios estudios piloto han demostrado la factibilidad de esta estrategia, no existe una prueba definitiva de su utilidad, su seguridad y su relación coste-efectividad. Además dichos estudios incluyen a pacientes con y sin enfermedad cardiovascular previa, lo que dificulta la interpretación de los resultados; en conjunto, demuestran que el policomprimido incrementa la adherencia al tratamiento en un 30%, sin resultados concordantes en control de la presión arterial o de la concentración de lípidos. Ninguno de estos estudios tenía potencia para detectar diferencias en la tasa de nuevos eventos coronarios. Habrá que esperar, pues, a los resultados de los estudios actualmente en marcha para conocer si el policomprimido debe ocupar un lugar en la prevención primaria de la enfermedad coronaria3–5.
Finalmente, se ha propugnado la utilización del policomprimido para pacientes con afección cardiovascular, especialmente quienes ya han sufrido un infarto de miocardio (prevención secundaria)6. Las razones que avalan esta estrategia, que ha ido ganando adeptos, son varias:
- •
Los pacientes con cardiopatía coronaria, especialmente aquellos que ya han sufrido un infarto de miocardio, deben tomar los 4 fármacos (cardioprotectores) con demostrada eficacia en reducir la mortalidad y prevenir nuevos eventos: ácido acetilsalicílico, estatinas, inhibidores de la enzima de conversión de la angiotensina y bloqueadores beta7–9.
- •
El estudio PURE demostró que, de los más de 5.600 pacientes con enfermedad coronaria previa reclutados en 17 países con distintos niveles de renta per cápita, más del 60% no recibía ninguno de estos fármacos y solo un 3% recibía los cuatro. Los países de renta más baja presentaban las peores cifras: hasta el 80% de los pacientes no reciben fármacos de ningún tipo tras un infarto de miocardio10.
- •
Las causas de la inadecuada prevención en estos países son evidentes. En primer lugar, la accesibilidad del sistema sanitario y, por lo tanto, la atención médica son deficientes. Por ejemplo, en el Study on Prevention on Recurrences of Myocardial Infarction and Stroke (WHO-PREMISE) de la Organización Mundial de la Salud, en determinados países se había determinado la concentración de colesterol a menos del 40% de los pacientes postinfartados. Además, la medicación no está disponible o es excesivamente cara, puesto que la cobertura sanitaria en ellos prácticamente no existe y los medicamentos en el mercado privado tienen precios altos. Como consecuencia, un trabajador puede necesitar más de la mitad de su sueldo mensual para comprar la medicación para el postinfarto11. Cualquier intento de aplicar una medicina individualizada en estos países siguiendo nuestros estándares es una utopía. La experiencia con el policomprimido CINIC-Ferrer en este tipo de países demuestra que el precio puede reducirse en un 50% respecto al precio de los fármacos genéricos en el mercado privado, al mismo tiempo que puede mejorar el acceso al incrementarse el número de pacientes que tienen la posibilidad de una mejor prevención secundaria. Incluso cuando los costes del policomprimido y de los medicamentos por separado sean parecidos (mercado público), la reducción de eventos cardiovasculares secundaria a la mejor adherencia determinará que aquella sea coste-efectiva.
- •
A pesar de los esfuerzos de las autoridades sanitarias, los profesionales de la salud y las sociedades científicas, la situación en los países desarrollados dista mucho de ser la ideal. En estos, la prevención secundaria es deficiente por dos causas principales: la prescripción inadecuada y la falta de adherencia de los pacientes al tratamiento. Numerosos estudios, especialmente registros internacionales y nacionales, entre los que destacan los patrocinados por la Sociedad Española de Cardiología y su Sección de Cardiopatía Isquémica, han demostrado que el seguimiento de las guías clínicas por los médicos no es perfecto12. Aunque con los años la mejora es evidente, todavía cerca del 50% de los pacientes no reciben bloqueadores beta o inhibidores de la enzima de conversión de la angiotensina después de un infarto agudo de miocardio. Además, los estudios también demuestran que la prescripción inadecuada se traduce en un control deficiente de los factores de riesgo y en un peor pronóstico.
- •
La falta de adherencia de los pacientes al tratamiento es un grave problema que hemos ignorado durante décadas. El problema es más evidente en el caso de los pacientes con enfermedades crónicas y se ha detectado en todos los países estudiados independientemente del tipo de sistema sanitario, la situación económica o el nivel educativo. Un metanálisis publicado recientemente puso de manifiesto que entre los pacientes con enfermedades cardiovasculares la adherencia era del 57% (intervalo de confianza del 95%, 50%-64%) tras un seguimiento medio de 24 meses13. Estas cifras se han confirmado en otros muchos estudios, que además han analizado las causas de esta falta de adherencia. Junto al tipo de fármaco, una de las razones principales de abandonar el tratamiento es su complejidad y, especialmente, el número de dosis (comprimidos, tabletas) que el paciente debe tomar cada día. Claxton et al14 revisaron 76 publicaciones sobre adherencia, y concluyeron que esta es inversamente proporcional al número de dosis diarias. En este sentido, un policomprimido puede mejorar la adherencia.
- •
La adecuada adherencia al tratamiento se asocia al mejor control de los factores de riesgo y menor morbimortalidad de los pacientes con infarto agudo de miocardio. El efecto beneficioso de un seguimiento adecuado de la medicación se ha demostrado con cada uno de los fármacos cardioprotectores por separado, pero también en combinación. Así, son muy reveladores los datos del registro alemán publicado por Zeymer et al15. De un total de 9.998 pacientes dados de alta tras un infarto de miocardio (todos tratados con bloqueadores beta), la mortalidad durante el primer año fue del 4,9% de los pacientes que recibían ácido acetilsalicílico, un inhibidor de la enzima de conversión de la angiotensina y una estatina, el 9,7% de los que tomaban solo 2 de estos fármacos y el 13,6% de los que tomaban uno o ninguno15. Otros registros y estudios prospectivos han confirmado esta relación entre adherencia y pronóstico tras el infarto agudo de miocardio.
- •
Una combinación de fármacos a dosis fijas o policomprimido mejora el cumplimiento terapéutico. Varios estudios en pacientes hipertensos o diabéticos han demostrado mayor adherencia al tratamiento con las combinaciones de fármacos a dosis fijas en comparación con la administración de los fármacos por separado. Además, actualmente se dispone de nuevos datos que confirman la eficacia del policomprimido en mejorar la adherencia. Los resultados del estudio UMPIRE, en 2.004 pacientes en riesgo elevado de sufrir un evento coronario, han confirmado que el policomprimido incrementa la adherencia de un 65% del grupo control al 86% de los tratados con el policomprimido16. Un segundo estudio más reciente con este mismo policomprimido ha confirmado la mejora significativa en la adherencia de los pacientes con y sin enfermedad cardiovascular previa17.
- •
A diferencia de los que sucede en prevención primaria, las agencias reguladoras más importantes no exigen estudios de eficacia para el policomprimido en prevención secundaria. Solo se requiere demostrar la bioequivalencia entre la nueva preparación y los fármacos administrados por separado, ya que la eficacia de estos es ampliamente conocida y está probada. De cualquier forma, es necesario señalar que conseguir un policomprimido que cumpla estos requisitos no es tarea fácil, y se requiere gran experiencia en el desarrollo galénico. De hecho, entre todos los policomprimidos que se están desarrollando en el mundo, solo las del proyecto CNIC-Ferrer han conseguido aprobación y registro en países diferentes del de origen.
- •
Al margen del policomprimido, se han propuesto diferentes intervenciones para mejorar la adherencia al tratamiento de los pacientes con enfermedades cardiovasculares. Las estrategias se basan en proporcionar al paciente información escrita, vídeos, charlas, contactos telefónicos frecuentes o consejos personalizados para motivarlo en el uso correcto de la medicación. En general, los estudios demuestran que la adherencia mejora con las intervenciones, pero el beneficio desaparece con el tiempo si no hay una actuación continua. El hecho de que estas estrategias requieran equipos multidisciplinarios y gran inversión de tiempo y medios limita su aplicabilidad a gran escala y, desde luego, las hace impensables en los sistemas sanitarios de países en desarrollo.
En resumen, parece que hay razones suficientes para incorporar el policomprimido como una estrategia válida en prevención secundaria: mejora la accesibilidad y la asequibilidad del tratamiento en países en desarrollo y reduce la falta de adherencia al tratamiento, muy frecuente en cualquier ámbito socioeconómico, con lo que se reducen la tasa de eventos y el coste sanitario.
La guía de prevención y manejo de la enfermedad cardiovascular, publicada recientemente por American Heart Association/American College of Cardiology, ponen énfasis en la necesidad de administrar altas dosis de estatinas (atorvastatina 80mg) a todos los pacientes que han sufrido un infarto de miocardio, pasando por alto la estrategia de fijar los objetivos concretos de colesterol unido a lipoproteínas de baja densidad que según las guías previas se debía alcanzar18. Esta nueva recomendación se ha visto como un grave inconveniente para el uso de los policomprimidos, que incluyen dosis moderadas de estatinas (simvastatina 40mg, atorvastatina 20mg). El policomprimido no es una estrategia de tratamiento diseñada para sustituir la prevención individualizada y personalizada que recomiendan las guías, posible solo en algunos países y para determinados pacientes adherentes al tratamiento, sino una intervención de salud que hace asequible la prevención a una gran parte de la población mundial marginada o, en nuestro ambiente, a individuos que, aun teniendo la medicación a su alcance, presentan mala adherencia. Por lo tanto, la selección de los fármacos por incluir en el policomprimido y sus dosis se basa en un compromiso entre eficacia y seguridad, que permita administrarla a pacientes con difícil acceso a la atención médica o sin una adecuada disciplina. Aunque las altas dosis de estatinas (p. ej., 80mg de atorvastatina) son seguras, la tasa de algunos efectos adversos (elevación de enzimas hepáticas) es mayor que con las dosis más bajas15. Además, la relación entre dosis de estatina y reducción de colesterol unido a lipoproteínas de baja densidad no es lineal: 20mg de atorvastatina determinan una disminución del 40% del colesterol unido a lipoproteínas de baja densidad, mientras que con 80mg se consigue un 52% de disminución19. Esto puede explicar que los estudios que compararon dosis moderadas-bajas con dosis altas de estatinas en los que se basan las recomendaciones de American Heart Association/American College of Cardiology, aun reduciendo la tasa de eventos combinados, no han conseguido demostrar una reducción de la mortalidad18.
En resumen, la utilidad del policomprimido para mejorar la accesibilidad del tratamiento y la adherencia a este en prevención secundaria está plenamente demostrada. En países en desarrollo, puede ser una intervención sanitaria con amplia repercusión social y económica. De hecho, puede marcar una inflexión en el avance de la epidemia y en su economía. En nuestro entorno, el policomprimido proporcionará un elemento para mejorar la adherencia en un numeroso grupo de pacientes con enfermedad cardiovascular establecida. La reducción de eventos en estos pacientes la convierte también en una opción coste-efectiva en países desarrollados. No se trata, pues, de establecer una controversia entre policomprimido y prevención secundaria personalizada: ambas son estrategias complementarias de las que dispondrá el médico para luchar contra la epidemia de las enfermedades cardiovasculares. El policomprimido es ya una realidad y tiene un gran futuro.
CONFLICTO DE INTERESESLos autores no tienen conflicto de intereses personales. EL CNIC tiene un proyecto para desarrollar policomprimidos con Ferrer en una iniciativa público-privada conjunta.