Palabras clave
La estimulación permanente del ápex ventricular derecho puede tener efectos no deseables1-4 y el tracto de salida no es alternativa clara5.
La estimulación del haz de His (StH) provoca una contracción ventricular fisiológica y no deteriora la función ventricular6-9.
Pretendemos averiguar cuántos pacientes con indicación para estimulación cardiaca permanente serían candidatos a StH y en cuántos se consigue.
MÉTODOS
Selección de pacientes
Desde enero a julio de 2006, los pacientes sin cardiopatía propuestos para estimulación cardiaca fueron considerados potenciales candidatos a StH, independientemente del tipo de bloqueo. Por presión asistencial, se seleccionó sólo a 1 de cada 3 pacientes consecutivos. Se obtuvo el consentimiento informado.
Para ser candidato a StH exigimos: indicación de estimulación cardiaca permanente10; umbral de captura hisiano máximo 2,5 V/1 ms; conducciones His:ventrículo 1:1, con un mínimo de 120 s/m, y ausencia de miocardiopatía.
Localización y estimulación temporal del haz de His
Para la localización y la StH temporal y definitiva, empleamos electrodos de fijación activa y baja polarización Tendril SDX (St Jude, Minneapolis) de 52 cm de longitud y 1 cm entre polos, según técnica ya publicada11,12.
Electrodo adicional y generadores empleados
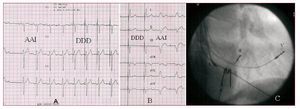
Cuando había trastorno de conducción intraventricular (TCIV) o bloqueo auriculoventricular completo (BAVC) considerado «infrahisiano» (hisiograma con H no seguido de V), además del electrodo en His, se implantaba otro de seguridad en el tracto de salida del ventrículo derecho (fig. 1C).
Fig. 1. A: bloqueo suprahisiano de segundo grado tipo I, tratado con marcapasos DDD con estimulación del haz de His (StH); captura pura de His. B: bloqueo auriculoventricular de primer grado con bloqueo de rama izquierda tratado con marcapasos DDD de StH; comportamiento de tipo troncular; captura pura de His. C: proyección oblicua anterior derecha; trastorno de conducción intraventricular tratado con marcapasos tricameral, electrodo auricular (A), His (H) y tracto de salida derecho (V).
Se emplearon marcapasos tricamerales Frontier II 5596 (St. Jude Medical, Sylmar, California, Estados Unidos), bicamerales Kappa 900 (Medtronic, Minneapolis, Minnesota, Estados Unidos) y monocamerales Insignia I AVT SR (Guidant Corporation, St. Paul, Minnesota, Estados Unidos), según las distintas situaciones clínicas. (fig. 1A y B).
RESULTADOS
Se seleccionó a 37 pacientes cuyos trastornos de conducción quedan reflejados en la tabla 1. De ellos, se excluyó a 6; en 3 con BAVC y escape ancho porque no se pudo registrar la deflexión hisiana; los otros 3 presentaban bloqueo de rama izquierda (BRI) que no se corregía con StH. En los 31 (83,3%) restantes, las anomalías en la conducción se corrigieron con StH; de ellos, 15 (71,4%) tenían anomalías de conducción infrahisiana (TCIV o BAVC) (tabla 2).
El umbral de StH agudo osciló entre 0,6 y 9 (3,1 ± 2,8) V en 1 ms en los 31 pacientes; de ellos, 11 (35,4%) fueron rechazados por umbral alto. Ninguno fue excluido por conducción His-ventrículo 1:1 < 120 s/m. Finalmente, 20 pacientes cumplieron requisitos para StH permanente. En 9 (45%) no pudo fijarse el electrodo. En los 11 (55%) restantes se fijó con éxito (tabla 2) (umbral, 1,5 ± 0,9 V; impedancia, 293 ± 103 W), y se consiguió StH pura en 6 y fusionada en 5.
Patrones de estimulación en His
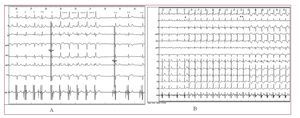
En presencia de bloqueos suprahisianos se obtuvieron dos patrones de QRS. El tipo 1 presentaba latencia de duración igual o menor que el intervalo HV, y los QRS tienen idénticas morfología y repolarización que los conducidos o de escape (fig. 2A). El tipo 2 carece de latencia y los QRS tienen morfología y repolarización diferentes de los propios y adquieren aspecto de «preexcitados» (fig. 2A y B).
Fig. 2. A: los QRS marcados con * son capturas puras del His, iguales a los propios (**); los QRS marcados con *** son de fusión. B: estimulación en His con descenso progresivo del voltaje a partir de *; hasta ** son complejos de fusión. Después de ** se pierde la captura de His.
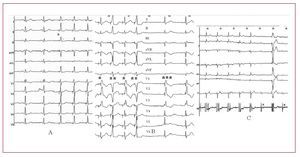
En presencia de TCIV y BAVC denominados «infrahisianos» se obtuvieron tres patrones de QRS: patrón A, latencia con desaparición de los TCIV/BAVC y normalización de los QRS (figs. 1B y 3A y C); patrón B, latencia y persistencia de los TCIV (fig. 3B), y patrón C, ausencia de latencia con desaparición de los TCIV sin normalización de los QRS (fig. 3B).
Fig. 3. A: bloqueo de rama derecha que desaparece con la estimulación del haz de His (StH) en *; comportamiento de tipo troncular. B: bloqueo de rama derecha en ***, que persiste con la StH en *; comportamiento de tipo periférico; los QRS marcados con ** son de fusión. C: bloqueo auriculoventricular completo «infrahisiano»; la StH provoca QRS normales; comportamiento de tipo troncular. H: hisiograma.
DISCUSIÓN
En nuestra serie, el 83,3% de las anomalías de conducción que requieren estimulación cardiaca permanente se corrigen con StH. Sin embargo, ésta sólo se consigue permanentemente en el 35,5% de los casos posibles y en el 55% de los intentos.
En los bloqueos suprahisianos, el patrón tipo 1 se debe a la StH «pura» y origina QRS normales porque el impulso es conducido vía red de Purkinje. La latencia refleja el tiempo de conducción desde la zona de captura hisiana a la de activación ventricular. El tipo 2 puede explicarse por captura simultánea del His y el miocardio adyacente, produciéndose fusión entre los dos frentes de activación que explica la imagen de QRS «preexcitado» y la ausencia de latencia.
En relación con los TCIV, es conocido que la StH puede hacer desaparecer los bloqueos de rama; sin embargo, no se ha publicado que provoque un QRS normal en presencia de BAVC considerado «infrahisiano» (fig. 3C). La teoría de la disociación longitudinal del haz de His13-16 explica estos fenómenos: las fibras asignadas a las ramas derecha e izquierda estarían histológicamente diferenciadas y aisladas en el tronco hisiano. Una lesión localizada en él puede dañarlas, y en el ECG se manifestaría como bloqueo de rama o auriculoventricular completo. La estimulación de la porción distal a la lesión normaliza los QRS.
Así pues, los TCIV y BAVC «infrahisianos» podrían clasificarse por su localización en troncular (haz de His) y periféricos, según desaparezcan o no con StH. El patrón A se produciría en presencia de TCIV troncular, cuando la captura hisiana es «pura» y distal a la zona de bloqueo; la despolarización ventricular se realiza vía sistema Purkinje, lo que explica la normalización de los QRS con latencia. El patrón B se justifica por un TCIV periférico con StH «pura», lo que explica la persistencia de los TCIV con latencia. El patrón C sería una «fusión» por captura del His y del miocardio adyacente. Habría preexcitación ventricular derecha que causaría pérdida de latencia y desaparición del bloqueo de rama derecha (BRD), independientemente de su localización troncular o periférica.
El patrón C en presencia de BRI sólo se obtendría en su localización troncular. Los QRS serían una fusión de la captura del His y la del miocardio. La primera produciría activación ventricular izquierda vía Purkinje, que explica la desaparición de BRI. La segunda, preexcitando el ventrículo derecho, explica la pérdida de latencia y la ausencia de normalización de los QRS.
La StH «pura» y la «fusionada» per se no deben provocar asincronía intraventricular izquierda, y su uso está limitado por el umbral de captura alto, que elimina, previo intento de fijación, a más de una tercera parte de los candidatos, o por dificultad para fijar el electrodo, lo que hace fracasar el 45% de los intentos.
En conclusión, la StH permanente puede considerarse cuando se requiere estimulación cardiaca definitiva.
Son necesarios nuevos electrodos que mejoren la captura y la estabilidad. Además, la incertidumbre en la evolución de los TCIV y BAVC «infrahisianos» aumenta la complejidad y el coste de la StH.
Full English text available from: www.revespcardiol.org
Correspondencia:
Dr. R. Barba Pichardo.
A. Sundheim, 30, 1.o C. 21003 Huelva. España.
Correo electrónico: rbphuelva@Yahoo.es
Recibido el 24 de agosto de 2007.
Aceptado para su publicación el 17 de enero de 2008.