Hay pocos datos sobre la evolución en adultos de la dilatación de la raíz neoaórtica (RAO) y la insuficiencia valvular neoaórtica (IA) tras la cirugía de switch arterial (SA) en la transposición de grandes arterias.
MétodosAnálisis retrospectivo de 152 pacientes con transposición de grandes arterias, mayores de 15 años, intervenidos mediante SA y seguidos durante 4,9±3,3 años en 2 centros de referencia. Se analizaron los cambios de diámetro de la RAO ajustados a superficie corporal y la progresión a grado moderado/grave de la IA con ecocardiografías seriadas. Se realizó un modelo de regresión de Cox para identificar factores predictores de progresión de la IA.
ResultadosInicialmente, 4 pacientes (2,6%) presentaban IA grave (3 habían precisado cirugía valvular) y 9 (5,9%) moderada. La RAO basal media era 20,05±2,4mm/m2, y al final del seguimiento, 20,73±2,8mm/m2 (p<0,001), con un crecimiento medio de 0,14 (IC95%, 0,07-0,2) mm/m2/año. La IA progresó en 20 (13,5%) y 6 (4%) fueron intervenidos. La progresión de IA se asoció con válvula bicúspide, IA inicial, dilatación de la RAO inicial y crecimiento de la RAO. La válvula bicúspide (HR=3,3; IC95%, 1,1-15,2; p=0,037), la IA inicial (HR=5,9; IC95%, 1,6-59,2; p=0,006) y el crecimiento de la RAO (HR=4,1; IC95%, 2-13,5; p=0,023) resultaron predictores independientes.
ConclusionesLa dilatación de la RAO y la IA progresan en el adulto joven intervenido mediante SA. La válvula bicúspide, la IA basal y el crecimiento de la RAO son predictores de progresión de IA.
Palabras clave
La transposición de grandes arterias (TGA) es la cardiopatía congénita cianótica más frecuente al nacimiento. Se han descrito varias técnicas de reparación, pero actualmente el procedimiento quirúrgico de elección es el switch arterial (SA). En esta técnica1 se realiza una reparación anatómica en periodo neonatal y tiene la ventaja de mantener el ventrículo morfológicamente izquierdo como ventrículo sistémico, aunque la unidad funcional que constituye la raíz neoaórtica (RAO) (válvula, anillo y porción sinusal) corresponde embriológicamente a la válvula y la arteria pulmonar.
Entre las más importantes complicaciones de la técnica, se encuentran la dilatación de la RAO y la insuficiencia valvular neoaórtica (IA). Los resultados en edad infantil son conocidos2,3 y aunque muchos pacientes presentan dilatación progresiva de aorta ascendente e insuficiencia valvular, en su mayoría son de grado ligero, por lo que son pocos los pacientes que requieren cirugía por esta complicación en la etapa pediátrica (1-3%)3.
Desde hace unos años, una nueva población de adultos jóvenes intervenidos de SA se valora en las unidades de cardiopatías congénitas del adulto (UCCA). Existen pocos estudios que analicen la evolución de la dilatación de la RAO e IA en estos pacientes, y además los resultados son controvertidos. Se han publicado trabajos que muestran una evolución favorable, con estabilización del tamaño de la RAO4 y de la IA5,6. Sin embargo, otros afirman que existe una progresión significativa de estas alteraciones, con una alta incidencia de reintervenciones7,8.
Los objetivos del estudio son describir la prevalencia de IA significativa, la necesidad de reintervención por complicaciones aórticas en el seguimiento y la incidencia de eventos clínicos graves en esta población, así como analizar si existe progresión en la dilatación neoaórtica y en el grado de IA y definir qué variables son predictoras de progresión de la insuficiencia valvular.
MÉTODOSPoblación de estudioAnálisis retrospectivo y longitudinal de una cohorte de pacientes diagnosticados de TGA o anomalía de Taussig-Bing y tratados con cirugía de SA seguidos en 2 UCCA de referencia. La inclusión de los pacientes tuvo lugar en el momento de su transferencia a la UCCA y se requirió un seguimiento superior a 1 año, con un estudio ecocardiográfico basal y en cada consulta anual. El estudio se ha realizado de acuerdo con la Declaración de Helsinki y se incluyó a los pacientes en el Registro Nacional de Cardiopatías Congénitas del Adulto (RECCA), aprobado por los comités éticos de ambos Hospitales (estudio 2017/0659).
Variables analizadasSe registraron retrospectivamente variables relacionadas con la anomalía estructural, la cirugía inicial y la evolución pediátrica. Las variables analizadas fueron demográficas, el tipo de TGA, las anomalías asociadas (comunicación interventricular, coartación de aorta, obstrucción del tracto de salida del ventrículo izquierdo, válvula pulmonar nativa bicúspide), patrón coronario (clasificadas como normal, coronaria derecha e izquierda naciendo del mismo seno, coronaria intramural u otras variantes), variables relacionadas con la cirugía de SA (edad a la intervención y cerclaje previo) y necesidad de reintervención (quirúrgica o percutánea).
Las variables analizadas en el seguimiento en la UCCA fueron: edad al inicio y el final del seguimiento, diámetro de la RAO sinusal (indexado a superficie corporal), grado de IA y eventos clínicos. Los eventos clínicos analizados fueron: fallecimiento, eventos coronarios graves (muerte, infarto de miocardio, revascularización coronaria), arritmias (taquicardia ventricular, fibrilación o flutter auricular), endocarditis y reintervención quirúrgica o percutánea.
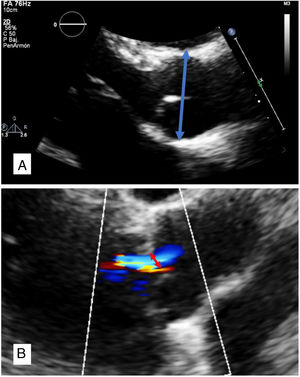
Con el fin de homogeneizar los resultados, las variables relacionadas con el estudio de la RAO se obtuvieron exclusivamente por ecocardiografías transtorácicas, realizadas por expertos ecocardiografistas de ambas UCCA. La medición de la aorta se realizó a nivel de los senos de Valsalva, en telediástole y de borde externo a borde interno (figura 1A). Se consideró dilatación de la RAO si presentaba un diámetro ≥ 20,6mm/m2 en varones y ≥ 20,7mm/m2 en mujeres. Este valor corresponde al obtenido de sumar la media + 1 desviación estándar de los valores normales de la aorta sinusal indexados por superficie corporal y ajustados a género, que Saura et al.9 definieron como diámetros normales en una cohorte de controles. El crecimiento se definió como la diferencia obtenida desde la medición inicial (primera visita en la UCCA) y la última realizada, expresándose de forma indexada a superficie corporal y dividida en años de seguimiento (mm/m2/año).
La IA se estudió mediante ecocardiografía Doppler color, analizando la vena contracta y clasificándola semicuantitativamente10 en leve (< 3 mm), moderada (3-6 mm) y grave (> 6 mm) (figura 1B). Se consideró significativa cuando el grado era moderado o grave. La presencia de progresión en el grado de regurgitación se definió por la evidencia de incremento del grado de IA tras 2 controles ecocardiográficos sucesivos y siempre que la insuficiencia alcanzara el grado de moderada o grave.
Análisis estadísticoLas variables continuas se expresan como media±desviación estándar si presentan distribución normal y con la mediana [intervalo intercuartílico] si tienen una distribución no gaussiana. Para las variables cualitativas se muestran sus porcentajes.
El tiempo de seguimiento computado fue el transcurrido desde la primera hasta la última ecocardiografía realizada en la UCCA. No se consideró para el análisis a los pacientes que no tuvieron ecocardiografía pasado el año de seguimiento.
Se realizó una comparación de las medias del diámetro de la RAO (calculadas al inicio y el final del seguimiento en la UCCA) con el test de la t de Student para medias relacionadas para confirmar la existencia de dilatación aórtica progresiva. El crecimiento medio de la RAO se expresó como la diferencia entre las mediciones inicial y final en mm/m2/años de seguimiento. Se realizó una comparación de medias para variables independientes para identificar factores asociados con el crecimiento de la RAO.
Los análisis de supervivencia libre de IA significativa y de cirugía de la RAO se realizaron mediante curvas de Kaplan-Meier. En el análisis de la progresión de la regurgitación aórtica, se excluyó a los pacientes que presentaban IA grave desde la etapa pediátrica (intervenidos o no) y se registró la fecha de la ecocardiografía donde se evidenció el incremento del grado de la insuficiencia. Los análisis de supervivencia libre de progresión se realizaron mediante curvas de Kaplan-Meier. La contribución individual de diversos factores de riesgo de progresión de la IA se analizó mediante regresión de Cox multivariante. Se consideró significativo un valor de p <0,05. El análisis estadístico se realizó utilizando el paquete SPSS 15.0 para Windows (SPSS Inc., Estados Unidos).
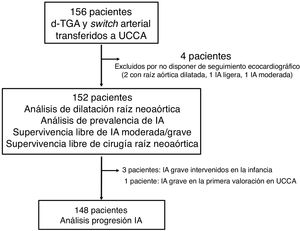
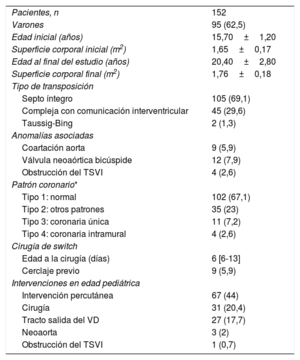
RESULTADOSSe transfirió de cardiología pediátrica a las UCCA a 156 pacientes (el 62,5% varones) diagnosticados de TGA y tratados con cirugía de SA. La media de edad inicial fue 15,7±1,2 años, y 152 pacientes completaron un seguimiento mayor de 1 año (se excluyó a 4 pacientes por pérdida de seguimiento) (figura 2). El seguimiento medio estuvo próximo a los 5 años (4,9±3,3), y la media de edad al final del estudio era 20,4±2,8 años.
En la tabla 1 se resumen las características demográficas, anatómicas y relacionadas con el SA, y las reintervenciones realizadas durante la edad pediátrica. La mayoría de los pacientes tenían diagnóstico de d-TGA, con comunicación interventricular asociada en casi un tercio. La válvula neoaórtica era bicúspide en el 7,9% de los pacientes. Durante el seguimiento pediátrico, 31 pacientes (20,4%) precisaron intervención quirúrgica, en su mayoría (27 pacientes) a nivel del tracto de salida del ventrículo derecho o el tronco pulmonar. Se intervino a 3 pacientes por IA (implante de prótesis en 2 de ellos y una reparación valvular) y a 1 paciente por obstrucción del tracto de salida del ventrículo izquierdo.
Características basales de los pacientes
| Pacientes, n | 152 |
| Varones | 95 (62,5) |
| Edad inicial (años) | 15,70±1,20 |
| Superficie corporal inicial (m2) | 1,65±0,17 |
| Edad al final del estudio (años) | 20,40±2,80 |
| Superficie corporal final (m2) | 1,76±0,18 |
| Tipo de transposición | |
| Septo íntegro | 105 (69,1) |
| Compleja con comunicación interventricular | 45 (29,6) |
| Taussig-Bing | 2 (1,3) |
| Anomalías asociadas | |
| Coartación aorta | 9 (5,9) |
| Válvula neoaórtica bicúspide | 12 (7,9) |
| Obstrucción del TSVI | 4 (2,6) |
| Patrón coronario* | |
| Tipo 1: normal | 102 (67,1) |
| Tipo 2: otros patrones | 35 (23) |
| Tipo 3: coronaria única | 11 (7,2) |
| Tipo 4: coronaria intramural | 4 (2,6) |
| Cirugía de switch | |
| Edad a la cirugía (días) | 6 [6-13] |
| Cerclaje previo | 9 (5,9) |
| Intervenciones en edad pediátrica | |
| Intervención percutánea | 67 (44) |
| Cirugía | 31 (20,4) |
| Tracto salida del VD | 27 (17,7) |
| Neoaorta | 3 (2) |
| Obstrucción del TSVI | 1 (0,7) |
Cx: arteria coronaria circunfleja; LAD: arteria coronaria izquierda descendente anterior; R: arteria coronaria derecha; TSVI: tracto de salida del ventrículo izquierdo; VD: ventrículo derecho.
Los valores expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
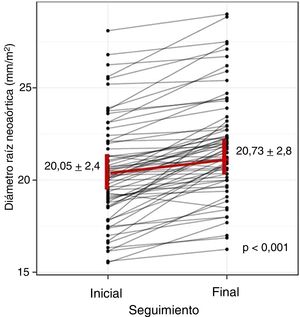
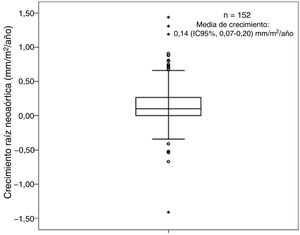
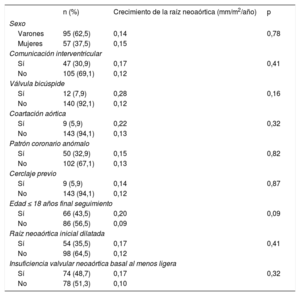
Basalmente, el 38,8% de los pacientes mostraban una RAO dilatada. Analizando los diámetros absolutos, el 10,5% era> 40mm y el 0,6%> 45 mm; en ningún paciente fue> 50mm. Al final del seguimiento, el 48,7% tenía una RAO dilatada; el 27,6%, una aorta> 40mm y el 9%> 45 mm y solo en 2 pacientes era> 50mm. Al comparar las medias de la RAO al inicio y final del estudio, se confirmó una dilatación progresiva y significativa (figura 3): 20,05±2,4 frente a 20,73±2,8mm/m2 (p <0,001), con una media de crecimiento (figura 4) de 0,14 (IC95%, 0,07-0,2) mm/m2/año. En cuanto a las variables que podrían estar en relación con la dilatación progresiva de la RAO, no se encontró significación estadística en ninguna de ellas (tabla 2).
Variables asociadas con el crecimiento de la raíz neoaórtica
| n (%) | Crecimiento de la raíz neoaórtica (mm/m2/año) | p | |
|---|---|---|---|
| Sexo | |||
| Varones | 95 (62,5) | 0,14 | 0,78 |
| Mujeres | 57 (37,5) | 0,15 | |
| Comunicación interventricular | |||
| Sí | 47 (30,9) | 0,17 | 0,41 |
| No | 105 (69,1) | 0,12 | |
| Válvula bicúspide | |||
| Sí | 12 (7,9) | 0,28 | 0,16 |
| No | 140 (92,1) | 0,12 | |
| Coartación aórtica | |||
| Sí | 9 (5,9) | 0,22 | 0,32 |
| No | 143 (94,1) | 0,13 | |
| Patrón coronario anómalo | |||
| Sí | 50 (32,9) | 0,15 | 0,82 |
| No | 102 (67,1) | 0,13 | |
| Cerclaje previo | |||
| Sí | 9 (5,9) | 0,14 | 0,87 |
| No | 143 (94,1) | 0,12 | |
| Edad ≤ 18 años final seguimiento | |||
| Sí | 66 (43,5) | 0,20 | 0,09 |
| No | 86 (56,5) | 0,09 | |
| Raíz neoaórtica inicial dilatada | |||
| Sí | 54 (35,5) | 0,17 | 0,41 |
| No | 98 (64,5) | 0,12 | |
| Insuficiencia valvular neoaórtica basal al menos ligera | |||
| Sí | 74 (48,7) | 0,17 | 0,32 |
| No | 78 (51,3) | 0,10 | |
Durante la edad pediátrica, 4 pacientes (2,6%) presentaron IA grave (se intervino a 3 de ellos) y en la primera visita a la UCCA, el 5,9% tenía una IA moderada y el 41,5%, ligera.
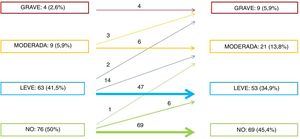
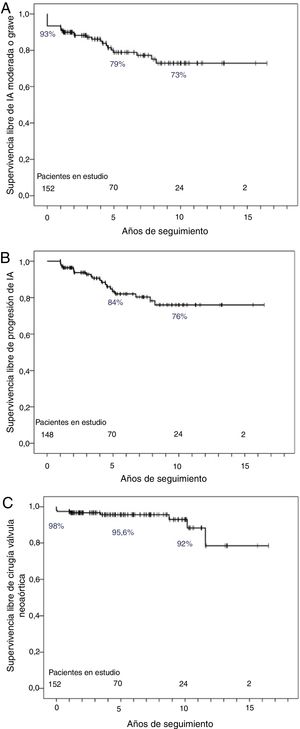
Al final del seguimiento, se confirmó una progresión del grado de IA en 20 pacientes (13,5%). Un 22% de los pacientes que partían de una IA ligera evolucionaron a moderada y 2 a grave. Tan solo 1 paciente (1,3%) que basalmente no tenía IA progresó a IA moderada. En la figura 5 se resume la progresión y la prevalencia de IA al final del seguimiento; destaca que más de la mitad de los pacientes presentaban algún grado de IA, y aunque en la mayoría era ligera, en casi el 20% era significativa o había requerido cirugía. Finalmente, la supervivencia libre de IA moderada o grave fue del 79 y el 73% a los 5 y a los 10 años de seguimiento respectivamente (figura 6A).
Prevalencia de insuficiencia de la válvula neoaórtica al inicio y al final del seguimiento. Diagrama de flechas que indica el número de pacientes que presentan progresión evolutiva en el grado de insuficiencia valvular neoaórtica (el número de pacientes que presentan progresión a insuficiencia valvular neoaórtica moderada o grave se expone en el lado izquierdo del diagrama).
Curvas de supervivencia actuarial de los pacientes analizados en el seguimiento. A: libres de insuficiencia valvular neoaórtica (IA) significativa (moderada/grave). B: libres de progresión de IA a grado moderado o grave (148 pacientes en estudio, excluidos los 4 pacientes que presentaban IA grave al inicio del seguimiento). C: libres de cirugía de la raíz neoaórtica sinusal y válvula neoaórtica.
En el subanálisis de los 148 pacientes que no presentaban IA grave en la primera valoración en la UCCA, la supervivencia libre de progresión de IA fue del 84 y el 76% a los 5 y a los 10 años respectivamente (figura 6B). Un dato muy relevante es la disminución de la incidencia de progresión de IA a partir de los 5 años de seguimiento (que corresponde aproximadamente a los 20 años de edad).
Durante el seguimiento en las UCCA, se trató a 6 pacientes con cirugía relacionada con la válvula neoaórtica, todos por IA grave: sintomática en 5 pacientes y por disfunción sistólica del ventrículo izquierdo en uno de ellos. En ningún caso por dilatación aislada de la RAO. Se realizaron 4 implantes de prótesis aórtica mecánica (en 2 de ellos se realizó cirugía mitral combinada) y 2 reparaciones de la válvula neoaórtica (uno de ellos con aortoplastia asociada). La supervivencia libre de cirugía de la válvula neoaórtica a los 5 y a los 10 años de seguimiento fue del 95,6 y el 92% (figura 6C).
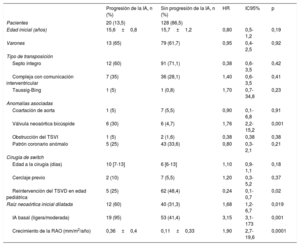
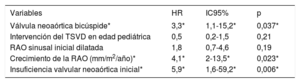
La progresión de la IA (tabla 3) se asoció con válvula bicúspide, IA basal, dilatación inicial de la RAO y crecimiento de la RAO, mientras que los pacientes que precisaron intervención quirúrgica en la infancia por complicaciones en el tracto de salida del ventrículo derecho presentaron menor progresión de IA. Fueron predictores independientes de progresión de IA (tabla 4) la válvula bicúspide (HR=3,3; IC95%, 1,1-15,2; p=0,037), IA basal (HR=5,9; IC95%, 1,6-59,2; p=0,006) y crecimiento de la RAO (HR=4,1; IC95%, 2-13,5; p=0,023).
Comparación de las características basales y el crecimiento de la RAO de los pacientes según presenten progresión de IA. Regresión de Cox univariada
| Progresión de la IA, n (%) | Sin progresión de la IA, n (%) | HR | IC95% | p | |
|---|---|---|---|---|---|
| Pacientes | 20 (13,5) | 128 (86,5) | |||
| Edad inicial (años) | 15,6±0,8 | 15,7±1,2 | 0,80 | 0,5-1,2 | 0,19 |
| Varones | 13 (65) | 79 (61,7) | 0,95 | 0,4-2,5 | 0,92 |
| Tipo de transposición | |||||
| Septo íntegro | 12 (60) | 91 (71,1) | 0,38 | 0,6-3,5 | 0,42 |
| Compleja con comunicación interventricular | 7 (35) | 36 (28,1) | 1,40 | 0,6-3,5 | 0,41 |
| Taussig-Bing | 1 (5) | 1 (0,8) | 1,70 | 0,7-34,8 | 0,23 |
| Anomalías asociadas | |||||
| Coartación de aorta | 1 (5) | 7 (5,5) | 0,90 | 0,1-6,8 | 0,91 |
| Válvula neoaórtica bicúspide | 6 (30) | 6 (4,7) | 1,76 | 2,2-15,2 | 0,001 |
| Obstrucción del TSVI | 1 (5) | 2 (1,6) | 0,38 | 0,38 | 0,38 |
| Patrón coronario anómalo | 5 (25) | 43 (33,6) | 0,80 | 0,3-2,1 | 0,21 |
| Cirugía de switch | |||||
| Edad a la cirugía (días) | 10 [7-13] | 6 [6-13] | 1,10 | 0,9-1,1 | 0,18 |
| Cerclaje previo | 2 (10) | 7 (5,5) | 1,20 | 0,3-5,2 | 0,37 |
| Reintervención del TSVD en edad pediátrica | 5 (25) | 62 (48,4) | 0,24 | 0,1-0,7 | 0,02 |
| Raíz neoaórtica inicial dilatada | 12 (60) | 40 (31,3) | 1,68 | 1,2-6,7 | 0,019 |
| IA basal (ligera/moderada) | 19 (95) | 53 (41,4) | 3,15 | 3,1-173 | 0,001 |
| Crecimiento de la RAO (mm/m2/año) | 0,36±0,4 | 0,11±0,33 | 1,90 | 2,7-19,6 | 0,0001 |
HR: hazard ratio; IA: insuficiencia valvular neoaórtica; IC95%: intervalo de confianza del 95%; RAO: raíz neoaórtica; TSVD: tracto de salida del ventrículo derecho; TSVI: tracto de salida del ventrículo izquierdo.
Los valores expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
Variables predictoras de progresión de la insuficiencia de la válvula neoaórtica. Regresión de Cox multivariada
| Variables | HR | IC95% | p |
|---|---|---|---|
| Válvula neoaórtica bicúspide* | 3,3* | 1,1-15,2* | 0,037* |
| Intervención del TSVD en edad pediátrica | 0,5 | 0,2-1,5 | 0,21 |
| RAO sinusal inicial dilatada | 1,8 | 0,7-4,6 | 0,19 |
| Crecimiento de la RAO (mm/m2/año)* | 4,1* | 2-13,5* | 0,023* |
| Insuficiencia valvular neoaórtica inicial* | 5,9* | 1,6-59,2* | 0,006* |
HR: hazard ratio; IC95%: intervalo de confianza del 95%; RAO: raíz neoaórtica; TSVD: tracto de salida del ventrículo derecho.
Un paciente falleció súbitamente durante el seguimiento. Se registraron 2 infartos de miocardio, ambos tras cirugía valvular aórtica y no hubo reintervención por causa coronaria. Se diagnosticaron 2 casos de endocarditis, ambas sobre la válvula neopulmonar, que no precisaron de cirugía y 4 arritmias (2 aleteos auriculares, una taquicardia supraventricular por reentrada nodular y una TV sostenida originada en el seno coronario derecho de la RAO que recurrió tras 2 ablaciones, por lo que se implantó un desfibrilador automático implantable, único en esta serie).
Al final del seguimiento, 13 pacientes (8,6%) fueron reintervenidos quirúrgicamente. A los 6 pacientes operados por IA, se sumaron 7 reintervenidos por disfunción del tracto de salida del ventrículo derecho.
Se sometieron a intervención percutánea 16 pacientes (10,5%), la mayoría por estenosis de ramas pulmonares (14 procedimientos). Un paciente recibió un implante de una prótesis pulmonar percutánea y otro un stent para tratar una recoartación de aorta.
DISCUSIÓNEl SA es la técnica de elección para la reparación de los pacientes con TGA, con una alta supervivencia a medio plazo, pero con complicaciones importantes en la evolución3,11, como son la dilatación de la RAO y la IA.
Se comienza a valorar un gran número de estos pacientes en las UCCA, pero hay pocos estudios que analicen la evolución de estas complicaciones en los adultos jóvenes5-7. Además, esta población todavía presenta cambios somáticos secundarios al crecimiento en los primeros años de seguimiento en las UCCA, lo que dificulta establecer si los cambios observados son patológicos.
En este sentido, se ha diseñado el primer estudio que analiza el crecimiento medio de la RAO indexado por superficie corporal en un grupo de pacientes en los que todavía se produce un cambio pondoestatural significativo e identifica variables predictoras de progresión de IA a partir de la valoración de los pacientes al inicio del seguimiento.
Dilatación de la raíz neoaórticaSe han descrito diferentes causas que pueden justificar la dilatación de la RAO. En primer lugar, histológicas12, pues se observa que la RAO presenta una capa de colágeno más delgada y con menor grado de organización, o anatómicas4 como la desproporción inicial entre aorta y pulmonar que se observa en pacientes con comunicación interventricular o en anomalías tipo Taussig-Bing. Por último, se ha atribuido a circunstancias inherentes a la cirugía como la denervación13 o la presencia de un ángulo aórtico14 excesivamente agudo, que puede motivar alteraciones en la dinámica del flujo aórtico e incrementar el estrés de pared arterial.
Aunque la dilatación de la RAO es un hecho reconocido tras la cirugía de SA, no hay consenso en su carácter progresivo. Mientras el grupo de Boston4 describe una dilatación hasta los 10 años de seguimiento, con estabilización posterior, otros trabajos refieren una dilatación progresiva15–17, aunque la mayoría de los estudios analizan a pacientes en edad pediátrica (< 15 años).
En el presente trabajo, se confirma una dilatación progresiva y significativa de la RAO, cuantificada en 0,14mm/m2/año (crecimiento medio en el intervalo de 0,23-0,25mm/año). La dilatación observada en nuestra serie es claramente superior a la que presentan los individuos sanos18 (0,08mm/año), aunque está lejos de la descrita en pacientes con enfermedad de Marfan19 (0,49mm/año), válvula bicúspide19 (0,42mm/año) o cirugía de Ross20 (0,43mm/año). Sin embargo, en un estudio reciente el crecimiento medio es de 0,63mm/año17, muy por encima del observado en nuestro estudio. Estas diferencias se pueden explicar por diferencias entre ambos estudios en la mediana de edad de los pacientes al final del seguimiento: 12,2 [1-39] frente a 19,5 [15-34] años respectivamente. Así, nuestros resultados son similares a los publicados por van der Bom et al.7, con un crecimiento de 0,28mm/año (población mayor de 17 años). En este trabajo los pacientes más jóvenes presentan un mayor crecimiento de la RAO, que se atenúa con la edad. También en nuestro estudio se observa una tendencia de mayor crecimiento de la RAO en los más jóvenes. Esto podría explicar por qué solo 2 de nuestros pacientes tuvieran al final del seguimiento un diámetro de la RAO> 50mm y que no se haya documentado ningún caso de rotura o disección de aorta. Además, en nuestra serie, no se intervino a ningún paciente de la RAO solo por el tamaño del aneurisma. Serán necesarios estudios que definan la progresión en pacientes más añosos y la influencia que puedan tener factores de riesgo como la hipertensión arterial en la evolución de la RAO.
Insuficiencia de la válvula neoaórtica: prevalencia, progresión y cirugíaLa IA es una complicación frecuente tras la cirugía de SA. En nuestro estudio, el 8,5% tenían una IA moderada o grave (3 de ellos intervenidos por este motivo) en su primera visita a la UCCA. Estos datos son comparables a los publicados en estudios pediátricos previos3,4,21 donde se muestra una prevalencia a los 15 años del 5,3-9,0%.
Al final del seguimiento, se confirmó una progresión del grado de IA en un 13,5%, con una supervivencia libre de IA moderada o grave del 79 y el 73% a los 5 y a los 10 años de seguimiento, resultados similares a los publicados por Lo Rito et al.8 y van der Bom et al.7. Por el contrario, Tobler et al.5 y Kempny et al.6 observaron en estudios realizados en población más adulta (medias de 21 y 25 años) que no había progresión de la IA pasados los 18 años y aunque la prevalencia de IA era alta (29-52%), el grado de la lesión valvular era fundamentalmente ligera. En nuestro estudio se observa una disminución de la progresión de la IA a partir de los 5 años de seguimiento (equivalente a 20 años de edad), que podría justificarse por la ralentización del crecimiento de la RAO descrita por van der Bom et al.7 en la población más adulta.
El presente trabajo identifica 3 causas que predicen la progresión de la IA: el crecimiento de la RAO, la válvula bicúspide y presencia de IA basal de cualquier grado en la primera visita a la UCCA. Aunque se ha descrito7 que la dilatación progresiva de la RAO no se asocia con la progresión de la IA, estudios con modelos mecánicos22 que simulan la RAO han demostrado que incrementos progresivos del diámetro de la unión sinotubular y sinusal aumentan el estrés en los velos aórticos, sobre todo en la vertiente aórtica, causando remodelado tisular con engrosamiento y calcificación del borde libre de los velos. Por lo tanto, la dilatación de la RAO causa IA por un mecanismo mixto (falta de coaptación por la dilatación y afección orgánica de los velos). En presencia de una válvula bicúspide, se añade con frecuencia al mecanismo asociado a la dilatación de la RAO un componente de prolapso o seudoprolapso, y aunque en estudios pediátricos4-21 la válvula bicúspide no se ha considerado como causa de IA, en un reciente trabajo14 con población adulta resulta un factor predictor importante.
Por último, la presencia de IA inicial identifica a los pacientes en riesgo de progresión a IA significativa8,21. En nuestra serie, tan solo 1 paciente (1,3%) que al inicio del seguimiento en las UCCA no tenía IA evolucionó a una insuficiencia moderada.
La supervivencia libre de cirugía de la válvula neoaórtica a los 5 y 10 años de seguimiento en las UCCA fue del 95,6 y el 92%, similar que en estudios previos5,6. Destacar que se realizó cirugía a todos los pacientes que contrajeron IA grave (tanto en edad pediátrica como después). La indicación fue por clínica o disfunción del ventrículo izquierdo y la baja tolerancia a esta situación hemodinámica adversa podría explicarse por la alta incidencia de disfunción diastólica y disminución de la contractilidad miocárdica (strain longitudinal) que se ha descrito en estos pacientes23,24.
Eventos clínicos en el seguimientoLa supervivencia del adulto joven tras la cirugía de SA es muy buena. En nuestro estudio hubo 1 fallecimiento y se registraron 2 infartos de miocardio, ambos tras cirugía de la válvula neoaórtica, sin otros eventos coronarios. Esta escasa incidencia concuerda con un metanálisis25 reciente, en el que se comunica una incidencia de complicaciones coronarias del 1,6%. Los resultados respaldan la recomendación actual26 de no realizar estudios de provocación de isquemia a pacientes asintomáticos.
La incidencia de reintervención quirúrgica en el adulto joven sigue siendo importante, del 8,6%, similar a las indicadas en otros centros5,6. A diferencia de lo que ocurre en el seguimiento pediátrico, la causa de la reintervención quirúrgica está equilibrada entre complicaciones de la RAO y válvula neoaórtica y disfunción del tracto de salida del ventrículo derecho. No obstante, el carácter progresivo de las lesiones de la neoválvula y la RAO sinusal y la influencia de factores de riesgo cardiovascular adquiridos en la edad adulta hacen presuponer un incremento de las indicaciones de cirugía por complicaciones de la RAO en el adulto de mayor edad.
LimitacionesEl estudio presenta limitaciones inherentes a su carácter retrospectivo. No obstante, el seguimiento de estos pacientes en las UCCA sigue las recomendaciones de la guía de cardiopatías congénitas del adulto26 y realiza una valoración clínica y ecocardiográfica anual.
Los estudios ecocardiográficos se realizaron por expertos en cardiopatías congénitas, pero en 2 centros diferentes y sin que se hicieran una revaluación posterior centralizada ni validación específica de la técnica en esta serie mediante tomografía computarizada o resonancia magnética.
En el análisis del crecimiento de la RAO se midió exclusivamente la porción sinusal de la aorta y no se dispuso de medidas del anillo o la unión senotubular. La cuantificación de la IA es semicuantitativa, siguiendo las recomendaciones actuales10. Estadísticamente, el relativamente bajo número de eventos de progresión de la insuficiencia valvular neoaórtica (n=20) supone una limitación en la fiabilidad del modelo multivariado, así como en la exactitud de los coeficientes obtenidos de este.
CONCLUSIONESEn el adulto joven con TGA intervenido mediante cirugía de SA, la dilatación de la RAO y la IA progresan a lo largo del seguimiento. La presencia de una válvula bicúspide, la IA inicial y el crecimiento de la RAO son predictores de progresión significativa en el grado de insuficiencia valvular. Serán necesarios estudios que definan si esta progresión continúa en pacientes de edades más avanzadas y la influencia que puedan tener factores de riesgo como la HTA en la evolución de las complicaciones relacionadas con la RAO y la válvula neoaórtica.
CONFLICTO DE INTERESESP. Gallego es editora asociada de Revista Española de Cardiología; se ha seguido el procedimiento editorial establecido en la Revista para garantizar la gestión imparcial del manuscrito.
- –
El switch de grandes arterias es la técnica quirúrgica de elección para los pacientes con TGA, y actualmente los adultos jóvenes representan una población emergente en las UCCA.
- –
La dilatación de la RAO es una complicación frecuente en la edad pediátrica, pero se desconoce si se produce una progresión patológica en una población que todavía presenta cambios somáticos por el crecimiento.
- –
La progresión de la IA en los pacientes adultos es controvertida, y es difícil identificar a los pacientes con mayor riesgo.
- –
La dilatación de la RAO continúa progresando en los adultos jóvenes, con un crecimiento medio estimado de 0,14mm/m2/año.
- –
La IA es una complicación frecuente y progresiva en los pacientes adultos tras la cirugía de SA, aunque la progresión se atenúa con el tiempo.
- –
El crecimiento de la RAO, una válvula bicúspide y la IA basal son predictores de progresión de la IA e identifica un grupo de pacientes que necesitará un seguimiento más frecuente de su valvulopatía.