El acceso transaxilar (ATx) se ha convertido en el acceso alternativo al transfemoral (ATF), más utilizado en pacientes sometidos a implante percutáneo de válvula aórtica (TAVI). El objetivo principal de este estudio es comparar la mortalidad total hospitalaria y a los 30 días de los pacientes incluidos en el registro español de TAVI a los que se trató por acceso ATx frente a ATF.
MétodosSe analizó a todos los pacientes incluidos en el registro español de TAVI tratados por ATx o ATF. Los eventos hospitalarios y a los 30 días de seguimiento se definieron según las recomendaciones de la Valve Academic Research Consortium. Se evaluó el impacto de la vía de acceso mediante emparejamiento por puntuación de propensión según las características clínicas y ecográficas.
ResultadosSe incluyó a 6.603 pacientes, 191 (2,9%) tratados por ATx y 6.412 con ATF. Después del ajuste (grupo de ATx, n=113; grupo de ATF, n=3.035), el éxito del dispositivo fue similar entre ambos grupos (el 94% en el grupo de ATx frente al 95% en el de ATF; p=0,95); sin embargo, se observó un incremento en la tasa de infarto agudo de miocardio (OR=5,3; IC95%, 2,0-13,8; p=0,001), complicaciones renales (OR=2,3; IC95%, 1,3-4,1; p=0,003) e implante de marcapasos (OR=1,6; IC95%, 1,01-2,6; p=0,03) en el grupo de ATx comparado con el de ATF. De mismo modo, la mortalidad hospitalaria y a los 30 días fueron superiores en el grupo de ATx (respectivamente, OR=2,2; IC95%, 1,04-4,6; p=0,039; y OR=2,3; IC95%, 1,2-4,5; p=0,01).
ConclusionesEl ATx se asocia con un aumento en la mortalidad total tanto hospitalaria como a los 30 días frente al ATF. Ante estos resultados, el ATx debe considerarse solo en caso de que el ATF no sea posible.
Palabras clave
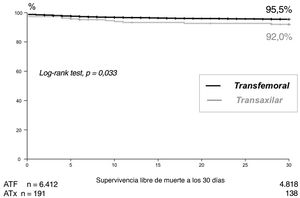
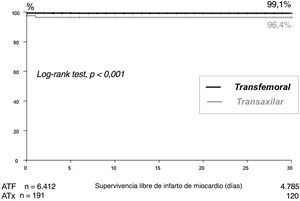
El implante percutáneo de válvula aórtica (TAVI) se ha convertido en una alternativa a la cirugía para el tratamiento de la valvulopatía aórtica degenerativa1,2. Desde los primeros estudios que evaluaron la seguridad y la eficacia del TAVI en pacientes con alto riesgo, el acceso más frecuente (70-80%) ha sido el acceso transfemoral (ATF), que sigue siendo el de preferencia para el TAVI3,4. Sin embargo, a pesar de la disminución en el tamaño del sistema liberador de las nuevas generaciones de válvulas, para un porcentaje de pacientes en los que no era factible el ATF se ha necesitado un acceso alternativo. Este fue exclusivamente transapical en la cohorte A del estudio PARTNER I5; sin embargo, en el estudio Corevalve6 el acceso fue transaxilar (ATx) o transaórtico. Actualmente, el ATF sigue sin ser posible en un 7-10% de los casos que se tratan con TAVI7,8. En este sentido, el ATx parece ser una buena alternativa al ATF9. En un metanálisis8 que incluyó a 10.528 pacientes, se mostró que la mortalidad hospitalaria y a los 30 días con el ATx y el ATF eran comparables. Por el contrario, en el seguimiento a medio-largo plazo de este estudio, la mortalidad fue superior con el ATx que con el ATF. Además, al comparar el ATx con otros accesos, como el transapical o el transaórtico, se observó un aumento de mortalidad en estos 2 últimos. En otro metanálisis en el que se comparó el ATx con el ATF en 4.500 pacientes, no se observaron diferencias en cuanto a mortalidad a los 30 días ni al año de seguimiento10. El objetivo principal de este estudio fue comparar los resultados en mortalidad temprana del TAVI según la vía de acceso, transfemoral o transaxilar, en una población de pacientes no seleccionados (figura 1 y figura 2).
El Registro Español de TAVI es un registro prospectivo, de carácter voluntario, promovido por la Asociación de Cardiología Intervencionista de la Sociedad Española de Cardiología, en el cual participan 45 centros españoles que realizan TAVI11. Los datos se registran en un base de datos dedicada y centralizada online, a la que se accede a través de la página web de la Asociación de Cardiología Intervencionista12. Para mantener la seguridad estricta y garantizar la validez de los datos, cada investigador tiene un nombre de usuario y una contraseña únicos para ingresar la información del paciente. También hay centros que utilizan su propia base de datos; para ello es necesario que se envíen los datos de forma segura en un formato específico. Todos los datos recopilados están anonimizados, y para la identificación de cada paciente se utiliza un código que cumple con la normativa vigente sobre la protección de datos. No existe un auditoria formal, pero la base de datos centralizada se revisa sistemática y periódicamente para identificar discordancias o ausencia de datos.
Se incluyó a todos los pacientes consecutivos tratados con TAVI incluidos en el registro desde 2009 hasta 2019. Se excluyó a los pacientes intervenidos por accesos transaórtico (56) o transapical (568). Los datos clínicos, de procedimiento y ecocardiográficos se recogieron prospectivamente y provienen de los servicios de cardiología y cirugía cardiaca.
Los eventos se definieron según las recomendaciones de la Valve Academic Research Consortium para los pacientes incluidos desde 2009 hasta 2013 y según las recomendaciones de la Valve Academic Research Consortium II para los incluidos desde 2014 hasta 201913,14. El seguimiento clínico se realizó mediante visitas clínicas o contacto telefónico en todos los centros. Todos los pacientes firmaron el consentimiento informado antes del procedimiento. Este estudio ha sido aprobado por el comité ético de referencia (21/385-E).
Análisis estadísticoLas variables cuantitativas se expresan como media±desviación estándar y las cualitativas, como frecuencias y porcentajes. Las comparaciones entre variables discretas se realizaron mediante la prueba de la χ2 o el estadístico exacto de Fisher. Para minimizar el sesgo de confusión, se evaluó el impacto de la vía de acceso de los procedimientos mediante emparejamiento por puntuación de propensión (opción k-nearest neighbors matching, PSmatch2, Stata, StataCorp, Estados Unidos) seleccionando, entre los pacientes tratados por ATx, a aquellos con probabilidad más parecida a los de ATF según las variables seleccionadas. Las variables seleccionadas para el análisis de propensión fueron las que presentaban diferencias estadísticamente significativas según la vía de acceso con p ≤ 0,05. Así se asegura que los grupos definidos por la vía de acceso son homogéneos en todas las variables consideradas: las que al inicio no mantenían diferencias estadísticamente significativas y las que sí las mantenían y se equiparan a través del emparejamiento. Solo se han considerado variables previas al procedimiento. Por eso para la puntuación de propensión no se tienen en cuenta variables angiográficas o hemodinámicas del procedimiento. Las puntuaciones de propensión se crean mediante el comando PSmatch2 de Stata con la opción de k-nearest neighbors matching, y se empareja a partir de los modelos logísticos, con una diferencia máxima de puntuaciones de propensión de 0,05 desviaciones estándar (caliper) y sin reemplazo. El método caliper define una región de soporte común y descarta las puntuaciones que están fuera del intervalo definido. No se hace un emparejamiento 1:M, sino que un paciente del grupo de acceso transaxilar se utiliza en varias ocasiones como coincidencia. De esta manera las puntuaciones globales de ambos grupos están equilibradas y la calidad promedio del emparejamiento aumenta y el sesgo disminuye. Es la metodología más adecuada con datos en los que la distribución de las puntuaciones de propensión es bastante diferente entre los grupos de emparejamiento. Se calculó la razón de probabilidad, odds ratio (OR), con su intervalo de confianza del 95% (IC95%). Se evaluó la colinealidad de la enfermedad vascular periférica (EVP) mediante el factor de inflación de la varianza, dado que se asoció con la vía de acceso por el método del comando collin (Stata). El valor de factor de inflación de la varianza fue de 1,8, es decir, no hay problemas de multicolinealidad graves al tener un valor de factor de inflación de la varianza<2. Se ha realizado un análisis de sensibilidad considerando EVP como el evento o enfermedad, y que el acceso transaxilar es el asociado con la EVP y el ATF con que no suceda la EVP. La clasificación tendría una sensibilidad del 75,43%. La curva de supervivencia se ha obtenido mediante el método de Kaplan-Meier. Para el análisis de los predictores de mortalidad, se construyó un modelo predictivo para estudiar las variables independientes relacionadas con el evento. Se introdujeron en el modelo las variables con p<0,05 en el análisis univariado o las consideradas clínicamente relevantes. El modelo predictivo se construyó con la estrategia escalonada por pasos hacia atrás, con una probabilidad de salida de 0,10. Se ha incluido la variable «año 2014» ya que, en un estudio previo que incluyó a pacientes del mismo registro11, se observó un incremento en la mortalidad de los pacientes tratados antes de 2014 (2009-2013) comparada con la de los pacientes intervenidos después, por lo que se consideró que esta variable era clínicamente relevante para este análisis. Los análisis estadísticos se realizaron con Stata 13 y SPSS 21.0 (IBM, Estados Unidos).
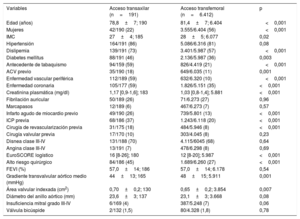
RESULTADOSCaracterísticas basalesSe incluyó a 6.603 pacientes, de los que se trató por ATx a 191 (2,9%) y por ATF a 6.412 (87,1%). Las características clínicas basales antes del emparejamiento se muestran en la tabla 1. Los pacientes tratados por ATx eran más jóvenes y con menor proporción de mujeres; sin embargo, tenían más factores de riesgo cardiovascular y más comorbilidades, como accidente cerebrovascular previo y enfermedad coronaria, y cifras de creatinina plasmática más elevadas que los pacientes tratados por ATF. Además, los pacientes con ATx tuvieron una puntación de EuroSCORE logístico mayor, un gradiente transvalvular aórtico medio menor y un área valvular indexada mayor. Las variables incluidas en el análisis de propensión fueron: edad, sexo femenino, historia de tabaquismo, índice de masa corporal, dislipemia, diabetes mellitus, accidente cerebrovascular previo, enfermedad coronaria, concentración plasmática de creatinina, EuroSCORE logístico y gradiente transvalvular aórtico medio previo al procedimiento. Las variables clínicas tras el emparejamiento se muestran en la tabla 2, en la que, mediante el análisis descriptivo de las variables tras el emparejamiento y los contrastes de hipótesis, se puede observar que ya no hay diferencias estadísticamente significativas entre los grupos de vía de acceso.
Características clínicas y ecocardiográficas basales de los pacientes incluidos en el estudio (antes del emparejamiento)
| Variables | Acceso transaxilar (n=191) | Acceso transfemoral (n=6.412) | p |
|---|---|---|---|
| Edad (años) | 78,8±7; 190 | 81,4±7; 6.404 | <0,001 |
| Mujeres | 42/190 (22) | 3.555/6.404 (56) | <0,001 |
| IMC | 27±4; 185 | 28±5; 6.077 | 0,02 |
| Hipertensión | 164/191 (86) | 5.086/6.316 (81) | 0,08 |
| Dislipemia | 139/191 (73) | 3.401/5.987 (57) | <0,001 |
| Diabetes mellitus | 88/191 (46) | 2.136/5.987 (36) | 0,003 |
| Antecedente de tabaquismo | 94/159 (59) | 826/4.419 (21) | <0,001 |
| ACV previo | 35/190 (18) | 649/6.035 (11) | 0,001 |
| Enfermedad vascular periférica | 112/189 (59) | 632/6.320 (10) | <0,001 |
| Enfermedad coronaria | 105/177 (59) | 1.826/5.151 (35) | <0,001 |
| Creatinina plasmática (mg/dl) | 1,17 [0,9-1,6]; 183 | 1,03 [0,8-1,4]; 5.881 | <0,001 |
| Fibrilación auricular | 50/189 (26) | 71/6.273 (27) | 0,96 |
| Marcapasos | 12/189 (6) | 467/6.273 (7) | 0,57 |
| Infarto agudo de miocardio previo | 49/190 (26) | 739/5.801 (13) | <0,001 |
| ICP previa | 68/186 (37) | 1.243/6.118 (20) | <0,001 |
| Cirugía de revascularización previa | 31/175 (18) | 484/5.946 (8) | <0,001 |
| Cirugía valvular previa | 17/170 (10) | 303/4.045 (8) | 0,23 |
| Disnea clase III-IV | 131/188 (70) | 4.115/6045 (68) | 0,64 |
| Angina clase III-IV | 13/191 (7) | 478/6.298 (8) | 0,69 |
| EuroSCORE logístico | 16 [8-26]; 180 | 12 [8-20]; 5.987 | <0,001 |
| Alto riesgo quirúrgico | 84/186 (45) | 1.689/6.260 (27) | <0,001 |
| FEVI (%) | 57,0±14; 186 | 57,0±14; 6.178 | 0,54 |
| Gradiente transvalvular aórtico medio (mmHg) | 44±13; 165 | 48±15; 5.911 | 0,001 |
| Área valvular indexada (cm2) | 0,70±0,2; 130 | 0,65±0,2; 3.854 | 0,007 |
| Diámetro del anillo aórtico (mm) | 23,6±3; 137 | 23,1±3; 3.668 | 0,08 |
| Insuficiencia mitral grado III-IV | 6/169 (4) | 387/5.248 (7) | 0,06 |
| Válvula bicúspide | 2/132 (1,5) | 80/4.328 (1,8) | 0,78 |
ACV: accidente cerebrovascular; FEVI: fracción de eyección del ventrículo izquierdo; ICP: intervención coronaria percutánea; IMC: índice de masa corporal.
Los valores expresan n/N (%), media±desviación estándar o mediana [intervalo intercuartílico]; n total.
Variables clínicas y ecográficas utilizadas para el emparejamiento (después del emparejamiento)
| Variables | Acceso transaxilar (n=113) | Acceso transfemoral (n=3.035) | p |
|---|---|---|---|
| Edad (años) | 78,1±6,7 | 77,5±6,8 | 0,54 |
| Mujeres, % | 22,1 | 25,0 | 0,6 |
| IMC | 27,3±5,1 | 27,5±4,5 | 0,79 |
| Dislipemia, % | 70 | 70 | 1 |
| Diabetes mellitus, % | 46,7 | 47,9 | 0,85 |
| Antecedentes de tabaquismo, % | 61 | 59 | 0,75 |
| ACV previo, % | 22,9 | 22,9 | 1 |
| Enfermedad coronaria, % | 59,0 | 62,7 | 0,56 |
| Creatinina plasmática (mg/dl) | 1,31±0,7 | 1,35±0,7 | 0,67 |
| EuroSCORE logístico | 19,5±14,2 | 19,6±11,4 | 0,94 |
| Gradiente transvalvular aórtico medio (mmHg) | 44,6±12,7 | 44,2±15,0 | 0,75 |
ACV: accidente cerebrovascular; IMC: índice de masa corporal.
Los valores expresan n o media±desviación estándar.
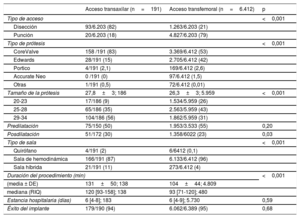
El ATx se realizó en la gran mayoría de los casos (82%) mediante disección quirúrgica, que solo se utilizó en un 21% de los ATF. Con respecto al tipo de prótesis, en el grupo ATx fue el 83% autoexpandible y el 15% expandible con balón, comparado con un 53% de prótesis autoexpandibles y un 42% de expandibles con balón en el grupo ATF. En el grupo de ATx, el procedimiento se realizó en una sala híbrida en el 11%, frente al 4% en el grupo ATF. La tasa de posdilatación y la duración del procedimiento fueron significativamente mayores en el grupo de ATx. El éxito del implante fue similar en ambos grupos (tabla 3).
Características del procedimiento
| Acceso transaxilar (n=191) | Acceso transfemoral (n=6.412) | p | |
|---|---|---|---|
| Tipo de acceso | <0,001 | ||
| Disección | 93/6.203 (82) | 1.263/6.203 (21) | |
| Punción | 20/6.203 (18) | 4.827/6.203 (79) | |
| Tipo de prótesis | <0,001 | ||
| CoreValve | 158 /191 (83) | 3.369/6.412 (53) | |
| Edwards | 28/191 (15) | 2.705/6.412 (42) | |
| Portico | 4/191 (2,1) | 169/6.412 (2,6) | |
| Accurate Neo | 0 /191 (0) | 97/6.412 (1,5) | |
| Otras | 1/191 (0,5) | 72/6.412 (0,01) | |
| Tamaño de la prótesis | 27,8±3; 186 | 26,3±3; 5.959 | <0,001 |
| 20-23 | 17/186 (9) | 1.534/5.959 (26) | |
| 25-28 | 65/186 (35) | 2.563/5.959 (43) | |
| 29-34 | 104/186 (56) | 1.862/5.959 (31) | |
| Predilatación | 75/150 (50) | 1.953/3.533 (55) | 0,20 |
| Posdilatación | 51/172 (30) | 1.358/6022 (23) | 0,03 |
| Tipo de sala | <0,001 | ||
| Quirófano | 4/191 (2) | 6/6412 (0,1) | |
| Sala de hemodinámica | 166/191 (87) | 6.133/6.412 (96) | |
| Sala híbrida | 21/191 (11) | 273/6.412 (4) | |
| Duración del procedimiento (min) | <0,001 | ||
| (media ± DE) | 131±50; 138 | 104±44; 4.809 | |
| mediana (RIQ) | 120 [93-158]; 138 | 93 [71-120]; 480 | |
| Estancia hospitalaria (días) | 6 [4-8]; 183 | 6 [4-9]; 5.730 | 0,59 |
| Éxito del implante | 179/190 (94) | 6.062/6.389 (95) | 0,68 |
DE: desviación estándar; RIQ: intervalo intercuartílico.
Los valores expresan n/N (%) o media±desviación estándar o mediana [intervalo intercuartílico]; n total.
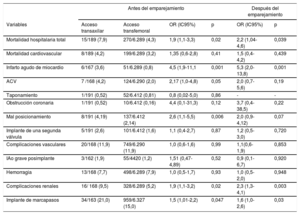
Con respecto a los eventos hospitalarios, la tasa de muerte por cualquier causa (OR=2,2; IC95%, 1,04-4,6; p=0,039), el infarto agudo de miocardio (OR=5,3; IC95%, 2,0-13,8; p=0,001), las complicaciones renales en general (OR=2,3; 1,3-4,1; p=0,003) y la necesidad de marcapasos (OR=1,56; 1,0-2,6; p=0,03) fueron significativamente mayores en el grupo de ATx tanto antes como después de emparejamiento (tabla 4). Por el contrario, no se objetivaron diferencias entre los grupos en las tasas de accidente cerebrovascular, complicaciones vasculares o hemorragias.
Eventos hospitalarios
| Antes del emparejamiento | Después del emparejamiento | |||||
|---|---|---|---|---|---|---|
| Variables | Acceso transaxilar | Acceso transfemoral | OR (IC95%) | p | OR (IC95%) | p |
| Mortalidad hospitalaria total | 15/189 (7,9) | 270/6.289 (4,3) | 1,9 (1,1-3,3) | 0,02 | 2,2 (1,04-4,6) | 0,039 |
| Mortalidad cardiovascular | 8/189 (4,2) | 199/6.289 (3,2) | 1,35 (0,6-2,8) | 0,41 | 1,5 (0,4-4,2) | 0,439 |
| Infarto agudo de miocardio | 6/167 (3,6) | 51/6.289 (0,8) | 4,5 (1,9-11,1 | 0,001 | 5,3 (2,0-13,8) | 0,001 |
| ACV | 7 /168 (4,2) | 124/6.290 (2,0) | 2,17 (1,0-4,8) | 0,05 | 2,0 (0,7- 5,6) | 0,19 |
| Taponamiento | 1/191 (0,52) | 52/6.412 (0,81) | 0,8 (0,02-5,0) | 0,86 | - | - |
| Obstrucción coronaria | 1/191 (0,52) | 10/6.412 (0,16) | 4,4 (0,1-31,3) | 0,12 | 3,7 (0,4-38,5) | 0,22 |
| Mal posicionamiento | 8/191 (4,19) | 137/6.412 (2,14) | 2,6 (1,1-5,5) | 0,006 | 2,0 (0,9-4,12) | 0,07 |
| Implante de una segunda válvula | 5/191 (2,6) | 101/6.412 (1,6) | 1,1 (0,4-2,7) | 0,87 | 1,2 (0,5-3,0) | 0,720 |
| Complicaciones vasculares | 20/168 (11,9) | 749/6.290 (11,9) | 1,0 (0,6-1,6) | 0,99 | 1,1(0,6-1,9) | 0,853 |
| IAo grave posimplante | 3/162 (1,9) | 55/4420 (1,2) | 1,51 (0,47-4,89) | 0,52 | 0,9 (0,1-6,7) | 0,920 |
| Hemorragia | 13/168 (7,7) | 498/6.289 (7,9) | 1,0 (0,5-1,7) | 0,93 | 1,0 (0,5-2,0) | 0,948 |
| Complicaciones renales | 16/ 168 (9,5) | 328/6.289 (5,2) | 1,9 (1,1-3,2) | 0,02 | 2,3 (1,3-4,1) | 0,003 |
| Implante de marcapasos | 34/163 (21,0) | 959/6.327 (15,0) | 1,5 (1,01-2,2) | 0,047 | 1,6 (1,0-2,6) | 0,03 |
ACV: accidente cerebrovascular; IAo: insuficiencia aórtica; IC95%: intervalo de confianza del 95%; OR: odds ratio.
Los valores expresan n/N (%).
En el seguimiento a los 30 días (el 80% de los pacientes), la tasa de mortalidad por cualquier causa fue significativamente mayor en el grupo de ATx (el 10,4 frente al 5,5%; tras el emparejamiento, OR=2,3; IC95%, 1,2-4,5; p=0,01).
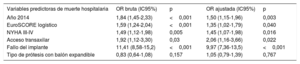
Se realizó un análisis multivariado introduciendo en el modelo variables previas y posteriores al procedimiento. Los predictores independientes de mortalidad hospitalaria (tabla 5) son haber sido tratado antes de 2014, el EuroSCORE logístico, una clase funcional de la New York Heart Association III-IV, el ATx y el fallo del implante.
Predictores de la mortalidad hospitalaria
| Variables predictoras de muerte hospitalaria | OR bruta (IC95%) | p | OR ajustada (IC95%) | p |
|---|---|---|---|---|
| Año 2014 | 1,84 (1,45-2,33) | <0,001 | 1,50 (1,15-1,96) | 0,003 |
| EuroSCORE logístico | 1,59 (1,24-2,04) | <0,001 | 1,35 (1,02-1,79) | 0,040 |
| NYHA III-IV | 1,49 (1,12-1,98) | 0,005 | 1,45 (1,07-1,98) | 0,016 |
| Acceso transaxilar | 1,92 (1,12-3,30) | 0,03 | 2,06 (1,16-3,66) | 0,022 |
| Fallo del implante | 11,41 (8,58-15,2) | <0,001 | 9,97 (7,36-13,5) | <0,001 |
| Tipo de prótesis con balón expandible | 0,83 (0,64-1,08) | 0,157 | 1,05 (0,79-1,39) | 0,767 |
IC95%: intervalo de confianza del 95%; NYHA: clase funcional de la New York Heart Association; OR: odds ratio.
Los principales hallazgos de este estudio son que, en una población emparejada por puntuación de propensión, el ATx en comparación con el ATF se asocia con una mayor mortalidad tanto hospitalaria como a los 30 días. Además, el ATx se asocia con mayores tasas de infarto agudo de miocardio, complicaciones renales totales y necesidad de marcapasos.
Las implicaciones más importantes de estos hallazgos están relacionadas con los pacientes a quienes se considera candidatos a ATx. El ATx debe considerarse exclusivamente cuando el procedimiento no es factible por ATF, no como una alternativa. De hecho, la evidencia científica de los beneficios del TAVI en pacientes con riesgo intermedio y riesgo bajo solo se ha obtenido con TAVI por ATF1,2,15.
Hay datos controvertidos sobre la seguridad del ATx comparado con el ATF. En un metanálisis que incluyó a 4.504 pacientes, no se encontraron diferencias entre esos accesos en eventos o mortalidad al año de seguimiento8. Del mismo modo, un estudio multicéntrico16 que incluyó a 21.611 pacientes del registro francés de TAVI, comparó la evolución clínica de 19.995 (92,5%) pacientes tratados por ATF y 1.616 (7,5%) con acceso periférico no transfemoral mediante un análisis de propensión preespecificado. En ese estudio no se encontraron diferencias en mortalidad ni en otros eventos, excepto un aumento de complicaciones vasculares mayores en el grupo de ATF. Las diferencias en los hallazgos de ese estudio pueden explicarse por diferencias en el diseño y el tipo de población incluida. A diferencia de nuestro estudio, en el registro francés se unen los resultados de 2 tipos de accesos, el ATx y el acceso transcarótideo; además, el periodo de tiempo de inclusión fue más corto.
Otro estudio que evaluó el impacto en la mortalidad en los pacientes tratados mediante diferentes accesos (ATx, ATF, transaórtico o transapical), es un metanálisis8 que incluyó a 10.528 pacientes y observó que la mortalidad total temprana (hospitalaria y a los 30 días) fue similar entre ATx y ATF. Sin embargo, el seguimiento a medio-largo plazo (6 meses-3 años) de este estudio mostró un aumento en la mortalidad y las tasas de infarto y accidente cerebrovascular en el grupo con ATx comparado con el grupo de ATF. Estos hallazgos están en consonancia con los del presente estudio, en el que se observa un incremento de la tasa de infarto de miocardio y una tendencia a mayor frecuencia de accidentes cerebrovasculares. Consideramos que, a pesar de haber emparejado todas las variables que diferían entre las poblaciones, incluida la enfermedad coronaria, y haber utilizado además una prueba estadística que minimiza el sesgo de selección, estas poblaciones no se pueden emparejar por EVP, ya que es una variable relacionada con el acceso. Sin embargo, el 41% del grupo de ATx no presentaba enfermedad periférica, por lo que a priori se podría utilizar ambos accesos. Esto hace que no haya problemas graves de colinealidad que invaliden este análisis, pero a pesar de esto, hay mayor frecuencia de EVP en el grupo de ATx (el 59 frente al 10%). Este aumento de EVP puede influir en el aumento de mortalidad, ya que se ha descrito que la presencia de enfermedad periférica se asocia con un incremento de la mortalidad de los pacientes tratados con TAVI17. Además, estos pacientes presentan mayor carga ateroesclerótica, que es el principal predictor de riesgo de eventos cardiovasculares y muerte, independientemente de que la enfermedad ateroesclerótica sea obstructiva o no18.
A su vez, una mayor carga ateroesclerótica puede estar relacionada con el incremento de la insuficiencia renal en los pacientes tratados con ATx que se observa en este estudio. Se ha descrito que la carga ateroesclerótica localizada en la aorta torácica se asocia con un incremento de insuficiencia renal en los pacientes tratados con TAVI, otro factor asociado con la mortalidad19,20. Se postula que otra posible causa de incremento de la insuficiencia renal podría ser un aumento de la cantidad de contraste empleada para posicionar la válvula, ya que el ángulo entre la arteria subclavia y el cayado, sobre todo en aortas horizontales, puede dificultar el posicionamiento en el ATx, especialmente si es del lado derecho. Además, la mayoría de las prótesis utilizadas con este acceso son autoexpandibles, cuyo posicionamiento es más lento y controlado, lo cual podría explicar la mayor duración de los procedimientos y el mayor consumo de contraste.
En el presente estudio se observó un aumento de la tasa de marcapasos en el grupo de ATx, en consonancia con los resultados del metanálisis de Takagi et al. Consideramos que el aumento de la tasa de marcapasos observado en nuestro estudio, al igual que en otros previos, está más relacionado con el tipo de válvula que con el tipo de acceso. En el presente estudio, se empleó una válvula autoexpandible en el 85% del grupo de ATx frente al 55% del grupo de ATF21–23.
Cada vez hay más datos sobre la seguridad y la factibilidad de un ATx totalmente percutáneo24. En este sentido, en un estudio que incluyó a 100 pacientes consecutivos tratados con TAVI por ATx, el 85% de los procedimientos se realizó por la arteria subclavia izquierda y el resto, por la derecha. El éxito del procedimiento fue del 95%. Ningún paciente sufrió una complicación mayor en el punto de acceso. En el estudio se señala la importancia de la curva de aprendizaje para este acceso, ya que es más laborioso que el ATF. Esto, unido a que generalmente se utiliza poco en nuestro país (el 3,3% de los procedimientos de TAVI en España), puede haber contribuido a los resultados clínicos del presente estudio25.
El ATx percutáneo es menos invasivo que el quirúrgico y, por lo tanto, más comparable al ATF; además, no hay estudios que comparen específicamente ambos accesos percutáneos, por lo que no existe evidencia para recomendar este tipo de acceso para pacientes en los que el ATF sea factible.
LimitacionesSe trata de un estudio observacional, con un tamaño de muestra pequeño y un periodo de seguimiento corto. Los pacientes incluidos en este estudio provienen del registro español de TAVI, si bien el 100% de los centros de alto volumen (> 100 TAVI/año) y el 92% de los centros de moderado volumen (50-100 TAVI/año) que realizan TAVI en nuestro país participan en este registro, no están todos, por lo que es posible que los resultados puedan estar condicionados por los centros con mayor experiencia en esta técnica. Además, se trata de un registro cuyos datos no se someten a una auditoría externa. No se recogen todas las variables del 100% de los pacientes, aunque la gran mayoría de las variables están recogidas en más del 90% de los casos. No se ha registrado en qué porcentaje de los casos el ATx fue izquierdo o derecho, lo cual puede influir en los resultados, dado que anatómicamente el acceso derecho podría ser más dificultoso. En el caso de las hemorragias y la insuficiencia renal, se trata de valores totales y no se dispone del grado o las causas, por lo que estos datos deben tomarse con precaución. Con respecto a la definición de infarto que incluye la determinación de biomarcadores, no se puede asegurar que se recogieran por sistema de todos los pacientes. Además, debido a la naturaleza no aleatorizada de este estudio, se ha intentado minimizar los sesgos de selección y confusión, aunque puede permanecer el sesgo oculto debido a las influencias de factores de confusión no medidos. En este sentido, a pesar de los ajustes por las variables de confusión conocidas, cabe la posibilidad de que otros aspectos no valorados fueran también más desfavorables en los pacientes seleccionados para el ATx.
CONCLUSIONESSe trata del primer estudio que, en una población ajustada mediante emparejamiento por puntuación de propensión, muestra que emplear el ATx se asoció con un aumento de la mortalidad hospitalaria y a los 30 días en comparación con el ATF y permaneció asociado de manera independiente tras ajustar por potenciales variables de confusión. Además, se observa un aumento de las tasas de infarto agudo de miocardio, complicaciones renales y necesidad de marcapasos.
FINANCIACIÓNLa Asociación de Cardiología Intervencionista de la Sociedad Española de Cardiología financia el mantenimiento y la explotación de la base de datos.
CONTRIBUCIÓN DE LOS AUTORESP. Jiménez-Quevedo: contribución a la concepción y el diseño, adquisición de datos, su análisis e interpretación, redacción del artículo y revisión crítica de su contenido intelectual. L. Nombela-Franco, E. Muñoz-García, R. del Valle-Fernández, R. Trillo, J.M. de la Torre Hernández, L. Salido, J. Elizaga, S. Ojeda, J. Sánchez Gila, B. García del Blanco, A. Berenguer, G. Lasa-Larraya, C. Urbano Carrillo, A. Albarrán, R. Ruiz-Salmeron, J. Moreu, L. Gheorghe, D. Arzamendi, G. Yanes-Bowden, J. Diaz, I. Pérez-Moreiras, M. Artaiz, B. Vaquerizo, I. Cruz-Gonzalez, V. Ruiz-Quevedo, R. Blanco-Mata, J.A. Baz, M. Villa, Á. Ortiz de Salazar, V. Tascón-Quevedo, S. Casellas y R. Moreno: contribución a la adquisición de datos y revisión crítica del contenido intelectual del manuscrito.
CONFLICTO DE INTERESESR. Trillo es proctor de válvulas transcateter para Medtonic y Boston Scientific. R. Moreno es proctor para Boston, Abbott, Biosensors/NVT; ha recibido honorarios por charlas y consultoría de Edwards, Boston, Abbott y Medtronic; ha recibido honorarios por investigación de Edwards, Abbott, Boston y Medtronic. L. Nombela-Franco es proctor para Abbott; ha participado y recibido honorarios por charlas de Edwards Lifesciences. J.M. de la Torre Hernández ha recibido honorarios por consultoría y por presentaciones de Medtronic, Abbott y Boston Scientific. I. Cruz-Gonzalez es proctor para Medtronic. D. Arzamendi es proctor para Abbott. El resto de los autores no tienen conflictos de intereses.
- –
Los resultados clínicos del acceso transaxilar frente al acceso transfemoral en pacientes tratados con TAVI son discrepantes.
- –
La mayoría de los registros o metanálisis no muestran diferencias en mortalidad entre estos 2 tipos de acceso, excepto un metanálisis que describe un incremento de mortalidad, infarto agudo de miocardio y accidente cerebrovascular en el seguimiento a medio-largo plazo.
- –
Es el primer estudio que demuestra un aumento de mortalidad por todas las causas hospitalaria y a los 30 días en los pacientes tratados con TAVI por acceso transaxilar frente al acceso transfemoral en una población emparejada.
- –
El acceso transaxilar, además, se asocia con un incremento de las tasas de infarto agudo de miocardio, insuficiencia renal y necesidad de marcapasos.
Los autores desean agradecer a la Dra. María José Pérez-Vizcayno por su ayuda en la revisión de los datos y en el análisis estadístico. Los autores están muy agradecidos a todas las personas involucradas y todos los centros que participan en el registro español de TAVI.