En los últimos años, se ha demostrado que los inhibidores del cotransportador de sodio-glucosa de tipo 2 (iSGLT2) tienen significativos efectos favorables en la insuficiencia cardiaca (IC) de pacientes con IC y fracción de eyección reducida (IC-FEr), independientemente de la presencia de diabetes mellitus tipo 2 (DM2)1. Se ha observado que los agonistas del receptor del péptido similar al glucagón tipo 1 (ar-GLP-1) también reducen significativamente las hospitalizaciones por IC de los pacientes con DM2, según un metanálisis de los ensayos clínicos fundamentales, aunque estos efectos favorables no se observaron en cada uno de los ensayos clínicos por separado2. Además, los datos proporcionados por los estudios observacionales son bastante limitados y controvertidos3.
Se llevó a cabo un estudio prospectivo, multicéntrico y en la práctica clínica en pacientes con DM2 e IC-FEr tratados con semaglutida (grupo sema-reducido) y sin semaglutida u otro ar-GLP-1 (grupo control-reducido) y seguidos durante 52 semanas entre junio de 2019 y mayo de 2023. El diagnóstico de IC-FEr se estableció según la guía de la Sociedad Europea de Cardiología de 20214.
En cada evaluación se recogieron datos sobre múltiples variables clínicas. El objetivo primario fue el número de episodios de IC (una combinación de visitas a los servicios de urgencias hospitalarios, ingresos hospitalarios y visitas ambulatorias no programadas). Los objetivos secundarios fueron: cada uno de los componentes del objetivo primario, la muerte cardiovascular, la mortalidad por cualquier causa, los ingresos hospitalarios por cualquier causa, la aparición de una nefropatía o su empeoramiento y una diferencia ≥ 5 puntos en el Cuestionario de Miocardiopatía de Kansas City (KCCQ) entre la puntuación total de síntomas al inicio y tras 52 semanas de seguimiento.
Para emparejar uno a uno a cada paciente de cada grupo, se utilizó un análisis de propensiones (AP). Se evaluó la idoneidad del AP con la diferencia estandarizada (se consideró desequilibrio importante una diferencia estandarizada > 10% entre las variables basales). Para estimar la probabilidad de iniciar el tratamiento con semaglutida, se utilizó un modelo de regresión logística. Se calculó el coeficiente de correlación de Pearson para estimar las correlaciones lineales. Para evaluar la relación entre el tratamiento y los resultados del estudio, se utilizaron regresiones logísticas de efecto mixto y se ajustaron por las variables de confusión.
Se incluyo a un total de 202 pacientes en el grupo sema-reducido y 162 en el grupo control-reducido. Tras el AP, se incluyó a 122 pacientes en cada grupo. Al cabo de 52 semanas, 104 pacientes (85,2%) habían recibido 1,00 mg semanal de semaglutida. En la tabla 1 se describen las características basales.
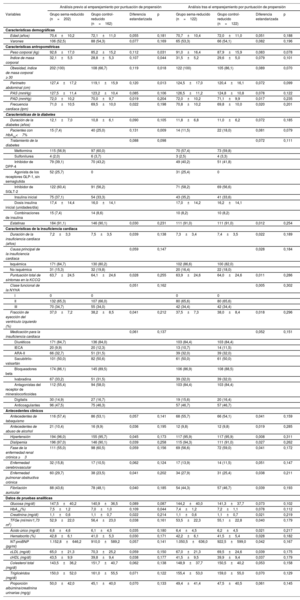
Características basales sociodemográficas, clínicas y terapéuticas: análisis de emparejamiento por puntuación de propensión
| Análisis previo al emparejamiento por puntuación de propensión | Análisis tras el emparejamiento por puntuación de propensión | |||||||
|---|---|---|---|---|---|---|---|---|
| Variables | Grupo sema-reducido (n=202) | Grupo control-reducido (n=162) | Diferencia estandarizada | p | Grupo sema-reducido (n=122) | Grupo control-reducido (n=122) | Diferencia estandarizada | p |
| Características demográficas | ||||||||
| Edad (años) | 70,4±10,2 | 72,1±11,0 | 0,055 | 0,181 | 70,7±10,4 | 72,0±11,0 | 0,051 | 0,188 |
| Varones | 106 (52,5) | 88 (54,3) | 0,077 | 0,169 | 65 (53,3) | 66 (54,1) | 0,082 | 0,196 |
| Características antropométricas | ||||||||
| Peso corporal (kg) | 92,6±17,0 | 85,2±15,2 | 0,112 | 0,031 | 91,0±16,4 | 87,9±15,9 | 0,083 | 0,078 |
| Índice de masa corporal | 32,1±5,5 | 28,8±5,3 | 0,107 | 0,044 | 31,5±5,2 | 29,6±5,0 | 0,079 | 0,101 |
| Obesidad, índice de masa corporal ≥ 30 | 202 (100) | 108 (66,7) | 0,119 | 0,018 | 122 (100) | 105 (86,1) | 0,089 | 0,070 |
| Perímetro abdominal (cm) | 127,4±17,2 | 119,1±15,9 | 0,120 | 0,013 | 124,5±17,0 | 120,4±16,1 | 0,072 | 0,099 |
| PAS (mmHg) | 127,5±11,4 | 123,2±10,4 | 0,085 | 0,106 | 126,5±11,2 | 124,8±10,8 | 0,078 | 0,122 |
| PAD (mmHg) | 72,0±10,2 | 70,0±9,7 | 0,019 | 0,204 | 72,0±10,2 | 71,1±9,9 | 0,017 | 0,235 |
| Frecuencia cardiaca (lpm) | 71,0±10,5 | 69,5±10,0 | 0,022 | 0,198 | 70,8±10,2 | 69,8±10,0 | 0,020 | 0,201 |
| Características de la diabetes | ||||||||
| Duración de la diabetes (años) | 12,1±7,0 | 10,8±6,1 | 0,090 | 0,105 | 11,8±6,8 | 11,0±6,2 | 0,072 | 0,185 |
| Pacientes con HbA1c<7% | 15 (7,4) | 40 (25,0) | 0,131 | 0,009 | 14 (11,5) | 22 (18,0) | 0,081 | 0,079 |
| Tratamiento de la diabetes | 0,088 | 0,098 | 0,072 | 0,111 | ||||
| Metformina | 115 (56,9) | 97 (60,0) | 70 (57,4) | 73 (59,8) | ||||
| Sulfonilurea | 4 (2,0) | 6 (3,7) | 3 (2,5) | 4 (3,3) | ||||
| Inhibidor de DPP-4 | 79 (39,1) | 70 (43,2) | 49 (40,2) | 51 (41,8) | ||||
| Agonista de los receptores GLP-1, sin semaglutida | 52 (25,7) | 0 | 31 (25,4) | 0 | ||||
| Inhibidor de SGLT-2 | 122 (60,4) | 91 (56,2) | 71 (58,2) | 69 (56,6) | ||||
| Insulina inicial | 75 (37,1) | 54 (33,3) | 43 (35,2) | 41 (33,6) | ||||
| Dosis insulina inicial (unidades/día) | 17,4±14,4 | 16,0±14,1 | 17,0±14,2 | 16,2±14,1 | ||||
| Combinaciones de insulina | 15 (7,4) | 14 (8,6) | 10 (8,2) | 10 (8,2) | ||||
| Estatinas | 184 (91,1) | 146 (90,1) | 0,030 | 0,231 | 111 (91,0) | 111 (91,0) | 0,012 | 0,254 |
| Características de la insuficiencia cardiaca | ||||||||
| Duración de la insuficiencia cardiaca (años) | 7,2±3,3 | 7,5±3,5 | 0,039 | 0,138 | 7,3±3,4 | 7,4±3,5 | 0,022 | 0,189 |
| Causa principal de la insuficiencia cardiaca | 0,059 | 0,147 | 0,028 | 0,184 | ||||
| Isquémica | 171 (84,7) | 130 (80,2) | 102 (86,6) | 100 (82,0) | ||||
| No isquémica | 31 (15,3) | 32 (19,8) | 20 (16,4) | 22 (18,0) | ||||
| Puntuación total de síntomas en la KCCQ | 63,7±24,5 | 64,1±24,6 | 0,028 | 0,255 | 63,9±24,6 | 64,0±24,6 | 0,011 | 0,286 |
| Clase funcional de la NYHA | 0,051 | 0,162 | 0,005 | 0,302 | ||||
| I | 0 | 0 | 0 | 0 | ||||
| II | 132 (65,3) | 107 (66,0) | 80 (65,6) | 80 (65,6) | ||||
| III | 70 (34,7) | 55 (34,0) | 42 (34,4) | 42 (34,4) | ||||
| Fracción de eyección del ventrículo izquierdo (%) | 37,0±7,2 | 38,2±8,5 | 0,041 | 0,212 | 37,5±7,3 | 38,0±8,4 | 0,018 | 0,296 |
| Medicación para la insuficiencia cardiaca | 0,061 | 0,137 | 0,052 | 0,151 | ||||
| Diuréticos | 171 (84,7) | 136 (84,0) | 103 (84,4) | 103 (84,4) | ||||
| IECA | 20 (9,9) | 20 (12,3) | 13 (10,7) | 14 (11,5) | ||||
| ARA-II | 66 (32,7) | 51 (31,5) | 39 (32,0) | 39 (32,0) | ||||
| Sacubitrilo-valsartán | 101 (50,0) | 82 (50,6) | 61 (50,0) | 61 (50,0) | ||||
| Bloqueadores beta | 174 (86,1) | 145 (89,5) | 106 (86,9) | 108 (88,5) | ||||
| Ivabradina | 67 (33,2) | 51 (31,5) | 39 (32,0) | 39 (32,0) | ||||
| Antagonistas del receptor de mineralocorticoides | 112 (55,4) | 94 (58,0) | 103 (84,4) | 103 (84,4) | ||||
| Digitalis | 30 (14,9) | 27 (16,7) | 19 (15,6) | 20 (16,4) | ||||
| Anticoagulantes | 96 (47,5) | 75 (46,3) | 57 (46,7) | 57 (46,7) | ||||
| Antecedentes clínicos | ||||||||
| Antecedentes de tabaquismo | 116 (57,4) | 86 (53,1) | 0,057 | 0,141 | 68 (55,7) | 66 (54,1) | 0,041 | 0,159 |
| Antecedentes de abuso de alcohol | 21 (10,4) | 16 (9,9) | 0,036 | 0,195 | 12 (9,8) | 12 (9,8) | 0,019 | 0,285 |
| Hipertensión | 194 (96,0) | 155 (95,7) | 0,045 | 0,173 | 117 (95,9) | 117 (95,9) | 0,008 | 0,311 |
| Dislipemia | 196 (97,0) | 146 (90,1) | 0,039 | 0,258 | 115 (94,3) | 111 (91,0) | 0,027 | 0,262 |
| Fase de la enfermedad renal crónica ≥3 | 111 (55,0) | 98 (60,5) | 0,059 | 0,156 | 69 (56,6) | 72 (59,0) | 0,041 | 0,172 |
| Enfermedad cerebrovascular | 32 (15,8) | 17 (10,5) | 0,062 | 0,124 | 17 (13,9) | 14 (11,5) | 0,051 | 0,147 |
| Enfermedad pulmonar obstructiva crónica | 60 (29,7) | 38 (23,5) | 0,041 | 0,202 | 34 (27,9) | 31 (25,4) | 0,038 | 0,211 |
| Fibrilación auricular | 88 (43,6) | 78 (48,1) | 0,040 | 0,185 | 54 (44,3) | 57 (46,7) | 0,039 | 0,193 |
| Datos de pruebas analíticas | ||||||||
| Glucosa (mg/dl) | 147,5±40,2 | 140,9±36,5 | 0,089 | 0,087 | 144,2±40,0 | 141,3±37,7 | 0,073 | 0,102 |
| HbA1c(%) | 7,5±1,2 | 7,0±1,0 | 0,109 | 0,044 | 7,4±1,2 | 7,2±1,1 | 0,078 | 0,112 |
| Creatinina (mg/dl) | 1,1±0,6 | 1,1±0,7 | 0,022 | 0,214 | 1,1±0,6 | 1,1±0,7 | 0,021 | 0,219 |
| TFGe (ml/min/1,73 m2) | 52,9±22,0 | 56,4±23,0 | 0,038 | 0,161 | 53,5±22,3 | 55,1±22,8 | 0,040 | 0,179 |
| Ácido úrico (mg/dl) | 6,6±4,6 | 6,1±4,5 | 0,035 | 0,180 | 6,4±4,5 | 6,2±4,5 | 0,021 | 0,217 |
| Hematocrito (%) | 42,8±6,1 | 41,0±5,3 | 0,030 | 0,171 | 42,2±6,1 | 41,5±5,4 | 0,028 | 0,182 |
| NT-proBNP (pg/ml) | 1.152,8±646,2 | 910,0±589,2 | 0,057 | 0,141 | 1.050,5±636,0 | 922,5±599,0 | 0,042 | 0,167 |
| cLDL (mg/dl) | 65,0±21,3 | 70,3±25,2 | 0,059 | 0,150 | 67,0±21,3 | 69,5±24,6 | 0,039 | 0,175 |
| cHDL (mg/dl) | 43,5±9,9 | 39,8±9,4 | 0,038 | 0,177 | 41,5±9,5 | 39,9±9,4 | 0,037 | 0,179 |
| Colesterol total (mg/dl) | 143,5±36,2 | 151,7±40,7 | 0,062 | 0,138 | 148,9±37,7 | 150,5±40,2 | 0,053 | 0,158 |
| Triglicéridos (mg/dl) | 150,0±52,0 | 161,0±55,5 | 0,071 | 0,122 | 155,4±53,0 | 159,0±55,0 | 0,070 | 0,129 |
| Proporción albúmina/creatinina urinarias (mg/g) | 50,0±42,0 | 45,1±40,0 | 0,070 | 0,133 | 49,4±41,4 | 47,5±40,5 | 0,061 | 0,145 |
ARA-II: antagonistas del receptores de la angiotensina II; cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; DPP4: dipeptidil peptidasa-4; GLP-1: glucagon-like peptide-1; HbA1c: glucohemoglobina; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; KCCQ: Kansas City Cardiomyopathy Questionnaire; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: New York Heart Association; PAD: presión arterial diastólica; PAS: presión arterial sistólica; SGLT-2: cotransportador de sodio y glucosa de tipo 2; TFGe: tasa de filtrado glomerular estimada.
Los valores continuos se expresan como media ± desviación estándar y los cualitativos, como n (%). Las diferencias entre grupos se determinaron con la prueba de la t de Student para 2 muestras o la prueba de suma de rangos de Mann-Whitney-Wilcoxon para las variables continuas y la prueba de la χ2 de Pearson para las variables cualitativas.
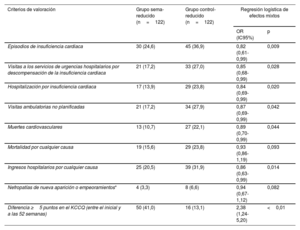
La administración de semaglutida se asoció con una reducción de los episodios de IC y de cada uno de sus componentes. Además, las muertes cardiovasculares y los ingresos hospitalarios por cualquier causa disminuyeron de manera significativa. Por último, entre los pacientes del grupo sema-reducido fue más probable que existiera una diferencia ≥ 5 puntos en el Cuestionario KCCQ —con una mejora, 18,7±3,2 frente a 8,2±1,7 puntos (p < 0,01) comparado con el grupo de control—. En la tabla 2 se muestran los resultados de las variables de valoración.
Criterios de valoración principal y secundarios
| Criterios de valoración | Grupo sema-reducido (n=122) | Grupo control-reducido (n=122) | Regresión logística de efectos mixtos | |
|---|---|---|---|---|
| OR (IC95%) | p | |||
| Episodios de insuficiencia cardiaca | 30 (24,6) | 45 (36,9) | 0,82 (0,61-0,99) | 0,009 |
| Visitas a los servicios de urgencias hospitalarios por descompensación de la insuficiencia cardiaca | 21 (17,2) | 33 (27,0) | 0,85 (0,68-0,99) | 0,028 |
| Hospitalización por insuficiencia cardiaca | 17 (13,9) | 29 (23,8) | 0,84 (0,69-0,99) | 0,020 |
| Visitas ambulatorias no planificadas | 21 (17,2) | 34 (27,9) | 0,87 (0,69-0,99) | 0,042 |
| Muertes cardiovasculares | 13 (10,7) | 27 (22,1) | 0,89 (0,70-0,99) | 0,044 |
| Mortalidad por cualquier causa | 19 (15,6) | 29 (23,8) | 0,93 (0,86-1,19) | 0,093 |
| Ingresos hospitalarios por cualquier causa | 25 (20,5) | 39 (31,9) | 0,86 (0,63-0,99) | 0,014 |
| Nefropatías de nueva aparición o empeoramientos* | 4 (3,3) | 8 (6,6) | 0,94 (0,67-1,12) | 0,082 |
| Diferencia ≥5 puntos en el KCCQ (entre el inicial y a las 52 semanas) | 50 (41,0) | 16 (13,1) | 2,38 (1,24-5,20) | <0,01 |
IC95%: intervalo de confianza del 95%; KCCQ: Kansas City Cardiomyopathy Questionnaire; OR: odds ratio.
Los valores expresan n (%). Para evaluar la relación entre el tratamiento y los resultados del estudio, se utilizaron regresiones logísticas de efecto mixto. Los valores del análisis de regresión expresan cociente de posibilidades (odds ratio) y sus intervalos de confianza del 95%. Todos los valores de p <0,05 se consideraron estadísticamente significativos.
En los pacientes tratados con semaglutida se constató una mayor reducción de la glucohemoglobina (HbA1c) (el 0,9±0,2 frente al 0,3±0,1%; p=0,011) y el peso corporal (11,8±3,8 frente a 2,5±1,1 kg; p < 0,01) que en el grupo de control. Hubo correlaciones negativas entre la puntuación del KCCQ y la HbA1c (r=0,532; p < 0,009) y el peso corporal (r=–0,649; p < 0,01).
Con respecto a la seguridad, se produjeron pocos eventos adversos graves entre los pacientes que recibieron semaglutida (24,6%). Los eventos adversos fueron principalmente gastrointestinales, y 11 pacientes (9,0%) suspendieron el tratamiento.
Mientras que se han observado robustos efectos favorables de los iSGLT2 en los objetivos de IC de los pacientes de IC con y sin DM2, los ar-GLP-1 no se han relacionado de manera clara con una reducción de los ingresos hospitalarios por IC2. Los datos de los estudios observacionales son bastante limitados y controvertidos, y en algunos estudios se relacionan con efectos neutros y en otros, con efectos favorables, junto con una reducción de los ingresos por IC3. Recientemente, la administración semanal de semaglutida se ha relacionado con efectos favorables cardiovasculares y en la IC en los pacientes con sobrepeso u obesidad y enfermedad cardiovascular preexistente5 e IC con fracción de eyección conservada6. Los efectos favorables de los ar-GLP-1 en la IC podrían obtenerse a través de múltiples mecanismos interrelacionados, tales como efectos directos en el endotelio, el tejido renal, el sistema renina-angiotensina y factores de riesgo cardiometabólico3,5.
Los efectos favorables en los objetivos de la IC ya mencionados y observados en varios estudios (en algunos se incluyó a pacientes con IC-FEr y enfermedad coronaria o enfermedad cerebrovascular) coinciden con los resultados del presente estudio. La implementación de programas terapéuticos estructurados que incluyan la administración de ar-GLP-1, junto con mejoras en la calidad de la dieta y ejercicio para conseguir a largo plazo una pérdida de peso corporal y un aumento de la masa magra, podría establecerse como un objetivo importante en el tratamiento de los pacientes con DM2, sobrepeso/obesidad e IC-FEr.
Aunque estos resultados proporcionan información valiosa, deberían considerarse en el contexto de ciertas limitaciones, como posibles factores de confusión no cuantificados, el número relativamente bajo de algunos criterios de valoración y la influencia de los cambios en el tratamiento de la IC y las recomendaciones generales establecidas durante el seguimiento.
En conclusión, en este estudio observacional y después de un AP, la administración semanal de semaglutida se relacionó con una reducción de los episodios de IC, las muertes cardiovasculares y las hospitalizaciones por cualquier causa en pacientes con DM2 e IC-FEr. Además, en los pacientes tratados con semaglutida fue más probable que se observara una diferencia ≥ 5 entre la puntuación total de síntomas del KCCQ al inicio y 52 semanas después. Se requieren más estudios sobre los ar-GLP-1 en la IC-FEr.
FINANCIACIÓNEste estudio no recibió ninguna subvención específica de organismos de financiación procedentes de los sectores público, comercial o sin ánimo de lucro.
CONSIDERACIONES ÉTICASEl estudio fue aprobado por el Comité de Ética de la Investigación de Málaga (código del comité de ética: REDIME-27-10-2016) y todos los participantes proporcionaron el consentimiento informado por escrito para la interconsulta de las historias clínicas. Este estudio se hizo conforme a la Declaración de Helsinki. La confidencialidad de los datos y el anonimato de los pacientes se mantuvieron rigurosamente durante el estudio.
No se hizo separación por sexos a partir de los resultados de este estudio.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALNo se utilizaron herramientas de inteligencia artificial para la preparación de este artículo.
CONTRIBUCIÓN DE LOS AUTORESM.A. Pérez-Velasco: análisis e interpretación de los datos y preparación del artículo. A. Trenas: análisis e interpretación de los datos y preparación del artículo. M.R. Bernal-López: análisis e interpretación de los datos y preparación del artículo. M.D. García de Lucas: análisis e interpretación de los datos y preparación del artículo. R. Gómez-Huelgas: idea y diseño, análisis e interpretación de los datos y preparación del artículo. L.M. Pérez-Belmonte: idea y diseño, adquisición de participantes y datos, análisis e interpretación de los datos y preparación del artículo. Todos los autores han participado en la redacción del manuscrito y han leído y aprobado la versión final del artículo. M.A. Pérez-Velasco y A. Trenas contribuyeron por igual en este artículo y comparten la primera autoría.
CONFLICTO DE INTERESESNinguno.