La insuficiencia mitral es la valvulopatía cardiaca de mayor prevalencia en el mundo. A pesar de la amplia disponibilidad de una intervención quirúrgica curativa, hay un considerable número de pacientes con insuficiencia mitral grave a los que no se interviene debido, en general, a la presencia de una disfunción ventricular izquierda, la edad avanzada y la presencia de comorbilidades. La sustitución percutánea de la válvula mitral es una prometedora alternativa terapéutica a la sustitución valvular quirúrgica tradicional. Sin embargo, las complicadas anatomía y fisopatología del complejo valvular mitral plantean retos importantes para el diseño y la aplicación satisfactorios de los nuevos dispositivos de sustitución percutánea de la válvula mitral. Los modelos tridimensionales y específicos para cada paciente, diseñados con ordenador, permiten una evaluación exacta de la anatomía de la válvula mitral y realizar simulaciones de los tratamientos transcatéter previas a la intervención. Esta información puede ser útil para perfeccionar las características de diseño de los nuevos dispositivos mitrales percutáneos y mejorar la planificación de la intervención. Describimos aquí un nuevo instrumento de procesamiento basado en las técnicas de imagen médicas, que facilita una evaluación exacta y no invasiva del complejo valvular mitral mediante la elaboración de modelos cardiacos tridimensionales precisos. Las reconstrucciones tridimensionales realizadas mediante ordenador se trasladan a un modelo físico empleando tecnología de impresión tridimensional, lo cual permite realizar evaluaciones de la interacción entre dispositivo y paciente que son específicas de cada paciente. Esto puede brindar nuevas oportunidades para un mejor conocimiento de la anatomía, la fisiopatología y la interacción de la válvula mitral con el dispositivo, lo cual podría ser de crucial importancia para el avance de las intervenciones de sustitución percutánea de la válvula mitral.
Palabras clave
La insuficiencia mitral (IM) tiene una prevalencia creciente y afecta a un 9% de las personas de edad ≥ 75 años1,2. Aunque la cirugía es el tratamiento estándar de referencia para la IM grave, aproximadamente la mitad de los pacientes con indicación para cirugía de la válvula mitral (VM) son rechazados o no se los remite a una intervención potencialmente curativa, principalmente debido a edad avanzada, comorbilidades importantes o disfunción ventricular izquierda, que hacen que el riesgo quirúrgico sea inaceptablemente alto3,4. Además, actualmente hay poca evidencia que respalde la intervención quirúrgica en los pacientes con una IM funcional5. En consecuencia, hay una importante necesidad clínica insatisfecha de una opción terapéutica menos invasiva para un porcentaje considerable de pacientes con IM.
La sustitución percutánea de la válvula aórtica ha puesto de manifiesto la seguridad y la eficacia de las intervenciones percutáneas en las válvulas cadiacas6–8. En cambio, el desarrollo de dispositivos para la sustitución percutánea de la VM (SPVM) se encuentra todavía en su primera infancia. Los estudios agudos y crónicos sobre la SPVM en animales han mostrado resultados alentadores9,10; más recientemente se han realizado varias primeras intervenciones en seres humanos empleando diversas prótesis valvulares11,12. La SPVM va por detrás de su equivalente aórtico debido a la anatomía compleja y muy variable de la VM, la interacción de la válvula con el ventrículo izquierdo y el efecto muy variable de diferentes enfermedades (IM primaria y secundaria) en el aparato valvular mitral.
Un mejor conocimiento de la anatomía, la fisiología y la interacción de la VM con el dispositivo tiene una importancia crucial para el avance en el campo de la SPVM. La influencia de la tomografía computarizada multicorte en los resultados de la sustitución percutánea de la válvula aórtica valida este concepto13, si bien la anatomía más compleja de la VM puede requerir una tecnología de imagen cardiaca específica para ello. Los nuevos programas informáticos de imagen permiten crear modelos cardiacos tridimensionales (3D) exactos y específicos de cada paciente, que pueden usarse para una impresión tridimensional. Las ventajas de esta tecnología incluyen: a) mejor diseño de los prototipos de la válvula; b) mejor selección de los pacientes antes de la intervención; c) guía durante la intervención, y d) vigilancia clínica después de la intervención y un mejor conocimiento de la interacción paciente-prótesis.
El objetivo de esta revisión es ilustrar el potencial de los modelos tridimensionales de la VM elaborados con ordenador empleando el programa Mimics©Innovation Suite (Materialise NV; Lovaina, Bélgica). Mostramos la forma en que se puede usar este programa para conocer mejor la anatomía de la VM (anatomía, posición y relaciones) y desarrollar simulaciones virtuales y una impresión tridimensional para optimizar la SPVM.
PAQUETE DE PROGRAMAS MIMICS©INNOVATION SUITELa clave para trasladar los datos anatómicos obtenidos con técnicas de imagen bidimensionales (ecocardiografía, fluoroscopia e imágenes monoplanares basadas en la tomografía computarizada multicorte o la resonancia magnética) a modelos tridimensionales es un proceso denominado segmentación. Los modelos del corazón tridimensionales reconstruidos mediante ordenador pueden imprimirse después con una impresora tridimensional, por completo o en parte según las estructuras de interés (p. ej., solo las cavidades cardiacas izquierdas). Existen diversos materiales y tecnologías para la impresión tridimensional (estereolitografía, sinterizado con láser, poliinyección, fijación de polvo, etc.) que permiten producir un modelo tridimensional para cada finalidad específica: conocimiento de la anatomía, diseño de prótesis, prueba de prótesis y planificación de la intervención.
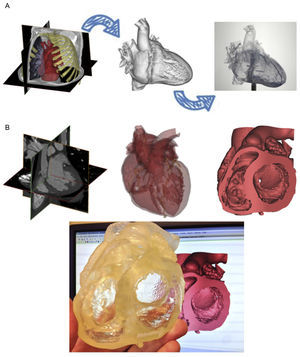
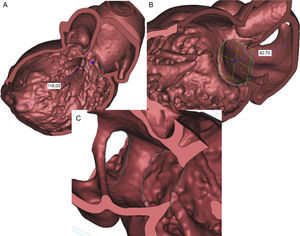
Mimics©Innovation Suite (Materialise NV) es un programa especializado que permite procesar datos de tomografía computarizada multicorte. Este programa incorpora múltiples operaciones, que van desde la simple medición hasta opciones complejas como la elaboración de modelos tridimensionales, el diseño de prótesis y la funcionalidad de medición tridimensional compleja. Permite la creación de precisos modelos tridimensionales del corazón para facilitar la evaluación anatómica específica de cada paciente y esclarecer la interacción entre la anatomía de un paciente concreto y un diseño de prótesis específico (figuras 1A y B).
A: el paquete informático Mimics© Innovation Suite permite la creación de modelos tridimensionales exactos a partir de los datos de exploraciones por imagen bidimensional. B: Mimics© (Materialise NV) permite la segmentación de los datos de la tomografía computarizada multicorte del área específica del corazón (complejo de la VM) de un paciente específico; de esta forma, se puede crear modelos tridimensionales exactos del complejo de la VM e imprimirlos en diversos materiales y colores.
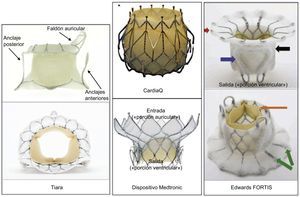
Es bien sabido que el diseño del dispositivo de VM para la sustitución percutánea es un proceso de extrema dificultad y constituye un verdadero reto. Esta complejidad deriva de: a) la necesidad de anclar la prótesis a la altura del anillo mitral en ausencia de un anillo rígido circular o calcificación de las valvas; b) el carácter voluminoso del aparato valvular submitral, muy específico de cada individuo (músculos papilares y cuerdas tendinosas), lo que constituye un obstáculo físico para aplicar, desplegar, alinear y expandir el dispositivo; c) la combinación de unas presiones de cierre superiores (sistólica) y un área del orificio grande indica fuerzas de desalojo superiores12; d) la variabilidad tanto de la enfermedad de la VM (insuficiencia funcional y degenerativa, estenosis) como de las dimensiones del anillo indica que son necesarios múltiples diseños y tamaños de las prótesis; e) la asociación anatómica entre el anillo mitral y el tracto de salida del ventrículo izquierdo (TSVI) podría conducir a obstrucción de este; f) la localización de la arteria coronaria circunfleja izquierda podría limitar la expansión radial; g) el gran diámetro del anillo y la necesidad de un sistema de recuperación del dispositivo exigen el empleo de catéteres de liberación de gran calibre (> 25 Fr), y h) las dimensiones del ventrículo izquierdo o la aurícula izquierda podrían limitar el espacio disponible para maniobrar con los catéteres grandes que requiere el despliegue de la prótesis.
Anatomía de la válvula mitralSe denomina anillo mitral a la transición entre la aurícula izquierda y el ventrículo izquierdo, y esta estructura da origen a las inserciones basales de las valvas de la VM. El anillo de la VM tiene una estructura en forma de D, con un diámetro intercomisural (septolateral) mayor que el diámetro anteroposterior14. Es de naturaleza fibrosa y deformable, rara vez está calcificado y se caracteriza por los cambios dinámicos de la geometría (forma/tamaño) del anillo mitral durante el ciclo cardiaco: reducción del área (30%) y la circunferencia del anillo (15%) durante la sístole ventricular10. La valva aórtica (anterior) de la válvula mitral está en continuidad, mediante un tejido fibroso, con la válvula aórtica y los trígonos fibrosos derecho e izquierdo. Esta región del anillo es, pues, fibrosa y menos propensa a la dilatación. Los dos tercios restantes del anillo son principalmente musculares.
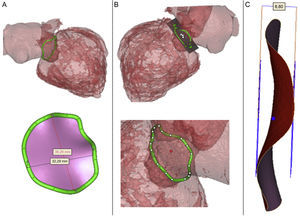
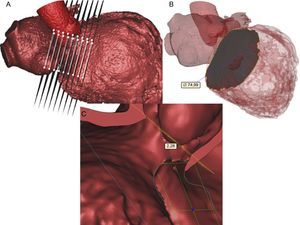
Como se muestra en las figuras 2A y B, el programa Mimics©Innovation Suite proyecta automáticamente el anillo tridimensional en el plano de mejor ajuste y muestra el centro geométrico del anillo de la VM antes de medir automáticamente el área y el perímetro del anillo. El diámetro medio se calcula mediante la media aritmética del diámetro aortomural y el intercomisural10. Estas mediciones son importantes, puesto que, de manera similar a lo que ocurre en el reemplazo percutáneo de la válvula aórtica, la determinación exacta y precisa del tamaño del anillo mitral puede ser una cuestión clave a la hora de elegir el tamaño adecuado del dispositivo de SPVM. A diferencia del reemplazo percutáneo de la válvula aórtica, en el que se utiliza la fuerza radial para el anclaje, la SPVM se basa en una fijación axial (figura 3). Se ha diseñado el sistema de fijación con una parte de entrada a la aurícula grande y una parte de salida del ventrículo izquierdo corta, con objeto de reducir el riesgo de obstrucción del TSVI. Un tamaño excesivo puede conducir a rotura del anillo u obstrucción del TSVI, con un gasto cardiaco subóptimo. Un tamaño insuficiente puede resultar en fuga paravalvular y/o embolización.
A: el programa Mimics© Innovation Suite realiza múltiples mediciones de los diámetros del anillo, la elipticidad, el perímetro y el área del anillo mitral. B: plano de mejor ajuste de la válvula mitral y centro geométrico. C: distancia entre los puntos más alto y más bajo del anillo mitral.
Son los componentes musculares del aparato mitral. Como unidad funcional, los músculos papilares incluyen una parte de la pared del ventrículo izquierdo adyacente. Generalmente se describen en posición anterolateral y posteromedial, y se sitúan a lo largo de los segmentos medio a apical del ventrículo izquierdo. Sin embargo, esta distribución puede presentar variaciones considerables, en especial en los pacientes con valvas de tipo mixomatoso15. Las mediciones realizadas con el programa Mimics© se toman desde un punto situado en la cabeza de cada músculo papilar hasta el centro geométrico del anillo de la VM (figura 4A) y el plano de la VM (perpendicular al plano) (figura 4B). Puede medirse la distancia lineal tridimensional entre el centro geométrico y la cabeza de cada músculo papilar y la distancia perpendicular entre el plano de mejor ajuste del anillo y la cabeza de cada músculo papilar (figura 4C). Mimics© permite obtener la anatomía tridimensional y transversal, lo cual hace posible una visualización óptima del número y la localización de los músculos papilares (figura 4D).
Músculo papilar. A: medición desde un punto de las cabezas de los músculos papilares hasta el centro geométrico del anillo de la válvula mitral. B: medición desde las cabezas de los músculos papilares hasta el plano mitral (perpendicular al plano). C: distancia lineal entre las puntas de los músculos papilares. D: flexibilidad para producir y cortar la anatomía para obtener una visualización óptima de los músculos papilares (número de músculos papilares).
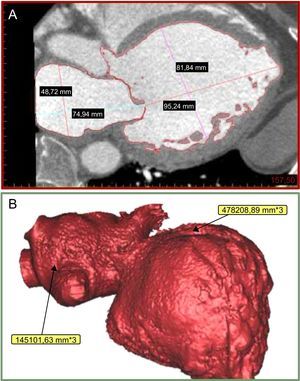
El tamaño, la forma y el anclaje de la prótesis no solo interaccionan con el anillo mitral, sino que pueden hacerlo también con estructuras anatómicas situadas en los lados auricular o ventricular del anillo. Las mediciones de la aurícula y el ventrículo izquierdos tienen como objetivo describir la forma de la cavidad y, lo que es más importante, definir de manera detallada la región situada inmediatamente por debajo y por encima del anillo mitral, incluido el TSVI. Con Mimics© se puede medir con exactitud el diámetro y el volumen del ventrículo y la aurícula izquierdos (figuras 5A y B). El diámetro de eje largo del ventrículo izquierdo se define como la distancia entre el centro geométrico del anillo mitral y el vértice del ventrículo izquierdo y el techo de la aurícula izquierda respectivamente (figuras 6A y B). Además, el programa permite realizar un análisis de la relación entre los orificios de la orejuela auricular izquierda y el anillo de la VM (figura 6C). Se puede analizar la aurícula y el ventrículo izquierdos en incrementos predeterminados (p. ej., 5 mm) a partir del anillo mitral, para valorar mejor el área y el perímetro a estos niveles y las posibles interacciones con las prótesis (figuras 7A y B). El estudio exacto de la región situada inmediatamente por debajo del anillo mitral es de especial interés, pues es la zona de aplicación de las prótesis utilizadas para la SPVM. Para valorar la importante relación entre el anillo mitral y el TSVI, hay varias mediciones especialmente interesantes en el contexto de la SPVM. Se determina el ángulo aortomitral que se forma entre el eje del TSVI y la línea central del anillo mitral. Se puede medir la distancia entre la cara medial del anillo mitral y la cara septal del plano del anillo aórtico (perpendicular al plano auriculoventricular) (figura 7C).
Diámetro de eje largo del ventrículo izquierdo. A: distancia desde el vértice hasta el centro geométrico del anillo de la válvula mitral. B: distancia desde el techo de la aurícula izquierda hasta el centro del anillo de la válvula mitral. C: relación entre los orificios de la orejuela auricular izquierda y el anillo de la válvula mitral (curvas azules). Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Cortes transversales por encima y por debajo de la válvula mitral. A: incrementos de 5 mm por encima y por debajo del anillo de la válvula mitral. B: corte transversal 10 mm por debajo del anillo de la válvula mitral en el ventrículo izquierdo, con la medición del diámetro de mejor ajuste. C: distancia del anillo mitral al plano del anillo aórtico (perpendicular al plano auriculoventricular).
La cardiología intervencionista tiene características comunes con las de otros tratamientos mínimamente invasivos, como las intervenciones laparoscópicas, y ello hace que sea apropiado el aprendizaje usando simuladores: requiere una apreciación compleja de la anatomía tridimensional a partir de imágenes bidimensionales y una coordinación oculomanual fina16. Las complicaciones derivadas de realizar de manera inadecuada las técnicas intervencionistas cardiacas pueden tener resultados catastróficos. Se debe alcanzar unas capacidades básicas antes de dominar las intervenciones más complejas. Varios estudios han puesto de relieve que el éxito de la intervención está relacionado con la cantidad de intervenciones realizadas por el operador17. En las intervenciones complejas, novedosas o que se llevan a cabo con poca frecuencia, la enseñanza tradicional de las técnicas invasivas que emplea un modelo de maestro-aprendiz, con intenso contacto personal entre el profesor y el alumno, puede ser insuficiente, y con un riesgo de complicaciones de la intervención potencialmente alto.
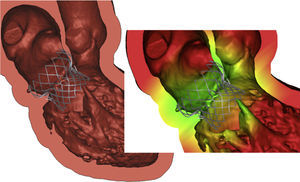
Partiendo de las imágenes de tomografía computarizada multicorte previas a la intervención y con el empleo del programa Mimics©Innovation Suite, el complejo valvular mitral, incluidas las calcificaciones, se puede segmentar y reconstruir en tres dimensiones. Se importa al Mimics© un modelo de diseño tridimensional asistido por ordenador de un dispositivo de VM transcatéter y se coloca en la anatomía reconstruida de los pacientes (figura 8). El conjunto puede exportarse a un resolutor de elementos finitos para realizar simulaciones. Con este modelo de prótesis, se puede usar simulaciones de elementos finitos, no lineales, avanzadas, para realizar varias predicciones: deformación del armazón del stent, aposición incompleta del armazón, movimiento del calcio y otras. Esto permite realizar una evaluación de diferentes lugares de acceso; acceso anterógrado a la VM por abordaje transauricular directo o a través del sistema venoso con acceso transeptal a la aurícula izquierda y abordaje transapical a través de una minitoracotomía izquierda. Se puede probar cuál de estos accesos permitiría alcanzar la mejor alineación coaxial del anillo de la válvula con la prótesis mitral para el despliegue adecuado de la válvula. Por último, se puede evaluar el riesgo de complicaciones, como obstrucción del TSVI, interacción con los músculos papilares o insuficiencia valvular, antes de realizar la intervención (figura 8).
MODELOS CARDIACOS FÍSICOS TRIDIMENSIONALES DEL COMPLEJO VALVULAR MITRAL ESPECÍFICOS DE CADA PACIENTE: TECNOLOGÍA DE IMPRESIÓN TRIDIMENSIONALLa impresión tridimensional es una técnica de fabricación que se emplea en ingeniería para generar modelos prototípicos mediante un proceso aditivo de capas sucesivas. Con la transferencia de esta técnica a la medicina, puede obtenerse un modelo tridimensional de la anatomía humana basado en las exploraciones de imagen de un paciente y puede realizarse una impresión tridimensional en forma de un objeto físico. Este proceso es posible gracias a la segmentación de los datos de imagen y su conversión a modelos de superficie que el ordenador convierte en tridimensionales. La fabricación se realiza con una tecnología de impresión tridimensional para obtener modelos físicos. La impresión tridimensional permite la creación de réplicas realistas de la anatomía humana a partir de diversas modalidades de diagnóstico médico por la imagen, como la tomografía computarizada, la resonancia magnética y la ecocardiografía tridimensional18,19. Dado que la fabricación aditiva, o impresión tridimensional, ha pasado a ser más práctica y accesible, se han planteado diversas aplicaciones de la tecnología al campo de las intervenciones cardiacas mínimamente invasivas y, en particular, las intervenciones cardiacas percutáneas18–23. Uno de los campos prometedores es el de la simulación de la sustitución percutánea de válvulas cardiacas.
El complejo de la VM simulado a través de este proceso con el programa Mimics© (Materialise NV) puede tener un notable potencial para facilitar la simulación previa a la intervención y una planificación de la SPVM específica para el paciente. Además, puede ser útil como método para mejorar el conocimiento de la anatomía compleja de la VM.
RESUMEN Y PERSPECTIVAS FUTURASEstán surgiendo con rapidez nuevas tecnologías valvulares percutáneas transcatéter y mínimamente invasivas para el tratamiento de la IM, pero su aplicación óptima no se ha establecido todavía. La sustitución percutánea de la VM es una técnica prometedora que se encuentra en la fase experimental en la aplicación humana, y para la que hay varias dificultades anatómicas y técnicas que será necesario superar antes de que pueda adoptarse de forma generalizada9–12.
Un mejor conocimiento de la anatomía, la fisiología y la interacción de la válvula mitral con el dispositivo es de gran interés y requiere el empleo de tecnologías de diagnóstico cardiaco por imagen. Las técnicas de imagen son parte integrante de las intervenciones estructurales transcatéter y desempeñan un papel importante en la selección de los pacientes (cribado), la planificación previa a la intervención y la toma de decisiones durante esta22. Además, las aplicaciones clínicas de la elaboración de modelos tridimensionales y la impresión tridimensional en la cardiopatía estructural son muy amplias. En tres décadas, la tecnología de impresión tridimensional ha pasado de un proceso de fabricación muy especializado a un sector de un volumen de 2.700 millones de dólares, que fabrica multitud de productos, como juguetes, relojes de pulsera, componentes de aviones, alimentos y otros. La aplicación de esta tecnología a la medicina puede acelerar un cambio igualmente extraordinario.
En el contexto de la SPVM, la creación de modelos tridimensionales específicos para cada paciente y modelos físicos mediante impresión tridimensional puede brindar nuevas oportunidades en diversos aspectos:
- 1.
Desde la perspectiva del cardiólogo intervencionista, puede permitir: a) una mejor apreciación de las interrelaciones de las diversas estructuras anatómicas del corazón; b) una detallada información anatómica y geométrica del complejo de la VM; c) planificar las estrategias técnicas empleando dispositivos virtuales, y d) apreciar las posibles dificultades de la intervención y evaluar la probabilidad de éxito o fracaso de la SPVM.
- 2.
Desde la perspectiva del fabricante, los modelos físicos específicos para cada paciente pueden ser de especial utilidad en el desarrollo preclínico de nuevos dispositivos al mostrar con exactitud las relaciones espaciales y el ajuste entre dispositivo y anatomía en todo el espectro de corazones afectados de pacientes que podrían ser candidatos a SPVM.
- 3.
Desde la perspectiva de la formación, al facilitar la apreciación anatómica y patológica de la valvulopatía mitral, los modelos físicos pueden mejorar el conocimiento de pacientes, estudiantes y médicos sobre la enfermedad estructural de la VM y pueden ser útiles para esclarecer los objetivos y las limitaciones de la SPVM.
Los modelos tridimensionales del corazón y la tecnología de bioimpresión están empezando a tener amplia disponibilidad a un coste más asequible. Prevemos, pues, que se produzca una rápida adopción de los modelos de impresión tridimensional en la medicina y en los tratamientos valvulares mínimamente invasivos. A pesar de estas posibles ventajas, son necesarios estudios clínicos para evaluar su papel en el campo de las intervenciones cardiacas percutáneas.
CONFLICTO DE INTERESESNinguno.