La trombosis intraventricular es una complicación temida del infarto de miocardio. Su prevalencia sigue siendo sustancialmente elevada pese a la revascularización temprana y a la mejora significativa en el tratamiento antitrombótico alcanzadas en las últimas décadas1. Hoy en día se estima una incidencia de trombosis intraventricular tras infarto de miocardio de entre un 3 y un 10%, dependiendo de la modalidad de imagen utilizada para su valoración2,3. En paralelo, la incidencia acumulada del ictus isquémico tras el infarto de miocardio es de aproximadamente un 3-5% en los 2 años posteriores al evento coronario4. En ausencia de fibrilación auricular, la mayor parte de los ictus isquémicos posinfarto son atribuibles a la presencia de un trombo intraventricular. En cuanto a su fisiopatología, la hipótesis más aceptada propone que la trombosis posinfarto es el resultado de la interacción entre 3 factores: a) un estado sistémico proinflamatorio/procoagulante; b) el daño endocárdico, que favorece la agregación y la activación plaquetaria, y c) la estasis sanguínea, resultado de la presencia de regiones miocárdicas acinéticas y discinéticas que alteran el tránsito normal de la sangre en la cavidad ventricular5.
Un diagnóstico preciso y precoz de una trombosis intraventricular afecta directamente al tratamiento y a la evolución clínica de los pacientes tras un infarto de miocardio. La resonancia magnética (RM) cardiaca es la modalidad de imagen de referencia para el diagnóstico de la trombosis intraventricular6. De hecho, aunque la ecocardiografía transtorácica (ETT) es la técnica diagnóstica de primera línea para la evaluación de la función biventricular y complicaciones mecánicas tras un infarto de miocardio, su sensibilidad para la detección de trombos es muy baja (un 30% en comparación con la RM cardiaca, aunque puede mejorar hasta un 64% si se administra contraste ecocardiográfico2). La superioridad de la RM cardiaca para la detección de trombosis intraventricular frente a la ETT se debe principalmente a su capacidad de caracterización tisular mediante secuencias de perfusión y realce tardío de gadolinio, en las que el trombo se distingue fácilmente del miocardio adyacente debido a su ausencia de vascularización5. No obstante, la limitada disponibilidad de la RM cardiaca en entornos clínicos y los largos tiempos de exploración necesarios (aproximadamente 45min para una evaluación cardiaca completa utilizando secuencias convencionales, que frecuentemente asocian malestar y claustrofobia del paciente), limitan su uso habitual en el paciente tras un infarto de miocardio. Todos estos factores han propiciado la búsqueda de técnicas alternativas que puedan mejorar la predicción del riesgo cardioembólico posinfarto. Una de ellas es la estasis sanguínea intraventricular, que puede identificarse y cuantificarse mediante técnicas de imagen. En esta línea, Rodríguez-González et al. en un reciente artículo publicado en Revista Española de Cardiología analizan de forma prospectiva la capacidad de la estasis sanguínea por ETT para predecir eventos cardioembólicos tras un infarto agudo de miocardio con elevación del segmento ST (IAMCEST)7. El estudio ISBITAMI incluyó prospectivamente a pacientes con un primer episodio de IAMCEST y fracción de eyección del ventrículo izquierdo (FEVI) ≤ 45% procedentes de un único centro, sin antecedente de fibrilación auricular u otra indicación de anticoagulación crónica, enfermedad carotídea o valvular significativas, enfermedad potencialmente causante de daño neurológico previo ni contraindicación para RM. Se realizó una ETT incluyendo evaluación de la estasis sanguínea y análisis de deformación longitudinal a nivel apical del ventrículo izquierdo mediante speckle-tracking en el momento de la inclusión, así como RM cardiaca y cerebral a la semana y a los 6 meses del IAMCEST. El objetivo primario combinado se basó en la incidencia de trombosis intraventricular, accidente isquémico transitorio o ictus isquémico, infarto cerebral silente agudo/subagudo, y/o embolia sistémica periférica entre la inclusión y la visita a los 6 meses. De los 92 pacientes inicialmente incluidos, a la semana se realizó RM cardiaca a 75. Tras excluir pérdidas en el seguimiento o muerte por otras causas, se incluyó en el análisis final a un total de 66 pacientes, el 78% varones con una mediana de edad de 58 años, una localización del infarto predominantemente anterior (89%) y una mediana de FEVI por ETT del 41%. De estos 66 pacientes, un 25% (n=17) presentó al menos uno de los eventos incluidos en el objetivo primario. Si bien esta incidencia es relativamente alta en comparación con otras cohortes4, en su mayoría se debió a la presencia de trombosis intraventricular (n=13), con solo 5 casos de infarto cerebral silente, 3 de ictus o accidente isquémico transitorio y ningún caso comunicado de embolia sistémica a otros niveles. Desde el punto de vista cronológico, todos los eventos salvo un infarto cerebral silente se detectaron en los estudios de RM cardiaca y cerebral a los 7 días del IAMCEST, lo cual concuerda con la literatura1. Al comparar por grupos, si bien no hubo diferencias en las características clínicas ni analíticas basales, los pacientes que experimentaron el objetivo primario se caracterizaron por presentar infartos de localización anterior en todos los casos, con una mediana de FEVI significativamente más baja; peor deformación longitudinal a nivel apical y tiempos de residencia (indicador de estasis ventricular) más prolongados en la ETT inicial. En un análisis de regresión multivariable, que incluyó tanto la FEVI como el tiempo de residencia y el strain apical, solo los últimos 2 parámetros se asociaron significativamente con el evento primario. Asimismo, por separado ambos parámetros mostraron mejora del estadístico C con respecto al de la FEVI, tanto por ecocardiografía como por RM cardiaca, lo que se traduce en una mejora de la capacidad discriminativa a la hora de predecir el desarrollo de trombosis intraventricular y eventos cardioembólicos, y que se incrementa al emplear ambos parámetros en combinación.
El primer punto que poner en valor es el objetivo relevante y pertinente del estudio, el cual, atendiendo a necesidades clínicas no resueltas, evalúa una herramienta que puede facilitar la toma de decisiones clínicas complejas, como lo es la profilaxis anticoagulante tras el infarto de miocardio, situación en la que el balance riesgo-beneficio conlleva considerar el riesgo hemorrágico asociado al tratamiento triple. En este contexto, las guías europeas de 2023 no incluyen recomendaciones preventivas específicas, pero hacen énfasis en la importancia de la monitorización individualizada por imagen, así como en la necesidad de más ensayos clínicos aleatorizados, dadas las diversas lagunas en la evidencia8. Debemos tener presentes algunas limitaciones metodológicas del presente trabajo, como el reducido tamaño muestral, una tasa considerable de pérdidas, la comparación con parámetros funcionales convencionales (FEVI) que tienen un valor limitado para el estudio de fuente embólica o el uso de un objetivo primario basado en una combinación de eventos cardioembólicos clínicos y subclínicos, así como en la propia detección de trombosis intraventricular. Los autores hacen una interpretación ajustada de sus resultados considerando su trabajo como una prueba de concepto que necesita validación futura.
Desde el punto de vista técnico, la estasis sanguínea se evaluó mediante el tiempo de residencia de una partícula en la cavidad miocárdica utilizando las medidas de velocidad adquiridas dentro de la cavidad segmentada del ventrículo izquierdo con estudios Doppler por ETT (bidimensionales). Para estimar el tiempo de residencia, Rodríguez-González et al. utilizaron una aproximación lagrangiana donde se asume una difusividad de la sangre nula con respecto al movimiento de la sangre resultante del latido cardiaco7. En un estudio preclínico previo de este mismo grupo, el tiempo de residencia mejoró la capacidad predictiva de hallar microembolias cerebrales posinfarto9, lo que motivó el desarrollo del presente trabajo7. Una pregunta adicional es si conocer la dinámica de los patrones de estasis en el seguimiento permitiría personalizar la duración óptima del tratamiento anticoagulante, dada la escasa evidencia clínica disponible. En este sentido, habría sido relevante conocer las trayectorias de los patrones de estasis en los pacientes del estudio ISBITAMI, aprovechando su diseño longitudinal. Por otra parte, queda por estudiar comparativamente la capacidad predictiva del tiempo de residencia con respecto a otros parámetros validados para cuantificar el flujo intracardiaco, como el flujo 4D por RM cardiaca, que sí emplea información tridimensional10.
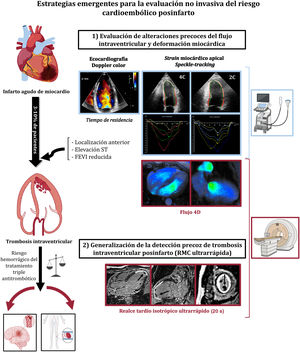
Como estrategia integral para mejorar la predicción de eventos cardioembólicos posinfarto, una alternativa a la evaluación temprana de la dinámica de flujo que proponen los autores de este artículo es la detección precoz de trombosis intraventricular generalizando el uso de RM cardiaca en el periodo posinfarto precoz (figura 1). En este sentido, el uso de secuencias ultrarrápidas, como ESSOS (enhanced SENSE by static outer volume subtraction), que permite adquirir una RM cardiaca completa (función biventricular y realce tardío isotrópico ultrarrápido) en solo 2 apneas (40 s), consigue superar la mayor parte de los inconvenientes ya comentados de la RM cardiaca convencional. Aunque esta secuencia se ha validado clínicamente en una variedad de escenarios clínicos cardiovasculares11, su potencial para modificar la estrategia terapéutica y eventualmente el pronóstico en pacientes posinfarto no se ha demostrado todavía.
Estrategias emergentes para la evaluación no invasiva del riesgo cardioembólico posinfarto. FEVI: fracción de eyección del ventrículo izquierdo; RMC: resonancia magnética cardiaca. Imágenes de flujo 4D por RMC cortesía de la Dra. Ana Álvarez-Vázquez, Hospital Universitario Quirónsalud Madrid. Figura creada con el apoyo de BioRender (https://biorender.com/).
En conclusión, el trabajo de Rodríguez-González et al.7 respalda el valor de una combinación de parámetros (deformación miocárdica y estasis intraventricular por ETT) para mejorar la predicción de complicaciones cardioembólicas tras un infarto de miocardio. La aplicabilidad del cálculo de la estasis sanguínea a otros cuadros clínicos diferentes (por ejemplo, la estasis ventricular en la miocardiopatía dilatada no isquémica con FEVI reducida sin otra indicación de anticoagulación o la estasis auricular izquierda) supone uno de los aspectos más interesantes del estudio y una puerta abierta a nuevas líneas de investigación. Asimismo, los autores dejan la posibilidad abierta a futuros ensayos clínicos que evalúen la eficacia de la anticoagulación oral profiláctica en pacientes seleccionados con base en las técnicas propuestas, lo cual, sin lugar a duda, son buenas noticias en un ámbito en el que se requiere evidencia contemporánea más sólida.
FINANCIACIÓNEl presente editorial no ha recibido financiación. El Centro Nacional de Investigaciones Cardiovasculares Carlos III cuenta con el apoyo del Instituto de Salud Carlos III, el Ministerio de Ciencia e Innovación y la Fundación ProCNIC y es un centro de excelencia Severo Ochoa (CEX2020-001041-S financiado por MICIN/AEI/10.13039/501100011033).
CONFLICTO DE INTERESESNinguno.