El tratamiento antitrombótico para los pacientes con anticoagulación oral por fibrilación auricular que se someten a intervención coronaria percutánea es especialmente complejo, sobre todo por el elevado riesgo hemorrágico que para estos pacientes implica la combinación de fármacos antiagregantes y anticoagulantes. Pese a que hay poca evidencia científica en este contexto, en los últimos años han aparecido varios ensayos clínicos que han intentado evaluar la seguridad y la eficacia de estrategias de tratamiento antitrombótico triple (combinación de doble antiagregación y un anticoagulante) y doble (combinación de un único antiagregante y un anticoagulante), bien con antagonistas de la vitamina K, bien con anticoagulantes de acción directa. El objetivo de este artículo es aportar una visión general del estado actual del conocimiento sobre las distintas estrategias de tratamiento antitrombótico triple y doble para pacientes anticoagulados por fibrilación auricular no valvular a los que se practica una intervención coronaria percutánea, además de proponer una serie de recomendaciones prácticas para la atención clínica de estos pacientes.
Información sobre el suplemento: este artículo forma parte del suplemento titulado «Actualización en el tratamiento de los pacientes con fibrilación auricular sometidos a intervención coronaria», que ha sido patrocinado por Boehringer Ingelheim.
Palabras clave:
El tratamiento antitrombótico para pacientes con necesidad de anticoagulantes orales (ACO) por fibrilación auricular (FA) a los que se practica una intervención coronaria percutánea (ICP) es un problema clínico de primera magnitud por su frecuencia (aproximadamente un 5-15% de los pacientes con FA requieren ICP a lo largo de su vida, mientras que un 5-10% de los pacientes que se someten a ICP tienen indicación de ACO a largo plazo, y la FA es la causa más frecuente) y por la complejidad que representa combinar de modo óptimo fármacos antiagregantes y anticoagulantes en este contexto clínico con la intención de minimizar eventos tromboembólicos, isquémicos y hemorrágicos1-3.
El tratamiento anticoagulante es claramente superior a la antiagregación, ya sea en monoterapia o tratamiento doble, para prevenir las complicaciones tromboembólicas derivadas de la FA3. Por otro lado, el tratamiento antiagregante plaquetario doble (TAPD) con ácido acetilsalicílico (AAS) y un antagonista del receptor P2Y12 es el tratamiento antitrombótico de elección (superior a los ACO) para la prevención de eventos isquémicos recurrentes en los pacientes sometidos a ICP, ya sea en el contexto de un síndrome coronario agudo (SCA) o en sujetos con cardiopatía isquémica estable1. Cuando coexisten los 2 escenarios es cuando el tratamiento antitrombótico se torna complejo, especialmente por el elevado riesgo hemorrágico que implica la combinación de ACO y TAPD, lo que se conoce como tratamiento antitrombótico triple (TATT); en concreto, se estima que el riesgo de una hemorragia mayor se incrementa en al menos 2-3 veces con TATT que con TAPD4. En los últimos años han aparecido numerosos documentos de consenso y guías clínicas que han intentado arrojar algo de luz al tratamiento antitrombótico en este contexto1-3,5-8, lo que pone de manifiesto su importancia, aunque se puede encontrar diferencias entre sus recomendaciones (que además presentan en su mayoría un nivel de evidencia bajo), lo que también demuestra la complejidad del tema9-11.
El objetivo del presente artículo es repasar la evidencia existente sobre las distintas estrategias de TATT y TAPD para pacientes que precisan ACO por FA no valvular (FANV) sometidos a ICP, además de aportar una serie de recomendaciones eminentemente prácticas para su asistencia clínica.
Estrategias de Tratamiento Para Pacientes con Fanv e ICPDesde un punto de vista eminentemente práctico, las posibles combinaciones de fármacos antitrombóticos en este contexto clínico se pueden resumir y clasificar en 3 tipos de estrategias: a) TATT: consistente en la combinación de 2 antiagregantes (AAS y un inhibidor del receptor plaquetario P2Y12 [iP2Y12]) y un ACO, ya sea un antagonista de la vitamina K (AVK) o un ACO de acción directa (ACOD); b) tratamiento antitrombótico doble (TATD): combinación de un antiagregante y un ACO, y c) TAPD: combinación de AAS y un iP2Y12.
Beneficios y riesgos de cada estrategiaEl problema evidente con el TATT es el importante aumento del riesgo hemorrágico en comparación con las otras estrategias antitrombóticas (TATD o TAPD), como se ha constatado en múltiples estudios, como los registros a gran escala y metanálisis de ensayos clínicos12-14, en los que por lo general no se ha encontrado un beneficio con el TATT en cuanto a la reducción de eventos isquémicos. Pese a que la incidencia de eventos hemorrágicos es mayor en los primeros 30 días tras la ICP, el aumento en el riesgo de hemorragia asociado con el TATT se mantiene en el tiempo15. Por lo tanto, una prolongación innecesaria del TATT podría conllevar un riesgo inaceptable de eventos hemorrágicos en determinados grupos de pacientes, al no obtener una contrapartida clara en forma de prevención de eventos isquémicos. De este punto se deduce que, siempre tras una evaluación cuidadosa e individual del riesgo aterotrombótico y hemorrágico de cada paciente, la duración del TATT debe reducirse tanto como sea posible para minimizar el riesgo hemorrágico.
La evidencia disponible actualmente, sin embargo, aún no permite llegar a la conclusión de que haya que eliminar por completo el TATT en este contexto. Como se ve más adelante, los ensayos clínicos aleatorizados que han evaluado estrategias de TATT frente a TATD no tenían potencia estadística suficiente para evaluar parámetros de eficacia (eventos aterotrombóticos), además de tener otras limitaciones como la aparente inclusión de pacientes con un riesgo de eventos isquémicos relativamente bajo (p. ej., bajo porcentaje de SCA). Por otro lado, merece la pena recordar los estudios de finales de los años noventa que compararon diferentes estrategias de tratamiento antitrombótico en pacientes sometidos a ICP con implante de stent coronario16-19. En general, dichos estudios mostraron un beneficio del TAPD (AAS + tienopiridina) en comparación con una estrategia de TATD (AAS + AVK) en cuanto a la prevención de eventos aterotrombóticos (figura 1), fundamentalmente en el primer mes tras el procedimiento16-18. Evidentemente, hay que tener cautela a la hora de trasladar la interpretación de estos estudios al momento actual por las diferencias entre la práctica clínica y los dispositivos y procedimientos de entonces (p. ej., stents metálicos sin recubrimiento, acceso femoral…) y la práctica actual; sin embargo, de sus resultados se puede inferir que podría no ser conveniente prescindir del TAPD en el primer mes tras el implante de un stent en pacientes con alto riesgo, ya que el TATD no sería igual de eficaz para prevenir eventos adversos isquémicos. En esta línea, también conviene recordar que los eventos aterotrombóticos como el infarto de miocardio (IM) o la trombosis del stent no solo tienen una incidencia mayor en los primeros 30 días tras la ICP, sino que también presentan un pronóstico peor a corto y largo plazo, en términos de mortalidad, que los sucedidos en fases tardía o muy tardía20,21. Por ende, dado que los eventos isquémicos precoces tienen un peor pronóstico, este aspecto iría también a favor de no prescindir por completo del TATT en pacientes con FANV sometidos a ICP, al menos en el periodo inicial tras el procedimiento.
Resultados de los ensayos clínicos que comparan la doble antiagregación con el tratamiento antitrombótico doble tras el implante de stent coronario. A: eventos adversos cardiacos mayores. B: eventos hemorrágicos.
Las definiciones de eventos adversos cardiacos mayores varían según el estudio. En el ISAR, muerte de causa cardiaca, infarto de miocardio, cirugía de revascularización o reintervención (quirúrgica o percutánea) a los 30 días; en el STARS, muerte, infarto de miocardio, trombosis del stent o revascularización de la lesión diana a los 30 días; en el MATTIS, muerte de causa cardiovascular, infarto de miocardio y nueva revascularización a los 30 días; en el FANTASTIC, muerte, infarto de miocardio u oclusión del stent a las 6 semanas. Las definiciones de evento hemorrágico varían según el estudio: en el ISAR y el STARS, cualquier sangrado a los 30 días; en el MATTIS, sangrado mayor o complicación vascular mayor a los 30 días; en el FANTASTIC, cualquier sangrado a las 6 semanas. TAPD: tratamiento antiagregante plaquetario doble; TATD: tratamiento antitrombótico doble.
Se ha mencionado también en este apartado el TAPD porque es una estrategia que todavía se usa en la práctica clínica en un porcentaje no despreciable de pacientes15. El ensayo ACTIVE-W demostró que el TAPD (AAS + clopidogrel) es claramente inferior a los ACO (warfarina) para la prevención de eventos tromboembólicos en pacientes con FA22. Por eso, de acuerdo con las guías de práctica clínica, consideramos que utilizar TAPD sin ACO no debería considerarse en general para los pacientes con FA e indicación absoluta de ACO (CHA2DS2- VASc ≥ 2 los varones y ≥ 3 las mujeres) sometidos a ICP, pues no aporta una protección adecuada contra complicaciones cardioembólicas.
Análisis de la EvidenciaVarios estudios observacionales publicados recientemente han evaluado la eficacia y la seguridad del TAPD frente al TATT, y muestran de manera bastante uniforme un aumento en el riesgo de hemorragia mayor con el TATT, mientras que los resultados en cuanto a la prevención de eventos adversos isquémicos han sido más heterogéneos2,23,24. Sin embargo, estos estudios adolecen en general de un tamaño muestral pequeño y las limitaciones inherentes a su diseño, como es la ausencia de aleatorización (lo que puede implicar un sesgo de selección importante en la prescripción de los diferentes regímenes antitrombóticos), por lo que no se puede sacar conclusiones definitivas de sus resultados, especialmente en lo que respecta a la valoración de eficacia. Por este motivo, este apartado se centra en los resultados de los ensayos clínicos aleatorizados que se han realizado en el contexto que nos ocupa.
Tratamiento antitrombótico triple o doble en la era de los antagonistas de la vitamina KDos ensayos clínicos aleatorizados han evaluado el impacto clínico de diferentes estrategias antitrombóticas (retirar el AAS o reducir el tiempo de TATT) en comparación con el TATT convencional con AVK. El primero y más importante es el ensayo WOEST, que aleatorizó a 573 pacientes con necesidad de ACO sometidos a ICP a recibir TATT (AAS + clopidogrel + AVK) frente a TATD (clopidogrel + AVK) y observó una reducción relativa del 64% en los episodios de sangrado (cualquier evento hemorrágico) al año de seguimiento en el grupo de TATD (el 19,4 frente al 44,4%; hazard ratio [HR] = 0,36; intervalo de confianza del 95% [IC95%], 0,26-0,50; p < 0,001)25. Se apreció también, inesperadamente, un beneficio del TATD frente al TATT en cuanto a la reducción de eventos trombóticos (como mortalidad por cualquier causa salvo la cardiaca), aunque el estudio no tenía potencia estadística adecuada para encontrar diferencias en los objetivos de eficacia, y estos hallazgos podrían atribuirse en parte a un posible abandono inadecuado de fármacos antitrombóticos ante hemorragias de escasa magnitud (tabla 1). Se han planteado numerosas limitaciones al ensayo WOEST: a) la ya mencionada falta de potencia estadística para analizar eficacia por el pequeño tamaño muestral; b) inclusión de pacientes con bajo riesgo (aproximadamente el 25% con SCA); c) duración del TATT demasiado larga (12 meses); d) beneficio en sangrados debido fundamentalmente a una reducción en las hemorragias menores; e) diversas indicaciones de ACO (algo menos del 70% con FA), y f) presencia de otros factores que pueden favorecer un aumento en la incidencia de hemorragias, como un uso escaso de inhibidores de la bomba de protones y una utilización mayoritaria de acceso femoral para la ICP26. Sin embargo, pese a todas las críticas, el estudio es muy relevante, pues cuestionó por primera vez el paradigma de la necesidad de TATT para todos los pacientes con necesidad de ACO que se someten a ICP.
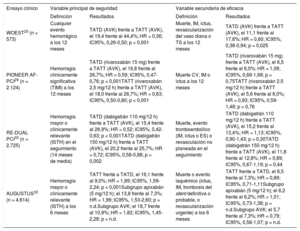
Ensayos clínicos aleatorizados sobre el tratamiento antitrombótico triple frente a doble en pacientes con indicación de ACO sometidos a ICP
| Ensayo clínico | Variable principal de seguridad | Variable secundaria de eficacia | ||
|---|---|---|---|---|
| Definición | Resultados | Definición | Resultados | |
| WOEST25 (n = 573) | Cualquier evento hemorrágico a los 12 meses | TATD (AVK) frente a TATT (AVK), el 19,4 frente al 44,4%; HR = 0,36; IC95%, 0,26-0,50; p < 0,001 | Muerte, IM, ictus, revascularización del vaso diana o TS a los 12 meses | TATD (AVK) frente a TATT (AVK), el 11,1 frente al 17,6%; HR = 0,60; IC95%, 0,38-0,94; p = 0,025 |
| PIONEER AF-PCI29 (n = 2.124) | Hemorragia clínicamente significativa (TIMI) a los 12 meses | TATD (rivaroxabán 15 mg) frente a TATT (AVK), el 16,8 frente al 26,7%; HR = 0,59; IC95%, 0,47-0,76; p < 0,001TATT (rivaroxabán 2,5 mg/12 h) frente a TATT (AVK), el 18,0 frente al 26,7%; HR = 0,63; IC95%, 0,50-0,80; p < 0,001 | Muerte CV, IM o ictus a los 12 meses | TATD (rivaroxabán 15 mg) frente a TATT (AVK), el 6,5 frente al 6,0%; HR = 1,08; IC95%, 0,69-1,68; p = 0,75TATT (rivaroxabán 2,5 mg/12 h) frente a TATT (AVK), el 5,6 frente al 6,0%; HR = 0,93; IC95%, 0,59-1,48; p = 0,76 |
| RE-DUAL PCI30 (n = 2.725) | Hemorragia mayor o clínicamente relevante (ISTH) en el seguimiento (14 meses de media) | TATD (dabigatrán 110 mg/12 h) frente a TATT (AVK), el 15,4 frente al 26,9%; HR = 0,52; IC95%, 0,42-0,63; p < 0,001TATD (dabigatrán 150 mg/12 h) frente a TATT (AVK), el 20,2 frente al 25,7%; HR = 0,72; IC95%, 0,58-0,88; p = 0,002 | Muerte, evento tromboembólico (IM, ictus o ES) o revasculación no planeada en el seguimiento | TATD (dabigatrán 110 mg/12 h) frente a TATT (AVK), el 15,2 frente al 13,4%; HR = 1,13; IC95%, 0,90-1,43; p = 0,30TATD (dabigatrán 150 mg/12 h) frente a TATT (AVK), el 11,8 frente al 12,8%; HR = 0,89; IC95%, 0,67-1,19; p = 0,44 |
| AUGUSTUS32 (n = 4.614) | Hemorragia mayor o clínicamente relevante (ISTH) a los 6 meses | TATT frente a TATD, el 16,1 frente al 9,0%; HR = 1,89; IC95%, 1,59-2,24; p < 0,001Subgrupo apixabán (5 mg/12 h); el 13,8 frente al 7,3%; HR = 1,99; IC95%, 1,53-2,60; p = n.d.Subgrupo AVK; el 18,7 frente al 10,9%; HR = 1,82; IC95%, 1,45-2,28; p = n.d. | Muerte o evento isquémico (ictus, IM, trombosis del stent definitiva o probable, o revascularización urgente) a los 6 meses | TATT frente a TATD, el 6,5 frente al 7,3%; HR = 0,89; IC95%, 0,71-1,11Subgrupo apixabán (5 mg/12 h); el 6,2 frente al 6,2%; HR = 1,01; IC95%, 0,73-1,38; p = n.d.Subgrupo AVK; el 5,7 frente al 7,3%; HR = 0,79; IC95%, 0,58-1,07; p = n.d. |
AVK: antagonistas de la vitamina K; CV: cardiovascular; ES: embolia sistémica; HR: hazard ratio; IM: infarto de miocardio; IC95%: intervalo de confianza del 95%; ISTH: International Society of Thrombosis and Haemostasis; n.d.: no disponible; TATD: tratamiento antitrombótico doble; TATT: tratamiento antitrombótico triple; TIMI: Thrombolysis in Myocardial Infarction; TS: trombosis del stent.
El ensayo ISAR-TRIPLE comparó una duración larga del TATT (6 meses de AAS + clopidogrel + AVK, seguido de AAS + AVK) frente a una corta (6 semanas de AAS + clopidogrel + AVK, seguido de AAS + AVK) en 614 pacientes con indicación de ACO (el 83,9% con FA) sometidos a ICP con implante de stent farmacoactivo27. No se encontraron diferencias entre las 2 estrategias (TATT corto frente a largo) en el objetivo principal de beneficio neto, un combinado de eventos isquémicos (muerte, IM, trombosis del stent definitiva e ictus) y hemorrágicos (sangrado mayor TIMI), a los 9 meses (el 9,8 frente al 8,8%; HR = 1,14; IC95%, 0,68-1,91; p = 0,63). Tampoco se evidenciaron diferencias en los eventos isquémicos y los hemorrágicos por separado, aunque en un análisis de los eventos a partir de las 6 semanas (una vez se abandonaba el clopidogrel en el grupo de TATT corto), sí se apreció un pequeño aumento (diferencia absoluta del 7,4%) de las hemorragias de cualquier tipo según la clasificación BARC (no así con la clasificación TIMI) en el grupo de TATT largo. Este estudio presenta algunas limitaciones, similares a las del WOEST, fundamentalmente el escaso tamaño muestral que condiciona una falta de potencia estadística para encontrar diferencias significativas en los objetivos de eficacia. Pese a ello, considerando ambos estudios en conjunto, los resultados obtenidos apuntan nuevamente a que la duración del TATT debe acortarse al mínimo tiempo necesario para cada paciente.
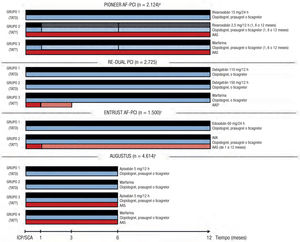
Tratamiento antitrombótico triple o doble en la era de los ACODLa guía de FA plantea el uso de ACOD (dabigatrán, rivaroxabán, apixabán y edoxabán) como primera opción de tratamiento anticoagulante en la FANV, con preferencia a los AVK3. Entre los beneficios de los ACOD, se encuentra un perfil de riesgo hemorrágico en general más favorable que el de los AVK28, aunque lo más recomendable sería una evaluación específica de este aspecto con cada uno de estos fármacos, lo cual escapa al objetivo del presente artículo. En cualquier caso, usar ACOD parece particularmente indicado en situaciones en que el riesgo hemorrágico es muy alto, como el contexto que nos ocupa, donde se combinan tratamientos antiagregantes y anticoagulantes. En el momento de redactar este artículo, se encuentran ya publicados 3 ensayos clínicos aleatorizados que han comparado estrategias de tratamiento antitrombótico con ACOD y con AVK, y hay otro en marcha; el diseño de estos estudios se representa esquemáticamente en la figura 2. Aunque estos ensayos se explican más detalladamente en otros artículos de este suplemento, se comentan brevemente a continuación los resultados principales.
Estrategias de tratamiento antitrombótico en los ensayos clínicos que comparan ACOD con AVK en pacientes con FA sometidos a ICP o que padecen un SCA. AAS: ácido acetilsalicílico; ICP: intervención coronaria percutánea; iP2Y12: inhibidor del receptor P2Y12; SCA: síndrome coronario agudo; TATD: tratamiento antitrombótico doble; TATT: tratamiento antitrombótico triple.
aEn el grupo 2 del ensayo PIONEER AF-PCI se administraba un TATT inicial con rivaroxabán 2,5 mg/12 h + un iP2Y12 + AAS durante 1, 6 o 12 meses, seguido de rivaroxabán 15 mg/día + AAS hasta completar 12 meses.
bEn el grupo 3 del ensayo RE-DUAL PCI se administraba AAS durante 1 mes en caso de implante de stent metálico y 3 meses en caso de stent farmacoactivo.
cEl tamaño muestral del ensayo ENTRUST AF-PCI (aún no publicado) es el planeado en el diseño del estudio.
El ensayo PIONEER AF-PCI comparó 3 estrategias de tratamiento antitrombótico en 2.124 pacientes con FANV sometidos a ICP: grupo 1, TATD: iP2Y12 y dosis reducida de rivaroxabán (15 mg/día) durante 12 meses; grupo 2, TATT inicial con dosis muy baja de rivaroxabán (2,5 mg/12 h) y TAPD durante 1, 6 o 12 meses, seguido de rivaroxabán 15 mg/día y AAS hasta completar 12 meses, y grupo 3, TATT con AVK (INR objetivo 2,0-3,0) durante 1, 6 o 12 meses, seguido de AAS + AVK hasta completar 12 meses. El sangrado clínicamente significativo según la clasificación TIMI a los 12 meses, el objetivo principal del estudio, se redujo de manera significativa en los grupos que recibieron rivaroxabán respecto al grupo de TATT «estándar» con AVK (grupo 1 frente a grupo 3, el 16,8 frente al 26,7%; HR = 0,59; IC95%, 0,47-0,76; p < 0,001; grupo 2 frente a grupo 3, el 18,0 frente al 26,7%; HR = 0,63; IC95%, 0,50-0,80; p < 0,001). No se observaron diferencias significativas entre los grupos en las tasas de eventos aterotrombóticos (tabla 1), aunque el estudio no tenía la potencia estadística adecuada para detectar diferencias en los objetivos de eficacia29. La principal crítica que ha recibido este ensayo es el empleo de dosis de rivaroxabán que no son las evaluadas y aprobadas para prevención de eventos tromboembólicos en pacientes con FANV (incluida la de 15 mg, que se emplea en FA como dosis «reducida» para pacientes con insuficiencia renal moderada o grave). Otras limitaciones serían la inclusión de pacientes con bajo riesgo (SCA con elevación de marcadores de daño miocárdico en poco más del 30% de los pacientes) o una duración del TATT con AVK más larga de lo recomendado en el grupo de control (se asignó inicialmente al 52,7% de los pacientes a una duración de 12 meses). Sin embargo, merece la pena resaltar que este ensayo fue el primero en evaluar el empleo de ACOD como alternativa al TATT «clásico» con AVK en este contexto tan complejo.
El ensayo RE-DUAL PCI evaluó 2 regímenes de tratamiento antitrombótico en 2.725 pacientes con FANV a los que se practicó una ICP, comparando una estrategia de TATD con dabigatrán (110 o 150 mg/12 h) más clopidogrel o ticagrelor con otra de TATT con warfarina en la que el AAS se interrumpía al cabo de 1 mes en caso de implante de stents convencionales y al cabo de 3 meses en caso de stents farmacoactivos (~83%). La variable de valoración principal era la hemorragia mayor o clínicamente relevante durante el seguimiento (14 meses de media) según la clasificación ISTH (tabla 1), y se objetivó una reducción significativa en el grupo de TATD con dabigatrán 110 mg/12 h respecto al grupo de TATT con warfarina (el 15,4 frente al 26,9%; HR = 0,52; IC95%, 0,42-0,63; p < 0,001 para no inferioridad y p < 0,001 para superioridad), mientras que el grupo de TATD con dabigatrán 150 mg/12 h mostró también una disminución de eventos hemorrágicos respecto al TATT con warfarina (el 20,2 frente al 25,7%; HR = 0,72; IC95%, 0,58-0,88; p < 0,001 para no inferioridad y p = 0,002 para superioridad)30. Inicialmente el estudio se planeó para incluir a 8.520 pacientes, con lo que habría tenido una potencia estadística adecuada para encontrar diferencias en eficacia (objetivo combinado de IM, ictus y embolia sistémica), aunque este tamaño muestral se redujo posteriormente debido a una inclusión de pacientes a un ritmo insuficiente, y dicho objetivo quedó como secundario. La incidencia de eventos aterotrombóticos fue no inferior en el grupo combinado de TATD con ambas dosis de dabigatrán al compararlo con el grupo de TATT con warfarina (el 13,7 frente al 13,4%; HR = 1,04; IC95%, 0,84-1,29; p = 0,005 para no inferioridad). Cabe señalar, sin embargo, que hubo un aumento estadísticamente no significativo en el número de eventos isquémicos (IM y trombosis del stent) con la dosis de dabigatrán 110 mg/12 h comparado con el TATT con warfarina. Pese a algunas limitaciones como la ya comentada modificación en el tamaño muestral o la inclusión de pacientes con riesgo relativamente bajo (SCA con elevación de marcadores de daño miocárdico en aproximadamente el 35% de pacientes), conviene resaltar como una característica muy relevante del ensayo que fue el primero en evaluar en pacientes sometidos a ICP el uso de dosis de ACOD con eficacia comprobada (no dosis reducidas) para la prevención de eventos tromboembólicos en la FANV31.
Un punto muy importante de estos 2 ensayos es que en ellos no se realizó estrictamente una comparación directa entre AVK y ACOD (a las dosis adecuadas para la prevención de eventos tromboembólicos), es decir, no se evaluó el TATT con ACOD frente al TATT con AVK ni el TATD con ACOD frente al TATD con AVK. Por tanto, la reducción de hemorragias en los grupos de tratamiento con ACOD puede deberse al mejor perfil de seguridad de estos fármacos frente a los AVK, a la reducción del número de fármacos antitrombóticos (TATD en lugar de TATT) o, lo que es más probable, a la suma de los 2 aspectos. Esta duda queda despejada en gran medida tras la reciente publicación del ensayo AUGUSTUS32, que comparó con un diseño factorial 2 × 2, por un lado, apixabán (5 mg/12 h) frente a AVK y, por otro, una estrategia de TATD (placebo, iP2Y12 y ACO) con otra de TATT (AAS, iP2Y12 y ACO) durante 6 meses en 4.614 pacientes con FANV y SCA o sometidos a ICP. Se objetivó una reducción significativa en la incidencia de hemorragia mayor o no mayor clínicamente relevante a los 6 meses según la clasificación ISTH (variable de valoración principal del estudio) en los pacientes que recibieron apixabán respecto a los que recibieron AVK (el 10,5 frente al 14,7%; HR = 0,69; IC95%, 0,58-0,81; p < 0,001 para no inferioridad y superioridad), además de una disminución en la incidencia combinada de muerte y hospitalización, todo ello sin evidencia de diferencias significativas en el combinado de muerte y eventos isquémicos (ictus, IM, trombosis del stent clara o probable y revascularización urgente). Es verdaderamente relevante que el beneficio de apixabán sobre el AVK se produjo de manera coincidente tanto con el régimen de TATT como con el de TATD, lo que refuerza todavía más el concepto de que en este contexto complejo, independientemente de la estrategia escogida (TATT o TATD), debe recomendarse sistemáticamente un ACOD con preferencia a un AVK. En cuanto a la otra comparación evaluada, se apreció un aumento en el riesgo hemorrágico de los pacientes con TATT respecto a los que recibieron TATD (el 16,1 frente al 9,0%; HR = 1,89; IC95%, 1,59-2,24; p < 0,001 para no inferioridad y superioridad), sin evidencia de diferencias en eficacia (combinado de muerte y eventos isquémicos). Sin embargo, es importante señalar que se evidenció un incremento estadísticamente no significativo en el número de eventos isquémicos coronarios (IM, trombosis del stent y revascularización urgente) en los pacientes que recibieron TATD, y se debe considerar además que esta tendencia constante se produjo en un ensayo que no tenía potencia estadística suficiente para hallar diferencias en eficacia. Otras limitaciones del estudio que se han planteado serían la duración del TATT más larga que lo recomendado para los pacientes con ICP electiva o SCA sin ICP (un ~63% de los pacientes con TATT) o la administración de AAS a todos los pacientes desde el evento índice hasta la aleatorización, con lo que incluso los asignados a TATD recibieron TATT durante una media de 1 semana (cubriendo parte del periodo de máximo riesgo de eventos coronarios isquémicos). El reclutamiento del ensayo ENTRUST-AF PCI (NCT 02866175), que compara una estrategia de TATD con edoxabán 60 mg/día y un iP2Y12 frente a TATT estándar con AVK en pacientes con FANV sometidos a ICP, ha finalizado y se espera que se presenten sus resultados próximamente, aunque cabe recordar que también es un estudio de seguridad sin la potencia estadística suficiente para evaluar las variables de eficacia.
Recomendaciones PrácticasUna vez repasada la evidencia existente sobre el uso de tratamiento triple o doble en pacientes con FA que se someten a ICP, en este apartado se aportan unas recomendaciones de utilidad para la práctica clínica mediante la respuesta a una serie de preguntas que pueden plantearse en este contexto.
¿Tratamiento antitrombótico de inicio triple o doble?Como se ha visto en los apartados anteriores, los ensayos aleatorizados que han evaluado el TATT frente al TATD (incluidos los ensayos con ACOD) o duraciones de TATT van claramente en la línea de reducir la duración al mínimo posible25,27,29,30. Sin embargo, ninguno de estos estudios tenía una potencia estadística adecuada para valorar la eficacia de las distintas estrategias analizadas en cuanto a prevención de eventos isquémicos o tromboembólicos. Además, no hay datos suficientes sobre la eficacia de las estrategias de TATD en pacientes con un riesgo alto de eventos coronarios isquémicos recurrentes o ictus. Por todo ello, la opinión de los autores es que la evidencia actual no justifica prescindir totalmente del TATT durante un tiempo limitado (el periodo en que cada sujeto sea más vulnerable a padecer eventos isquémicos) para la mayoría de los pacientes. De hecho, las guías de práctica clínica más recientes recomiendan emplear el TATT para los pacientes con FA e indicación de ACO que se someten a ICP, dejando como alternativa el TATD de inicio para los pacientes con un riesgo hemorrágico elevado que se considera mayor que el aterotrombótico1. En caso de escoger el TATD, las guías prefieren el clopidogrel como antiagregante de elección en este contexto, aunque conviene recordar que existe un porcentaje de pacientes (aproximadamente 15-30%) que presentan una respuesta subóptima a este fármaco33, por lo que la combinación de AAS y ACO también puede y debe considerarse.
¿Duración del tratamiento triple?Una valoración cuidadosa y personalizada de los riesgos de eventos isquémicos, tromboembólicos y hemorrágicos de cada paciente es absolutamente imprescindible no solo para decidir entre TATD y TATT, sino también para escoger su duración. Para ello pueden ayudar las escalas de riesgo (CHA2DS2-VASc, HAS-BLED, ABC…), haciendo hincapié en los factores de riesgo hemorrágico modificables1-3. Al igual que para escoger la duración del TAPD tras la ICP convencional, este abordaje individualizado basado en el equilibrio entre los riesgos isquémico y hemorrágico debe incorporar la evaluación de factores relacionados con el paciente (presencia de comorbilidades), con el procedimiento (anatomía coronaria de riesgo o procedimiento) y con el tipo de dispositivo empleado (la guía europea vigente no diferencia para la duración del tratamiento antitrombótico entre stents metálicos y farmacoactivos, aunque puede haber otros dispositivos que requieran consideraciones particulares, como los armazones vasculares reabsorbibles)34. La guía europea recomienda una duración de 1 mes para los pacientes en los que prevalece la preocupación por el riesgo hemorrágico, para quienes también se puede valorar la alternativa de un TATD, y de entre 1 y 6 meses para aquellos en los que se asume que prevalece el riesgo isquémico1. De manera absolutamente empírica, se puede considerar que 1 mes de TATT probablemente sea suficiente para la mayoría de los pacientes con cardiopatía isquémica estable y entre 3 y 6 meses para los pacientes con SCA (reservando la duración de 6 meses para los pacientes con un riesgo aterotrombótico claramente alto), aunque cabe recordar que lo recomendable siempre es individualizar la decisión según los factores anteriormente mencionados.
¿Uso de iP2Y12 potentes en combinación con ACO?La combinación de ACO con un iP2Y12 potente, como prasugrel o ticagrelor, se ha estudiado en un número de pacientes muy pequeño. De hecho, los datos existentes se limitan a las pequeñas proporciones de pacientes incluidos en el PIONEER AF-PCI (< 6%)29, el RE-DUAL PCI (ticagrelor en un 12%)30 y el AUGUSTUS (~7%)32, además de algunos estudios observacionales en los que se ha observado una incidencia de hemorragia inaceptablemente alta entre los pacientes que tomaban prasugrel o ticagrelor como parte del TATT35,36. Por todo ello, se recomienda claramente evitar en general el uso de prasugrel o ticagrelor como parte del TATT1. Únicamente de manera excepcional podría valorarse su uso en caso de que un paciente tenga episodios aterotrombóticos (como trombosis del stent) mientras toma un TATT que incluya clopidogrel, tras haber comprobado un correcto cumplimiento terapéutico y que la anticoagulación sea correcta (ACOD a dosis adecuada o AVK en rango terapéutico), especialmente si se evidencia una respuesta subóptima al clopidogrel. En cuanto al uso de prasugrel o ticagrelor como parte de un TATD en combinación con AVK o ACOD, la escasez de datos en la literatura obliga a ser prudentes al respecto y no permite hacer recomendaciones definitivas. Sin embargo, si el objetivo que se persigue con el TATD es reducir las complicaciones hemorrágicas, no parece coherente usar sistemáticamente un iP2Y12 potente en este contexto.
¿Uso de anticoagulantes orales de acción directa? ¿A qué dosis?Pese a las ya comentadas limitaciones de los ensayos clínicos realizados hasta la fecha29,30,32, este contexto en que el riesgo hemorrágico es particularmente alto parece especialmente favorable para la utilización de ACOD, por el potencial beneficio de estos fármacos en comparación con los AVK en cuanto a la reducción de eventos hemorrágicos. De hecho, la guía europea de revascularización coronaria publicada recientemente se ha posicionado de manera clara a este respecto (clase IIa con nivel de evidencia A), y recomienda el uso de ACOD con preferencia a los AVK para los pacientes con FANV que requieren la combinación de tratamiento antiagregante y anticoagulante1.
Un aspecto de importancia capital es el de las dosis de ACOD, y ha de quedar claro que se debe usar la dosis mínima del ACOD que se ha evaluado en los ensayos fundamentales de FA y que ha demostrado eficacia para la prevención de ictus1-3. Por lo tanto, no han de utilizarse dosis «reducidas» de manera inapropiada, ya que este aspecto puede asociarse con un aumento de eventos tromboembólicos37. Pese a ello, el uso de la dosis «reducida» de rivaroxabán 15 mg/día se puede considerar según la guía, pues se empleó en el ensayo PIONEER AF-PCI, aunque la recomendación es únicamente de clase IIb, y parece más coherente seguir la recomendación general de usar las dosis con eficacia demostrada en los ensayos de FA (clase IIa). El ensayo RE-DUAL PCI fue el primero publicado en que las dosis del ACOD (dabigatrán) empleadas habían mostrado eficacia para la prevención de eventos tromboembólicos en la FA. Se generó cierta preocupación en cuanto al TATD que combina la dosis de 110 mg/12 h con un único antiagregante, debido al ya mencionado aumento (que no alcanzó significación estadística) en el número de eventos isquémicos (IM y trombosis del stent) con dicha dosis comparado con el TATT con warfarina, cosa que no sucedió con la dosis más alta de 150 mg/12 h30. Por este motivo, en caso de elegir dabigatrán como anticoagulante, parece aconsejable usar la dosis de 110 mg/12 h mientras el paciente reciba TATT y la de 150 mg/12 h una vez que el paciente reciba TATD (ya sea de inicio o al acabar el periodo estipulado de TATT), y así se refleja también como recomendación en la guía de revascularización1.
ConclusionesLa elección del tratamiento antitrombótico y su duración para los pacientes anticoagulados por FA que se someten a ICP es compleja y requiere una valoración cuidadosa e individualizada de los riesgos isquémico, tromboembólico y hemorrágico de cada sujeto. Pese a las limitaciones de la escasa evidencia científica existente, los datos disponibles permiten proponer una serie de recomendaciones: a) la duración del TATT debe reducirse tanto como sea posible y limitarse al tiempo considerado estrictamente necesario para minimizar el riesgo hemorrágico, aunque con la evidencia actual no parece justificado prescindir totalmente del TATT en la mayoría de los pacientes; b) el TATD desde el inicio tras la ICP se puede valorar para los pacientes con alto riesgo hemorrágico que se considera que prevalece sobre el isquémico; c) en general, se desaconseja claramente el uso de un iP2Y12 potente (prasugrel o ticagrelor) como parte del TATT, y d) el empleo de ACOD en este contexto parece particularmente beneficioso y la guía de práctica clínica más reciente lo recomienda de modo preferente sobre los AVK, aunque es importante señalar que deben utilizarse dosis de ACOD con eficacia para la prevención de eventos tromboembólicos demostrada en los estudios fundamentales en FA. Están en marcha más ensayos clínicos que sin duda aportarán información relevante en el futuro próximo para ayudar a seleccionar y personalizar el tratamiento antitrombótico en este contexto.
Conflicto de InteresesJ.L. Ferreiro declara que ha recibido honorarios por ponencias de Eli Lilly Co., Daiichi Sankyo Inc., AstraZeneca, Roche Diagnostics, Pfizer y Boehringer Ingelheim; honorarios por consultoría de AstraZeneca, Eli Lilly Co. y Ferrer, y becas de investigación de AstraZeneca. L.M. Lugo no tiene conflicto de intereses.
Información Sobre el SuplementoEste artículo forma parte del suplemento titulado «Actualización en el tratamiento de los pacientes con fibrilación auricular sometidos a intervención coronaria», que ha sido patrocinado por Boehringer Ingelheim.