El implante valvular aórtico percutáneo ha surgido recientemente como alternativa terapéutica para pacientes con estenosis aórtica severa sintomática y alto riesgo quirúrgico. Se presenta la experiencia inicial en el tratamiento de la disfunción de la bioprótesis aórtica mediante el implante percutáneo de prótesis aórtica CoreValve en 4 pacientes, tanto con estenosis como con insuficiencia aórtica, y se analiza los resultados hospitalarios y a medio plazo. El procedimiento se realizó con anestesia local y guiado por angiografía. Se implantaron con éxito en todos los casos, si bien uno precisó una segunda prótesis por posicionamiento alto de la primera. No hubo complicaciones mayores. Tras un seguimiento medio de 7±4,7 meses, todos los pacientes se encuentran asintomáticos.
Palabras clave
La incidencia de estenosis valvular aórtica en el mundo crece actualmente de forma exponencial secundaria al aumento de la esperanza de vida1,2. La sustitución valvular aórtica es el tratamiento estándar y las prótesis biológicas han sido las de elección en pacientes de edad avanzada o con comorbilidad3. Estas prótesis biológicas cardiacas presentan una corta vida media, que puede disminuir por diferentes procesos degenerativos4, y la reintervención supone un riesgo muy elevado en este grupo de pacientes5.
El reemplazo valvular aórtico percutáneo se plantea como alternativa en el tratamiento de la estenosis valvular aórtica severa sintomática con alto riesgo quirúrgico6,7,8,9,10. La disfunción de una bioprótesis aórtica puede considerarse un subgrupo de pacientes en alto riesgo. Presentamos la experiencia inicial en el tratamiento de la disfunción de la bioprótesis aórtica, tanto por estenosis como por insuficiencia, mediante el implante percutáneo de la prótesis valvular aórtica CoreValve.
MétodosEn 2008 se inició en nuestro centro un programa de evaluación e implante percutáneo con la prótesis aórtica CoreValve para pacientes con alto riesgo quirúrgico o edad avanzada (> 80 años) que rechazaban la cirugía de sustitución valvular. En la selección de los pacientes se han seguido las recomendaciones de las diferentes sociedades científicas11, además de cumplir los criterios anatómicos necesarios para el implante percutáneo6.
En el periodo comprendido entre abril de 2008 y noviembre de 2009, 69 pacientes fueron tratados consecutivamente con la prótesis aórtica percutánea CoreValve por valvulopatía aórtica severa sintomática con alto riesgo quirúrgico. Cuatro pacientes presentaban una bioprótesis aórtica disfuncionante: 2 con insuficiencia aórtica severa y 2 con estenosis aórtica.
Los pacientes fueron evaluados clínicamente, y se estimó su riesgo quirúrgico mediante el EuroSCORE logístico. Se realizó ecocardiograma, coronariografía, aortografía de la raíz aórtica y angiografía del eje iliofemoral.
Para diámetros de la bioprótesis quirúrgicas ≥ 23 mm, se seleccionó la prótesis CoreValve grande, y para diámetros < 23 mm, la pequeña.
Descripción del dispositivo y procedimientoLa prótesis aórtica CoreValve es una prótesis biológica trivalva, de pericardio porcino, montada y suturada sobre una estructura autoexpandible de nitinol. Existen dos tamaños de válvulas: pequeña, que mide 26 mm en la porción insertada en el anillo nativo, y grande, que mide 29 mm. La longitud de la prótesis es de 50 mm.
ProcedimientoLos procedimientos se realizaron con anestesia local y sedación superficial. En los 4 casos el acceso fue la arteria femoral, con introductor de 18 Fr. La punción femoral se cerró con el dispositivo percutáneo Prostar XL®. La liberación de la prótesis aórtica se realizó con controles angiográficos. En el caso de disfunción de la bioprótesis con insuficiencia aórtica, no se realizó valvuloplastia previa al implante de la prótesis. No hubo dificultades en el avance de la prótesis CoreValve a través de la bioprótesis quirúrgica. Se realizó control ecocardiográfico a las 72 h.
Se consideró éxito del procedimiento el implante correcto con la prótesis normofuncionante en ausencia de mortalidad hospitalaria.
ResultadosLa media de edad de los pacientes con la bioprótesis disfuncionante fue 77,2±13,5 (60-89) años y el EuroSCORE logístico, 33,7%±24,6% (7,14%-63,9%). En la Tabla 1 se resumen las características basales. Los 2 pacientes con disfunción protésica por estenosis severa eran portadores de bioprótesis Carpentier-Edwards de 19 y 27 mm. La bioprótesis aórtica de los pacientes con insuficiencia aórtica eran sin soporte y con anillo radiotransparente: Intac 23 mm (Medtronic) y Mosaic 21 mm (Medtronic).
Tabla 1. Características basales de los pacientes con prótesis biológica degenerada*
| 1 | 2 | 3 | 4 | |
| Edad (años) | 60 | 87 | 73 | 89 |
| Sexo | Varón | Mujer | Mujer | Mujer |
| EuroSCORE log (%) | 7,14 | 41,92 | 22,1 | 63,9 |
| Enfermedad coronaria | Sí | Sí | Sí | Sí |
| Disnea, clase funcional NYHA | IV | IV | IV | IV |
| Fracción de eyección (%) | 66 | 68 | 57 | 75 |
| Bioprótesis | C-E 27 mm | C-E 19 mm | Intac 23 mm | Mosaic 21 |
| Grado de calcificación | Leve | Moderada | Moderada | Leve |
| Duración de la bioprótesis (años) | 3 | 11 | 14 | 9 |
| Disfunción | Estenosis | Estenosis | Insuficiencia | Insuficiencia |
| Comorbilidad | Cirrosis hepática | Artritis reumatoide |
C-E: Carpentier-Edwards; NYHA: New York Heart Association.
*El paciente 1 presentaba como comorbilidad una cirrosis hepática complicada con hipertensión portal. La paciente 3, como comorbilidad tenía una artritis reumatoide, con deformación del tórax.
El implante de la prótesis aórtica CoreValve se realizó con éxito en los 4 pacientes. En 2 casos fueron prótesis pequeñas y 2, prótesis grandes. El tiempo medio del procedimiento fue 117±11,5 min y el de liberación de la prótesis aórtica, 7,7±2,8 min.
La liberación de la prótesis aórtica CoreValve fue más fácil en los casos con anillo radiopaco, por visualizarse con radioscopia el anillo de la bioprótesis (Figura 1), a diferencia de la bioprótesis sin soporte (Figura 2). Tras el implante de la prótesis aórtica CoreValve, se obtuvo mejoría hemodinámica y desapareció el gradiente aórtico. En un caso hubo que implantar una segunda prótesis en el mismo procedimiento, porque la primera prótesis quedó en posición supraanular que condicionaba insuficiencia aórtica severa (Figura 3). El grado de regurgitación aórtica tras el procedimiento fue trivial en 2 pacientes y leve en los otros 2. No hubo ninguna complicación cardiovascular ni cerebrovascular.
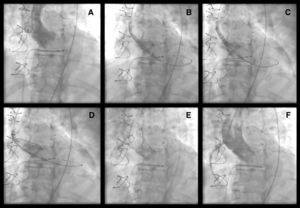
Figura 1. A: prótesis biológica Carpentier-Edwards disfuncionante por estenosis severa. B-D: diferentes momentos de la liberación de la prótesis CoreValve. E-F: resultado angiográfico tras el implante.
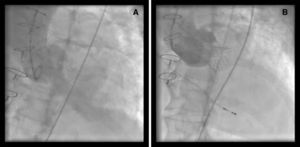
Figura 2. Bioprótesis aórtica sin soporte disfuncionante. A: insuficiencia aórtica severa. B: resultado angiográfico tras el implante.
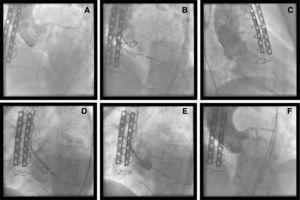
Figura 3. Prótesis biológica degenerada. A: insuficiencia aórtica severa. B: liberación de la prótesis. C: insuficiencia aórtica severa tras implante alto de la prótesis. D-E: implante de una segunda prótesis CoreValve. F: resultado angiográfico.
El gradiente aórtico máximo y medio ecocardiográfico disminuyó de 66,7±25,7 a 24±7,4 mmHg y de 44±22,7 a 14,7±5,6 mmHg, respectivamente.
Un paciente precisó de marcapasos a los 4 días del procedimiento por bloqueo auriculoventricular paroxístico al tercer día.
La estancia hospitalaria fue de 5,2±0,9 días (4-6). Al alta, la NT-proBNP disminuyó de 5.308 a 3.418 pg/ml, y los pacientes presentaron mejoría clínica, pasando de un grado funcional IV a I-II de la New York Heart Association.
Tras un seguimiento medio de 7±4,7 meses (4-14), todos los pacientes permanecen asintomáticos.
DiscusiónEl implante percutáneo de la prótesis aórtica CoreValve supone una nueva oferta en el tratamiento de la estenosis aórtica severa con alto riesgo quirúrgico6,7,8,9,10. Sin embargo, tras la curva inicial de aprendizaje y observar los excelentes resultados tanto periprocedimiento como a medio plazo, se han extendido a otras indicaciones que inicialmente no se consideraba. Una de ellas es la disfunción de una bioprótesis aórtica, fundamentalmente por insuficiencia aórtica, siguiendo el concepto de una válvula sobre otra válvula12.
Las prótesis biológicas cardiacas tiene una corta vida media a pesar de la gran mejora experimentada con las nuevas generaciones de prótesis. Así, el porcentaje de pacientes libres de reemplazo valvular aórtico con la primera generación de prótesis Carpentier-Edwards (implantadas a finales de los años setenta) a los 15 años es del 58%4, mientras que para la segunda generación (implantadas en los años ochenta y noventa) es del 83%13. Las reintervenciones suponen un riesgo muy elevado en este grupo de pacientes, teniendo en cuenta que gran parte ellos son octogenarios. En la serie de Langanay et al14, que analizan la cirugía valvular aórtica en octogenarios, el principal factor predictor de mortalidad fue la reoperación. Por ello, un acercamiento terapéutico de menor riesgo puede ofrecer ventajas indudables a un mayor número de pacientes.
Otro aspecto importante es la edad a la que se implanta una bioprótesis frente a una prótesis mecánica. Es una controversia en la que se enfrentan el riesgo de la reoperación y el riesgo de la anticoagulación crónica. En un estudio reciente, la supervivencia libre de eventos sería mejor para las bioprótesis a partir de la edad de sesenta años15. Si a esto añadimos que en el futuro podremos ofrecer el implante percutáneo a pacientes en alto riesgo en vez de la reoperación, la utilización de prótesis mecánicas y la consecuente anticoagulación podrían quedar reservadas para pacientes más jóvenes.
Con el implante de una prótesis percutánea en estos casos, cabría esperar una incidencia de fenómenos adversos (fugas paravalvulares o embolias cerebrales) menor que en el tratamiento de una válvula aórtica nativa calcificada. En nuestros pacientes no tuvimos ninguna complicación en este sentido, aunque habrá que esperar a series más amplias para confirmarlo.
En conclusión, los resultados obtenidos con el implante percutáneo de la prótesis aórtica CoreValve indican que este tratamiento es factible y conlleva una mejoría hemodinámica y clínica para los pacientes con disfunción de una bioprótesis aórtica.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Recibido 27 Enero 2010
Aceptado 9 Marzo 2010
Autor para correspondencia: Servicio de Cardiología. Hospital Universitario Virgen de la Victoria. Campus de Teatinos, s/n. 29010 Málaga. España. ajmunozgarcia@secardiologia.es